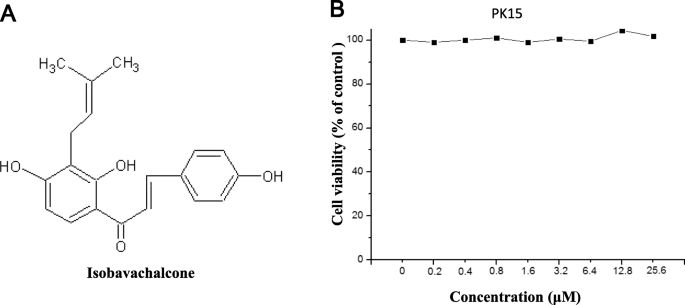
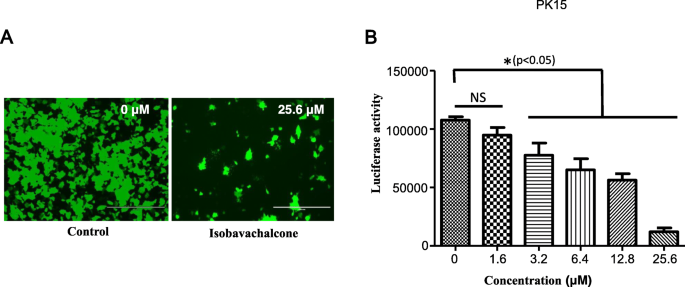
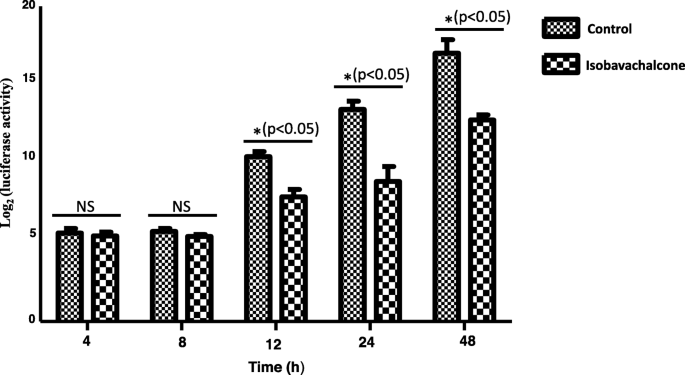
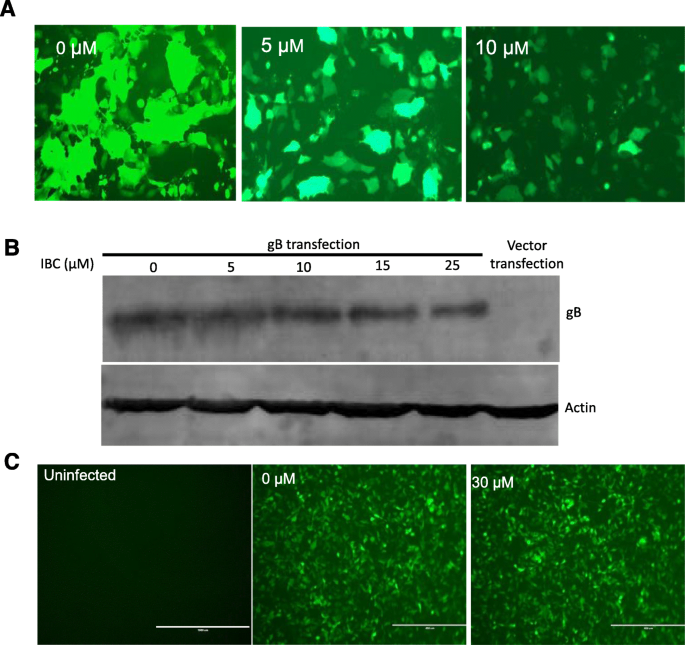
伪狂犬病病毒(PRV)是一种猪阿尔法疱疹病毒,可引起猪的奥耶斯基氏病[1,2].PRV对养猪业构成严重威胁,特别是自2011年新型PRV变种开始出现以来[3.,4].最重要的是,最近的研究报告指出,人类可被PRV感染[5,6,7],显示PRV亦对人类构成潜在威胁[6].因此,探索新型抗伪狂犬病毒制剂可能是控制伪狂犬病毒的有效手段。在本研究中,我们探讨了中药异巴achalcone (IBC)潜在的抗prv活性。IBC结构如图所示。1a. IBC首次分离自补骨脂于1968年推出,并拥有广泛的生物活性[8].在最近的一项研究中,IBC还在病毒RNA合成的早期阶段表现出抗猪繁殖与呼吸综合征病毒(PRRSV)的活性[9].为了探索IBC是否具有抗prv活性,我们首先根据制造商的说明,使用Cell Counting Kit-8 (CCK8, Dojindo Laboratories, Japan)评估了IBC对PK15细胞的细胞毒性。当IBC浓度达到25 μM时,细胞活力相对于对照细胞没有变化。接下来,我们通过表达增强绿色荧光蛋白(EGFP)和萤火虫荧光素酶的重组PRV报告病毒评估了IBC的抗病毒活性[10].这些结果表明,与对照组相比,ibc处理组的EGFP表达和荧光素酶活性均显著降低(图2)。2a和b),表明PRV复制被显著抑制。然而,PRV复制中受IBC影响的步骤尚不清楚。为了确定病毒生命周期中的哪些步骤受到影响,我们首先用IBC处理PK15细胞,2小时后用PRV报告病毒以MOI为0.01感染PK15细胞。在感染后12至48小时,IBC显著抑制PRV,而在感染后4和8小时,PRV复制不受影响。3.).根据伪狂犬病毒一步生长曲线的结果,病毒滴度在感染后约14 h达到峰值,因此我们认为感染后4和8 h为早期。这种模式表明IBC在病毒生命周期的后期抑制PRV。此外,这些结果表明,IBC抑制PRV和PRRSV的机制可能不同,因为在我们之前的研究中,IBC在早期阶段就抑制了PRRSV [9].PRV可以在生命周期的晚期诱导细胞间融合,这是病毒传播的一个非常重要的步骤。在这里,为了研究IBC是否在这一阶段抑制PRV复制,我们进行了基于瞬时转染的细胞间融合实验,如前所述[11,12].简单地说,每个EGFP表达质粒转染200 ng的RK13细胞(pDC315-EGFP [13])或根据制造商说明使用Lipofectamine 2000对gB、gL和gH PRV糖蛋白进行表达质粒(在本研究中通过将这些基因亚克隆到pCAGGS-HA载体中构建)。6小时后,将细胞培养基更换为含或不含IBC的培养基,转染24 h后固定细胞,荧光显微镜下分析合胞体形成情况。与我们的假设一致,IBC显著抑制PRV糖蛋白诱导的细胞间融合(图2)。4a).为了排除IBC抑制gB表达导致细胞间融合的可能性,我们接下来用gB特异性单克隆抗体(1:200;gB单抗由中国农业科学院哈尔滨兽医研究所田志军教授提供)。我们发现IBC处理后,gB的表达不受IBC的影响(图。4b).上述结果表明,IBC主要在生命周期后期的细胞-细胞融合阶段抑制PRV复制。为了进一步证实这一发现,我们评估了IBC对非包膜腺病毒的活性。如果IBC抑制腺病毒复制,它也可能在细胞与细胞融合之外的生命周期步骤中发挥抗病毒作用。表达egfp的腺病毒[13]感染HEK293细胞(MOI = 0.1)。24小时后,结果显示,在HEK293细胞中,腺病毒未被IBC抑制(图2)。4c),进一步证实IBC在细胞-细胞融合步骤抑制PRV复制。在我们之前的研究中,我们证明了CRISPR/Cas9系统可能是抑制和消除PRV的强大工具[14,15].然而,这种方法需要基因转移工具将CRISPR系统的组件引入细胞。因此,像IBC这样的抗病毒药物可能更适合于当前环境下的病毒控制。
总之,我们证明了IBC对PRV具有抗病毒活性,并证明IBC治疗显著阻断了PRV介导的细胞间融合。因此,IBC可能是进一步治疗猪PRV感染的候选药物。