病毒细胞和载体gydF4y2Ba
DEV CHV菌株(基因库:JQ647509.1)在实验室分离并保存[gydF4y2Ba22gydF4y2Ba].gydF4y2Ba
鸭胚成纤维细胞(DEF)在最低必需培养基(MEM;Gibco, Meridian Road Rockford,美国)补充10% (gydF4y2BavgydF4y2Ba/v)胎牛血清(FBS;Gibco,子午路罗克福德,美国)37°C, 5% COgydF4y2Ba2gydF4y2Ba.对于病毒感染,添加添加2%胎牛血清的维持培养基。实验室制备了常用试剂。gydF4y2Ba
重组β-actin质粒[gydF4y2Ba32gydF4y2Ba]和兔抗ul47蛋白多克隆抗体。gydF4y2Ba
重组表达载体的构建gydF4y2Ba
所有引物均采用Primer Premier 5软件设计(见表2)gydF4y2Ba1gydF4y2Ba).野生型DEV UL41 (GenBank: AFC61841.1)编码区使用特异性引物(PgydF4y2Ba1gydF4y2Ba和PgydF4y2Ba2gydF4y2Ba)构建pET-32a(+)-UL41,并在真核质粒pEGFP-C2中使用特异性引物(PgydF4y2Ba3.gydF4y2Ba和PgydF4y2Ba4gydF4y2Ba)创建pEGFP-C2-UL41。野生型DEV UL47 (GenBank:gydF4y2BaAFC61835.1gydF4y2Ba利用特异性引物(PgydF4y2Ba5gydF4y2Ba和PgydF4y2Ba6gydF4y2Ba),创建pcDNA3.1(+)-UL47。接下来,我们构建了真核质粒pcDNA3.1(+)-UL47gydF4y2BaΔ40 - 50gydF4y2Ba和pcDNA3.1 (+) -UL47gydF4y2BaΔ768 - 777,gydF4y2Ba它们分别缺失了DEV ul47编码蛋白(pUL47)的40 - 50个氨基酸和768 - 777个氨基酸(aa)。gydF4y2Ba
UL41-his融合蛋白的原核表达gydF4y2Ba大肠杆菌gydF4y2Ba
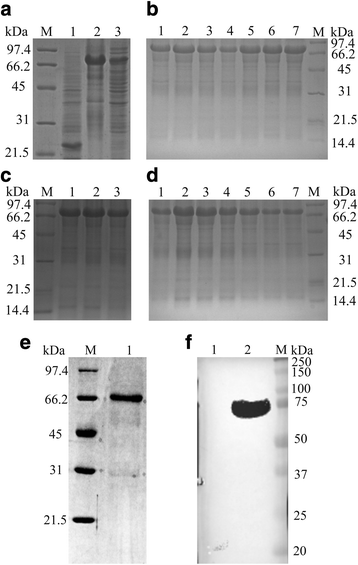
pET-32a(+)-UL41转化为gydF4y2Ba大肠杆菌gydF4y2BaBL21 (DE3)活性细胞。细菌培养于含有50μg/ml氨苄青霉素的Luria-Bertani (LB)培养基中,37℃。通过添加IPTG诱导蛋白表达(St Louis, MO, USA)。研究了不同诱导浓度(0.1、0.2、0.4、0.6、0.8、1.0和1.2 mM)、诱导时间(2、4、6、8和10 h)和诱导温度(25、30和37℃),以优化条件获得最高水平的UL41蛋白表达[gydF4y2Ba33gydF4y2Ba].IPTG诱导后,在4℃下离心收集不同时间点的细菌,并用超声波中断。同时对病媒控制培养进行了分析。十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)以12%的溶解凝胶和5%的堆积凝胶分析所有表达水平。gydF4y2Ba
融合蛋白的纯化及多克隆抗体的制备gydF4y2Ba
通过凝胶和电洗脱纯化UL41蛋白,并用纯化后的蛋白在小鼠体内生成多克隆抗体。将约1.1 mg纯化蛋白与等量的QuickAntibody-Mouse3W佐剂(Biodragon, Beijing, China)混合,通过肌内注射免疫11只小鼠。最后一次免疫后1周,取眼球放血,离心(9600×gydF4y2BaggydF4y2Ba, 20分钟,4℃)。gydF4y2Ba
西方墨点法gydF4y2Ba
如前所述[gydF4y2Ba29gydF4y2Ba],在感染后7、24、36、48、60、72 h (hpi)在6孔培养皿中收集dev感染的DEF细胞,去除上清液。通过12% SDS-PAGE分解的蛋白质进一步转移到聚偏氟乙烯(PVDF)膜上。膜在5%脱脂牛奶中阻塞2小时,然后用一抗孵育,用酶标二抗(Bio-rad Lab, CA, USA)在37℃下检测1小时。所有抗体用1%的脱脂牛奶稀释。在用PBST清洗几次以去除未结合的抗体后,根据制造商的说明使用Western BLoT化学发光HRP底物(Takara,大连,中国)检测信号。gydF4y2Ba
间接免疫荧光法(IFA)gydF4y2Ba
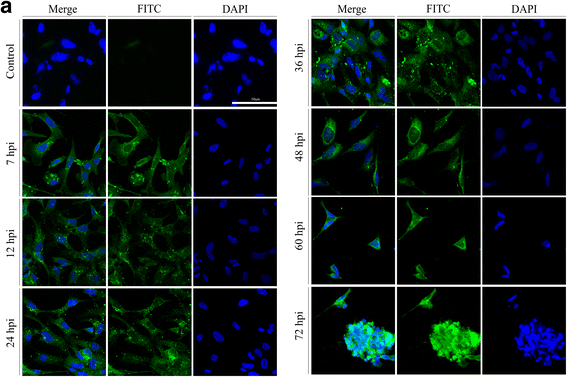
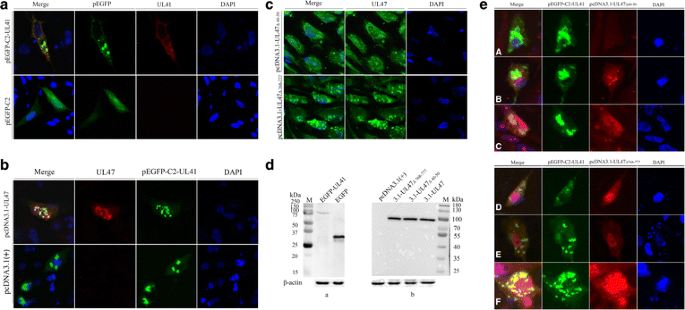
如前所述[gydF4y2Ba35gydF4y2Ba], 6孔培养皿中dev感染的DEF细胞在0、7、12、24、36、48、60、72 hpi时收集在盖板上,4%多聚甲醛PBS固定30 min, 0.25% Triton X-100 PBS在4℃渗透30 min, 5% BSA PBS在37℃封闭1 h。此外,细胞先用一抗孵育1小时,再用二抗体孵育1小时(赛默飞世尔科学公司,Meridian Road Rockford, USA)。所有抗体用1% BSA PBS稀释。最后,用DAPI (Roche, Mannheim, Germany)在室温下观察细胞核15分钟。盖片用甘油缓冲液密封在载玻片上,用共聚焦显微镜检查细胞(尼康A1,日本)。gydF4y2Ba
RT-qPCRgydF4y2Ba
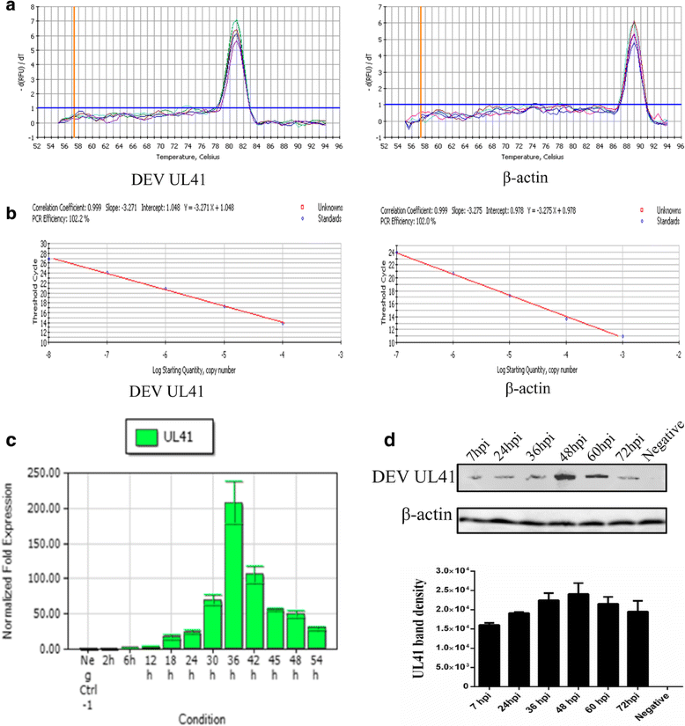
根据制造商的建议,使用TRIzol试剂l (Invitrogen, CA, USA)从dev感染的DEF细胞在不同时间点(0、2、6、12、24、36、42、45、48和54 hpi)中提取总RNA。分别用1%琼脂糖凝胶电泳和NanoDrop分光光度计测量光密度(OD260/OD280比值)来评价提取的RNA的完整性和纯度。随后,使用PrimeScript®RT试剂盒和gDNAeraser (Takara, Beijing, China)将RNA反转录为cDNA。UL41 (PgydF4y2Ba7gydF4y2Ba和PgydF4y2Ba8gydF4y2Ba)和β-肌动蛋白(PgydF4y2Ba9gydF4y2Ba和PgydF4y2Ba10gydF4y2Ba) [gydF4y2Ba35gydF4y2Ba使用之前描述的引物检测基因(表gydF4y2Ba1gydF4y2Ba).RT-qPCR条件设置如下:95°C初始变性1 min, 95°C变性5 s, 59°C退火20 s, 72°C延伸25 s。所有的反应都在三个重复和至少两个独立的实验中进行。测定阈值时的循环数(Ct值),分析UL41和β-actin基因的转录,并使用2gydF4y2Ba——ΔΔCTgydF4y2Ba方法(gydF4y2Ba25gydF4y2Ba].gydF4y2Ba
药物鉴定病毒粒子基因类型gydF4y2Ba
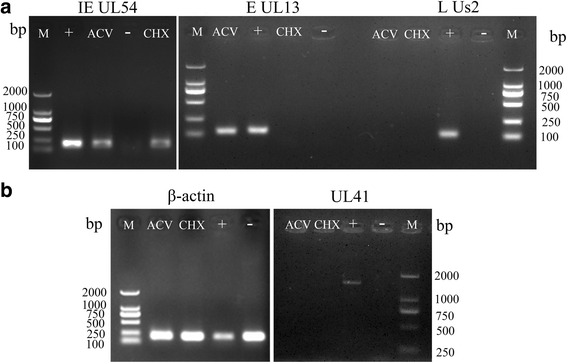
dev感染的DEF细胞在6孔培养皿中分别用300 μg/ml的阿昔洛韦(Glaxo SmithKline)或50 μg/ml的环己亚胺(Meilunbio, Dalian, China)孵育2 h。用TRIzol在24 hpi下提取总RNA,随后反转录为cDNA。采用引物对UL41进行PCR检测gydF4y2Ba1gydF4y2Ba和PgydF4y2Ba2gydF4y2Ba)和β-肌动蛋白(PgydF4y2Ba9gydF4y2Ba和PgydF4y2Ba10gydF4y2Ba),用1%琼脂糖凝胶确认。直接早期(IE)基因UL54 (PgydF4y2Ba11gydF4y2Ba和PgydF4y2Ba12gydF4y2Ba) [gydF4y2Ba35gydF4y2Ba],早期(E)基因UL13 (PgydF4y2Ba13gydF4y2Ba和PgydF4y2Ba14gydF4y2Ba) [gydF4y2Ba36gydF4y2Ba晚期(L)基因Us2 (PgydF4y2Ba15gydF4y2Ba和PgydF4y2Ba16gydF4y2Ba) [gydF4y2Ba37gydF4y2Ba]作为实验对照。gydF4y2Ba
病毒粒子净化gydF4y2Ba
收集dev感染的DEF细胞,采用低速离心(2000×gydF4y2BaggydF4y2Ba, 30分钟,4℃)。细胞外DEV病毒粒子经超离心(40000 ×gydF4y2BaggydF4y2Ba, 2小时,4°C)在贝克曼Ti70转子通过30% (wt/vol)蔗糖垫。用酒石酸钾连续梯度30 ~ 60% (wt/vol)等速梯度超离心收集TBS (40000 ×gydF4y2BaggydF4y2Ba, 2 h, 4°C),在贝克曼SW60转子中,TBS稀释10倍,然后通过超离心(20,000×gydF4y2BaggydF4y2Ba, 60分钟,4℃)。最后将颗粒在TBS中重悬,并在−80°C保存。gydF4y2Ba
质谱分析gydF4y2Ba
纯化的病毒粒样品采用12% SDS-PAGE分析。凝胶经考马斯亮蓝(Sigma)染色后送往中国上海生工生物技术公司进行液相色谱-串联质谱(LC-MS/MS)分析[gydF4y2Ba38gydF4y2Ba].所有数据也在NCBI中进行了搜索gydF4y2Ba牛gydF4y2Ba数据库。只有吉祥物得分大于30的序列才被考虑。被至少一种独特肽识别的蛋白质被接受。并使用指数修正蛋白质丰度指数(emPAI)来估计完整病毒粒子提取物的蛋白质相对丰度[gydF4y2Ba39gydF4y2Ba,gydF4y2Ba40gydF4y2Ba,gydF4y2Ba41gydF4y2Ba].gydF4y2Ba