摘要
背景
Belimumab是一种抗b细胞活化因子抗体,被批准用于治疗具有高度疾病活动性的自身抗体阳性系统性红斑狼疮。抗cd20b细胞清除与利妥昔单抗也用于难治性SLE,尽管有不同的反应。我们假设不完全的B细胞耗竭,与利妥昔单抗治疗后BAFF水平的激增有关,可导致持续的疾病活动和发作。Synbiose 1研究主要关注免疫效应,并显示了利妥昔单抗与贝利单抗联合治疗SLE的初步临床获益。Synbiose 2研究将评估贝利单抗联合利妥昔单抗治疗严重SLE患者的临床疗效,允许泼尼松龙和霉酚酸盐逐渐减少。
方法
Synbiose 2是一项3期、多中心、随机、对照、开放标签的2年临床试验。70名包括狼疮肾炎在内的严重SLE患者将以1:1的比例随机分配,接受由强的松龙和霉酚酸盐组成的标准治疗作为诱导和维持治疗,或贝利单抗和利妥昔单抗联合标准治疗作为诱导治疗,然后接受泼尼松龙和贝利单抗作为维持治疗。主要目的是评估联合B细胞治疗是否会减少治疗失败。次要终点是完全和部分临床和肾脏反应以及sle特异性自身免疫现象的改善。安全性终点包括不良事件的发生率,特别关注感染。
讨论
Synbiose 2试验是首个研究联合B细胞靶向治疗SLE(包括狼疮肾炎)的多中心3期临床试验。这项研究的结果将为这种新的治疗策略在严重SLE中的临床疗效提供进一步的证据。
试验注册
ClinicalTrials.govNCT03747159。于2018年11月20日注册
本研究的优势和局限性
◦这是一项随机、对照的3期试验,随访2年,专门针对包括狼疮肾炎在内的严重SLE患者
◦该研究的假设建立在belimumab和rituximab作为单药和联合用药在SLE患者的临床前和临床研究的强大科学基础之上
◦设计包括逐渐减少麦考酚酸盐和强的松龙作为干预组的维持治疗
◦该研究比较了两种不同的治疗策略,而不是单一的附加安慰剂对照剂,这可能被认为是一个局限性。然而,这种设置与临床实践密切相关,使结果直接转化为患者护理
◦该研究受其开放标签设计的限制
介绍
系统性红斑狼疮(SLE)是一种慢性自身免疫性疾病,其对核酸及其结合蛋白的耐受性丧失导致自身抗体的产生,从而引发和传播涉及各个器官系统的组织损伤性炎症。许多患者需要终生免疫抑制,通常使用大剂量皮质类固醇、环磷酰胺或霉酚酸酯,非特异性靶向免疫系统以减少炎症。这导致只有25-44%的患者长期处于低水平的疾病活动,而持续的完全缓解是罕见的[1,2,3.,4]。此外,大约10%的狼疮肾炎(LN)患者在5年内发展为终末期肾脏疾病,在15年内增加到20%以上[5]。目前治疗策略的副作用是短期(机会性)感染,长期有恶性肿瘤和心血管疾病的风险,导致SLE患者的预期寿命缩短[6,7]。这证实需要制定更好的策略来预防和治疗SLE的后遗症。
用生物制剂治疗SLE患者是有吸引力的,因为它们具有特异性靶向SLE发病机制中的关键罪魁祸首的潜力,与传统的免疫抑制剂相比,可能提高疗效并降低感染或恶性肿瘤的风险。利妥昔单抗是一种B细胞消耗抗cd20单克隆抗体,在几项回顾性和开放标签研究中显示出疗效[8,9,10,11,12,13,14,15,16,17]。然而,两项3期双盲安慰剂对照试验未能达到其主要终点,限制了其临床应用于标签外治疗难治性SLE [18,19]。LN患者的事后分析表明,B细胞去除深度与利妥昔单抗治疗后的完全肾反应相关,这表明更深度的B细胞去除会产生更好的临床结果[20.]。这一前提得到了最近一项obinutuzumab阳性2期研究的证实,obinutuzumab是一种新型抗cd20单克隆抗体疗法,其特点是改善B细胞消耗[21]。
对于利妥昔单抗不同疗效的另一种解释是它与B细胞活化因子(BAFF,也称为BLyS)水平升高有关。BAFF是B细胞存活、活化、向浆细胞分化和生发中心完整所必需的细胞因子。狼疮患者BAFF水平升高,并与疾病活动和发作有关[22,23,24,25]。在利妥昔单抗诱导的B细胞耗竭后,观察到BAFF水平升高,这可能触发B细胞和T细胞激活的反馈循环,导致体液自身免疫反应激增[26,27]。在一项队列研究中,这反映在抗双链DNA (anti-dsDNA)水平的上升和复发上[28]。这些观察结果表明,抗cd20介导的b细胞衰竭的临床疗效可以通过添加baff抑制剂来提高。
belimumab是一种抗循环baff的重组单克隆IgG1λ抗体,在两项关键的3期临床试验和随后的LN试验的结果之后,被批准作为成人活动性、自身抗体阳性SLE的附加治疗,尽管采用标准治疗,但疾病活动性很高。29,30.,31]。尽管与标准治疗相比,贝利单抗显示出优越的疗效,但单独作为附加治疗的贝利单抗无法在LN中实现超过30%的完全肾脏缓解。合成酶1 (狼疮中的协同B细胞免疫调节)研究首次全面描述了利妥昔单抗联合贝利单抗在严重难治性SLE患者队列中的临床和免疫学效果[27,32,33]。从这项研究中,我们了解到利妥昔单抗联合贝利单抗是安全的,耐受性良好,具有临床相关的阳性反应。简而言之,Synbiose 1表明,长期贝利单抗治疗抑制了B细胞的完全再生,导致抗dsdna、抗c1q和ENA自身抗体和中性粒细胞胞外陷阱(NETs)的长期减少。在67%的高度难治性患者中,观察到临床反应,其中80%的患者在2年随访期间继续进行贝利单抗维持治疗,允许停药霉酚酸酯,并逐渐减少皮质类固醇至7.5mg或更少。随后,CALIBRATE和BEAT-LUPUS在随机2期研究中证实,贝利单抗和利妥昔单抗联合治疗难治性SLE和LN患者是安全的,并且达到了相关的免疫学和临床终点[34,35]。这些研究表明,B细胞再生受到抑制,自身反应性B细胞的阴性选择增强,抗dsdna水平降低,联合B细胞治疗可降低严重急性发作的风险。总的来说,这些研究促使我们开展了Synbiose 2研究,这是一项3期随机研究,旨在研究贝利单抗联合利妥昔单抗治疗严重SLE患者的长期疗效和安全性。
方法
研究设计
这是一项在荷兰进行的为期2年的多中心、随机、对照、开放标签、非劣效性的3期研究,目的是研究belimumab联合利妥昔单抗的疗效和安全性。参与的学术和非学术医院的名单可在www.clinicaltrials.gov。
研究人群
该研究将包括严重疾病伴主要器官受累的成年SLE患者,包括LN。简而言之,患者年龄在18岁以上,并且根据系统性狼疮国际合作诊所(SLICC)的标准进行SLE临床诊断。严重疾病定义为SLE疾病活动性指数(SLEDAI)≥12,主要器官系统出现新的或进行性活动,或尽管进行了常规免疫抑制治疗,但疾病活动性仍然很高,这需要缓解诱导治疗。详细的纳入和排除标准总结于表中1。
随机化
70名患者将以1:1的比例随机分配到计算机生成的两种治疗策略中的一种,进入标准治疗组,由皮质类固醇加霉酚酸盐作为诱导和维持治疗,或干预组,诱导治疗由标准治疗组加上贝利单抗和利妥昔单抗,以及低剂量强的松龙和贝利单抗的维持治疗。入组和随机化将由患者治疗医师研究员或研究中心的主要研究者进行,并在筛选并获得知情同意后尽快进行,最好是在开始缓解诱导治疗之前,最多4周之后。
研究治疗
所有患者将给予标准护理,包括3次500 mg (< 60 kg)或1000mg (> 60 kg)静脉注射甲基强的松龙。随后将逐渐减少口服强的松龙,起始剂量为每天60mg,同时开始剂量为500mg,每天两次,每周增加,滴定以达到目标AUC为60-90mg*h/L,最大剂量为每天4000mg。在治疗药物监测(TDM)是不可能的情况下,霉酚酸盐剂量将滴定白细胞计数和病人的耐受性。随机分配到干预组的患者将接受标准护理,并在贝利单抗开始治疗后4周和6周,每周自行皮下注射贝利单抗200mg,并静脉注射两剂1000mg的利妥昔单抗。在输注利妥昔单抗之前,静脉注射100毫克甲基强的松龙,静脉注射2毫克克莱马斯汀,口服1000毫克对乙酰氨基酚。
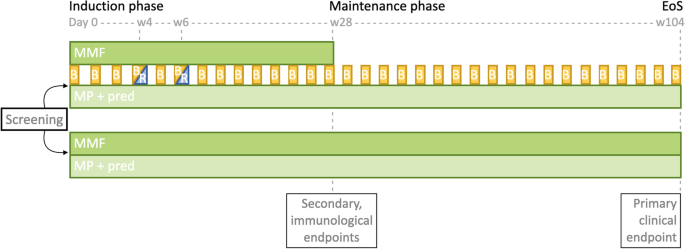
在两个治疗组中,口服强的松龙将在第28周之前逐渐减少到7.5mg,在第52周之前减少到5mg,并在剩余的研究期间继续以低剂量使用。剂量降至零可根据患者的耐受性进行个性化调整,由治疗医师判断。在对照组中,霉酚酸酯将在第28周减少50%,并在剩余的研究期间继续使用。干预组在第16周时将霉酚酸盐剂量减少50%,并在第28周停用。Belimumab将在整个研究期间继续使用。因此,在第28周后,患者将进入维持期,他们将接受强的松龙和霉酚酸盐(对照组)或强的松龙和贝利单抗(干预组)(图2)。1)。在研究期间,将对患者进行密切监测,在纳入后的前8周内,每2周进行一次实验室评估和研究访问,在研究的剩余时间内,间隔时间逐渐延长,最终达到2个月。研究访问的概况和每次访问的评估总结在表中2。
在SLE疾病活动严重发作时,将考虑替代治疗方案,这可能导致受试者退出研究。随机分配到标准治疗组的患者在出现严重急性发作或治疗反应不足需要更换药物的情况下,可以转到干预组。然后,他们将被认为达到了治疗失败的主要终点,如果他们符合纳入标准,将重新进入研究,并接受上述干预组的完整研究治疗。
伴随药物
复方新诺明、抗疟药、关节内注射、非甾体抗炎药和他汀类药物可在研究期间开始或继续使用。根据国家指南,抗蛋白尿药物可以由治疗医师自行决定。
在研究期间的任何时间以及第0天之前的60天内,禁止使用抗肿瘤坏死因子治疗、环磷酰胺和除贝利姆单抗和利妥昔单抗以外的生物制剂。在第0天之前的30天内禁止使用活疫苗。霉酚酸酯不允许与以下药物联合使用:甲氨蝶呤、硫唑嘌呤、来氟米特、钙调磷酸酶抑制剂、西罗莫司、6-巯基嘌呤和沙利度胺。最后,禁止本研究之外的任何研究药物。
研究端点
主要临床终点是试验期间治疗失败的患者比例,定义为死亡、发展为终末期肾脏疾病、主要肾脏或肾外光斑、血清肌酐持续翻倍、临床或肾脏无反应、需要诱导治疗或血浆置换、需要减少剂量或停止使用霉酚酸(除方案规定外)分别超过14天或7天。停药超过连续三次,无法完成两次利妥昔单抗治疗,因任何原因停药,或失去随访。
次要临床终点将在28周和104周时进行评估。临床缓解的定义是SLEDAI降低≥4分,医师总体评估(PGA)评分在0-3分范围内> 0.3分没有恶化。其他次要终点是临床缓解(定义为满足临床缓解标准,并额外达到类固醇减量至≤5mg /天),肾脏反应(完全肾脏反应为每24小时蛋白尿< 0.75克,血清肌酐在基线的125%以内),低水平疾病活动性(SLEDAI≤4,无主要器官系统活动,溶血性贫血或胃肠道活动,无新疾病,PGA≤1和≤7.5mg强的松龙当量),和疾病控制(SLEDAI≤2,每天≤5mg类固醇)[36]。患者报告的结果测量包括SF-36生活质量问卷[37]。其他临床次要终点是通过监测不良事件的发生,特别注意感染,联合治疗的可行性和安全性。
主要的免疫学终点是28周时抗dsdna和其他疾病特异性自身抗体的减少,104周时也进行评估。次级免疫终点是相关自身抗体的减少,持续的B细胞消耗,以及免疫复合物介导的过度NET产生在28周和104周的消退。
样本量计算
确定该研究样本量的功效分析基于Synbiose 1试验(即贝利单抗和利妥昔单抗联合治疗)和ALMS试验(即霉酚酸酯和类固醇的标准治疗)的数据[32,38]。为了显示治疗失败率的显著降低,我们假设在104周的研究期间,标准护理组的治疗失败率为54%(根据ALMS研究结果),而干预组的治疗失败率为23%(根据Synbiose 1研究结果)。我们计算出,为了证明风险比为2.97,且至少有80%的威力,使用5%的alpha误差置信水平和0.20的beta概率,该研究将需要总共70名患者随机分配,每组35名患者。
统计分析
统计分析将主要针对有意向治疗的人群进行。对于无偏倚的免疫学终点,将进行每个方案分析,以评估在标准治疗中添加贝利单抗和利妥昔单抗的病理生理效应。观察到的治疗失败率将显示在生存曲线中,治疗组之间的差异将使用log-rank检验进行评估。
将探讨基线特征、免疫终点和临床反应的差异。自身抗体滴度、记忆B细胞和NET形成的绝对和百分比降低将使用非参数Mann-Whitney作为连续变量进行分析U测试来比较治疗组。根据上述反应标准分类的临床疾病活动将使用卡方检验对二分类变量进行分析。免疫抑制剂的剂量将使用曼-惠特尼法作为连续变量进行分析U因为病人数量有限。缺失的数据将作为该受试者先前的观测值输入。从对照组过渡到干预组的患者将被视为达到了治疗失败的主要终点,并作为新受试者重新进入研究。因此,它们将包括在意向治疗分析中。此外,它们将在额外的事后分析中作为自己的控制。
安全性、毒性和不良事件将被记录,并且被认为至少可能与研究治疗相关的事件将按严重程度和治疗组进行总结。感染性AE将提交给独立的传染病专家评估其严重程度及其与研究参与的关系。
道德考虑及传播
这项由研究者发起的研究由莱顿-海牙-代尔夫特医学伦理委员会审查和批准,并在www.clinicaltrials.gov(NCT03747159)。所有参与站点在启动时将由其当地执行委员会对站点能力和适用性进行额外审查。该试验将按照国际协调会议-良好临床实践质量标准和所有其他适用的监管要求进行,并遵守源自赫尔辛基宣言的伦理原则。协调中心将负责整体试验和数据管理,监测和沟通各站点,并对试验进行一般监督。指导委员会将由协调中心和参与中心的主要调查人员组成。他们将全面监督,确保试验按照上述标准进行。
在开始任何研究特定程序或数据收集之前,所有患者都应获得书面知情同意,包括同意在潜在的后续研究中使用参与者数据和标本。所有数据都以标准化的方式存储在电子数据采集平台中,访问受限。数据完整性通过以下机制实现。所有的数据输入都是由研究小组的一名专职成员完成的。源数据将保存在参与场址的档案中,并将在定期监测访问时对数据库中存储的数据进行一致性检查。变更的文档将通过审计跟踪提供。通过将提交给电子数据采集平台的所有数据去标识化并使用受试者识别码,确保患者隐私。首席研究员将有权访问所有数据,其他主要研究人员将有权访问参与他们自己医疗中心的患者的试验数据集。所有患者都有权在试验期间的任何时间退出研究。值得注意的是,在严重急性发作或对标准治疗反应不足的情况下,交叉治疗的可能性增加了患者参与的优势,因为这使他们有资格在治疗选择可能有限的情况下接受新的治疗策略。 Follow-up evaluations will be performed for all patients at least 3 months after completing the 2-year follow-up and once a year thereafter if possible.
监测将每年进行两次,监测过程将独立于调查人员。审计委员会认为必要时将进行审计访问。严重不良事件将在24小时内报告给申办者。基于研究的风险,不需要数据监测委员会。然而,为了确保受试者的安全,每年将与独立专家举行四次安全会议,以监测和评估不良事件、治疗失败和退出。根据荷兰的法律要求,临床试验保险为研究受试者因研究造成的伤害提供赔偿。在医学上有指示的情况下,可以根据需要加强试验访问,或者在试验期间发生不良事件或伤害的情况下由试验的独立医生补充。在试验期间或由于试验而产生的额外卫生保健需求将由调查人员充分解决。
采用了几种方法来提高参与者的保留率和随访完成率,最大限度地减少患者的负担和实际意义。日程安排预约是计划好提前时间和提醒包括在内。非计划访问学习中心将提供旅行津贴。此外,退出研究药物的患者将按照协议规定定期随访,除非知情同意被撤回。研究期间的治疗定义为长达104周,之后可以继续使用belimumab治疗,或者根据治疗医生与患者共同决定,患者可以切换到另一种免疫抑制方案。在荷兰,贝利姆单抗由保险公司承保,用于LN患者的治疗,在研究完成后,在常规临床实践中继续使用任何治疗组的任何药物都没有障碍。
重要的议定书修订将与所有相关方进行沟通。我们将提交我们的研究结果供同行评审,开放获取出版物,并且该随机临床试验的数据以及其他相关文件将根据合理要求提供。本文符合标准方案项目:介入性试验建议(SPIRIT)方案报告建议[39]。
病人及公众参与
患者和公众没有参与这项研究的发展。
讨论
这项由研究者发起的试验是通过分析使用利妥昔单抗和贝利单抗联合治疗的SLE患者的临床和免疫学数据而开发的,利妥昔单抗和贝利单抗是一种靶向和免疫协同治疗,在自身抗体介导的疾病(如SLE和LN)中有很大的希望。Synbiose 2研究将通过评估2年研究期间的治疗失败来比较两种治疗策略的疗效——单独标准治疗与标准治疗加贝利姆单抗和利妥昔单抗。随后,该研究将允许通过开始皮下贝利姆单抗治疗和利妥昔单抗治疗来研究靶向自身反应性B细胞的潜在改进,并研究对B细胞消耗和再生、循环自身抗体和NET形成的免疫学影响。最终,通过评估减少累积类固醇剂量和迅速减少霉酚酸酯的能力,同时避免疾病活动的爆发,本研究解决了长期免疫抑制剂毒性的临床问题,以及专门针对SLE患者的体液自身免疫反应。因此,即使在与既定治疗策略具有相同疗效的情况下,也可以支持使用联合B细胞靶向治疗。
Synbiose 2研究设计的一个重要特征是在利妥昔单抗之前开始使用贝利单抗。由于几个原因,从免疫学的角度来看,每种药物的起始顺序非常相关。首先,利妥昔单抗有效且几乎完全消耗循环中的B细胞。然而,大量的耐药B细胞存在于淋巴组织,如骨髓、淋巴结和炎症组织中[40,41,42]。因此,我们在Synbiose 1研究中观察到,在该研究中引入了贝利单抗后利妥昔单抗-未成熟B细胞的再生被贝利单抗阻止,早期再生主要由记忆B细胞和浆细胞主导,这些细胞可能对利妥昔单抗的消耗具有抗性。其次,在贝利单抗附加治疗后的头几周,几项研究描述了循环记忆B细胞显著但意想不到的激增[43,44,45,46]。最近的一项研究证实了这一现象,并确定belimumab会破坏记忆B细胞的运输[47]。这些观察结果为Synbiose 2研究设计奠定了基础,该研究旨在受益于贝利单抗在循环中的记忆B细胞激增,然后利妥昔单抗易使其消耗。
在研究设计中,纳入了霉酚酸酯的TDM,以确保两组的最佳免疫抑制方案。充分的TDM不仅对治疗方案的免疫结果参数的公平比较很重要,而且考虑到本研究中交叉的可能性。在对照组中,如果治疗反应不足或在充分免疫抑制的情况下出现严重的急性发作,则过渡到贝利单抗和利妥昔单抗治疗,这是通过使用TDM来确保的。重要的是要强调,交叉治疗的选择允许包括复发患者,否则他们的治疗选择可能有限。值得注意的是,交叉的患者将提供额外的信息,通过在事后分析中作为自己的对照,允许个体内部比较。为了避免干预组免疫系统的累积过度抑制,霉酚酸盐剂量将迅速逐渐减少,并在维持期开始时停止,尽管可以假设在b细胞消耗更深的情况下,其对b细胞的细胞毒性作用已经减弱。
总之,Synbiose 2研究建立在先前的2期研究基础上,证实了联合B细胞靶向治疗SLE的安全性和临床获益的初步证据[32,34,35]。Synbiose 2研究侧重于严重SLE和LN患者,这是对3期随机BLISS-BELIEVE研究(NCT03312907)的补充,该研究研究了非肾性SLE的类似治疗方案。这项研究的结果将为严重SLE的新治疗策略提供进一步的证据,并可能挑战目前贝利姆单抗标签上的限制,即警告不要与另一种b细胞消耗剂联合使用[48]。
试验状态
试验于2018年11月开始招募,估计于2025年9月完成。当前协议版本为10(2022年4月4日)。
数据和材料的可用性
该试验的结果将提交在同行评审的开放获取期刊上发表。写作委员会将由本手稿的作者和参与试验的医疗中心的所有主要研究者组成。试验结果数据将在主要研究结果公布后应合理要求提供。同意书范本已作为稿件的补充提供。其他文件(如研究方案)可能是可用的。
缩写
- Anti-dsDNA:
-
Anti-double-stranded DNA
- 高飞球的一击:
-
B细胞活化因子
- LN:
-
狼疮肾炎
- NET:
-
中性粒细胞胞外陷阱
- 职业:
-
医生整体评估
- 系统性红斑狼疮:
-
系统性红斑狼疮
- 咽部菌:
-
系统性红斑狼疮疾病活动指数
- SLICC:
-
系统性狼疮国际合作诊所
- TDM:
-
治疗药物监测
参考文献
刘建军,刘建军,刘建军,等。系统性红斑狼疮患者临床缓解期的研究进展。中华风湿病杂志,2014,41(9):1808-16。
罗维茨M, Feletar M, Bruce IN, Ibanez D, Gladman DD.系统性红斑狼疮的长期缓解。中华风湿病杂志,2005;32(8):1467-72。
戈尔德V,曾ASMWP。SLE的治疗目标:缓解和低疾病活动状态。风湿病学(牛津大学)。2020; 59 (Suppl5): v19-28。
Zen M, Iaccarino L, Gatto M, Bettio S, Nalotto L, Ghirardello A,等。白种人SLE患者的长期缓解:患病率和结果。中国生物医学工程学报,2015,35(6):557 - 557。
Mahajan A, Amelio J, Gairy K, Kaur G, Levy RA, Roth D,等。系统性红斑狼疮、狼疮肾炎和终末期肾病:一项绘制疾病严重程度和进展的实用综述。狼疮。2020;29(9):1011 - 20。
陈伟,杨建军,陈伟。系统性红斑狼疮患者的总体死亡率和病因特异性死亡率:一项观察性研究的荟萃分析。关节炎护理中心(霍博肯)。2014年,66(4):608 - 16。
Tselios K, Gladman DD, Sheane BJ, Su J, Urowitz M.加拿大安大略省系统性红斑狼疮患者全因、病因特异性和年龄特异性标准化死亡率(1971-2013)。中国生物医学工程学报,2019;33(6):591 - 591。
Albert D, Dunham J, Khan S, stanberry J, Kolasinski S, Tsai D,等。系统性红斑狼疮患者抗cd20b细胞耗竭的生物学反应变异性。中国生物医学工程学报,2008,35(6):559 - 561。
Lu TYT, Ng KP, Cambridge G, Leandro MJ, Edwards JCW, Ehrenstein M,等。回顾性分析在伦敦大学学院医院使用B细胞消耗疗法治疗系统性红斑狼疮的7年:前50例患者。Arthrit Rheum-Arthr。2009年,61(4):482 - 7。
胡珀R, Griffith M, Kirwan C, Levy J, Taube D, Pusey C,等。利妥昔单抗是一种有效的治疗狼疮肾炎,并允许减少维持类固醇。肾移植杂志,2009;24(12):3717-23。
a . Terrier B, Amoura Z, Ravaud P, Hachulla E, Jouenne R, Combe B,等。利妥昔单抗治疗系统性红斑狼疮的安全性和有效性:来自法国自身免疫和利妥昔单抗登记的136例患者的结果中华风湿病杂志,2010;62(8):2458-66。
Vital EM, Dass S, Buch MH, Henshaw K, Pease CT, Martin MF等。系统性红斑狼疮患者利妥昔单抗反应的B细胞生物标志物。中华风湿病杂志,2011;63(10):3038-47。
Condon MB, Ashby D, Pepper RJ, Cook HT, Levy JB, Griffith M,等。前瞻性观察单中心队列研究,评估利妥昔单抗和霉酚酸酯治疗狼疮性肾炎的有效性,但不口服类固醇。中国生物医学工程学报,2013,32(8):1280 - 1260。
Witt M, Grunke M, prof F, Baeuerle M, Aringer M, Burmester G等。利妥昔单抗治疗系统性红斑狼疮(SLE)患者的临床结局和安全性——来自德国全国队列研究(GRAID)的结果狼疮。2013;22(11):1142 - 9。
Iaccarino L, Bartoloni E, Carli L, Ceccarelli F, Conti F, De Vita S,等。适应症外使用利妥昔单抗治疗难治性狼疮的疗效和安全性:来自意大利多中心注册中心的数据中国临床风湿病杂志,2015;33(4):449-56。
李春华,李春华,李春华,等。利妥昔单抗治疗系统性红斑狼疮的临床观察。关节炎护理中心(霍博肯)。2017, 69(2): 257 - 62。
McCarthy EM, Sutton E, Nesbit S, White J, Parker B, Jayne D,等。利妥昔单抗治疗难治性系统性红斑狼疮的短期疗效和安全性:来自不列颠群岛狼疮评估小组生物制剂注册的结果。风湿病学(牛津大学)。57 2018;(3): 470 - 9。
Merrill JT, neuwell CM, Wallace DJ, Shanahan JC, latinins KM, Oates JC等。利妥昔单抗治疗中重度活动性系统性红斑狼疮的疗效和安全性:随机、双盲、利妥昔单抗II/III期系统性红斑狼疮试验评价中华风湿病杂志,2010;32(1):222-33。
Rovin BH, Furie R, Latinis K, Looney RJ, Fervenza FC, Sanchez-Guerrero J,等。利妥昔单抗治疗活动性增殖性狼疮性肾炎的疗效和安全性:用利妥昔单抗评估狼疮性肾炎的研究。中华风湿病杂志,2012;64(4):1215 - 1226。
Gomez Mendez LM, Cascino MD, Garg J, Katsumoto TR, Brakeman P, Dall'Era M,等。利妥昔单抗治疗狼疮性肾炎后外周血B细胞耗竭及完全缓解。中华临床医学杂志,2018;13(10):1502-9。
Furie RA, Aroca G, Cascino MD, Garg JP, Rovin BH, Alvarez A等。b细胞消耗与obinutuzumab治疗增生性狼疮性肾炎:一项随机,双盲,安慰剂对照试验中国生物医学工程学报,2013;31(1):391 - 391。
张建军,张建军,张建军,等。风湿性关节炎患者血清B淋巴细胞刺激因子水平升高的研究进展。中华风湿病杂志,2001;44(6):1313 - 139。
张杰,Roschke V, Baker KP,王忠,Alarcon GS, Fessler BJ,等。前沿:B淋巴细胞刺激剂在系统性红斑狼疮中的作用。中华免疫学杂志,2001;16(1):1 - 6。
李建军,李建军,李建军,等。系统性红斑狼疮患者血浆B淋巴细胞刺激物水平与疾病活动性的关系。中华风湿病杂志,2008;58(8):2453-9。
Roth DA, Thompson A, Tang Y, Hammer AE, Molta CT, Gordon D.系统性红斑狼疮患者BLyS水平升高:相关因素和对贝利单抗的反应。狼疮。2016;25(4):346 - 54。
滕永康,何志刚,何志刚,何志刚,何志刚,何志刚,何志刚,何志刚,何志刚等。难治性类风湿关节炎患者诱导长期b细胞耗损优先影响自身反应性免疫而非保护性体液免疫。中国生物医学工程杂志,2012,31(2):557。
Kraaij T, Kamerling SWA, de Rooij ENM, van Daele PLA, Bredewold OW, Bakker JA,等。利妥昔单抗联合贝利单抗治疗严重系统性红斑狼疮的净效应。[J] .中国医学杂志,2018;31(1):45 - 54。
系统性红斑狼疮患者B细胞耗竭治疗后血清BAFF水平升高与抗双链DNA抗体水平升高和疾病爆发相关。中华风湿病杂志,2013,35(10):672 - 679。
Navarra SV, Guzman RM, Gallacher AE, Hall S, Levy RA, Jimenez RE,等。贝利单抗在活动性系统性红斑狼疮患者中的疗效和安全性:一项随机、安慰剂对照的3期试验柳叶刀》。2011;377(9767):721 - 31所示。
Furie R, Petri M, Zamani O, Cervera R, Wallace DJ, Tegzova D,等。belimumab是一种抑制B淋巴细胞刺激剂的单克隆抗体,用于系统性红斑狼疮患者的III期随机、安慰剂对照研究。中华风湿病杂志,2011;63(12):3918-30。
fuie R, Rovin BH, Houssiau F, Malvar A, Teng YKO, Contreras G,等。belimumab治疗狼疮性肾炎为期两年的随机对照试验。中华医学杂志,2020;31(12):1217 - 1228。
克拉杰,李建军,李建军,等。b细胞免疫调节联合利妥昔单抗和贝利单抗治疗严重难治性系统性红斑狼疮的长期疗效:2年结果肾移植杂志;2011;36(8):1474-83。
van Dam LS, Osmani Z, Kamerling SWA, Kraaij T, Bakker JA, Scherer HU,等。利妥昔单抗、利妥昔单抗联合贝利单抗或硼替佐米对SLE体液自身免疫反应影响的反向翻译研究风湿病学(牛津大学)。2020; 59(10): 2734 - 45。
alatisha - fregoso Y, Malkiel S, Harris KM, Byron M, Ding L, Kanaparthi S,等。利妥昔单抗联合环磷酰胺联合贝利单抗治疗狼疮性肾炎的II期随机试验。中国生物医学工程学报,2013;31(1):391 - 391。
Shipa M, empleton - thirsk A, Parvaz M, Santos LR, Muller P, Chowdhury K,等。利妥昔单抗治疗系统性红斑狼疮后贝利单抗的有效性:一项随机对照试验。中华医学杂志,2011;17(3):344 - 344。
刘国强,刘国强,刘国强,刘国强,等。狼疮低疾病活动状态(LLDAS)的定义和初步验证。中国生物医学工程学报,2016,35(9):559 - 561。
Aaronson NK, Muller M, Cohen PD, Essink-Bot ML, Fekkes M, Sanderman R,等。荷兰语版SF-36健康调查在社区和慢性病人群中的翻译、验证和规范中华流行病学杂志。1998;51(11):1055 - 1068。
Appel GB, Contreras G, Dooley MA, Ginzler EM, Isenberg D, Jayne D,等。霉酚酸酯与环磷酰胺诱导治疗狼疮性肾炎。中国生物医学工程学报,2009;20(5):1103 - 1120。
Chan AW, Tetzlaff JM, Gotzsche PC, Altman DG, Mann H, Berlin JA,等。SPIRIT 2013解释与阐述:临床试验方案指南。BMJ。2013; 346: e7586。
Pijpe J, Meijer JM, Bootsma H, van der Wal JE, Spijkervet FK, Kallenberg CG,等。唾液腺恢复的临床和组织学证据支持利妥昔单抗治疗干燥综合征的疗效。中华风湿病杂志,2009;60(11):3251-6。
刘建军,刘建军,刘建军,等。抗cd20治疗对类风湿关节炎患者骨髓B细胞发生的影响。中国生物医学工程杂志,2009;11(4):391 - 391。
Teng YK, Levarht EW, Hashemi M, Bajema IM, Toes RE, Huizinga TW,等。免疫组织化学分析作为预测对利妥昔单抗治疗反应性的手段。中华风湿病杂志,2007;56(12):391 - 398。
Wallace DJ, Stohl W, Furie RA, Lisse JR, McKay JD, Merrill JT,等。belimumab在活动性系统性红斑狼疮患者中的II期、随机、双盲、安慰剂对照、剂量范围研究。中华风湿病杂志,2009;61(9):1168 - 778。
Stohl W, Hiepe F, latininm, Thomas M, Scheinberg MA, Clarke A,等。贝利单抗降低自身抗体,使低补体水平正常化,并减少系统性红斑狼疮患者的选择B细胞群。中华风湿病杂志,2012;64(7):2328 - 2337。
李建军,李建军,李建军,等。贝利单抗治疗难治性系统性红斑狼疮患者BLyS水平变化与B和T细胞区室组成的关系前沿医药,2019;10:433。
田中阳,Bass D, Chu M, Egginton S, Ji B, Struemper H,等。静脉注射贝利单抗治疗日本系统性红斑狼疮患者的疗效和安全性:一项3期随机安慰剂对照试验的亚组分析现代风湿病杂志,2019;29(3):452-60。
endds EJ, Zlei M, Tipton CM, Osmani Z, Kamerling S, Rabelink T,等。贝利单抗附加疗法动员记忆B细胞进入Sle患者的循环。中国生物医学工程学报(英文版);2011;38(5):585。
Benlysta (belimumab)产品特性总结。都柏林,葛兰素史克制造有限公司2016。
致谢
不适用。
资金
YKOT的工作由荷兰科学组织(90713460)和荷兰肾脏基金会(KJPB12.028 & 17OKG04)资助。葛兰素史克(GlaxoSmithKline)为本文中描述的临床研究免费提供belimumab和额外资金。资助者不会参与本研究的数据收集、分析和解释,也不会参与论文的撰写。
作者信息
作者及单位
贡献
EJA, TJR和YKOT发起并设计了这项研究。EJA和YKOT制定了研究方案。YKOT是首席调查员和赞助商。MS, EJA, DS, EO, KL, ML, PP, TWJH, REMT, CK, TJR和YKOT参与了稿件的准备和后续的修改,并对发表的版本提供了最终的批准。所有作者同意对工作的各个方面负责,并确保与工作的任何部分的准确性或完整性相关的问题得到适当的调查和解决。所有作者都认可了手稿的最终版本。
相应的作者
道德声明
伦理批准并同意参与
该试验已获得莱顿-海牙-代尔夫特当地医学伦理委员会批准(方案标识NL65720.058.18,参考编号P18.087),并于2018年11月在clinicaltrials.gov上注册(NCT03747159)。所有参与者在参与前提供书面知情同意书。可应要求提供同意书范本。将向伦理委员会提出实质性修订,并与所有相关方沟通。
发表同意书
不适用。
相互竞争的利益
YKOT已获得葛兰素史克公司的研究支持和咨询费。
额外的信息
出版商的注意
伟德体育在线施普林格·自然对已出版的地图和机构关系中的管辖权要求保持中立。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,该协议允许以任何媒介或格式使用、共享、改编、分发和复制,只要您适当地注明原作者和来源,提供知识共享许可协议的链接,并注明是否进行了更改。本文中的图像或其他第三方材料包含在文章的知识共享许可协议中,除非在材料的署名中另有说明。如果材料未包含在文章的知识共享许可中,并且您的预期用途不被法律法规允许或超过允许的用途,您将需要直接获得版权所有者的许可。如欲查阅本许可证副本,请浏览http://creativecommons.org/licenses/by/4.0/。创作共用公共领域免责声明(http://creativecommons.org/publicdomain/zero/1.0/)适用于本文中提供的数据,除非在数据的信用额度中另有说明。
关于本文
引用本文
van Schaik, M., Arends, e.j., Soonawala, D.。et al。贝利单抗联合利妥昔单抗治疗严重系统性红斑狼疮的疗效:多中心、随机、开放标签Synbiose 2试验的3期研究方案试用23, 939(2022)。https://doi.org/10.1186/s13063-022-06874-w
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/s13063-022-06874-w
关键字
- 全身性自身免疫性疾病
- 系统性红斑狼疮
- 狼疮肾炎
- Belimumab
- 利妥昔单抗
- 临床试验