患者特点
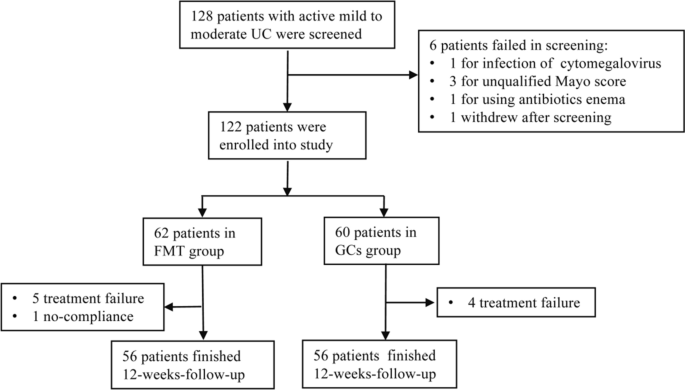
2015年9月至2021年9月,在上海总医院招募了128例轻度至中度UC患者(Mayo评分4-10分),其中6例患者因以下原因被排除:1例为巨细胞病毒感染;Mayo评分不合格3分;1 .为使用抗生素灌肠;1人筛查后退出。
总的来说,122例患者被考虑参加试验,FMT组62例,GCs组60例(图2)。2).两组患者在性别、年龄、病程、疾病程度、疾病严重程度(包括Mayo总评分和内镜Mayo评分)和临床炎症参数方面的基线差异无统计学意义(表2)1).
FMT在诱导UC缓解方面与糖皮质激素一样有效
6例患者在研究治疗期间退出FMT组(图。2).FMT组3例中度UC男性患者持续不适,退出接受静脉类固醇治疗。FMT组1例男性患者因肛周脓肿在第6周接受抗生素治疗。FMT组1例女性患者于第3周恶化,大量粪血,需住院静脉注射类固醇和抗肿瘤坏死因子治疗。FMT组1例男性患者随访时因不遵医嘱使用抗生素而退出。
4例患者退出GCs研究治疗(图。2).1例中度女性患者在GCs治疗期间病情恶化,拒绝接受生物治疗并行结肠切除术。1例男性患者在GCs后因临床恶化和巨细胞病毒感染而退出,并接受了结肠切除术。GCs组1例男性患者持续不适,1例男性患者在类固醇减量期间病情恶化,随后转入抗肿瘤坏死因子治疗。
FMT组34例(54.8%)和GCs组29例(48.3%)达到主要结局,在诱导UC临床和内镜缓解方面无显著差异(RR 1.13, 95% CI 0.8-1.6;p= 0.59)2).在UC疾病早期(≤1年)和慢性(> 1年),FMT治疗后达到主要结局的患者比例相似(19/ 33,55.9%)vs。15/28, 53.6%,p= 0.53)。
FMT组40人(64.5%)和GCs组34人(56.7%)临床缓解(RR 1.14, 95% CI 0.85-1.52;p= 0.46)。FMT组43人(69.4%)和GCs组39人(65.0%)有临床反应(RR 1.14, 95% CI 0.83-1.37;p= 0.7)。两者内镜缓解率(19/62,30.6%)vs。17/60, 28.3%) (rr 1.08, 95% ci 0.62-1.87;p= 0.84),内镜反应率(38/ 62,61.3%)vs。35/60, 58.3%) (rr 1.05, 95% ci 0.79-1.40;p= 0.85), FMT组略高于GCs组,但差异无统计学意义(表2 - 4)2).
作为一个开放的前瞻性队列,FMT或GCs的管理是基于临床实践和患者的自由裁量,而不是随机化,这可能会在我们的分析中引入偏倚。虽然两组的基线特征无显著性差异(表1),进行亚组分析(表3.),以避免潜在的选择偏差。在按年龄、性别、疾病程度和病程进行的亚组分析中,FMT组和GCs组患者达到主要预后的比例无显著差异。
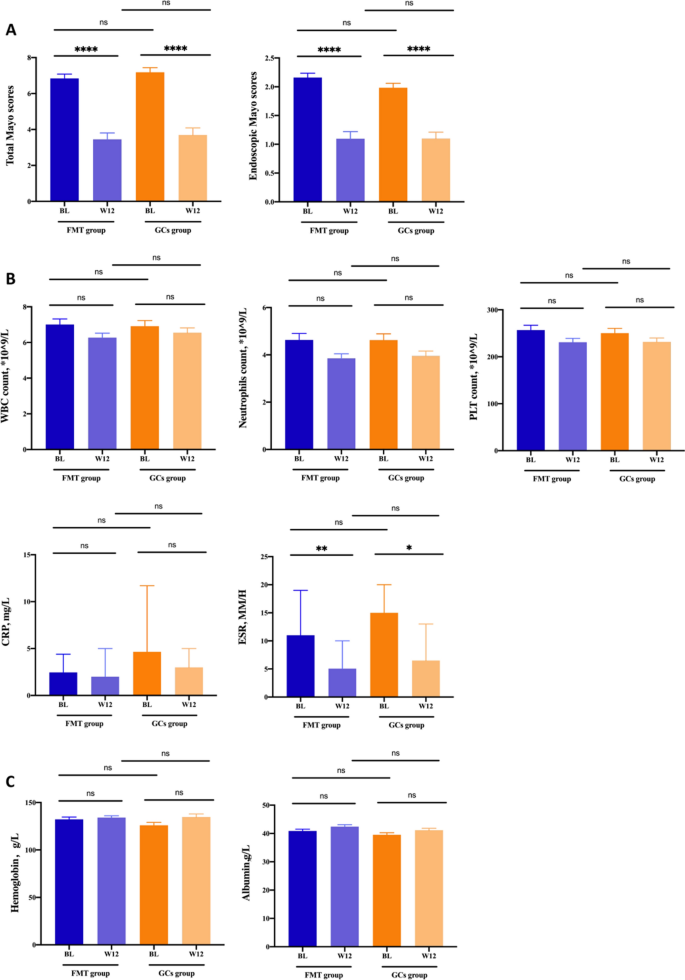
干预后,FMT组和GCs组的Mayo总分均显著下降(p分别< 0.001),而在第12周时,两组之间无显著差异(图。3.A)。就Mayo内镜评分而言,两组患者在第12周时评分也较基线时显著降低(p分别< 0.001)。两组患者12周Mayo内镜评分比较,差异无统计学意义。
FMT和FMT组ESR水平均显著降低。p= 0.008)和GCs组(p= 0.023),而其他炎症参数(包括WBC计数、中性粒细胞计数、PLT计数和CRP水平)的降低无显著性差异(图。3.B).第12周时,两组血清白蛋白和血红蛋白水平均有升高,但无明显差异(图。3.C)。
FMT组不良事件较少
在FMT组,14例患者(22.6%)报告了至少一次不良事件,主要是轻度和自限性的胃肠不适和发热。在GCs组,36例(60.0%)患者报告了至少一种不良事件,如结肠切除术、白细胞减少、肝功能异常、电解质紊乱、巨细胞病毒感染、高血压、高血糖、胃肠不适和失眠。GCs组的不良事件明显高于FMT组(p< 0.001)(表4).GCs治疗期间观察到2例严重不良事件。1例中度女性患者在GCs治疗期间病情恶化,拒绝接受生物治疗并行结肠切除术。1例男性患者表现为结肠炎恶化,随后诊断为巨细胞病毒感染并行结肠切除术。
生活质量评估显示FMT组和GCs组均有改善
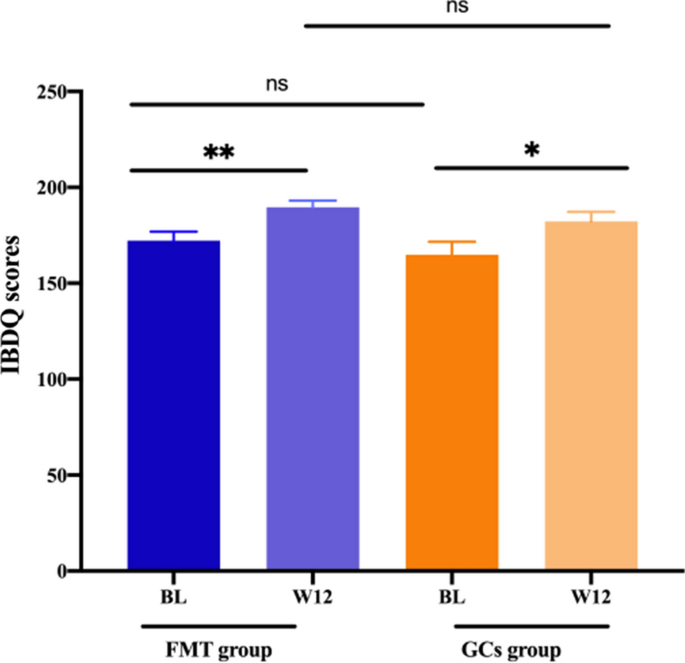
参与者被要求填写IBDQ,每组56名患者在基线和第12周完成了IBDQ。干预后,FMT组和GCs组的IBDQ评分均显著增加。4).干预后GCs组评分虽略低于FMT组,但差异无统计学意义。
FMT组TNF-α、IL-6水平降低与缓解相关
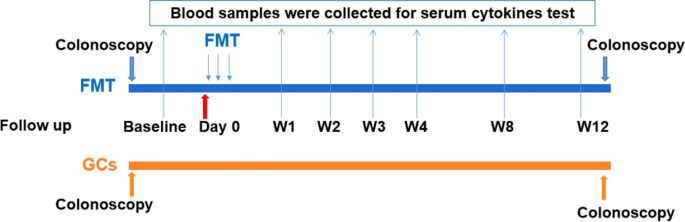
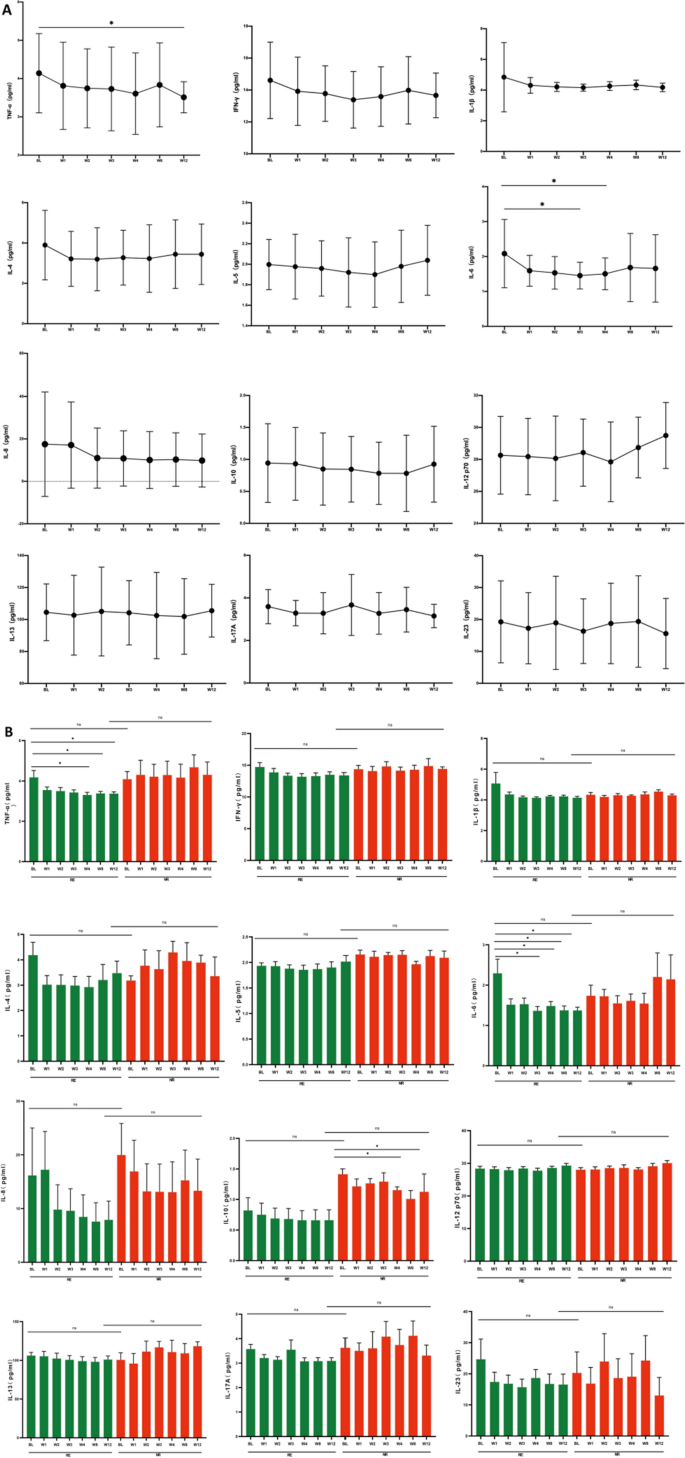
测定FMT组血清TNF-α、IFN-γ、IL-1β、IL-4、IL-5、IL-6、IL-8、IL-10、IL-12p70、IL-13、IL-17A、IL-23等细胞因子在基线及FMT干预后1、2、3、4、8、12周的水平。
FMT治疗后TNF-α、IFN-γ、IL-1β、IL-6、IL-8水平均有明显下降趋势(图;5A).第12周TNF-α水平较基线显著降低,第3周和第4周IL-6水平分别较基线显著降低(p< 0.05)。
根据第12周的主要结果,FMT组62例患者分为RE组(n = 34, 54.8%)和NR组(n = 28, 45.2%)。进一步分析RE组和NR组在FMT干预前后的血清细胞因子(图2)。5B)。
对于所有细胞因子,RE组和NR组在基线时没有发现显著差异。虽然RE组大部分细胞因子呈下降趋势,但FMT治疗后只有TNF-α和IL-6明显下降(p< 0.05)。与基线相比,第4、8、12周TNF-α水平显著降低,第3、4、8、12周IL-6水平显著降低(p< 0.05)。而NR组TNF-α、IL-6无明显变化。另一方面,NR组IL-10下降趋势比RE组更明显,NR组在第4周和第12周出现明显下降(p< 0.05)。
尽管RE组和NR组在FMT干预后第12周的细胞因子均无显著差异,但TNF-α和IL-6的降低被认为与FMT后UC的缓解有关,而IL-10的降低与无缓解有关。