NGS测序和患者研究队列特征
为了优化评估与RT毒性相关的正常组织功能,我们建立了一个包括体细胞肿瘤和配对正常组织的下一代测序(NGS)数据库[33 ,34 ].对所有样本使用相同的测序平台进行NGS,以最大限度地提高发现与RT毒性有关的种系变异的一致性数据输出。我们的数据集包括37例具有NGS数据的HNSCC患者(n = 37);其中34例为以治疗为目的的HNSCC患者,并分析了临床结果。它们的特点总结在表中1 .排除的患者包括1例诊断时转移性疾病和2例局部局部进展性皮肤鳞状细胞癌。由于无法评估某些结果(如无转移生存期)的时间,转移性疾病被排除在外。由于治疗模式、病程和预后的差异,皮肤SCC患者被排除在外。虽然这些患者没有对临床结果进行评估,但他们被保留用于NGS分析,以评估与不同辐射AEs相关的潜在生物标志物。
RT患者种系变异与晚期毒性增加相关
此前有报道称,HNSCC在急性和晚期毒性中存在不同的组织反应,其中急性毒性与炎症有关,而坏死发展可能导致晚期毒性结果[35 ].为了分离早期和晚期反应的遗传因素,根据其毒性特征将患者队列分为两组(A组和B组)。具体而言,对于这一分组,A组患者的晚期毒性显著增加,而B组患者的晚期毒性没有发生变化。根据这些标准将18例患者指定为A组,19例患者指定为B组。
我们测试了种系变异与RT毒性结果的相关性,限制在至少25% MAF中存在且A组和B组之间显著p值≤0.05的种系变异。在A组和B组的前30个种系变异中,我们确定了5个符合我们的选择标准:人白细胞抗原(HLA-A)、结节性硬化症复合体2 (TSC2)、增殖标志物Ki-67 (MKI67)、干扰素诱导的四肽重复序列蛋白2 (IFIT2)和白细胞介素10受体亚基α (IL10RA)。
HLA-A Arg68Lys/Val91Met种系变异
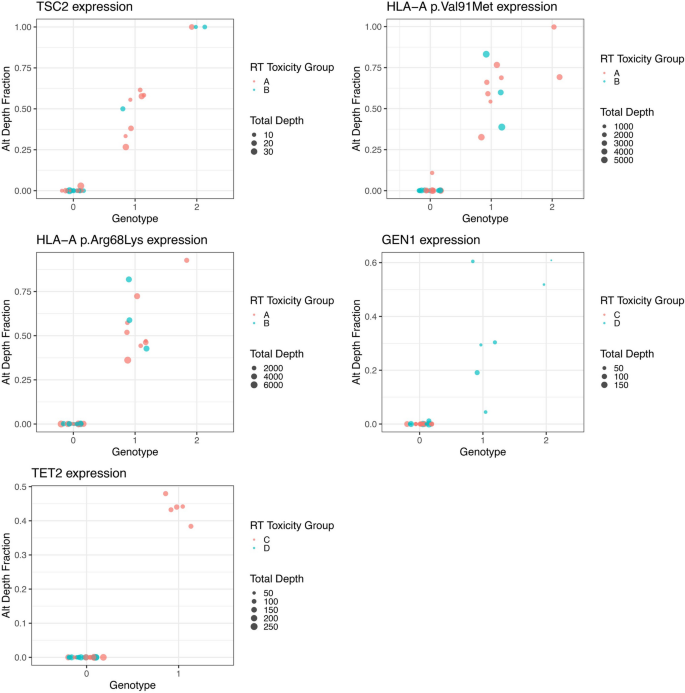
我们发现13例患者携带HLA-A Arg68Lys/Val91Met变体,占队列的37.1%,其中A组10例,B组3例(p值= 0.052,表2)2 ).
表2卡方结果:复发的freebayes突变扩展到肿瘤抑制基因和癌基因之外
所有携带HLA-A Val91Met变异(rs79361534)的患者同时携带HLA-A Arg68Lys变异(rs707910)。这种特殊的变体被记录在HLA-A多态数据库中,在1000个种群中具有低MAF [36 ].我们发现了这种HLA-A变体的新特征,这些特征以前没有报道过。这种特殊的变体共龋两个分离的单核苷酸变化,导致蛋白质位置68和91的两个氨基酸取代。由于这两种变化是分开发生的,并导致两个HLA-A多态性基因(rs79361534和rs707910),因此以前没有报道过。为了检查这些变化对编码蛋白的结构和功能的影响,我们进行了3D建模分析(图2)。1 ).我们发现第91位被蛋氨酸取代的缬氨酸位于由两个α-螺旋组成的蛋白肽结合槽中,因此有理由推测这种氨基酸取代可能是修饰肽结合亲和力导致新抗原呈递的一个因素。68号位置的精氨酸与赖氨酸的取代可能会引入一个新的泛素结合位点,此外,利用SIFT算法预测该变异是有害的[37 ].该HLA变体与PFS (p = 0.402)、LRR (p = 0.173)、MFS (p = 0.769)和OS (p = 0.757)的差异无显著相关性3. ).该变异的效应值较高(6.67),表明晚期RT毒性的几率较高,并可能作为RT分层的生物标志物。
表3这些变异体患者与非变异体患者PFS、LRR、MFS和OS的p值
TSC2剪接变体
我们的数据分析发现了插入子C>T TSC2变体(rs1800720)位于剪接供体位点两侧,在我们的n37队列中有10例患者(28.6%)出现,在a组有显著富集的趋势。a组有8例患者检测到该变体,B组有2例(p = 0.0577,表2 ).与gnomAD数据(MAF = 0.0968)相比,我们的队列中TSC2变体(MAF = 0.189)特别丰富[30. ].有趣的是,我们队列中的MAF与非洲/非裔美国地精人群密切一致(MAF = 0.202)。
这种特异性TSC2剪接区域被确定为结节性硬化症相关的种系变异。TSC2与TSC1复合物通过调节雷帕霉素激酶(mTOR)信号通路的机制靶点发挥抑癌作用[38 ].mTOR通路的异常激活在鼻鳞癌中广泛存在[39 ],这种TSC2变体可能通过对mTOR通路的影响与HNSCC相关。该变异的KM分析与较低的LRR风险相关(p = 0.018),但与PFS (p = 0.216)、MFS (p = 0.702)和OS (p = 0.685)无相关性3. ).据我们所知,这是首次在HNSCC中发现这种种系变异。
HNSCC中的其他低频种系变异
我们检测到9种与早期和晚期毒性相关的生殖系变异,由于发生频率低于25%,不符合我们的生物标志物选择标准(表2)2 ).范可尼贫血互补组D2 (FANCD2 ) pPro714Leu (rs3864017);动力蛋白细胞质2重链1 (DYNC2H1 ) pGly304Leu (rs12146610;rs72989734);蛋白质磷酸酶1调节亚基15A (PPP1R15A ) pAla32Thr (rs3786734);SLX4结构特异性核酸内切酶亚基(SLX4 ) pSer71Asn, pAsn457Lys, pArg204Cys (rs77985244, rs74319927, rs97842542);主要组织相容性复合体,II类,DQ alpha 2 (HLA-DQA2 )拼接站点(rs4398729);主要组织相容性复合体,II类,DM β (HLA-DMB ) pSer71Asn, pAsp49Val, pThr28Ala (rs17617321, rs17617333, rs17583782);主要组织相容性复合体,II类,DM α (HLA-DMA ) pArg210His, pGly181Ala (rs41555121, rs6926628);范可尼贫血互补A组(FANCA ) pVal6Asp, (rs1800282);而黑素皮质素1受体(受体 ) pArg160Trp (rs1805008)。这些基因的已知功能分为两个主要功能家族,8个中的3个是与范可尼贫血相关的DNA修复基因:FANCD2, SLX4和FANCA [40 ,41 ,42 ,43 ,44 ,45 ],而8个基因中有3个是HLA基因,包括涉及免疫的主要组织相容性复合体(MHC)。其余基因与骨骼新生有关[46 ,47 ,48 ],蛋白质合成稳态[49 ]和皮肤色素沉着[50 ].所有这些种系变异之前都在一般人群中报道过,验证了我们的发现,但它们在各自编码蛋白中的结构功能关系尚待鉴定。我们在这里报道,这些基因变异发生在HNSCC患者中,并可能与晚期毒性有关。根据我们的研究设计,我们发现FANCD2、DYNC2H1、PPP1R15A和HLA-A变体与晚期毒性显著增加相关,而SLX4、HLA-DQA2、HLA-DMB、HLA-DMA、FANCA和MC1R变体与晚期RT毒性事件相关。
累积RT毒性变异
除了早期和晚期毒性基因变异效应外,我们还分析了同一队列患者中C组(2-4级)和D组(0-1级)的累积毒性关联(n = 37,表4 ).
表4卡方结果:复发的freebayes突变超出抑癌基因和癌基因范围
毫不奇怪,在我们之前的研究设计中检测到的TSC2剪接位点变体(rs1800720)显示出显著的累积毒性关联。此外,我们检测到一个新的变体GEN1,一个Holliday连接5 '皮瓣内切酶(GEN1) pLys839Glufs (rs149936944),与RT治疗诱导的毒性有显著的保护作用。我们发现9例患者携带该变异,其中2例为双等位基因(图2)。2 ).我们通过分析RNA-seq数据证实了这一发现。参考GEN1蛋白长度为908个氨基酸。我们检测到的变异具有帧移突变,在第839位引入了一个终止密码子,导致GEN1蛋白c端缺失69个氨基酸的截断信使RNA (mRNA),有可能发生无意义介导的RNA衰变。纯合子性的存在(图。2 )意味着GEN1冗余,然而,这种变化可能导致另一种生物学功能。事实上,Wang等人已经报道了GEN1冗余[51 ].他们发现GEN1和必要的减数分裂结构特异性内切酶1 (EME1)在小鼠模型中的减数分裂重组中发挥冗余作用,并且这两个基因的缺失在小鼠中具有合成致死率[51 ].此外,GEN1基因敲除小鼠是可行的[52 ,53 ].
我们发现核受体辅阻遏因子2 (NCOR2) Gln510dup变体(rs35831183)与D组有很强的相关性(p = 0.008151)。
与所选种系变异相关的临床结果
我们还检查了两组之间的临床结果和某些变异的影响。在这部分分析中,仅包括接受确定性或术后放疗/化疗的HNSCC患者。共有34名患者接受了放射治疗,时间从2009年1月到2021年1月。有14例患者(41.2%)在术后进行了治疗。31例(91.2%)患者可用辐射剂量,范围60-70 Gy (Gy)。27例患者(79.4%)同时接受全身治疗,最常见的是顺铂(70.4%)。治疗时的中位年龄为62.5岁(范围37-85岁,表1 ),中位随访时间为42.5个月(范围7-205)。在A组与B组和C组与D组之间,在年龄、分期、原发部位、HPV状态、使用手术或同时化疗方面没有显著差异。患者特征见表1 .11.7%的患者存在3级早期粘膜炎或吞咽困难,29.4%的患者存在3级吞咽困难;无4级或5级不良事件记录。
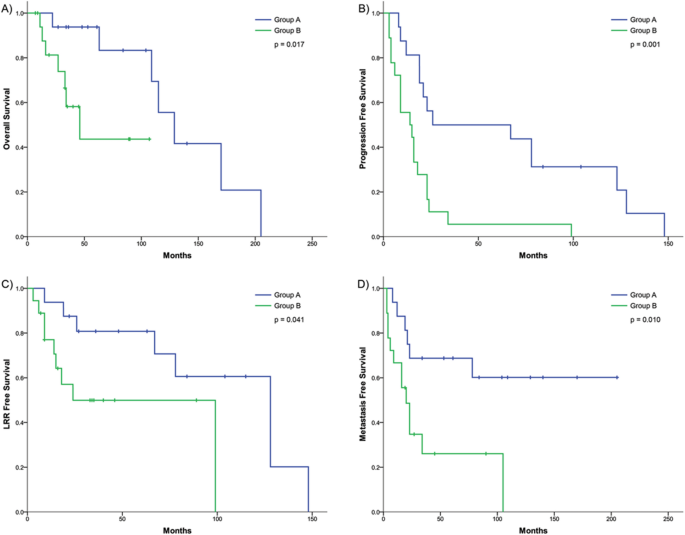
A组患者的OS明显优于B组(p = 0.017)。3. ).PFS (p = 0.001)、LFS (p = 0.041)、MFS(0.010)也有显著差异。如前所述,晚期毒性升高的A组TSC2改变更为普遍,TSC2变异患者的LFS也有显著改善(p = 0.018,表3. ).FANCD2在A组中也更普遍,与PFS (p = 0.039)和MFS (p = 0.018)的改善相关,PPP1R15A与PFS (p = 0.008)和LFS(0.028)相关。仅在B组患者中存在5种HLA-DMB/HLA-DMA变异,与较高的LRR风险相关(p = 0.041)。在C组和D组中,HLA-F N353L主要变体在D组中明显更普遍,并与更频繁的远处转移相关(p = 0.046)。