家庭及临床检查
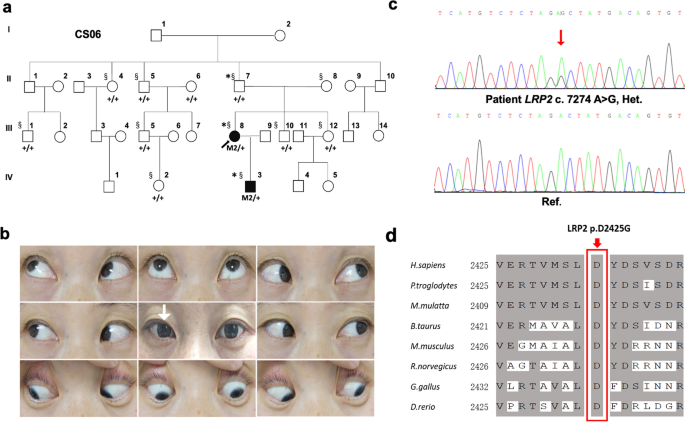
来自14个不相关家庭的47名非综合征性cs患者和18名cs未受影响的兄弟姐妹(1名内斜视,13名外斜视;无花果。1一个和3.a、附加文件2a-l),包括一个庞大的四代家庭(CS08),在南京医科大学附属第一医院进行临床随访。根据《赫尔辛基宣言》原则,本研究经南京医科大学附属第一医院伦理委员会(2019-SR-134)批准,并获得参与者和每个孩子父母的书面知情同意,用于样本收集和遗传分析。
在接受任何治疗之前,对可用的参与者进行常规眼部检查,包括视力、裂隙灯生物显微镜检查和眼底检查评估。在距离(5米)和近(0.3米)处进行偏移角,采用盖/盖试验、交替棱镜和盖试验或Krimsky试验(在年轻或不合作的患者中)。使用自动折光计测量屈光不正。对CS08家族先证者进行眼、脑磁共振成像(MRI)检查。使用来自CS08和CS06家族的两个先验者的尿液和血液样本研究肾功能。斜视治疗史的数据,包括既往手术或贴片,均在检查前从参与者本人或通过电话交谈获得。
斜视的定义是在远处或近处出现任何斜视,戴眼镜或不戴眼镜,并根据斜视的主要方向(内斜视、外斜视、垂直斜视)进行分类。斜视可根据凝视不同方向上的偏差程度变化,分为CS(共视性斜视)和不共视性斜视(各种斜视)。如果近距离注视和远距离注视都是恒定的,斜视被认为是恒定的斜视;否则,被认为是间歇性斜视。为尽量减少环境和证候因素的影响,排除符合以下标准的病例[13]:(i)继发性斜视;(ii)任何不同时性斜视;(iii)已知CS危险因素,如早产(< 35周龄)、低出生体重(< 1.8 kg);(iv)剥夺或重症肌无力引起的斜视。
另外还招募了100名无血缘关系、种族匹配、无脑部和眼部疾病的正常对照组。使用TIANamp Genomic DNA Kit (TIANGEN, Beijing, China)从外周静脉血(5ml)中分离基因组DNA。
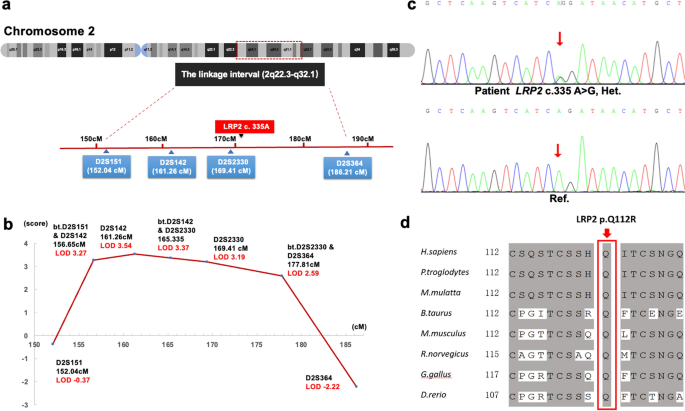
全基因组连锁分析
对最大的家族CS08进行全基因组连锁筛选,包括12例患者(图8)。1一个;II:1, II:8, II:12, III:1, III:6, III:9, III:14, III:17, III:19, IV:1, IV:4和IV:5)和两个未受影响的构件(图。1一个;III:12和IV:3)。此外,利用Fam标记的引物,通过聚合酶链式反应(PCR)扩增了横跨整个人类基因组的366个微卫星标记和3个单核苷酸多态性(SNPs),间隔约为10 cM (Weber set 6.0)1).PCR产物根据等位基因大小和标记进行适当的聚合,与GeneScanTM-500 Liz尺寸标准(Applied Biosystems, Foster City, CA)混合,变性,加载到6%标准变性聚丙烯酰胺凝胶上,并使用ABI 3730xl分析仪(Applied Biosystems)进行荧光检测。谱系显示雄性间传播(图。1一个;II:1和III:1)的疾病和几乎相同数量的受影响的男性和女性,表明一种AD遗传模式(图。1a).采用疾病等位基因频率分别为0.0001和0.01,外显率范围分别为80 ~ 100%的AD遗传模型计算多点LOD评分。使用Genemapper 4.1软件包(Applied Biosystems)收集和分析基因分型数据。采用MERLIN程序进行多点联动分析(http://www.sph.umich.edu/csg/abecasis/Merlin/index.html).家族和单倍型数据使用西里尔文,版本2.1程序生成。
全外显子组测序和Sanger测序
采用9例患者的基因组DNA进行平行WES(图2)。1一个;与连锁筛选相比,不包括III:6、IV:1和IV:5)和1个未受影响的CS08家族成员(III:12)。对来自13个不相关家庭的31名额外患者(14名男性和17名女性,附加文件)的基因组DNA进行WES2).WES使用SureSelect Human All Exon 50 Mb Kit (Agilent Technologies, Santa Clara, CA)进行,并在HiSeq 2000平台(Illumina, San Diego, CA)上进行测序。使用CASAVA v1.8.2将Illumina BCL文件转换为FASTQ文件。使用Trimmomatic 0.32版本过滤低质量的底座和适配器[19].然后,通过Burrows-Wheeler Aligner (BWA-MEM v0.7.15-r1140)将序列读取数据映射到具有默认参数的人类参考序列(GRCh37) [20.].使用GATK最佳实践管道调用单核苷酸变体(SNVs)和小插入和删除(INDELs) [21].GATK套件3.5.0版本对基本质量评分重新校准和INDELs周围的局部校准进行了改进。我们使用snpEff (v4.3-3)以群体频率、系统发育保守评分、基因区域和外显子功能标注变异,然后将所有标注的变异加载到GEMINI (v0.19.1) [22].Sanger测序和家族内共分离分析所有患者共有和未受影响成员不存在的变异。
在硅分析中
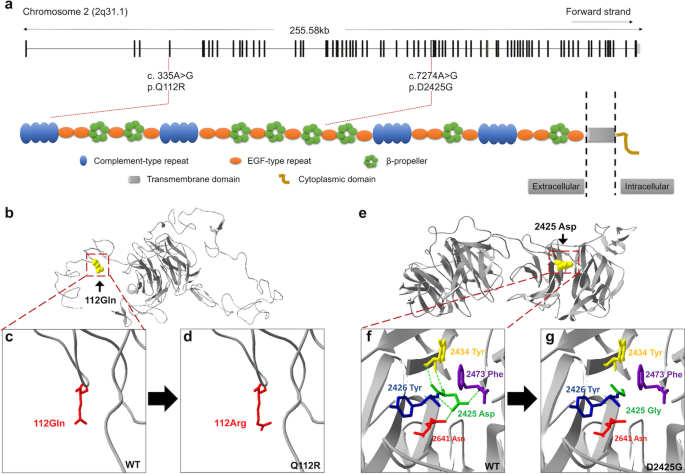
采用三种在线突变致病性评价软件进行致病性预测:SIFT (http://sift.jcvi.org/);PolyPhen-2 (http://genetics.bwh.harvard.edu/pph2/);及变异品尝师(http://www.mutationtaster.org/).利用Ensemble Genome Server数据库BLAST / BLAT Tools对突变残基的进化保守性进行分析,方法是将人类LRP2的蛋白序列与以下同源蛋白序列进行比对:黑猩猩(XP_515882.2),解剖(XP_001104179.2),牛(XP_002685354.2),亩骶(NP_001074557.1),鼠形(NP_110454.1),背带吊裤带(XP_004942820.1),鲐鱼类(NP_001181916.1)。利用SWISS-MODEL在线服务器构建了野生型和突变型LRP2的晶体结构模型。预测结构用PyMol软件(1.5版)显示。