摘要
在精准医疗、数字技术和人工智能时代,药物发现和开发面临着前所未有的产品和商业模式创新机遇,从根本上改变了药物发现、开发和营销的传统方式。这一转变的关键是在药物开发过程中采用新技术,促进从偶然发现驱动到数据驱动的医学转变。这种范式的转变伴随着翻译和精确的需求,导致了现代转化精准医学药物发现和开发方法。主要组成部分转化精准医学多组学分析,数字生物标记,基于模型的数据集成,人工智能,生物标志物引导的试验设计和以患者为中心的伴随诊断。在这篇综述中,我们总结并批判性地讨论了人工智能的潜力和挑战转化精准医学从跨行业的角度来看。
背景
传统上,大型制药公司的药物开发被认为是一门保守和风险规避的学科,流程受到高度监管,对外部创新的适应速度较慢。然而,在快速发展的医疗保健生态系统中,需要新技术和如何利用这些技术的创新概念来加速临床试验,降低流失率,减轻与研发(R&D)相关的风险,并整体提高药物研发效率[1,2].未来研发成功的关键是将变革性治疗概念和具有一流潜力的药物靶点、量身定制的数字技术和以患者为中心的药物开发结合起来,与更广泛的范式转变有关放之四海而皆准的医学迈向精准医疗(正确的药,在正确的时间,以正确的剂量,给正确的病人) [3.,4].虽然精准医疗是一个吸引人的概念,但如前所述,从实验室到床边的实施存在几个核心挑战[5,6,7].
药物开发的主要瓶颈之一是翻译[8],特别是在药物发现和早期临床开发的界面,简称转化差距[8,9,10].为了缩小这一差距并促进转化科学的发展,美国国立卫生研究院(NIH)已经建立了国家推进转化科学中心,是推动和整合学术界、工业界和非营利组织创新转化活动的核心枢纽[11].转化医学的定义欧洲转化医学学会[12该公司整合了多种研发工具,以弥补转化差距,指导早期药物开发。由于药物开发中的转化医学和精准医学方法是重叠和交织的,我们在这里使用这个术语转化精准医学指这门新兴的学科
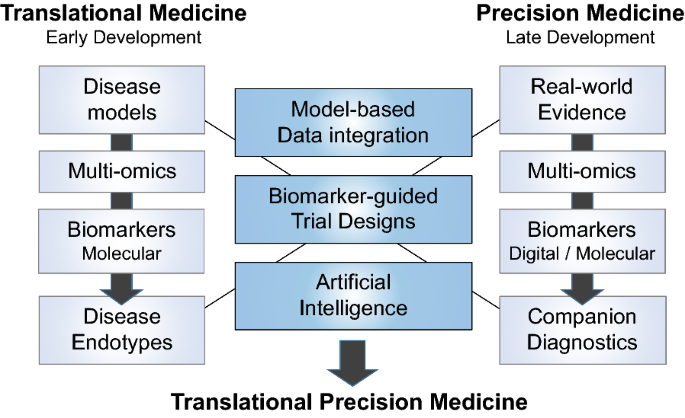
的转化精准医学Concept将转化医学(基于机制的早期药物开发)和精准医学(以患者为中心的晚期药物开发)的核心组件集成到端到端生物标志物引导的药物开发周期中。成功的关键因素转化精准医学是否(i)将机制从研究转化为早期临床开发(提出翻译/基础研究到临床应用)、(ii)从后期临床发展洞察到药物发现的反向转换(反向翻译/反向翻译/bedside-to-bench) [13], (iii)数据驱动机制-指示配对[14], (iv)将组学特征转化为临床相关的生物标志物和内型[15]和(v)开发为患者量身定制的伴随诊断和精准药物[3.].在这里,我们将重点关注以下关键组件转化精准医学(无花果。1):
Multi-omics剖析
生物标志物引导的试验设计
基于模型的数据集成
人工智能(AI)
数字生物标志物
病人接触。
Multi-omics剖析
临床数据可以分为表型(如人口统计学、生理评估、疾病评分、成像、健康问卷、数字患者评估)或分子(如基因组学、转录组学、蛋白质组学、代谢组学)。捕获与某种疾病相关的综合表型数据可被称为表现型(或phenomics),这是传统和最常用的分类方法,不论疾病的生物来源如何。利用数据集在分子水平上定义疾病亚型可被称为endotyping,以呼吸内科为例[16,17]或肿瘤学[18].美国国家科学院发起了一项新的分子分类运动,根据分子内型而不是传统的临床症状来定义疾病[19].然而,内分型需要深入的病理生理疾病的见解和大的分子数据集才能成功。在过去的20年里,高通量组学技术为内分型和数据驱动医学提供了基础[20.,21].随着测序技术的快速发展,遗传学已经彻底改变了我们对单基因疾病的理解,如囊性纤维化[22]或突变驱动的癌症[23],但大多数人类疾病是多基因的,因此解剖起来更加复杂。为了在遗传水平上接近这些疾病,多基因风险评分有望预测疾病或治疗的遗传易感性[24],特别是与电子健康档案结合使用时[25].转化基因组学旨在将遗传和临床数据结合起来,作为精准医疗方法的基础[7].除了遗传学,尤其是蛋白质组学[26,27]正为临床生物标志物和药物开发提供动力[28].与质谱不同,下一代蛋白质组学检测原理,如基于适体的技术[29],通常需要较低数量的材料(低至1ul/样品),并且可以更容易地应用于大型患者队列,以确定因果蛋白作为治疗靶向的候选蛋白[28,30.,31,32,33].与更成熟的组学层(如转录组学)相比,蛋白质组学提供了直接测量蛋白质水平的好处,从而促进了蛋白质生物标志物最常用的临床转化。
除了单一组学技术,multi-omics分析平台正在出现,包括基因组学,表观基因组学,转录组学,蛋白质组学,脂质组学,代谢组学,微生物组学和其他[34,35].多组学分析集成了几个生物学层面,使研究人员能够充分了解遗传学、基因调控和蛋白质之间的相互作用,并获得支持复杂疾病的分子模式的更完整的图像。因此,多组学能够很好地识别多层聚合的关键疾病节点,最大限度地提高识别新药物靶点、内源性或生物标志物的机会。网络提供了一种有效的方法来整合和可视化多组学分析的结果,特别是当证据不是集中在单个基因水平上,而是在生物途径内时[36],而网络传播方法可以应用于利用网络拓扑来识别关键节点[37].多组学对于N1次试验的结果[38],以了解药物与药物的相互作用,以及设计治疗性药物组合[39,40,41].尽管有这种潜力,但多组学在应用于临床药物开发时仍存在一些注意事项和局限性:
组学技术通常以半定量的方式评估大量基因/蛋白质,并对分析前过程高度敏感[42]例如批量效应[43].因此,为了建立可靠的临床应用案例,必须在实验设计中包括适当的控制,并通过正交定量方法验证最高命中值[43,44].
合并不同的多组学数据集[45]在不同数据格式和数据碎片化的情况下,对数据传输、集成和协调提出了挑战。此外,分析大型复杂数据集,如单细胞多组学[46],会增加假阳性的机会,因此需要使用适当的统计方法对数据进行适当的处理、归一化和分析[44,47].
临床试验的可行性[15,48],特别是对于多中心和组织来源的组学,仍然是一个挑战。限制精心挑选的临床站点的数量、严格的标准操作程序(SOPs)、跨站点控制和合格的分析核心设施对于可靠的数据生成至关重要。精心策划的生物库[49]是进一步将多组学数据与疾病特征和临床试验结果联系起来的关键。人类生物样本可及性、FAIR数据原则的一致性[50]和传播政策也是成功的多组学合作网络的关键。
生物标志物引导的试验设计
生物标志物由NIH/FDA的生物标志物定义工作组定义为“一种被客观地测量和评价为正常生物过程、致病过程或对治疗干预的药理学反应的指标的特征“(51].在药物开发中,生物标志物被广泛用于告知靶点接触、通路激活、药代动力学/药效学(PK/PD)建模和给药原理、诊断/患者选择、疾病分层、预后和预测以及监测疾病、安全性和治疗疗效。生物标志物分为分子、细胞、生理、成像和数字模式。作为临床试验终点,生物标记物提供了定量和客观的(病理)生物学测量的优势,相比之下,基于医生的评估往往是主观和可变的。生物标记物是跨物种转化PD反应的关键,也是弥合早期药物开发中转化差距的关键[9,10,52],尤其适用于多因素全身性疾病[53例如全身性免疫介导疾病。从药物开发的角度来看,阿斯利康小分子药物组合的纵向分析(五维(5 r)框架)表明,与没有生物标志物的可比项目相比,将生物标志物纳入早期药物开发(Ph2研究)与活跃或成功的项目相关[2].
新的生物标志物的开发是一个复杂、多步骤和迭代的过程,包括生物标志物的发现(通常基于组学数据)、分析前验证、评估不同的生物液(最佳接近疾病)、分析验证以及最终的临床验证和应用[48].对于每一个新的药物靶点和疾病适应症,通常会探索几种生物标志物模式和候选者,以缩小药物靶点和适应症相关的模式和候选者,如本文讨论的类风湿性关节炎等自身免疫性疾病[54].对于在临床试验中使用的生物标志物,关键是定义的表达(8) (15,55,56].CoU的范围从诊断、安全监测、PD反应到预测和预后生物标志物应用。有关生物标志物CoU的详细列表,读者可参考FDA-NIH生物标志物工作组及其相关在线资源BEST(生物标记,终点和其他工具)[51].预后和可预测的CoU对临床药物开发至关重要:预后基线的生物标志物指示独立于干预的疾病结局(对于确定高危患者以进行充实试验很重要),而预测基线的生物标志物指示对特定治疗的反应(反应预测)。
在药物开发中整合生物标记物有两种基本途径:(1)在a的背景下特定药物开发计划或(2)官员FDA生物标志物鉴定计划(BQP)。的特定药物开发计划Path是制药行业最常见的策略,药物开发人员/赞助商在临床试验中包括选定的生物标志物,主要用于内部决策,并负责生物标志物开发的所有方面。FDA BQP要求生物标记物作为通用药物开发工具[57使它们适用于多种药物开发项目,并有资格成为监管药物审批工具,这是一个正式而漫长的过程,通常涉及由多个学术和行业合作伙伴组成的财团。在FDA BQP中,候选生物标志物符合预先指定的CoU。FDA提供了最新的bqp合格生物标志物在线列表[58].值得注意的是,通过BQP鉴定CoU的生物标志物或鉴定测量生物标志物的特定测试是两种不同且独立的方法。对于生物标记物测试/测定鉴定,例如开发配套诊断测定(见下文),分析前和测定性能特征是关键。除了美国/FDA,其他区域/国家生物标志物指南和监管框架,如欧洲药品管理局(EMA)、亚太(APAC)监管机构、国家药品监督管理局(NMPA)和/或药品和医疗器械管理局(PDMA)的指南,必须考虑到生物标志物鉴定和临床实施。
一般来说,生物标记物的影响程度取决于三个关键因素:(i)生物标记物的验证和鉴定状态,(ii) CoU和(iii)生物标记物与CoU之间的科学证据。临床试验中的生物标记物主要用作探索性终点,以探索新的机制假设并为内部决策提供信息。如果生物标记物被认为更有影响和临床相关,生物标记物被用作次要或主要临床终点。这里的典型例子是生理生物标志物,如血压,临床建立的蛋白质生物标志物,如c反应蛋白,或成像读数。如果有来自独立流行病学研究和临床试验的令人信服的证据表明,生物标志物与临床结果评估密切相关,生物标志物可以被认为是替代临床终点替代终点,这对于那些使用传统临床终点需要很长时间才能获得结果的疾病具有重要意义。例如发生中风时的收缩压或发生心脏病时的低密度脂蛋白胆固醇水平。为了在制药工业试验中实施生物标志物,必须进一步考虑药物开发的几个方面,包括知情同意/数据保护考虑、临床试验后勤/可行性、对临床决策的影响和成本效益[48,59,60,61].
积极引导临床试验流程,生物标志物引导的试验设计都是选择的方法[62,63],这对于使用主方案(篮子、伞形和自适应平台试验)的新型临床试验设计特别有用[64].关于生物标记物引导试验设计的全面概述,读者可参考BiGTeD在线资源[65].对于生物标记物指导的试验设计,生物标记物应在临床实验室改进修订(CLIA)认证(美国)或同等(非美国)实验室进行分析。两种最常用的生物标志物引导试验设计是分层[66),浓缩[67].基于生物标志物的分层,或分层随机化,意味着在随机化之前测量所有患者的生物标志物,并用于就生物标志物状态按比例/平等地平衡治疗组与安慰剂组。生物标记物分层设计的优点是,如果患者是生物标记物阴性,则不会被排除在外。下一个更严格的生物标志物试验设计水平是富集。对于这种设计,将个体患者纳入临床试验取决于确定的生物标志物评估。使用这种方法时,对生物标志物和分析实验室的质量要求更高,因为协议定义的治疗决策直接依赖于生物标志物。当基于生物标记物-反应和/或生物标记物-安全关系(如CYP代谢)治疗生物标记物阴性患者在伦理上不合理时,富集设计尤其有用。FDA最近关于浓缩的指南[68建议在NDA/MAA提交前至少一次试验中纳入智能富集、适应性富集和生物标志物阴性人群(有明确的例外)。除了分层和富集设计,其他更复杂的生物标志物引导试验设计总结如下biomarker-strategy设计[65].所有生物标志物引导的试验设计都可以在非适应性或适应性环境中实施。后者为试验提供了更大的灵活性,但实施起来也更具挑战性。除了介入性生物标记物引导的试验设计外,最近在肿瘤学领域提出了使用主方案的非介入性(观察性)生物标记物引导的试验设计(掌握观察性试验) [69].
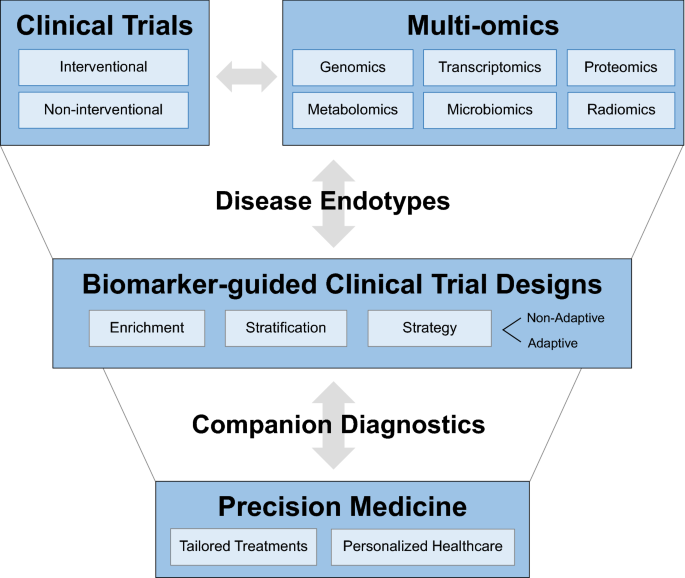
生物标志物引导的试验设计最终为精准医疗铺平了道路,即根据特定的患者特征定制药物开发[3.,70].2015年,美国政府发起了一项精准医疗计划[71,72].精准医疗侧重于个体而不是平均的治疗反应,并导致的概念N1次试验的结果[38],理想情况下是基于纵向多组学数据。虽然精准医疗方法已经广泛应用于肿瘤学和罕见遗传疾病,但其他治疗领域才刚刚开始根据这些原则定制药物开发[3.].生物标志物可以使精准医疗通过开发同伴诊断[73,74,75],主要建立在肿瘤学[76].伴随诊断被分类为体外诊断(IVD)医疗设备(IVD类I, II或III),通常与药物共同开发,通过降低药物的反应率来提高反应率numbers-needed-to-treat和/或避免患者接触到极有可能失败甚至造成伤害的药物。从一种探索性生物标志物到一种完整的IVD伴随诊断的开发路径是复杂的,需要风险投资,并且应在药物开发的早期开始,与卫生当局密切合作[74,75,77,78].伴随诊断应广泛提供给相关医疗保健专业人员,以供临床常规使用。FDA提供已批准或已批准的伴随诊断设备清单[79].伴随诊断[80]均受卫生当局/食品及药物管理局严格管制[81],并与补充诊断有所区别[82,83因为它们对治疗决策至关重要,而补充诊断只是支持治疗决策。由于从非肿瘤患者中获得活检组织通常具有挑战性,“液体活检”(来源于外周血/血清/血浆)是伴随诊断的主要领域,然而检测性能特征,如敏感性和特异性,是该领域成功的关键。数字2说明了从基于多组学的内分型,在生物标记物指导下的试验设计到基于伴发诊断的精确医学方法的流程。
为了提高候选药物的收益-风险比,安全方面越来越成为生物标记物引导的精准医疗方法的一个组成部分。例如,观察到接受检查点抑制剂治疗的患者经历免疫相关不良事件也表现出改善的治疗反应,最近被证明与多基因风险评分有关[84].此外,首次可以建立多基因风险评分来预测药物性肝损伤,这是临床中常见且非常难以预测的不良事件[85].
当结合观察时,生物标记物引导的试验设计提供了理想的工具,以催化从经验和临床的转变physician-centric数据驱动和成规精准医疗方法[70,86,87].然而,技术(伴随诊断试验开发)、临床(复杂的生物标志物指导试验设计、主方案)和监管(伴随诊断作为医疗设备的要求)障碍必须解决,特别是在非肿瘤适应症方面[83,88].
基于模型的数据集成
鉴于临床前实验和早期临床试验中每个受试者的样本量小且数量少,在转化医学中分析和利用生物标志物数据仍然具有挑战性。提高检测信号的统计能力的一种方法是使用纵向(即依赖于时间的)基于模型的数据集成。数学模型用于描述PK和PD/生物标志物结果的时间过程,以便更好地理解药理学并预测未来的实验结果[89].早在20世纪30年代,数学方程就被用来描述PK数据[90],但随着计算机的发展,更广泛的基于模型的方法开始起飞,并在20世纪70年代至80年代被引入药物开发。对治疗窗口小且需要剂量个性化的化合物的需求最高。这对于暴露和生物标志物PD反应之间存在显著延迟的化合物尤其具有挑战性。因此,描述学科间变异性的初始方法(群体“PopPKPD”模型)在麻醉学中得到了发展[91]和抗凝血剂(例如华法林)[92])。
人口模型最常使用简化的模型结构来模拟观测数据(即主要以血浆/血液或体外).当考虑化疗时,如甲氨蝶呤,出现了关于化合物肿瘤相关组织分布的问题[93].因此,第二类基于生理的模型被开发出来,以更详细地描述小分子的整个解放、吸收、分布、代谢和排泄(LADME)过程,这些过程严重依赖于它们的物理化学性质[94].这种方法用于预测药物-药物相互作用,但也用于转化医学领域从动物到人类的扩展——或者用于popk模型。
跨物种PK参数的缩放主要基于异速缩放,它使用固定指数的幂函数描述物种内部和物种之间生理方面(体积、代谢率、清除率等)的重量依赖性。这适用于PK参数[93],但由于途径表达、产生速率或整个生理网络的种间差异,对生物标志物来说可能是一个挑战。通过整合系统生物学和定量系统药理学,这些方法获得了更多的吸引力[95].第三个概念是应用物理和生物学假设,例如单调的暴露-响应、潜在信号的连续性/平滑性或异速缩放。这些模型可以用于高维数据(如多组学),当每个个体有多个采样时间点可用时,可以减少噪声。
最后,FDA已经建立了一个新的模型知情药物开发框架[96):“FDA正在实施模型知情药物开发(MIDD)试点计划,以促进基于暴露的、生物的和来自临床前和临床数据源的统计模型的开发和应用,称为MIDD方法。MIDD方法使用各种定量方法来帮助平衡药物开发中的风险和收益。当成功应用时,MIDD方法可以提高临床试验效率,增加监管成功的概率,并在没有专门试验的情况下优化药物剂量/治疗个性化。“这个MIDD试点项目是基于制药行业和欧洲卫生当局/EMA之间的联合讨论,并于2016年发表了一篇关于良好建模实践的论文[97].后者包括建模和药物开发的学习和确认循环的概念,其中基于模型的预测为下一步研究设计提供信息,例如,从动物数据到首次人体研究的PK和疗效或安全生物标志物的预测。卫生当局对MIDD方法的接受甚至推动[98]表示基于模型的数据集成的价值很高。
人工智能
在药物研发中产生和收集的数据量正在以前所未有的速度增长。结合信息处理的改进和更强大的硬件,机器学习、深度学习和人工智能总体上被定位为颠覆药物发现和基于算法的研发[99].深度学习已经彻底改变了几个行业,特别是在图像分析和识别领域,而它在生物医学研发中的影响仍有待充分发挥。One hundred.].来自大型纵向临床研究的高维多组学数据集为机器学习的应用提供了理想的基础[101]和AI [99].对药物发现和开发有影响的例子包括:靶标鉴定[102,103,104],生物标志物发现[105,106]和患者内分型[107,108].当应用于数字生物标记数据时,机器学习和深度学习算法也是强大的分析方法,允许将来自传感器和连接的数字设备的纵向、多模态和复杂的原始数据转换为端点和临床相关措施[109,110].
考虑到传统的基于意外发现和前向翻译的药物开发框架的僵化,转向一种新的思维方式,拥抱使用人工智能来发现和开发药物是成功的关键因素转化精准医学[111].最近,一项全面的跨行业分析列出了各大制药公司与人工智能相关的活动。112],得出的结论是,与领先的技术公司(如微软,谷歌)相比,大多数制药公司仍处于一个早期的成熟在研发中使用人工智能的阶段。然而,越来越多的医疗保健公司现在已经开始了他们的数字化之旅,在许多研发领域建立人工智能能力和数据素养[112].例如,强生(Johnson & Johnson)和诺华(Novartis)已经开始将基于人工智能的产品和服务商业化。医疗人工智能应用目前主要集中在基于电子病历、数字病理学和生物标志物的疾病诊断[113,114].为了超越并充分利用人工智能技术进行临床药物开发,必须优化和验证用于临床试验和结果预测的人工智能算法。人工智能驱动的方法有可能通过解剖复杂的高维患者数据集和定制药物开发来实现精准医疗,特别是在慢性疾病条件下[115].虽然传统上监管机构可能对生物医学研发中的先进人工智能模型不太感兴趣,但这一领域正在迅速演变,以人工智能医疗设备领域最近的发展为例[116,117以及FDA最近的试点项目新药的创新科技途径(ISTAND)鼓励使用基于人工智能的算法来评估患者,开发新的终点,或为研究设计提供信息。展望未来,制药组织继续在早期建设性地与监管部门合作,以创新方式设计和评估临床试验,包括在药物开发中更广泛地使用人工智能技术,这将是至关重要的。
总的来说,人工智能在药物发现和临床开发方面的影响将在很大程度上取决于底层数据及其内在局限性。基于人工智能的多组学分析以及电子病历的分析主要取决于所提供的分子和临床数据集的质量和数量,以及未来需要克服的关键限制和挑战。
不久的将来将显示这些新兴的人工智能算法是否以及如何帮助科学家(i)识别现有药物的新靶点或新适应症,(ii)揭示可以告知疾病发病机制或药物反应的潜在因素,(iii)发现可预测的生物标志物,使患者分层策略能够优化临床试验设计,以及(iv)最终影响药物开发价值链。关于人工智能在药物发现和开发中的更详细的概述,我们建议读者参考该领域的专门评论[87,101,111,118].
数字生物标志物
最近传感器技术的发展以及智能手机和其他联网数字产品的广泛使用,使全面收集和分析健康相关数据成为可能[119,120,121].将传感器数据转化为临床见解的算法和分析方法的进步促进了数字生物标志物的快速发展[122,123].数字生物标志物被定义为通过数字设备(如便携式、可穿戴设备、植入式和可消化设备)收集的表征、影响或预测与健康相关结果的生理和行为测量[124,125].与传统的临床评估相比,数字生物标志物具有几个潜在的优势。客观数据可在现实生活环境中以定量和无偏的方式频繁或连续地收集,从而提高统计能力、增强敏感性和特异性[122,126].在临床试验中,这些特征可使样本量更小、研究访视次数更少、研究持续时间更短以及为早期决策提供实时反馈[120,122,126,127].纵向数字患者数据可用于推进精准/个性化医疗方法。此外,在药物开发中使用数字生物标记物可以实现以患者为中心,整合真实世界的证据,减少患者参与试验的负担,增加患者登记的包容性[121],分散的试验[128]以及更好的产品差异化[129].尽管数字生物标记是一项很有前途的新技术,但确保在整个过程中保护患者相关敏感数据是对数字生物标记的一个主要要求和挑战。
数字生物标志物的成功例子是在神经退行性疾病领域,在该领域,传统的临床结果测量是稀疏的、高度可变的和评分依赖的[130].基于智能手机的测量方法已经开发出来并应用于临床试验,以监测帕金森病的症状[131,132];而来自惯性测量单元特征的特征最近已被用于预测帕金森病的严重程度[133].计算机化认知测试的易感性/风险生物标记物被用于对晚发性阿尔茨海默病高危成年人进行分类[134,135].从惯性可穿戴传感器中确定临床相关的步态参数,以评估亨廷顿病的步态损害[136].
虽然涉及数字技术的研究数量正在增长,并扩展到更多的技术、生物标志物类别和治疗领域[119,121],由于多层的复杂性,目前使用数字生物标志物作为临床终点仍处于早期研究阶段。数字生物标记产品通常是多个单独硬件(传感器)和软件(操作系统和算法)组件组合的结果[123].因此,在将数字生物标记物作为临床终点之前,彻底验证技术和分析解决方案并在所需的队列和使用环境中进行临床验证是至关重要的[123,127,137].目前的大部分工作仍然集中在工程上,解决算法开发和传感器性能问题[120].到目前为止,非常有限的解决方案正在进行临床验证。
将数字设备数据转换为经过验证的临床端点是一个漫长的过程,涉及工程、机器学习、数据科学、临床研究和监管互动等多个学科的合作。一个基于透明度、元数据标准、外部验证和数据共享的开放验证框架对于协调方法、评估和改进临床环境中的数字生物标志物是必要的[123].最近,出现了多项具体的努力,并正在塑造和加速经过验证的数字生物标志物的发展:(i)来自于临床试验转化计划(CTTI) [138),数字医学协会[139]和EMA [140];(ii)实用的适切验证框架[137,141];(iii)开源平台,例如数字生物标记发现管道[142];(iv)公开基准测试挑战[143];(v)和若干创新医学计划(IMI),如MOBILISE-D [144], idea-fast [145]及RADAR-AD [146].
数字生物标志物向以患者为中心的精准医疗发展的未来机遇是:(i)基于来自多种连接技术和现实环境中上下文信息的纵向/实时复合生物标志物的算法[123], (ii)分子/多组学和数字生物标志物的整合,以及(iii)患者分层的数字表型[147,148,149].
病人接触
自20世纪80年代艾滋病大流行以来,制药行业与患者互动的方式发生了根本变化,从整个药物开发价值链上的被动接受者转变为积极贡献者。这在过去十年中表现得尤为明显,大多数制药公司都成立了患者参与小组,积极倾听患者的声音[150,151].业界终于意识到,患者参与并不是一个额外的负担,而是可以改善和实际上加速药物开发。同样,卫生当局越来越多地将患者的意见纳入其监管指导中[152].例如,FDA以患者为中心的药物开发该倡议为行业提供了如何最好地识别对患者重要的东西的指导。在欧洲,EMA形成了病人及消费者工作小组.与患者、他们的护理人员、患者专家和患者倡导团体的接触已被证明对患者和行业都有好处[153,154].增加患者在这一过程中的参与,可以确保行业专注于真正的医疗需求,确保研究方案以患者为中心,并确保新的治疗方法更快面世。相反,行业受益于更有力地识别患者需求、更快地进行临床试验、更快地进入市场以及整体更高的可信度和可持续性[155].患者不仅增加了对行业的参与,也增加了对监管机构的参与,并进入了管理机构。主要的里程碑是基础国际病人组织联盟,以病人为中心的结果研究所[156]和以患者为中心的药物开发[157,以及其他以患者为中心的举措。事实上,患者参与整个医疗生态系统的影响正在推动各个层面的变化:成为患者自身的可靠来源,改善获取和护理,推动研发,并倡导与政府合作的政策变化。
传统上,患者参与主要是在新药已经上市后才考虑的。关于该分子及其临床开发路径的大部分决定,包括未满足的医疗需求,都已经由该公司做出。然而,研究表明,患者视角的早期整合,特别是在临床前研究和早期开发中,对为患者、企业和社会创造价值的影响最大[158].由于临床前研究是一门通常不与患者直接合作的学科,因此在这一阶段改变思维方式,包括患者的声音可能具有挑战性,但这代表着明确的未来patient-led研究[159].最近的一篇论文指出了在临床前研究中实施患者参与的主要挑战,并提供了克服当前障碍的可能解决方案[160].在CTTI对患者群体、行业和学术界进行的访谈中,患者代表认为与研究伙伴的合作具有特别大的益处。患者主导的组织热衷于更多地了解他们的疾病,并对在研究项目中合作非常感兴趣,并愿意为研究和临床开发提供数据(匿名并遵循严格的数据保护政策)[161].对行业的一个关键建议是,从研发项目开始就尽早听取患者的意见,以改善试验设计和临床执行[162].
个性化医疗保健(PHC)、精准医疗和分层医疗已被互换使用,用来描述根据患者的个人病理为其量身定制治疗的概念。随着新的诊断和数据驱动方法的兴起,加深了我们对疾病分子基础的理解,这个数百年的梦想已经接近现实。如今,患者群体也开始意识到PHC的潜力,其意义远远超出了精准医疗。PHC包含了通过结合常规临床数据集、分子特征(如遗传学)、环境、生活方式和个人需求来定制治疗和医疗的一切。该领域的一些关键创新包括数字医疗解决方案,该技术将数字患者信息/电子病历与可穿戴设备、移动应用程序、远程医疗和使用人工智能的数字助理连接起来[163],亦请参阅上述有关章节。该领域的一大要求和挑战是在整个过程中保护患者的相关敏感数据和患者权利。患者、护理人员和医疗保健提供者承认这些方法在关键领域的实用性和先进性,如患者教育、准确诊断、患者结果、生活质量、疾病预防和医疗保健价值[164],最近不同的计划,如欧盟健康数据太空竞赛,更强调了这一点[165]或美国精准医疗计划[166].所有这一切的总体目标是作为一个集成的研发合作伙伴,与患者共同制定医疗保健决策。
结论
转化精准医学伴随着一种范式的转变放之四海而皆准的以生物标记为导向,以病人为中心的医学。在药物开发中采用这一原则的关键成功因素包括正向和反向翻译的结合,将疾病状况分类为多组学定义的内型,基于人工智能和算法的研发概念的集成,将数字生物标志物作为临床终点的实施以及伴随诊断的开发。数据驱动和基于算法的研发的兴起,需要建立一种新的思维模式,即如何有效地使用数据挖掘和人工智能工具来发现和开发新药[111].不久的将来,我们将看到这些新兴的基于人工智能的数字工具是否以及如何揭示新的靶点、致病疾病特征、优化临床试验设计,并对整个制药行业的药物开发产生整体影响。以患者为中心的真实世界证据(RWE)工具、电子病历、多组学分析、数字生物标记物和基于人工智能的数据分析的融合,将为生物标记物支持的基于算法的精确研发铺平道路。
前景
的转化精准医学进化伴随着不同的挑战:(i)multi-omics如果数据揭示了与疾病结局和/或治疗反应相关的新药物靶点或生物标志物特征,则这些数据对药物发现和开发主要有用[61];(二)基于多组学的患者和疾病分层需要准确诊断和详细的临床注释/电子病历;(3)数字生物标志物由于临床终点提供了客观和定量的措施,但仍需要更广泛的临床使用和卫生当局的接受;(iv)生物标志物引导的试验设计而且精密医学方法已经在肿瘤学和罕见病中广泛实施,而其他非肿瘤学领域刚刚开始追求这些概念和(v)精密医学/同伴诊断这些方法带来了巨大的开发成本和报销障碍。一个重要的问题是,患者如何看待这些新技术和评估,因为接受和坚持临床解读是招募患者试验和长期参与的关键。目前正在实施以患者为中心的新型交互方法,以使患者更积极地参与研发、RWE网络和临床试验。用于与监管机构互动的新型云数据系统和平台[167],用于工业界和学术界之间共享数据集,用于公私伙伴关系,或用于管理跨行业伙伴关系和多学科计划,例如信息交换与数据转换(知情)食品及药物管理局的倡议[168将进一步塑造数据驱动医学的道路。
COVID-19时代从多个层面上极大地颠覆了传统的药物研发方法[169,170,171,172]:(i)虚拟、基于数据的数据共享(包括bioRxiv和medRxiv等开放存储库)以及合作研究和药物发现/开发概念正在获得更高的吸引力;(ii)系统分析了从COVID-19患者收集的大型纵向数据集,为多组学研究提供了巨大潜力[173,174,175]和基于人工智能的分析[169,176,177,178],支持诊断、基础疾病了解、内分型、图像分析、药物靶点识别和药物再利用[169,179];(iii)临床试验加速、分散,并越来越多地包括数字端点、生物传感器、家庭护理、以患者为中心的采样和远程临床试验招募和监测策略[171,180],并附有FDA关于在COVID-19期间进行临床试验的指南[181].结合起来,这些新兴概念在COVID-19疫情期间迅速和成功地实施,有望在大流行时期之后提高药物研发效率,减轻患者负担。
新兴治疗方式,包括CAR - t细胞[182]、基因治疗[183,184],诱导蛋白质降解[185]或以mrna为基础的原则[186,187],以及患者来源的类器官用于体外药物反应测试,以指导个性化治疗[188]进一步增加了生物标记物引导的翻译精度的复杂性。最后,未来的核心挑战为转化精准医学至于药物开发总体上仍然是如何利用和拥抱新的分子和数字技术,以一种可行的方式进行更大规模的临床试验,并被监管机构接受,最重要的是被患者接受。
数据和材料的可用性
不适用。
缩写
- 人工智能:
-
人工智能
- 最好的:
-
生物标记,终点和其他工具
- BQP:
-
生物标志物鉴定计划
- CLIA:
-
修订临床化验所改善计划
- 咨询:
-
的表达
- CTTI:
-
临床试验转化计划
- 电子健康档案:
-
电子健康记录
- 教育津贴:
-
欧洲药品管理局
- 食品药品监督管理局:
-
美国食品和药物管理局
- 试管:
-
体外诊断
- LADME:
-
释放,吸收,分配,代谢,排泄
- MIDD:
-
模型知情的药物开发
- 国家卫生研究院:
-
美国国立卫生研究院
- 帕金森病:
-
药效学
- 过去:
-
个性化医疗
- PK:
-
药代动力学
- 研发:
-
研发
- 莱茵集团:
-
真实的证据
- SOP:
-
标准操作程序
参考文献
Paul SM, Mytelka DS, Dunwiddie CT, Persinger CC, Munos BH, Lindborg SR,等。如何提高研发效率:制药业面临的重大挑战。新药品发现,2010;9(3):203-14。
Cook D, Brown D, Alexander R, March R, Morgan P, Satterthwaite G,等。从阿斯利康(AstraZeneca)药物管道的命运中学到的教训:一个五维框架。中国医药科学。2014;13(6):419-31。
Dugger SA, Platt A, Goldstein DB。精准医疗时代的药物研发。新药品发现,2018;17(3):183-96。
seseyhan AA, Carini C.精准医疗的创新和新技术是否为以患者为中心的护理开辟了新时代?《翻译医学》2019;17:114。
费尔德曼。基础研究到临床应用;临床和转化研究;个性化医学;精准医疗——名字有什么意义?中华医学杂志2015;8(3):171-3。
嘿SP, Gerlach CV, Dunlap G, Prasad V, Kesselheim AS。精准医疗的证据景观。中国生物医学工程学报,2020;29(4):374 - 374。
杰吉尼E,格洛因AL,巴顿AC,韦恩LV。转化基因组学和精准医学:从实验室走向临床。科学。2019;365(6460):1409 - 13所示。
奥斯汀CP翻译翻译。中国医药科学,2018;17(7):455 - 56。
翻译研究:跨越死亡之谷。大自然。2008;453(7197):840 - 2。
弥合翻译差距——新希望,新挑战。基金临床药物,2011;25(2):163-71。
国家卫生研究院。国家推进转化科学中心(HCATS)。https://ncats.nih.gov/.
沙赫扎德A,唐G,柯尔斯RJ。欧洲转化医学学会对转化医学的定义。新地平线翻译医学。2015;2(3):89-91。
是时候反转我们的思维了:反向翻译研究范式。中国临床医学杂志,2018;11(2):98-9。
史伟辉,张旭,阿罗诺夫。从治疗机制和适应症的角度看药物发现的有效性。中国医药科学,2018;17(1):78。
Frank R, Hargreaves R.药物发现和开发中的临床生物标志物。中国医药科学,2003;2(7):566-80。
Kaur R, Chupp G.成人哮喘的表型和内型:向精准医疗迈进。中华过敏临床杂志,2019;44(1):1 - 12。
Dean K, Niven R.哮喘表型和内型:个体化治疗的意义。BioDrugs。2017年,31(5):393 - 408。
Ricker CA, Crawford K, Matlock K, Lathara M, Seguin B, Rudzinski ER,等。胚胎型横纹肌肉瘤的定义。中国生物医学杂志,2020;6(2):a005066。
迈向精准医疗:为生物医学研究和新的疾病分类建立知识网络。国家研究院收藏:由国家卫生研究院资助的报告。华盛顿特区;2011.https://pubmed.ncbi.nlm.nih.gov/22536618/.
Shah NH, Tenenbaum JD。即将到来的数据驱动医学时代:转化生物信息学的下一个前沿。中华医学杂志2012;19(E1): E2-4。
Mayo CS, Deasy JO, Chera BS, Freymann J, Kirby JS, Hardenberg PH.我们如何影响数据驱动医学的文化变革?中华放射医学杂志,2016;29(3):344 - 344。
沙玛N,卡廷GR.囊性纤维化的遗传学和基因组学。《囊肿纤维杂志》2020;19:S5-9。
Stratton MR, Campbell PJ, Futreal PA。癌症基因组。大自然。2009;458(7239):719 - 24。
李志刚,李志刚,李志刚。多基因风险评分的个人和临床应用。科学通报。2018;19(9):581-90。
李锐,陈勇,Ritchie MD, Moore JH。预测疾病风险的电子健康记录和多基因风险评分。科学通报。2020;21(8):493-502。
Petricoin EF, Zoon KC, Kohn EC, Barrett JC, Liotta LA。临床蛋白质组学:将临床承诺转化为临床现实。中国医药科学,2002;1(9):683-95。
Dupree EJ, Jayathirtha M, Yorkey H, Mihasan M, Petre BA, Darie CC.自下而上蛋白质组学的关键回顾:这个领域的好、坏和未来。蛋白质组。2020;8(3):14。
Lamb JR, Jennings LL, Gudmundsdottir V, Gudnason V, Emilsson V.这是我们血液中的:个性化医疗的一瞥。趋势Mol医学2020;27(1):20-30。
Gold L, Walker JJ, Wilcox SK, Williams S.利用SOMAscan蛋白质组学平台在大规模人类蛋白质组学方面的进展。中国生物工程学报。2012;29(5):543-9。
贾文杰,吴文杰,李文杰,李文杰,等。大规模基于适体的蛋白质组学分析在计划心肌梗死中的应用。循环。2018;137(12):1270 - 7。
Gudmundsdottir V, Zaghlool SB, Emilsson V, Aspelund T, Ilkov M, Gudmundsson EF,等。循环蛋白特征和2型糖尿病的因果候选者。糖尿病。2020;69(8):1843 - 53年。
Emilsson V, Ilkov M, Lamb JR, Finkel N, Gudmundsson EF, Pitts R,等。人类血清蛋白的共同调节网络将遗传与疾病联系起来。科学。2018;361(6404):769 - 73。
埃米尔松五世,古德纳松五世,詹宁斯二世。用深层血浆蛋白质组预测健康和寿命。中华医学杂志2019;25(12):1815-6。
孙玉武,胡玉军。多组学数据的综合分析,用于复杂人类疾病的发现和功能研究。Adv Genet, 2016; 93:147-90。
王晓明,王晓明。多组学在疾病研究中的应用。基因组生物学,2017;18:83。
王志强,王志强,王志强,等。网络医学:一种基于网络的疾病治疗方法。科学通报。2011;12(1):56-68。
李文杰,李文杰,李文杰。网络传播对遗传关联的影响。植物学报,2017;18(9):551-62。
肖克新泽西。个性化医疗:个人试验的时间到了。大自然。2015;520(7549):609 - 11所示。
Forst简历。网络基因组学是后基因组时代生物系统分析的一种新方法。Mol生物学杂志2002;29(3):265-80。
高文伟,李艳华,钟敏,王磊。生物网络分析方法的进步如何赋予蛋白质组学以力量。蛋白质组学。2012;12(4 - 5):550 - 63。
赵淑娟,艾扬格。系统药理学:网络分析识别药物作用的多尺度机制。2012; 52:505-21。
Ruiz-Godoy L, Enriquez-Carcamo V, Suarez-Roa L, Lopez-Castro ML, Santamaria A, Orozco-Morales M,等。血浆和血清样本中特异性分析前质量控制标记的鉴定。肛门Methods-Uk。2019; 11(17): 2259 - 71。
马志刚,马志刚,李志刚。基于动态规划算法的高通量筛选数据批量效应识别。35生物信息学。2019;(11):1885 - 92。
山田瑞,冈田东,王娟,王志强,小山山。组学数据分析的解释。中国科学(d辑),2018;26(1):49 - 51。
王晓燕,王晓燕,王晓燕,等。生物标志物研究中成功数据整合的关键因素。新药品发现,2016;15(6):369-70。
胡玉军,安强,薛坤,Trejo B,范世祥,郭艳。单细胞多组学技术:方法与应用。前沿细胞发育生物学。2018;6:93-102。
Verheijen M, Tong WD, Shi LM, Gant TW, Seligman B, Caiment F.对组学数据分析框架的开发。Regul毒理学药品。2020;112:104621。
克劳斯VB。生物标记物作为药物开发工具:发现、验证、鉴定和使用。风湿醇。2018;14(6):354-62。
生物储存库:建立更好的生物库。大自然。2012;486(7401):141 - 6。
Wilkinson MD, Dumontier M, Aalbersberg IJ, Appleton G, Axton M, Baak A,等。科学数据管理和管理的FAIR指导原则。科学数据。2016;3:160018。
BEST(生物标记,终点和其他工具)资源。https://www.ncbi.nlm.nih.gov/books/NBK326791/.
Roberts SF, Fischhoff MA, Sakowski SA, Feldman EL。视角:将科学转化为医学:临床科学家如何跨越研究的“死亡之谷”。中国医学杂志,2012;37(3):344 - 344。
Akhtar A.动物实验的缺陷和对人类的危害。健康伦理。2015;24(4):407-19。
seseyhan AA, Carini C.精准医疗的创新和新技术是否为以患者为中心的护理开辟了新时代?中华医学杂志2019;17(1):114。
拉瑟尔MN, Johnson KR, Boers M, Tugwell P, Brooks P, Simon L,等。生物标记物和替代终点的定义和验证标准:定量分层证据方案的开发和测试。中华风湿病杂志。2007;34(3):607-15。
Bravo-Merodio L, Williams JA, Gkoutos GV, Acharjee A.转化医学组学生物标志物鉴定管道。《中国医学杂志》2019;17:155。
食品及药物管理局。https://www.fda.gov/drugs/biomarker-qualification-program/list-qualified-biomarkers.
威廉姆斯SA,斯莱文DE,瓦格纳JA,韦伯斯特CJ。生物标记物鉴定和接受的成本效益方法。中国医药科学,2006;5(11):897-902。
Trusheim MR, Berndt ER, Douglas FL.分层医学:结合药物和临床生物标志物的战略和经济意义。新药品发现,2007;6(4):287-93。
Hurko O, Jones GK。生物标记物的评估。新药品发现,2011;10(4):253-4。
Mandrekar SJ, Sargent DJ。预测性生物标志物验证的临床试验设计:一种尺寸不适合所有。生物危害杂志,2009;19(3):530-42。
Antoniou M, Kolamunnage-Dona R, Jorgensen AL.生物标志物引导的非适应性试验II期和III期设计:方法学综述。中华泌尿外科杂志,2017;7(1):1。
朴俊杰,西登E,佐拉蒂MJ,德龙L,哈拉里O,辛格J,等。篮子试验、伞式试验和平台试验的系统回顾:主方案的景观分析。试验。2019;20(1):572。
Ivison S, Des Rosiers C, Lesage S, Rioux JD, Levings MK.生物标记物引导的自身免疫患者生物治疗分层。中国医学杂志,2017;49:56-63。
弗莱德林B,科恩EL。生物标记物富集策略:将试验设计与生物标记物凭证相匹配。中华儿科杂志。2014;11(2):81-90。
Dickson D, Johnson J, Bergan R, Owens R, Subbiah V, Kurzrock R.主观察性试验:推进精准医学的新一级主方案。细胞。2020;180(1):9-14。
Kalaitzopoulos D.精准医疗的潜力。新地平线翻译医学,2016;3(2):63-5。
Mullard A.耗资2.15亿美元的精准医疗计划初具规模。Nat Rev Drug Disc. 2015;14(3):155。
Collins FS, Varmus H.精准医疗的新举措。中华实用医学杂志,2015;29(3):344 - 344。
Doble B, Tan M, Harris A, Lorgelly P.在靶向肿瘤治疗经济评估中的伴生诊断建模:系统回顾和方法学检查表。中国病理学杂志,2015;15(2):235-54。
约根森JT。伴随诊断:个性化医疗的关键。中国病理学杂志,2015;15(2):153-6。
Mankoff DA, Edmonds CE, Farwell MD, Pryma DA。伴随诊断的发展。中国核医学杂志,2016;46(1):47-56。
Hersom M, Jorgensen JT。伴发和补充诊断-关注非小细胞肺癌中PD-1/PD-L1检查点抑制剂的PD-L1表达测定。药物监测,2018;40(1):9-16。
林娥,钱杰,王福生,范俊杰。伴随诊断中下一代测序的挑战和机遇。中国病理学杂志,2015;15(2):193-209。
Tsourounis M, Stuart J, Pignato W, Toscani M, Barone J.个性化医疗和伴随诊断的当前趋势:来自DIA个性化医疗和伴随诊断会议的摘要。中国生物医学工程学报,2015;49(4):530-43。
FDA对伴随诊断的观点:一个不断发展的范式。临床癌症杂志2014;20(6):1453-7。
食品及药物管理局。https://www.fda.gov/medical-devices/in-vitro-diagnostics/companion-diagnostics.
Milne CP, Bryan C, Garafalo S, McKiernan M.补充与伴发诊断:苹果和橘子?生物标志医学,2015;9(1):25-34。
约根森JT。伴随和补充诊断:临床和监管观点。癌症趋势。2016;2(12):706-12。
Khan Z, Di Nucci F, Kwan A, Hammer C, Mariathasan S, Rouilly V,等。皮肤自身免疫多基因风险影响膀胱癌免疫检查点阻断美国国家科学研究院。2020; 117(22): 12288 - 94。
Koido M,川上E, Fukumura J,野口Y,大堀M, Nio Y,等。多基因结构提示药物性肝损伤的潜在易感性。中华医学杂志2020;26(10):1541-8。
罗芙-高J,皮尔A,瑞琼-帕里拉JC,恩尼斯K,罗维特R,曼卡A,等。精准医疗的未来:对卫生技术评估的潜在影响。药物经济学。2018;36(12):1439 - 51。
Filipp阵线。人工智能推动精准医疗的机遇。2019;7(4): 208-13。
张志刚,张志刚,张志刚,等。精准医疗发展的监管障碍。中国生物医学工程学报。2016;1(3):319-29。
Vicini P, Gastonguay MR, Foster DM.基于模型的生物标志物发现和评估方法:一项多学科综合综述。中国生物医学工程杂志,2002;30(4):379-418。
Torsten Teorell,药物动力学之父。中华医学杂志,2001;20(1):1 - 6。
施希纳,史丹斯基,李志强,李志强,李志强。d-tubocurarine的药代动力学和药效学研究。临床药物学杂志1979;25(3):358-71。
胡佛NH。华法林的临床药代动力学和药效学。《临床药典》1986;11(6):483-504。
Anderson BJ, Holford NH。药代动力学中基于机制的大小和成熟度概念。《药理学年鉴》2008;48:303-32。
李文杰,李文杰,李文杰,等。IMI -口服生物制药工具项目-自下而上PBPK预测成功的评估第3部分:通过分析不同化合物类别的in Silico性能来识别系统参数中的差距。中国医药科学,2017;96:626-42。
Krauss M, Mueller C, Schlender J, Schuppert A, Block M, Kuepfer L.跨患者群体的转化学习和药代动力学预测的系统药理学方法。中国药典杂志,2016;43:S67-8。
食品及药物管理局。https://www.fda.gov/drugs/development-resources/model-informed-drug-development-pilot-program.
工作组EM, Marshall SF, Burghaus R, Cosson V,张SY, Chenel M,等。基于模型的药物发现和开发的良好实践:实践、应用和文档。中国药理学杂志。2016;5(3):93-122。
王勇,朱浩,Madabushi R,刘强,黄明明,Zineh I.模型知情药物开发:美国当前监管实践和未来考虑。中国药物学杂志,2019;29(4):369 - 369。
麦建奎,杨晓明。人工智能在药物开发中的应用。今日药物发现,2019;24(3):773-80。
Ching T, Himmelstein DS, beaulieue - jones BK, Kalinin AA, Do BT, Way GP,等。深度学习在生物学和医学领域的机遇和障碍。中国机械工程,2018;29(6):366 - 366。
范文文,陈志强,李志强,等。机器学习在药物研发中的应用。新药品发现2019;18(6):463-77。
费雷罗E,邓汉姆I, Sanseau P.在利用基因疾病关联数据的新治疗靶点的硅预测。中华医学杂志,2017;15:1-6。
Rouillard AD, Hurle MR, Agarwal P.对不同Omic数据的系统查询揭示了临床成功治疗靶点的可解释、可靠和可推广的转录组学特征。科学通报。2018;14(5):e1006142。
Patel-Murray NL, Adam M, Huynh N, Wassie BT, Milani P, Fraenkel E.一个多组学可解释的机器学习模型揭示了小分子的作用模式。科学通报2020;10(1):954。
王晓明,王晓明,王晓明,王晓明。基于机器学习的蛋白质组学研究进展。组学。2013; 17(12): 595 - 610。
Bravo-Merodio L, Williams JA, Gkoutos GV, Acharjee A.转化医学组学生物标志物鉴定管道。中华医学杂志2019;17(1):155。
Sharifi-Noghabi H, Zolotareva O, Collins CC, Ester M. MOLI:多组学晚期整合深度神经网络用于药物反应预测。生物信息学,2019,35 (14):i501-9。
Exarchos KP, Beltsiou M, Votti CA, Kostikas K.哮喘的人工智能技术:现有文献的系统回顾和批判性评价。中国生物医学工程学报,2010;29(3):366 - 366。
张宏,邓凯,李宏,Albin RL,关勇。深度学习识别自我报告帕金森病的数字生物标志物。模式。2020;1(3):100042。
Guthrie NL, Carpenter J, Edwards KL, Appelbaum KJ, Dey S, Eisenberg DM,等。数字生物标记物的出现预测和修改治疗效果:机器学习研究。英国医学杂志,2019;9(7):e030710。
施耐德P, Walters WP, Plowright AT, Sieroka N, Listgarten J, Goodnow RA Jr,等。人工智能时代对药物设计的反思。中国医药科学,2020;19(5):353-64。
Schuhmacher A, Gatto A, Hinder M, Kuss M, Gassmann O.成为数字制药公司的好处。今日药物发现。2020;25(9):1569-74。
李志强,李志强,李志强。数字病理学中的人工智能——诊断和精准肿瘤的新工具。中华儿科杂志,2019;16(11):703-15。
黄松,杨娟,方松,赵强。人工智能在癌症诊断和预后中的机遇与挑战。癌症杂志2020;471:61-71。
苏勃拉曼尼恩,沃伊图西辛恩,Favre L, Boughorbel S, Shan J, Letaief KB,等。人工智能时代的精准医疗:对慢性疾病管理的影响。中华医学杂志2020;18(1):472。
Benjamens S, Dhunnoo P, Mesko B.基于fda批准的医疗设备和算法的人工智能状态:一个在线数据库。Npj数字医学2020;3:118。
马莫申,李志强,李志强。深度学习在生物医学中的应用。Mol Pharm. 2016;13(5): 1445-54。
裴瑞B, Herrington W, Goldsack JC, Grandinetti CA, Vasisht KP, Landray MJ,等。2010-2016年临床研究中使用移动设备测量结果:系统文献综述数字生物标记,2018;2(1):11-30。
Bakker JP, Goldsack JC, Clarke M, Coravos A, Geoghegan C, Godfrey A,等。促进临床研究中使用移动技术的可行性研究的系统回顾。中华数字医学杂志2019;2(1):47。
Marra C, Chen JL, Coravos A, Stern AD。量化临床研究中互联数字产品的使用。中华数字医学杂志2020;3(1):50。
杨晓东,陈晓明,陈晓明,等。用于评估临床试验终点的生物特征监测设备:开发生态系统。中国医药科学,2017;16(10):736。
Coravos A, Khozin S, Mandl KD。开发和采用安全有效的数字生物标志物,以改善患者的预后。中华数字医学杂志2019;2(1):14。
多尔西ER。数字时代的数字期刊。数字生物标记,2017;1:1-3。
Sim I.移动设备和健康。中华实用医学杂志,2019;36(10):956-68。
Dodge HH, Zhu J, Mattek NC, Austin D, Kornfeld J, Kaye JA。使用高频家庭监测数据可以减少临床试验所需的样本量。PLoS ONE。2015; 10 (9): e0138095。
Cohen AB, Mathews SC.数字结果测量。数字生物标记,2018;2(3):94-105。
Khozin S, Coravos A.在现实世界证据时代的分散试验和临床调查的包容性。临床药物治疗。2019;106:25-7。
Rodarte C.药学视角:数字生物标志物和上下文数据将如何使治疗环境成为可能。数字生物标记,2017;1(1):73-81。
多西ER, Papapetropoulos S,熊m, Kieburtz K.第一个前沿:神经退行性疾病的数字生物标志物。数字生物标记,2017;1(1):6-13。
Lipsmeier F, Taylor KI, Kilchenmann T, Wolf D, Scotland A, Schjodt-Eriksen J,等。评估基于智能手机的帕金森病1期临床试验的探索性结果测量。音乐学报。2018;33(8):1287-97。
詹A,莫汉S, Tarolli C,施耐德RB,亚当斯JL,夏尔马S,等。使用智能手机和机器学习来量化帕金森病的严重程度:移动帕金森病评分。中国神经医学杂志,2018;75(7):876-80。
谢晓明,孙晓明,孙晓明,等。众包数字健康措施预测帕金森病的严重程度:帕金森病数字生物标志物梦想挑战。bioRxiv。2020; 4(1): 53。
Ritchie K, Carriere I, Su L, O 'Brien JT, Lovestone S, Wells K,等。晚发型阿尔茨海默病高危成年人的中年认知特征:预防研究老年痴呆症,2017;13(10):1089-97。
Kourtis LC, Regele OB, Wright JM, Jones GB。阿尔茨海默病的数字生物标志物:移动/可穿戴设备的机会。中华医学杂志2019;2(1):9。
安哲耶夫斯基,杜林AV,斯塔姆勒D,费龙TJ,哈里斯DA,黄C,等。亨廷顿病的可穿戴传感器:初步研究。中华亨廷顿病杂志2016;5(2):199-206。
Goldsack JC, Coravos A, Bakker JP, Bent B, Dowling AV, Fitzer-Attas C,等。验证、分析验证和临床验证(V3):确定生物特征监测技术(BioMeTs)适合用途的基础。中华数字医学杂志2020;3(1):55。
CTTI。https://www.ctti-clinicaltrials.org/blog/category/mobile-clinical-trials.
李文杰,李志强,李志强,等。医药领域的数字技术:塑造成功的框架。新药发现。2020;19:573-4。
Kruizinga MD, Stuurman FE, Exadaktylos V, Doll RJ, Stephenson DT, Groeneveld GJ,等。为临床试验开发新颖的、基于价值的数字端点:一种适合目的验证的结构化方法。中国医药科学,2020;72(4):899-909。
DBDP。https://dbdp.org/.
bionetwork年代。https://sagebionetworks.org/challenges-benchmarking/.
MOBILISE-D。https://www.mobilise-d.eu/.
IDEA-FAST。https://idea-fast.eu/.
RADAR-AD。https://www.radar-ad.org/.
数字表型:行为学新科学的技术。《美国医学协会杂志》上。2017; 318(13): 1215 - 6。
Huckvale K, Venkatesh S, Christensen H.面向临床数字表型:考虑目的、质量和安全性的及时机会。中华数字医学杂志2019;2(1):88。
深度数字表型和精确健康的数字双胞胎:是时候深入挖掘了。中国医学网络学报,2020;22(3):e16770。
Geissler J, Ryll B, di Priolo SL, Uhlenhopp M.提高患者参与药物研发:一个实际的路线图。中国生物医学工程学报,2017;51(5):612-9。
李志强,李志强,李志强,等。EUPATI和药物研发中的患者:指导患者参与监管过程。Front Med. 2018;5:23 30。
马夫里斯M, Furia Helms A, Bere N.参与药品监管:两个机构的故事。新药品发现,2019;18(12):885-6。
克罗克JC, Ricci-Cabello I,帕克A,赫斯特JA, Chant A, Petit-Zeman S,等。患者和公众参与对临床试验登记和保留的影响:系统回顾和荟萃分析。BMJ。2018; 363: k4738。
胡志强,李志强,李志强,等。在药物开发和生命周期中与患者合作:行动呼吁。中国生物医学工程学报,2015;49(6):929-39。
关于患者参与药物开发的演变的思考。中华医药杂志2019;33(3):179-85。
PCORI。https://www.pcori.org/sites/default/files/Engagement-Rubric.pdf.
张志刚,张志刚,张志刚,张志刚,等。文化和流程改变是患者参与药物开发的优先事项。中国生物医学工程学报,2017;51(1):29-38。
Chalmers I, Bracken MB, Djulbegovic B, Garattini S, Grant J, Gulmezoglu AM,等。当研究重点确定后,如何增加价值和减少浪费。柳叶刀》。2014;383(9912):156 - 65。
马凯西J,盖琳S,威尔逊AG,多丽丝ER。促进公众和病人参与基础和临床前健康研究。PLoS ONE。2019; 14 (5): e0216600。
Chawla NV, Davis DA。将大数据引入个性化医疗:以患者为中心的框架。中华外科杂志2013;28(增刊3):S660-5。
Garg S, Williams NL, Ip A, Dicker AP.医疗保健中数字解决方案的临床整合:癌症护理中数字技术的现状概述。JCO临床癌症通报。2018;2:1-9。
丁乐C,创R, Chokshi S, Mann D.可穿戴健康技术与电子健康记录集成:范围回顾与未来方向。JMIR移动健康Uhealth. 2019;7(9):e12861。
委员会给欧洲议会、理事会、欧洲经济和社会委员会以及各区域委员会的来文;欧洲数据战略。https://ec.europa.eu/info/sites/default/files/communication-european-strategy-data-19feb2020_en.pdf.
Khoury MJ, Bowen MS, Clyne M, Dotson WD, Gwinn ML, Green RF,等。从公共卫生基因组学到精准公共卫生:20年历程。国际医学杂志,2018;20(6):574-82。
Robertson AS, Malone H, Bisordi F, Fitton H, Garner C, Holdsworth S,等。药品监管中基于云的数据系统:行业视角。新药品发现2020;19(6):365-6。
Khozin S, Pazdur R, Shah A. INFORMED:美国FDA的孵化器,旨在推动数据科学和敏捷技术的创新。新药研究。2018;17(8):529-30。
周勇,王峰,唐杰,Nussinov R,程峰。人工智能在新冠肺炎药物再利用中的应用。《柳叶刀》手指健康杂志2020;2(12):e667-76。
Ting DSW, Carin L, Dzau V, Wong TY.数字技术与COVID-19。中华医学杂志2020;26(4):459-61。
史俊,肖勇,张勇,耿东,丛东,史kx,等。COVID-19大流行期间药物开发面临的挑战:临床试验设计的关键考虑因素中国临床药物杂志,2020;87(5):2170-85。
2021年5月m日:大流行后世界的研究和医学趋势。中华医学杂志2020;26(12):1808-9。
苏勇,陈东,袁东,Lausted C,崔杰,戴春林,等。多重组学解决了COVID-19轻度和中度疾病状态的急剧转变。细胞。2020;183(6):1479 - 95。
Barh D, Tiwari S, Weener ME, Azevedo V, Goes-Neto A, Gromiha MM,等。基于多组学的SARS-CoV-2感染生物学鉴定和抗COVID-19候选药物《计算机生物医学》2020;126:104051。
舒涛,宁伟,吴东,徐娟,韩强,黄敏,等。血浆蛋白质组学识别COVID-19的生物标志物和发病机制。免疫力。2020;53(5):1108 - 22所示。
Whetton AD, Preston GW, Abubeker S, Geifman N.蛋白质组学和信息学,用于了解COVID-19疾病的阶段和识别生物标志物。中国生物医学工程学报,2016;19(11):419 - 432。
张凯,刘旭,沈娟,李忠,桑勇,吴旭,等。应用计算机断层扫描技术对COVID-19肺炎进行准确诊断、定量测量和预后预测的临床应用AI系统。细胞。2020;181(6):1423 - 33所示。
金超,陈伟,曹勇,徐震,谭震,张旭,等。新冠肺炎诊断人工智能系统开发与评估。自然科学进展。2020;11(1):5088。
Weisberg E, Parent A, Yang PL, satler M,刘q,刘q,等。重新利用激酶抑制剂治疗COVID-19。Pharm res 2020;37(9):167。
黄志强,何德泰,谭亚仁,周敏,刘亚敏,唐梅,等。使用可穿戴生物传感器在检疫对象中早期检测COVID-19的人工智能移动健康平台:随机对照试验协议。英国医学公开赛。2020;10(7):e038555。
Depil S, Duchateau P, Grupp SA, Mufti G, Poirot L.“现成的”异体CAR - T细胞:发展和挑战。新药品发现2020;19(3):185-99。
Cavazzana M, Bushman FD, Miccio A, Andre-Schmutz I, Six E.靶向造血干细胞治疗遗传性疾病的基因治疗:进展与挑战。新药品发现2019;18(6):447-62。
高KA, Roncarolo MG。基因治疗。中华实用医学杂志,2019;26(5):455 - 464。
Lai AC, Crews CM。诱导蛋白质降解:一种新兴的药物发现范式。新药品发现,2017;16(2):101-14。
Sahin U, Kariko K, Tureci O.基于mrna的治疗方法——开发一类新的药物。中国医药科学,2014;13(10):759-80。
Pardi N, Hogan MJ, Porter FW, Weissman D. mRNA疫苗——疫苗学的新时代。新药品发现,2018;17(4):261-79。
Berkers G, van Mourik P, Vonk AM, Kruisselbrink E, Dekkers JF, de Winter-de Groot KM,等。直肠类器官可实现囊性纤维化的个性化治疗。2019;26(7): 1701-8。
确认
感谢诺华和罗氏的所有同事参与相关讨论。
资金
由Projekt DEAL启动和组织的开放获取资金。本出版物尚未收到任何资助。
作者信息
作者及隶属关系
贡献
DH对稿件进行了起草、概念化和整体监督,VdL、SC、EF、RS、MF、SA、LP对具体章节进行了贡献和修改,AK对稿件进行了修改,JL对稿件进行了修改。JM修改了手稿,AS修改了手稿,MH修改了手稿。所有作者都阅读并批准了最终的手稿。
相应的作者
道德声明
伦理批准并同意参与
不适用。
发表同意书
不适用。
相互竞争的利益
作者宣称不存在利益竞争。DH, VdL, AK, JL, SC, EF, RS, MF和MH为诺华工作,LP和AR为罗氏工作。
额外的信息
出版商的注意
伟德体育在线施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可协议中,除非在材料的信用额度中另有说明。如果材料未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。如欲查看本牌照的副本,请浏览http://creativecommons.org/licenses/by/4.0/.创作共用公共领域奉献弃权书(http://creativecommons.org/publicdomain/zero/1.0/)适用于本条所提供的资料,除非在资料的信用额度中另有说明。
关于本文
引用本文
哈特尔,D,德卢卡,V,科斯蒂科娃,A。et al。精准转化医学:行业视角。翻译医学杂志19, 245(2021)。https://doi.org/10.1186/s12967-021-02910-6
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/s12967-021-02910-6
关键字
- 转化医学
- 精密医学
- 药物开发
- 生物标记物
- Multi-omics
- 建模
- 人工智能
- 制药行业
- 数字生物标志物
- 同伴诊断