摘要
背景
部分新冠肺炎患者出院后再次检测SARS-CoV-2 RNA阳性,有或无发热、干咳等临床症状。
方法
选择1008例经鼻咽拭子和口咽拭子混合标本实时荧光定量PCR (RT-qPCR)检测SARS-CoV-2 RNA阳性的重症COVID-19患者,在住院期间采用RT-qPCR对12种标本进行SARS-CoV-2 RNA监测。选择20例新型冠状病毒肺炎出院患者,在释放隔离期前,采用RT-qPCR检测7种标本的SARS-CoV-2 RNA。
结果
在纳入的1008例重症患者中,鼻咽拭子标本中SARS-CoV-2 RNA阳性率最高(71.06%),其次为肺泡灌洗液(66.67%)、口咽拭子(30.77%)、痰液(28.53%)、尿液(16.30%)、血液(12.5%)、粪便(12.21%)、肛拭子(11.22%)、角膜分泌物(2.99%),其他类型标本均未检出SARS-CoV-2 RNA。在隔离期间出院的20例病例中,SARS-CoV-2 RNA阳性率为30% (6/20):2例阳性痰在第八和第九天出院后,分别在鼻咽拭子1例是积极的在放电后第六天,1例是积极在肛门拭子在放电后第八天,和3 1例是积极的标本(鼻咽拭子、口咽拭子和痰)同时在放电后第四天,并没有积极SARS-CoV-2 RNA检测粪便等标本,在出院病人尿液和血液。
结论
应在鼻咽拭子、口咽拭子、痰液等多个标本中检测新冠病毒RNA,必要时在患者出院时考虑临床治愈和隔离期释放前同时进行粪便和肛门拭子标本检测。
简介
在过去的几个月里,2019冠状病毒病(COVID-19)已成为一种大流行,截至2020年5月22日,超过215个国家、地区或领土报告了4,962,707例确诊病例和326,459例死亡(数据来自约翰霍普金斯大学COVID-19仪表板网站)[1,2,3.].此外,目前还没有治疗COVID-19的特异性药物或疫苗[4,5因此,控制和减少传染源是抗击疫情的关键措施。
严重急性呼吸综合征冠状病毒2型(SARS-CoV-2) [6],在鼻咽拭子、口咽拭子、痰液、粪便、肛拭子、外周血等多种标本中均检出新冠病毒[7,8].COVID-19患者症状符合临床治愈标准,且连续2例呼吸道标本实时荧光定量PCR (RT-qPCR)检测SARS-CoV-2 RNA阴性(采样时间间隔至少1天)时即可出院[9].然而,有报道称,在一些COVID-19康复患者中,检测到的病毒RNA结果转为“阳性”[10,11].目前尚不清楚这些患者是否因假阴性结果出院或再次感染。迫切需要完善病毒RNA检测标准,以监测疾病进展和出院患者。
本研究的目的是描述COVID-19患者出院时的恢复阳性,即SARS-CoV-2 RNA未完全清除。首先,对住院新型冠状病毒肺炎患者鼻咽拭子、口咽拭子、痰液、支气管肺泡灌洗液(BALF)、粪便、肛拭子、尿液、腹膜透析液(PDF)、血液、汗液、脑脊液(CSF)、角膜分泌物等12种不同类型标本进行病毒RNA检测,分析其可能感染部位。此外,我们对临床治愈的COVID-19患者进行了鼻咽拭子、口咽拭子、痰液、血液、粪便、肛拭子和尿液等7种不同标本的相同检测,以评估是否适合设定鼻咽拭子病毒RNA检测持续阴性的出院标准。
材料与方法
病人
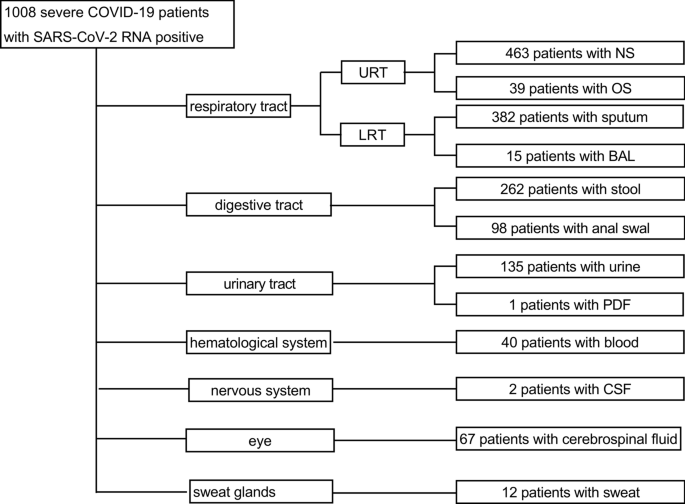
选择2020年2月1日至2月28日在武汉大学人民医院东分院住院的SARS-CoV-2 RNA RT-qPCR法检测阳性的重症COVID-19患者,采用鼻咽拭子和口咽拭子混合标本共1008例。COVID-19诊断标准参照《2019中国冠状病毒病诊疗指南(第七版)》[12].重症患者应符合以下任何一项标准:(1)呼吸窘迫(≧30次/分钟);(2)静止时氧饱和度≤93%;(3)动脉血氧分压(PaO2)/吸入氧分数(FiO .2)≦300mmhg (l mmHg = 0.133 kPa)。在高海拔地区(海拔1000米以上),PaO2/ FiO2应按以下公式校正:PaO2/ FiO2×[大气压(mmHg)/760]。胸部影像学显示24-48 h内病变进展明显> 50%;(4)呼吸衰竭,需要机械通气;(5)冲击;(6)其他器官功能衰竭,需要ICU监护。根据患者的诊断和症状,采集患者上呼吸道(鼻咽和口咽)、下呼吸道(痰液和肺泡灌洗液)、消化系统(肠道和肛门)、泌尿系统(尿液)、血液系统(外周血)、结膜(结膜分泌物)、神经系统(脑脊液、CSF)、腹膜透析液(PDF)、新冠肺炎住院患者的角膜分泌物和汗腺(汗液)(图2)。1).所有标本均采集于重症患者住院第一天至最后一天。本研究由武汉大学人民医院伦理委员会批准(WDRY2020-K078),无需知情同意。
新冠肺炎出院病例20例,标准[12为临床治愈后达到隔离期(14天)标准的患者,连续2份呼吸道标本(至少采样时间间隔1天)检测SARS-CoV-2病毒RNA阴性,在隔离期选取鼻咽拭子、口咽拭子、痰、粪便、肛拭子、尿液和血液等多份标本检测SARS-CoV-2病毒RNA。本研究由武汉大学人民医院伦理委员会批准(WDRY2020-K078),并获得患者书面知情同意。
标本采集和预处理
所有采集的标本均在RNA提取前进行预处理。用淋巴细胞分离缓冲液从外周血标本中分离出外周血单个核细胞。尿液标本在3500rpm下离心20分钟,得到沉积物。用4% NaOH液化痰液5分钟。将豆大小的粪便标本与生理盐水混合。所有拭子标本均与细胞储存缓冲液混合并涡旋5至10秒。
RT-qPCR检测SARS-CoV-2 RNA
使用磁珠RNA提取试剂盒(Health Gene Technologies, Ningbo, China)和SuperPure全自动核酸提取仪(Fosun Pharma, Shanghai, China)根据制造商的方案提取样本中的RNA。采用SARS-CoV-2 RT-qPCR试剂盒(上海汇瑞生物科技有限公司,中国上海)和Roche Light Cycler 480 (Roche,巴塞尔,瑞士)检测SARS-CoV-2 ORF1ab基因、N基因和内部标记基因的表达。Ct值小于40的标本为阳性。本研究在标本中随机放置3个阴性对照、1个阳性对照和1个弱阳性同时检测。
统计分析
变量的描述性分析用数字(%)表示。符合正态分布的测量数据用均数±标准差(Mean±SD)表示。
结果
新型冠状病毒肺炎住院患者12种标本SARS-CoV-2 RNA检测
SARS-CoV-2病毒可以攻击人体不同的组织和器官。为了解新冠肺炎重症患者鼻咽拭子463例(30.54%),口咽拭子39例(2.57%),痰382例(25.20%),BALF 15例(0.99%),粪便262例(17.28%),肛拭子98例(6.46%),尿液135例(8.91%),腹膜液1例(0.07%),血液40例(2.64%),脑脊液2例(0.13%),角膜分泌物67例(4.42%),汗液12例(0.79%)。1).
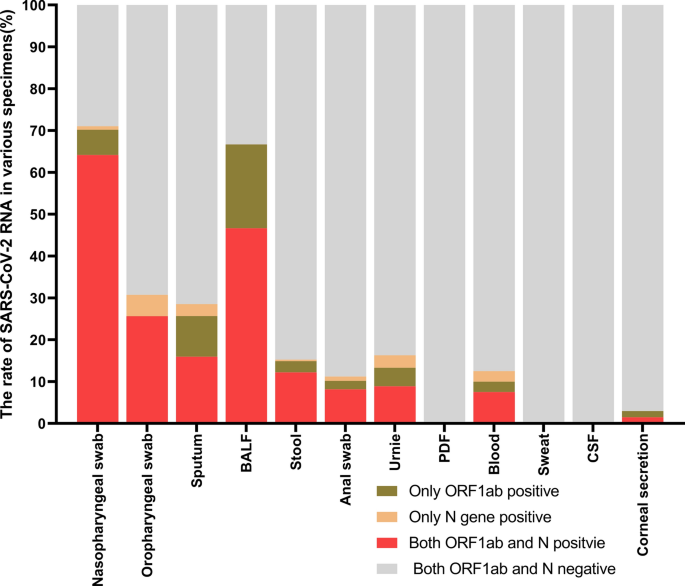
对1008例新冠肺炎住院患者的12种标本进行SARS-CoV-2 RNA检测(表2)1).ORF1ab基因和N基因双阳性的鼻咽拭子为64.15% (297/463),BALF为46.67%(7/15),口咽拭子为25.64%(10/39),痰为15.97%(61/382),粪便为12.21%(32/262),尿液为8.89%(12/135),肛拭子为8.16%(8/98),血液为7.50%(3/40),角膜分泌物为1.49%(1/67)(图)。2).ORF1ab基因或N基因单次阳性在BALF中分别为20.00%(3/15)、痰中12.57%(48/382)、尿中7.40%(10/135)、鼻咽拭子中6.91%(32/463)、口咽拭子中5.13%(2/39)、血液中5.00%(2/40)、粪便中3.05%(8/262)(图)。2).PDF和CSF标本均未检测到SARS-CoV-2 RNA。
新型冠状病毒肺炎出院患者7种标本SARS-CoV-2 RNA的检测
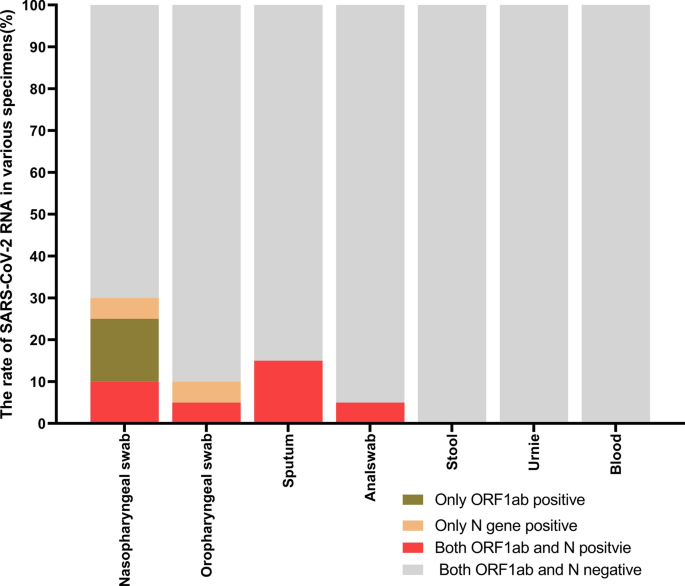
为了解释所谓恢复阳性的原因,我们进一步分析了20例COVID-19出院患者在隔离时间(14天)内的鼻咽拭子、口咽拭子、痰、粪便、肛拭子、尿液和外周血7种标本。SARS-CoV-2 RNA阳性时间为出院后8.1±3.4天,从出院后4天到出院后14天不等2).6例患者鼻咽拭子中至少有一个基因的病毒RNA阳性,2例ORF1ab和N基因均阳性,3例仅ORF1ab阳性,2例N基因阳性。5例至少在1个标本中同时检测到ORF1ab和N基因RNA双阳性,痰2例,鼻咽拭子1例,肛拭子1例,3个标本(鼻咽拭子、口咽拭子和痰)同时检测到1例。20例出院患者的粪便、尿液和血液标本均未检测出SARS-CoV-2 RNA阳性(表1)2).
20例患者在隔离期间,鼻咽拭子、口咽拭子、痰液和肛拭子的新冠病毒阳性率分别为30%(6/20)、10%(2/20)、15%(3/20)和5%(1/20)。25%(5/20)的病例至少在一个标本中同时出现ORF1ab和N基因RNA双阳性(图。3.).
讨论
越来越多的证据表明,SARS-CoV-2 RNA不仅可以在呼吸道中检测到,还可以在胃肠道中检测到[7,13].本研究对1008例住院重症COVID-19患者进行呼吸道、胃肠道、泌尿系统、血液、眼睛、神经系统和汗液12种标本检测,检测出SARS-CoV-2 RNA阳性。鼻咽拭子标本阳性率最高(71.06%),其次为BALF(66.67%)、口咽拭子(30.77%)、痰液(28.53%)、血液(12.5%)、粪便(12.21%)和肛拭子(11.22%)。尿液中也发现了SARS-CoV-2(16.30%)。我们在各种组织中病毒阳性率结果的这些特征与之前的研究有很大不同[14].本研究中,鼻咽拭子中SARS-CoV-2 RNA阳性率最高,为71.06%,其次为BALF中66.67%,口咽拭子中30.77%,痰中28.53%,尿液中16.30%,血液中12.50%,粪便中12.21%,肛拭子中11.22%,角膜分泌物中2.99%。这些结果表明标本应先采集鼻咽拭子,再采集口咽拭子,然后采集痰液、粪便、肛拭子或血液。支气管插管患者可在住院期间采集BALF标本。疑似COVID-19患者如有眼部症状,可采集角膜分泌物标本。
部分患者出院1个月或更长时间后SARS-CoV-2 RNA恢复阳性。目前迫切需要了解病毒RNA恢复阳性是二次感染所致,还是患者自身未治愈所致。因此,对于临床治愈后达到隔离时间标准(14天)并治疗出院的患者,我们的数据引发了讨论的焦点,是否适合仅对连续2个呼吸道标本(至少采样时间间隔1天)进行病毒RNA检测[9].在本次研究中,在呼吸道、胃肠道、泌尿系统、血液和眼睛中发现了SARS-CoV-2 RNA,这意味着这种病毒可能出现在人体内的几乎所有地方。针对临床治愈但仍处于隔离期的20例患者,根据其器官感染情况及样本采集方便,选取鼻咽拭子、口咽拭子、痰液、粪便、肛拭子、尿液、血液7种标本,同时检测新型冠状病毒RNA。
20例出院患者中,5例ORF1ab基因和N基因RNA同时表达阳性,其中痰2例阳性,鼻咽拭子1例阳性,肛拭子1例阳性,3个标本(鼻咽拭子、口咽拭子和痰)1例同时阳性。这5例患者被诊断为SARS-CoV-2携带者。这一结果表明,虽然符合出院标准,但新冠病毒恢复阳性可能表明患者当时出院时尚未完全治愈。结果似乎不支持病毒再次感染的可能性。因此,目前的出院标准可以根据临床结果进行改进,仅在呼吸道标本中检测SARS-CoV-2 RNA似乎不太充分。患者出院前需采集多种类型标本检测病毒RNA,但可能符合临床治愈标准。一旦患者在隔离时间内检测出SARS-CoV-2 RNA阳性,建议再隔离14天,直到7种标本的病毒RNA均为阴性。
我们在本研究中使用的7种标本可能是一个很好的选择,但如果患者同时患有其他疾病,也可能会扩大额外入组标本的研究范围。此外,需要纳入更大的样本,以排除我们队列中含有SARS-CoV-2 RNA的腹膜液和脑脊液的可能性。除上述5例外,另有1例(表P8)2)在隔离期间仅检出鼻咽拭子ORF1ab基因RNA和口咽拭子N基因RNA,该患者不符合病毒携带者标准。这可能表明SARS-CoV-2病毒已经死亡,正在被患者清除。已知重症患者呼吸道标本RNA检测假阴性是不可避免的[15].因此,应同时对多种标本进行分析,排除出院患者再次成为传染源的可能性。
结论
SARS-CoV-2可能存在于来自不同组织器官的不同标本中。新型冠状病毒肺炎患者出院时,需要在多种标本中检测SARS-CoV-2 RNA。建议在释放隔离期前检测SARS-CoV-2 RNA,以避免假阴性患者出院。
数据和材料的可用性
在这项研究中产生或分析的所有数据都包含在这篇发表的文章中。
缩写
- COVID-19:
-
2019冠状病毒病
- SARS-CoV-2:
-
严重急性呼吸综合征冠状病毒
- RT-qPCR:
-
实时荧光定量PCR
- PBMCs:
-
外周血单个核细胞
- CSF:
-
脑脊髓液
- PDF格式:
-
腹膜透析液
参考文献
黄超,王勇,李霞,任玲,赵娟,胡勇,张磊,范刚,徐娟,顾鑫,等。武汉地区新型冠状病毒感染患者临床特征分析《柳叶刀》杂志。2020;395:497 - 506。
周鹏,杨晓玲,王小刚,胡斌,张磊,张伟,司海仁,朱勇,李波,黄春林,等。与一种可能来自蝙蝠的新型冠状病毒有关的肺炎爆发。大自然。2020;579:270-3。
吴震,McGoogan JM。中国2019冠状病毒病(COVID-19)暴发的特征和重要教训:中国疾病预防控制中心72314例病例报告摘要《美国医学协会杂志》上。2020; 323:1239-42。
卢生。及时研制新型冠状病毒疫苗。新兴微生物感染,2020;9:542-4。
庞杰,王明明,Ang IYH, Tan SHX, Lewis RF,陈吉,Gutierrez RA, Gwee SXW, Chua PEY,杨强,等。2019新型冠状病毒(2019- ncov)潜在的快速诊断、疫苗和治疗方法:系统综述中华临床医学杂志2020;9:623。
与严重急性呼吸综合征相关的冠状病毒:将2019-nCoV分类并命名为SARS-CoV-2。生物学报。2020;5:536-44。
陈伟,兰勇,袁旭,邓旭,李勇,蔡旭,李林,何锐,谭勇,邓旭,等。血液中检测到2019-nCoV病毒RNA是进一步临床严重程度的有力指标。新兴微生物感染,2020;9:469-73。
陈楠,周敏,董霞,曲娟,龚芳,韩艳,邱艳,王娟,刘艳,魏勇,等。武汉市99例2019年新型冠状病毒肺炎的流行病学和临床特征:描述性研究《柳叶刀》杂志。2020;395:507-13。
金玉华,蔡林,程志生,程宏,邓涛,范亚平,方超,黄东,黄丽青,黄强,等。新型冠状病毒感染的肺炎诊疗快速建议指南(标准版)Mil Med res 2020;7:4。
曹慧,阮兰,刘娟,廖伟。8例COVID-19患者出院后RT-PCR检测阳性的临床特征J医学病毒,2020年。https://doi.org/10.1002/jmv.26017.
兰玲,徐东,叶刚,夏超,王松,李勇,徐慧。新型冠状病毒肺炎康复患者RT-PCR检测结果阳性。《美国医学协会杂志》上。2020; 323:1502-3。
2019冠状病毒病诊疗指南(第七版)中国国家卫生健康委员会。https://exploreim.ucla.edu/covid19/chinas-national-health-commission-guidelines-for-covid-19-treatment-2-2/).
彭玲,刘娟,徐伟,罗强,陈东,雷铮,黄铮,李霞,邓凯,林斌,高哲。新型冠状病毒可在尿液、血液、肛拭子和口咽拭子标本中检测到。J医学病毒,2020年。https://doi.org/10.1002/jmv.25936.
王伟,徐勇,高锐,卢锐,韩凯,吴刚,谭伟。不同类型临床标本SARS-CoV-2的检测。《美国医学协会杂志》上。2020; 323:1843-4。
肖婷婷,童艳霞,张松。COVID-19 RT-PCR假阴性与延长核酸转化:而不是复发。J医学病毒,2020年。https://doi.org/10.1002/jmv.25855.
确认
不适用。
资金
本工作由宁夏回族自治区重点研发计划专项科技合作项目(2018BFG02008)、宁夏回族自治区新型冠状病毒肺炎疫情防控专项(2020BEG01004)资助。
作者信息
作者及隶属关系
贡献
LY, WHM和ZZJ提出了研究思路。TYQ、BAY和CHB参与了文献综述。本研究由LY、WHM、ZZJ和TYQ共同设计。数据采集采用HJT、LZH、FLN和ZHY进行。数据分析由ZHY, WZG, CY, WYN和CHB进行。分子分析采用HJT、LZH、FLN、BL和QB。图和表格由TYQ, BAY和CHB创建。所有作者都对撰写最后报告作出了贡献。所有作者已对所提交的手稿的全部内容承担责任,并已批准提交。所有作者都阅读并批准了最终的手稿。
相应的作者
道德声明
伦理批准并同意参与
本研究获得武汉大学人民医院伦理委员会批准(WDRY2020-K078)。
发表同意书
获得患者的书面知情同意。
相互竞争的利益
作者宣称他们之间没有利益冲突。
额外的信息
出版商的注意
伟德体育在线施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可协议中,除非在材料的信用额度中另有说明。如果材料未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。如欲查看本牌照的副本,请浏览http://creativecommons.org/licenses/by/4.0/.创作共用公共领域奉献弃权书(http://creativecommons.org/publicdomain/zero/1.0/)适用于本条所提供的资料,除非在资料的信用额度中另有说明。
关于本文
引用本文
童,Y,鲍,A,陈,H。et al。新型冠状病毒肺炎(COVID-19)患者出院时多种标本中检测SARS-CoV-2 RNA的必要性翻译医学杂志18, 411(2020)。https://doi.org/10.1186/s12967-020-02580-w
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/s12967-020-02580-w
关键字
- 新型冠状病毒肺炎
- SARS-CoV-2
- RT-qPCR
- 多个样本
- 排放标准