摘要
背景
在重症监护室(ICU),机械通气(MV)是挽救患者生命的常用手段。然而,呼吸机诱导的膈功能障碍(VIDD)会阻碍危重患者的脱机并恶化预后,从而使治疗复杂化。本研究的目的是鉴定参与VIDD内源性保护机制的潜在基因。
方法
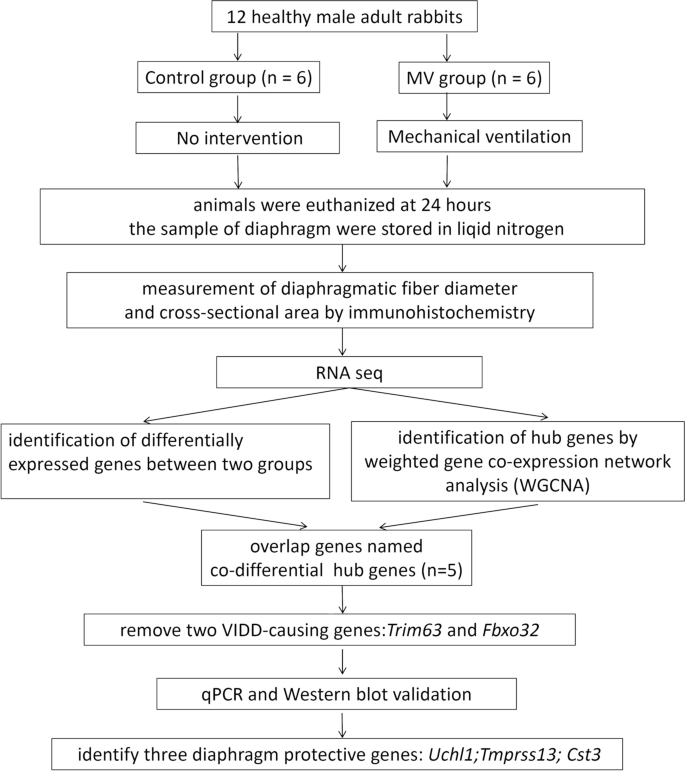
在相同麻醉条件下,将12只成年雄性兔子分为MV组和对照组。免疫染色和定量形态测定法用于评估膈肌萎缩,RNA-seq用于研究两组之间的分子差异。此外,利用WGCNA分析了核心模块和轮毂基因,并通过将差异表达基因(DEGs)与WGCNA中的轮毂基因重叠,发现了共差异表达的轮毂基因。通过western blotting (WB)和定量实时聚合酶链式反应(qRT-PCR)对鉴定的基因进行鉴定。
结果
在成功建立VIDD模型后,在MV组和对照组之间发现了1276个deg。绿松石色和黄色模块被确定为核心模块Trim63,Fbxo32,Uchl1,Tmprss13,Cst3被鉴定为5个共差异表达的中枢基因。在两个萎缩相关基因(Trim63而且Fbxo32),其余三个基因/蛋白质(Uchl1/ UCHL1,Tmprss13/ TMPRSS13,Cst3/CST3)均在MV组显著升高(P< 0.05),提示存在潜在的抗蛋白酶体、抗凋亡和抗自噬机制对抗隔膜功能障碍。
结论
目前的研究有助于揭示一种潜在的重要的内源性保护机制,可以作为对抗VIDD的新的治疗靶点。
背景
在2019冠状病毒病(COVID-19)大流行期间,机械通气对于挽救严重低氧性呼吸衰竭患者至关重要[1].然而,涉及大鼠模型的研究表明,短至12小时的MV周期可以减少膈肌纤维的大小,并在称为呼吸机诱导膈肌功能障碍(VIDD)的情况下减少膈肌中特定力的产生[2].VIDD的主要特征是早期膈肌收缩能力丧失,随后出现肌肉萎缩[3.,4].在一些患者中,废用引起的萎缩甚至可导致膈肌厚度平均每天减少6% [5].此外,VIDD的发展与许多并发症相关,包括呼吸机相关性肺炎,医院死亡率增加,危重患者临床预后差,使呼吸机的停用越来越困难[6,7].
鉴于VIDD是由蛋白质合成受损和蛋白质水解增加引起的,了解这些过程对于保护隔膜至关重要[8].在这种情况下,有报道称,在MV 12小时后,通过破坏胰岛素样生长因子(IGF)/蛋白激酶B (AKT)/哺乳动物雷帕霉素靶点(mTOR)信号通路,隔膜内的蛋白质合成下调[9].此外,在MV期间,线粒体中活性氧(ROS)水平的增加可以激活膈内所有主要的蛋白水解系统(钙蛋白酶系统、凋亡、泛素-蛋白酶体系统[UPS]和自噬),这一过程对蛋白水解有显著的贡献[10,11].结果,横膈膜蛋白质稳态被破坏,导致肌肉萎缩。在细胞过程中,UPS保证蛋白质质量控制和稳态。然而,对大鼠和人类膈肌的研究表明,MV导致肌肉特异性E3连接酶(atrogin1/muscle atrophy F-box和MuRF1/muscle无名指-1)表达增多[12],也有报道称会导致20S蛋白酶体活性增加[13].总之,这些发现表明,MV诱导UPS在膈肌中被越来越多地激活。另一个可能参与VIDD的分解代谢过程是自噬,其中细胞质蛋白和细胞器被溶酶体降解。MV已被证明可以增加人类和动物膈肌的自噬,由于过氧化氢酶和过氧化物酶体的清除,这最终会损害细胞的抗氧化能力。另一项研究发现,一些主要的自噬基因(beclin1,Atg7,Atg5)均被MV上调,自噬体标记物微管相关蛋白轻链3-II (LC3B)的表达也随之增加[14,15],支持了自噬对VIDD确实至关重要的观点。另有证据表明MV甚至可以通过激活caspase-3引起大鼠膈肌细胞凋亡[16,它是一种半胱氨酸蛋白酶,可以进一步激活核酸酶,破坏双链DNA,导致肌核的丢失。在人类MV的情况下,凋亡过程也由bcl2相互作用的细胞死亡中介物(Bim)介导[17].这些结果进一步证明细胞凋亡参与了VIDD的进展。Calpain激活是通过促进快速蛋白水解直接参与VIDD的另一个因素。例如,在肌浆网(SR)中,ryanodine受体/Ca的修饰2 +由于线粒体的高水平ROS导致Ca的释放通道2 +SR和钙酸钙的激活[18].此外,作为一种通过将靶蛋白裂解为生理活性片段来协助细胞通讯的特化蛋白酶,calpains可能在隔膜纤维的细胞质内起作用,将PKC-δ和DRP1裂解为片段,随后参与mv诱导的线粒体功能障碍[19].总的来说,上述发现支持这样的观点,即膈肌mv相关纤维萎缩是由于高水平的活性calpains引起的蛋白水解增加,UPS活性升高,凋亡和自噬增加。
虽然许多研究都考虑了VIDD背后的过程,但只有少数研究了针对VIDD的内生保护机制。在此背景下,一项对新生羔羊膈肌MV期间的研究表明,组蛋白去乙酰化酶Sirtuin1 (Sirt1)作为一种保护因素,通过下调导致萎缩的基因,如Atrogin1而且Murf1[20.].同样,由于压力引起的热休克蛋白(HSPs)水平的增加对于防止肢体肌肉因固定而损失至关重要。通常,膈肌HSPs负责维持肌肉完整性,促进肌肉再生和恢复,特别是HSP72可以通过抑制核因子κB (NF-κB)和叉头盒O (FoxO)等转录因子的活性来降低细胞的氧化应激,从而预防VIDD [21,22].在VIDD中,肾素-血管紧张素系统(RAS)通过其主要肽血管紧张素II引起氧化应激并诱导萎缩。然而,RAS也具有反调节轴,其中肽血管紧张素(1-7)减少氧化应激和蛋白水解,从而防止VIDD的发生[23,24].虽然先前的研究结果清楚地表明,SIRT1、HSP72和血管紧张素(1-7)对于维持VIDD中的膈功能至关重要,但在MV期间保护膈的内在抗自噬、抗凋亡和抗蛋白酶体机制尚不清楚。因此,识别可能参与上述保护机制的标志基因是很重要的。
2005年,加权基因共表达网络分析(WGCNA)被提出作为一种基于基因子集之间的相互联系及其与表型关联的识别潜在生物标志物的方法[25].通过这种方法,一组研究人员确定了涉及肌肉萎缩的三种mrna的共表达网络(Myog,Trim63,Fbxo32)和一些新发现的长非编码rna (NONRATT026958.2, NONRATT026957.2和NONRATT008228.2等),这些rna对VIDD至关重要[26].在本研究中,除了通过高通量RNA测序(RNA-seq)来识别对照组(CON)和MV处理组之间的差异表达基因(DEGs)外,还进行了WGCNA来探索MV后膈肌中的核心模块。通过将核心模块中的deg基因和枢纽基因重叠,确定了一组共同基因,标记为共差异表达的枢纽基因。虽然膈肌转录组已在MV模型中进行了分析,并且已经研究了特定mirna的活性[27],但对于对抗VIDD的潜在内部保护机制知之甚少。因此,基于高通量RNA-seq和WGCNA,本研究旨在揭示膈肌中可能参与MV内源性机制的共差异表达的中枢基因。
方法
动物
体重2.2至2.5公斤的成年雄性兔子来自山西医科大学(中国太原),并被安置在12小时明暗循环的环境中,不受限制地获得食物和水。动物实验经长治医学院伦理委员会批准,按照《实验动物护理与使用指南》进行。
呼吸机致膈肌功能障碍(VIDD)模型
12只成年雄性兔子随机分为两组。在对照组(n= 6)时,动物接受麻醉,但不保持通气,而在MV组(n= 6)时,给予MV 24 h(图;1).然后腹腔注射戊巴比妥钠(40 mg/kg)麻醉家兔,并使用电动泵连续输注(10 mg/kg/h)。接下来,进行气管造口术,将动物连接到小型呼吸机(Inspira ASVV 55-7058;Harvard Apparatus, Cambridge, MA, USA)在呼吸频率、潮气量(Vt)和呼气末正压为每分钟40次循环、6 mL/kg和2 cmH的条件下2分别啊。同时在颈静脉和颈动脉插管测量血压,持续给药。在整个通气过程中,使用恒温毯系统将动物体温维持在37°C,并监测动脉血气水平(ABL80 FLEX;Radiometer Medical, Carlsbad, CA, USA),以确保PaCO2在35到45毫米汞柱之间,PaO2在80到100毫米汞柱之间MV期结束后,处死两组动物。然后从右肋膈的中间部分快速取活检样本。保留一条用于组织学评估,其余的则在液氮中快速冷冻并保存在−80°C下,直到进一步分析。
组织措施
肌肉样本在4%多聚甲醛中固定后,用石蜡包埋并切成切片。随后,在用苏木精-伊红(HE)染色之前,对切片进行脱蜡和再水化。用2%牛血清白蛋白(BSA)阻断切片1 h,以小鼠抗快速肌球蛋白骨骼重链(ab51263, Abcam, Cambridge, UK)为一抗,4℃孵育过夜,PBS洗涤3次,再以山羊抗兔IgG (ab205719, Abcam)为二抗,室温孵育1 h。染色样本图像使用BX41显微镜(Olympus, Tokyo, Japan)获得,一名对样本基因型状态不知情的研究人员使用Image-Pro Plus 6.0版软件(Media Cybernetics, Bethesda, MD, USA)测量肌肉纤维的直径和截面积(CSA)。
RNA测序(RNA-seq)和生物信息分析
应用高通量RNA-seq研究mRNA表达的变化。TRIzol试剂(15596026;在Agilent 2100生物分析仪(Thermo Fisher Scientific, Waltham, MA, USA)测定RNA完整性之前,首先使用Ambion, Austin, TX, USA)从膈组织中提取总RNA。RNA完整性数(RIN)≥7作为后续实验的入选标准。在MGISEQ-2000测序平台上制备文库并测序后,在Dr. Tom平台上进行数据分析(http://report.bgi.com;华大基因科技服务有限公司,深圳)。MV组和对照组之间的deg随后被a问值< 0.05和|日志2FC| > 1为阈值。此外,通过火山图对DEGs的分布进行了说明,并通过热图对前40个DEGs进行了说明。使用R(4.0.5版本)中的WGCNA包(1.70-3)对与MV相关的核心模块中的hub基因进行了探索。模块特征基因(ME)是表示模块中共表达基因的主要成分。由于ME可以反映一个模块中所有基因的特征,因此使用Pearson相关检验对处理的二元状态(对照组和MV组的特征)与ME进行相关分析。具有P选取相关系数最高的值< 0.05。模块隶属度(MM)被定义为个体基因与ME之间的相关性。另外,基因显著性(GS)表示基因与群体特征之间的相关性。模块内的hub基因分别为MM>0.8和GS>0.8。维恩图工具(https://bioinfogp.cnb.csic.es/tools/venny/)进行核心模块中DEGs与hub基因的交集分析。构建共差异表达枢纽基因的共表达网络,然后使用Cytoscape 3.8.2进行可视化(www.cytoscape.org).
实时定量聚合酶链反应(qRT-PCR)
RNA-seq实验结果通过qRT-PCR对这三个基因进行验证Uchl1,Tmprss13,Cst3.按照上述方法提取总RNA,然后使用PrimeScript II逆转录酶(2690A, Takara Bio USA Inc., San Jose, CA, USA)合成cDNA。随后在CFX-Connect实时PCR检测系统(Bio-Rad, Hercules, CA, USA)上,将1 μL cDNA加入到SYBR FAST qPCR Master Mix试剂盒(KM4101, Kapa生物系统,Woburn, MA, USA)的20 μL反应混合物中,进行qRT-PCR。本实验以β-肌动蛋白为内控,对靶基因表达进行归一化处理,采用比较周期阈值法进行相对定量。结果表示为相对于控制值的折叠变化。引物序列(5 ' -3 ')如下:Uchl1,正向:GTCCCCTGAAGACAGAGCAAG,反向:GCATTCGCCCATCAAG;Tmprss13,正向:CATCATCAACGGCAACTACAC,反向:CGTCTGTCTCCTTGGTCTTG;而且Cst3,正向:GGCAGATCGTAAGTGGCG,反向:GTCGTGGAAAGGACAGTTGG。
Western blot分析
如前所述进行Western blotting [28].简单地说,使用RIPA裂解缓冲液(R0010, Solarbio科技有限公司,北京,中国)从肋膈组织中提取蛋白质,然后根据制造商的说明使用二氯二烯酸(BCA)蛋白测定法(PC0020, Solarbio)进行定量。然后用SDS-PAGE分离蛋白,转移到聚偏氟乙烯(PVDF)膜上,与以下一种一抗在4℃下孵育过夜:抗tmprss13 (JL-T0294,中国上海江莱)、抗uc - l1 (NBP2-29420,诺威生物,利特尔顿,CO,美国)、抗cst3 (C8950,美国生物公司,塞勒姆,马萨诸塞州,美国)或抗-β-肌动蛋白(PAB36265,中国武汉Bioswamp)。次日,以山羊抗兔IgG (SAB43714, Bioswamp)为二抗,室温孵育1 h。最后,利用Tanon GIS 4.2版(Tanon Technology, Shanghai, China)对western blot图像进行扫描和分析,以量化可见条带的密度,并将结果与β-actin的结果进行归一化。
统计分析
采用SPSS 25.0进行统计学分析。所有数据均以均数±标准差(SD)表示。标准的双尾t在5%显著性水平下,用检验分析两组均数的差异。将对照池表达设置为1,对PCR数据进行分析。
结果
VIDD模型建立
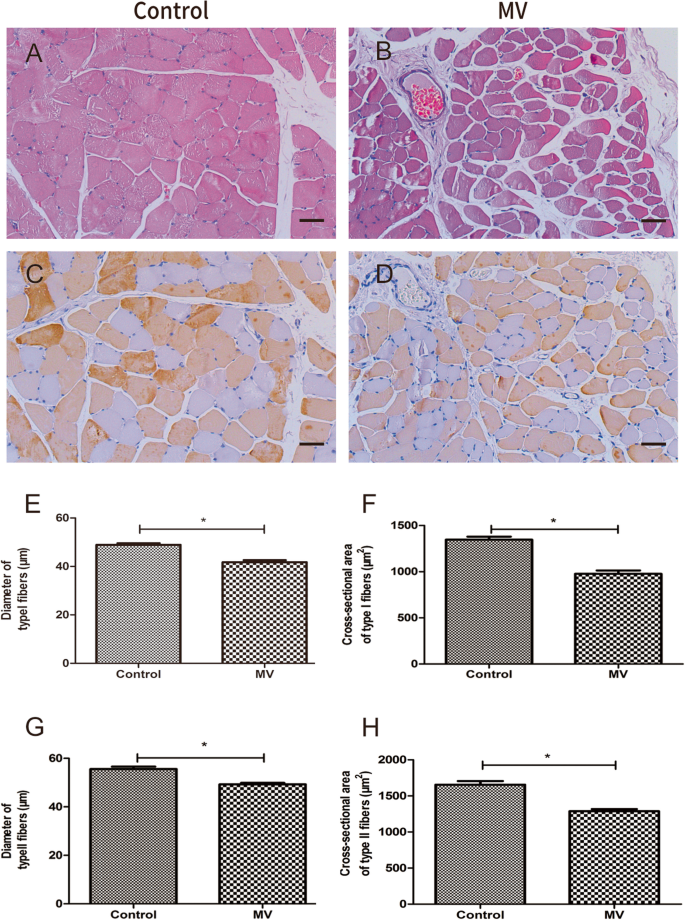
成功建立了VIDD模型。在MV之前,两组动物的体重没有发现显著差异。此外,如表所示1,两组生理参数无明显差异(P> 0.05),如动脉血氧分压(PaO2)和二氧化碳(PaCO2)、收缩压(SBP)、心率(HR)和pH值,表明这些参数在整个MV中保持相对恒定。然而,免疫组化结果显示,MV组膈肌快、慢肌纤维的CSA和直径明显低于对照组(图2)。2).
差异基因表达分析
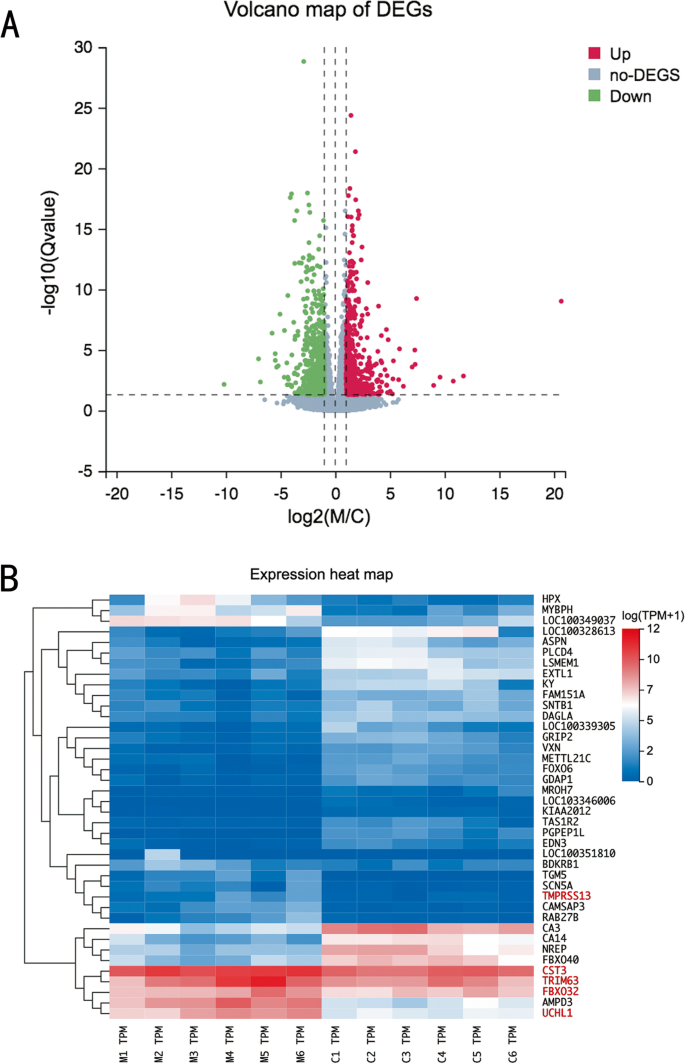
进行RNA-seq实验,以确定两组之间表达差异的基因。本研究共发现1276个deg,与对照组相比,MV组下调760个,上调516个。一个火山图被创建来显示所有的deg(图。3.此外,前40个deg在热图中进行了说明(图。3.B)。
WGCNA
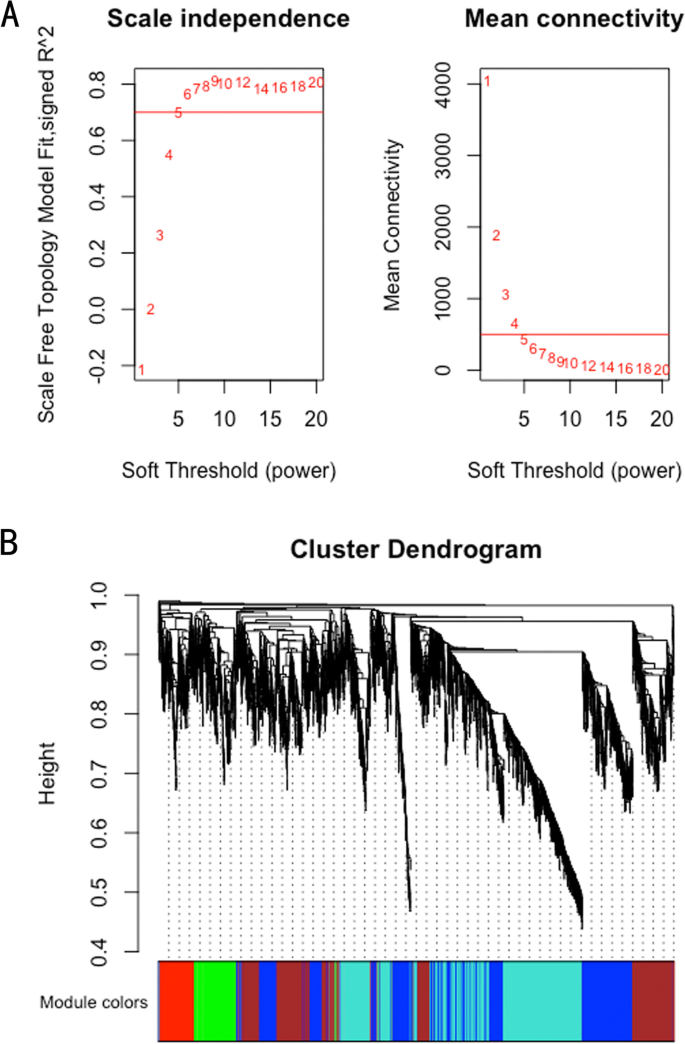
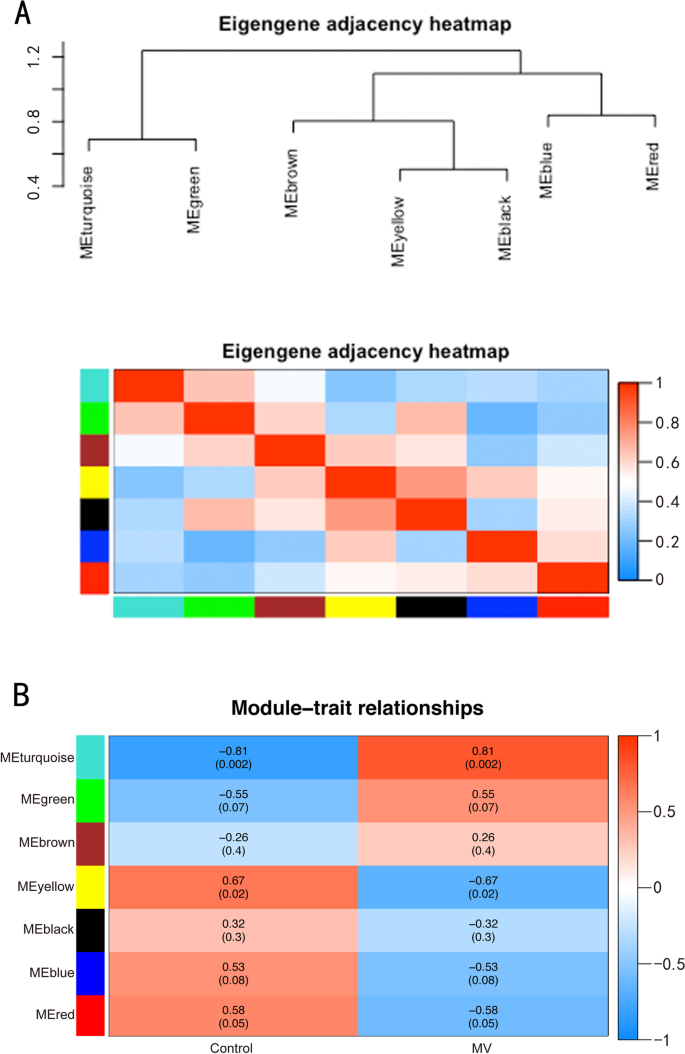
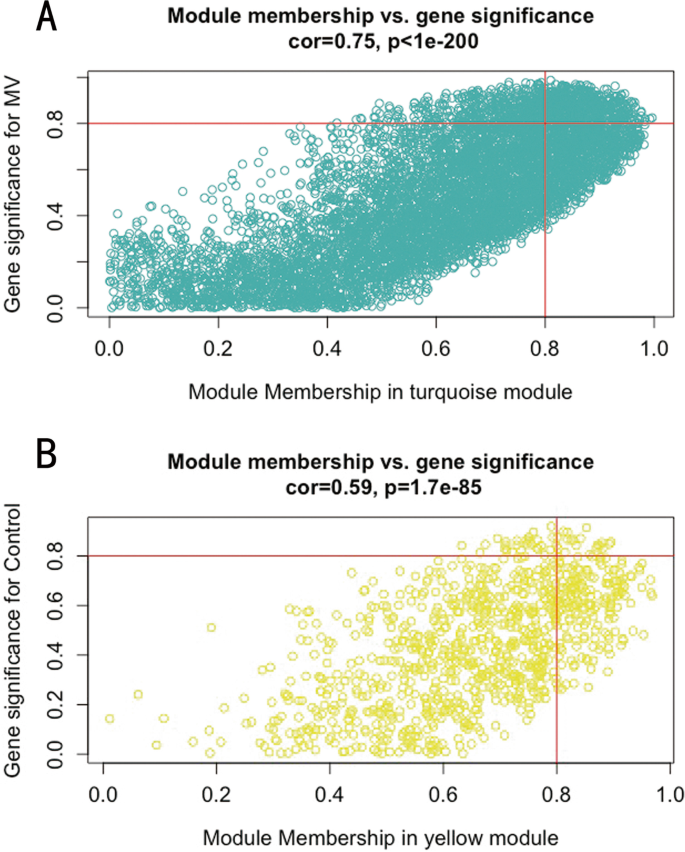
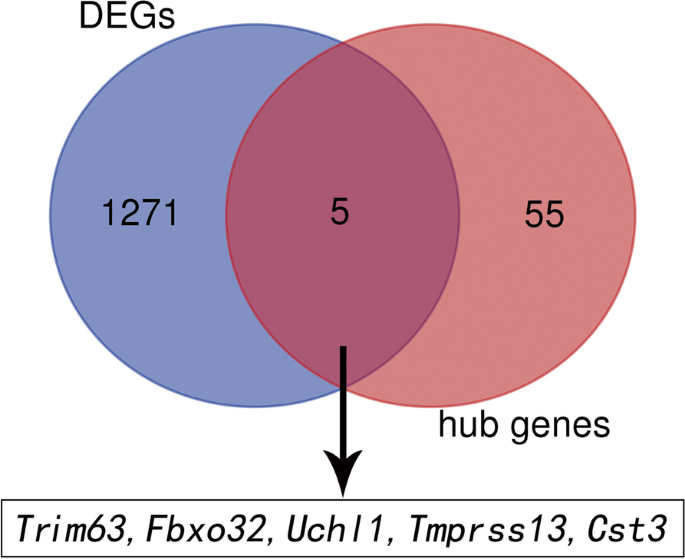
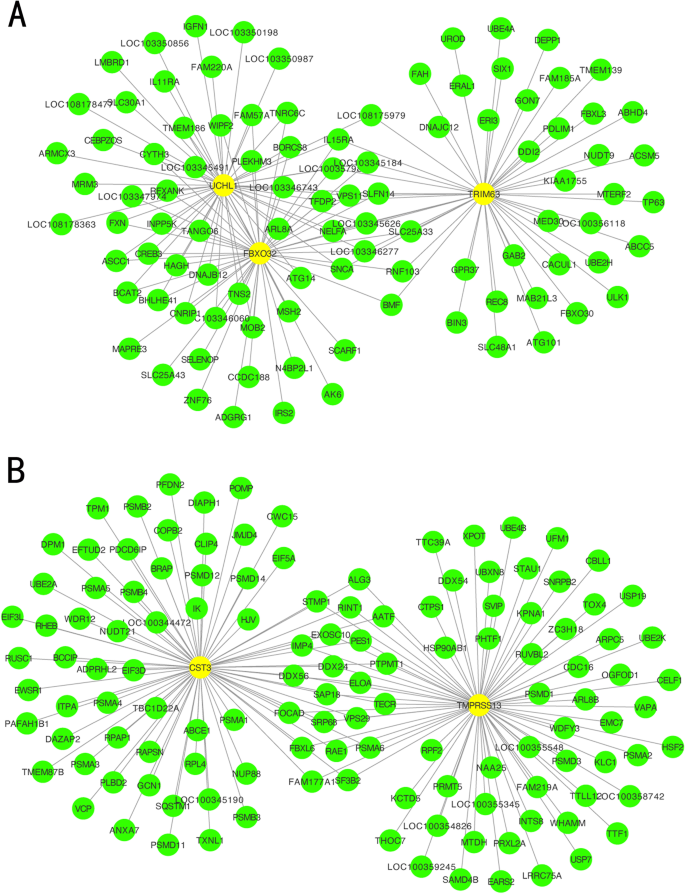
对膈肌表达谱进行WGCNA,以筛选参与VIDD进展的核心模块中的枢纽基因。采用动态分支切割和层次聚类构建共表达模块(图2)。4),七个模块之间的关系及其群特征如图所示。5.其中,绿松石模块与接受MV状态显著正相关(r= 0.81,P =0.002),黄色模块与对照条件显著正相关(r= 0.76,P= 0.02)。五个共差异表达的中枢基因(Uchl1,Tmprss13,Cst3,Fbxo32,Trim63除了来自绿松石和黄色模块的枢纽基因外,这些基因被鉴定为两组间差异表达的重要候选基因。其中两个与肌肉萎缩有关(Fbxo32而且Trim63)被排除在研究之外,而其余三个(Uchl1,Tmprss13,Cst3)分别进行qRT-PCR和western blotting。本研究选取蓝绿色和黄色模块中MM和GS较高的60个关键基因作为枢纽基因(MM>0.8;GS >(图0.8)。6).如图Venn图所示,1276个deg与绿松石和黄色模块中的60个hub基因之间的5个重叠基因被定义为共差异表达hub基因(图2)。7).最后,将5个hub共差异表达的hub基因及其靶基因构建两个共表达网络,并在Cytoscape (v3.8.2)中进行可视化(图。8).一个网络Trim63,Fbxo32,Uchl1作为核心基因与UPS平衡密切相关,其他网络与Tmprss13而且Cst3核心基因显示细胞凋亡与自噬之间存在一定程度的串扰。
5个共差异表达中枢基因的共表达网络。5个hub共差异表达基因及其靶基因在Cytoscape 3.8.2中构建共表达网络(www.cytoscape.org).每个节点代表一个基因。每条边(线)代表两个基因之间的相互作用。黄色节点表示由DEG和WGCNA鉴定的共差异表达的枢纽基因。一个网络与Trim63,Fbxo32,Uchl1作为核心基因,这些基因与泛素-蛋白酶体系统(UPS)平衡密切相关。B另一个网络Tmprss13而且Cst3作为核心基因,表明凋亡与自噬之间存在一定程度的串扰
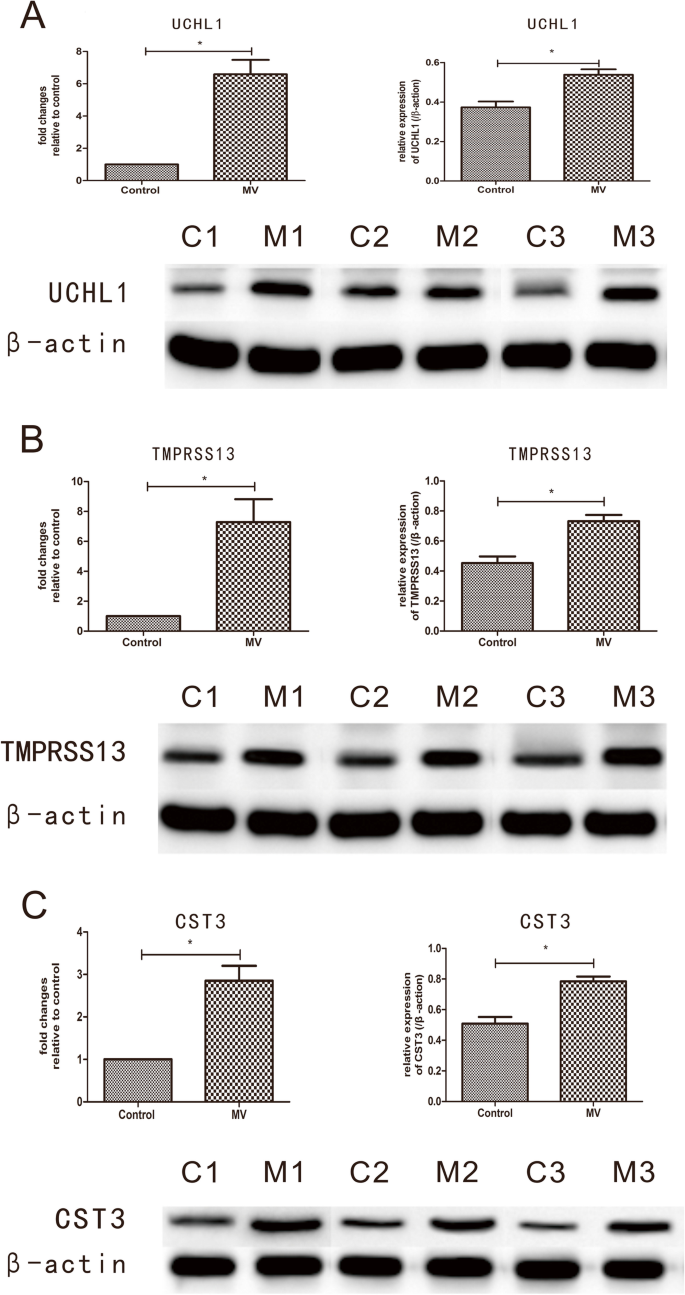
qRT-PCR和western blotting
所选基因/蛋白质的表达水平,即Uchl1 /UCHL1,Tmprss13/ TMPRSS13,Cst3 /经qRT-PCR和western blotting验证。qRT-PCR和western blotting结果证实了测序结果。与对照组相比,MV组3个基因均显著上调(P< 0.01)。此外,相应的蛋白质水平被发现显著增加(P< 0.05);9).
讨论
本研究首次通过WGCNA鉴定共差异表达的hub基因,系统地研究了对VIDD的内源性保护机制。在兔体内成功建立MV模型后,高通量RNA-seq建立了1276个基因在MV后的差异表达;其中下调760个,上调516个。利用WGCNA构建共表达网络进一步帮助识别核心模块和中心基因。绿松石模块与接受MV状态相关性最大,黄色模块与对照条件呈显著正相关。五个候选的共差异表达的中枢基因(Uchl1,Tmprss13,Cst3,Fbxo32,Trim63)最终通过在核心模块中重叠DEGs和枢纽基因来确定。其中,两种导致萎缩的基因(Trim63和Fbxo32)被排除在研究之外。其余三个基因(Uchl1,Tmprss13,Cst3)经qRT-PCR和western blotting验证,以支持RNA-seq的结果。总的来说,这些基因的鉴定可能有助于阐明VIDD背后的生理和病理过程。
虽然传统的DEG分析已经提供了大量有用的信息,但WGCNA可以说是发现与临床特征相关的共表达基因模块的唯一方法。在共表达网络中,一组具有相同表达模式的基因聚在同一个模块中,并建立了模块与临床特征之间的关联[29].在本研究中,5个共差异表达的中枢基因(Trim63,Fbxo32,Uchl1,Cst3,Tmprss13)是基于RNA-seq和WGCNA发现的。在MV期间,膜片纤维中一个关键的蛋白水解系统是UPS [12,13],其主要功能是分解多泛素化蛋白。在鉴定的5个共差异表达的中枢基因中,Trim63和Fbxo32在UPS系统中编码两种肌肉特异性E3泛素连接酶,已发现在VIDD大鼠模型中,由于表达水平的增加,促进分子运动肌球蛋白的降解。虽然这两个基因的鉴定支持了它们参与VIDD的早期发现,但它们被排除在进一步的分析之外[30.].相反,随后的分析集中在剩下的三个基因和蛋白质上(Uchl1/ UCHL1,Cst3/ CST3,Tmprss13/TMPRSS13),不仅在MV组中表达增加,而且可能通过在膈肌中发挥抗蛋白酶体、抗凋亡和抗自噬作用来减轻MV相关的生理应激。
泛素c端水解酶1 (UCHL1)最初被认为是大脑中丰富的蛋白质,从小底物中分离泛素。此外,它在恢复泛素稳态方面具有至关重要的作用[31].这种蛋白质也影响骨骼肌的发育和功能。例如,在去神经损伤后,UCHL1水平倾向于在脊髓性肌萎缩时上升,试图通过保留泛素水平和避免不受控制的降解来恢复泛素稳态[32].本研究中UCHL1表达的增加表明该蛋白可能对维持游离泛素水平很重要,从而对VIDD发挥保护作用。
胱氨酸抑素C (CST3)是一种高度丰富的半胱氨酸蛋白酶抑制剂,几乎存在于身体的所有器官和生物体液中。其基因表达的增强可能是对抗VIDD进展的保护因素。考虑到进化上保守的自噬过程,这似乎是合理的,在自噬过程中,细胞成分被运输到溶酶体,在那里它们被分解和回收[33].的确,在肌纤维中,MV可诱导快速去除细胞质蛋白和健康的细胞器,从而导致膈肌萎缩[15].然而,这一过程可以通过Cst3这是一种在人类和小鼠中都存在的保守基因,编码半胱氨酸蛋白酶抑制剂,对保存精原干细胞(ssc)至关重要。事实上,在小鼠造血干细胞中,敲除该基因可增强自噬活性,表明相应蛋白可负向调节造血干细胞的自噬[34].对这一功能的推断表明,增加CST3表达,如本研究中观察到的,可以抑制自噬,而自噬是已知的导致VIDD的原因。此外,上调自噬可诱导内源性抗氧化过氧化氢酶选择性降解,从而增加ROS水平。在这种情况下,CST3抑制自噬可能会减少ROS的生成,避免氧化应激驱动的自噬导致更多ROS积累和自噬的正反馈循环。
II型跨膜丝氨酸蛋白酶(TTSP)亚家族包括20种结构不同的多结构域丝氨酸蛋白酶,代表了锚定在膜上的丝氨酸蛋白酶的一个相对较新的分类[35].这些蛋白表达在大多数器官的上皮细胞表面,参与组织稳态和上皮细胞的发育。hepsin/TMPRSS亚家族是TTSP家族的一个亚分类,包括跨膜蛋白酶丝氨酸13 (TMPRSS13) [36],一种蛋白质,其能力促进乳腺癌和结直肠癌(CRC)的进展,由于其抗凋亡的性质,最近已被报道。在这种情况下,一项研究表明基因消融Tmprss13能促进小鼠肿瘤细胞凋亡[37].相比之下,转基因过表达Tmprss13导致caspase-3的切割显著减少,从而导致CRC细胞产生抗凋亡特性[38].综上所述,本研究观察到TMPRSS13的相对高表达可能提示存在一种通过阻断caspase-3来预防VIDD的抗凋亡机制。
当多细胞生物在发育过程中遇到细胞应激时,可能会有一种代偿性增殖机制有助于组织的恢复,以确保生物的生存[39].在这种情况下,我们推测高水平的UCHL1、TMPRSS13和CST3可能参与膈纤维的修复。验证这一推测将有助于理解VIDD的进展。UCHL1可能在促进成肌细胞增殖的同时抑制成肌细胞分化,从而促进肌肉再生和修复[40].类似地,在TMPRSS13的情况下,最近有报道称,该蛋白可以在损伤后通过将单链原肝细胞生长因子(HGF)转化为具有生物活性的HGF来再生各种组织,HGF在各种细胞中起着动力原、有丝分裂原和形态发生的作用[36,41].最后,在最近的体外和体内研究中,CST3已被证明通过细胞增殖发挥保护作用[42].特别是,CST3使肾小球大鼠系膜细胞以自分泌方式增殖[43].敲低编码基因可降低小鼠齿状回亚颗粒区神经发生的基础水平,从而突出了该分子在神经发生中的作用[44].尽管已鉴定的基因推测具有抗凋亡、抗蛋白酶体和抗自噬作用,但很可能它们无法完全抵消在MV期间影响膈纤维的凋亡、蛋白酶体和自噬过程,从而最终导致VIDD。因此,旨在确定加强这些保护作用以恢复平衡的方法的额外研究可能与针对预防VIDD的特定分子途径的研究同样重要。
限制
这项研究并非没有局限性。首先,虽然基于生物信息学分析鉴定出三个共差异表达的中枢基因(Uchl1,Tmprss13,Cst3),基于前人的研究结果推测这些基因在VIDD中具有抗凋亡、抗蛋白酶体和抗自噬作用。因此,还需要进一步的研究来确定这些基因的实际功能。其次,每组使用的动物数量相对较少可能会限制结果。未来对更多动物的研究将提供更准确和可推广的结果。第三,通过VIDD中三个共差异表达的hub基因的作用,修复机制与隔膜纤维代偿反应之间的关系还有待研究。
结论
结合差异基因表达分析和WGCNA显示,UCHL1、TMPRSS13和CST3是三种内源性分泌蛋白,在保护隔膜免受VIDD的影响中发挥重要作用。本研究的结果进一步表明,研究已识别基因的功能(Uchl1,Tmprss13,Cst3),他们参与VIDD中横膈膜的再生机制将是必不可少的。
数据和材料的可用性
在这项研究中产生或分析的所有数据都包含在这篇发表的文章中。
缩写
- 女子:
-
Bcl2-interacting中介
- BSA:
-
牛血清白蛋白
- CST3:
-
半胱氨酸蛋白酶抑制物C
- 儿童权利公约:
-
结肠直肠癌
- 度:
-
差异表达基因
- g:
-
基因的意义
- 他:
-
Hematoxylin-eosin
- 人力资源:
-
心率
- IGF:
-
胰岛素样生长因子
- MM:
-
会员模块
- MV:
-
机械通风
- mTOR:
-
雷帕霉素的哺乳动物靶点
- MSPL:
-
镶嵌丝氨酸蛋白酶大形式
- 我:
-
模块eigengene
- PVDF:
-
聚乙二烯二氟化物
- PaO2:
-
动脉氧分压
- 帕科2:
-
二氧化碳的动脉分压
- 存在:
-
实时定量聚合酶链反应
- ROS:
-
活性氧
- RNA-seq:
-
RNA序列
- SR:
-
肌浆网
- SIRT1:
-
Sirtuin1
- SBP:
-
收缩压
- SSC:
-
精原干细胞
- TTSP:
-
II型跨膜丝氨酸蛋白酶
- TMPRSS13:
-
跨膜蛋白酶丝氨酸13
- UPS:
-
Ubiquitin-proteasome系统
- UCHL1:
-
泛素c端水解酶
- VIDD:
-
呼吸机诱导的膈肌功能障碍
- WGCNA:
-
加权基因共表达网络分析
- 白平衡:
-
免疫印迹
参考文献
Lentz S, Roginski M, Montrief T, Ramzy M, Gottlieb M, Long B. COVID-19低氧性呼吸衰竭和ARDS的急诊机械通气初步策略。中华急诊医学杂志2020;38(10):2194-202。
Smuder A, Sollanek K, Min K, Nelson W, Powers S.抑制forkhead box特异性转录可防止机械通气诱导的膈肌功能障碍。重症监护医学。2015;43(5):e133-42。
Hermans G, Agten A, Testelmans D, Decramer M, Gayan-Ramirez G.机械通气持续时间增加与横膈膜力降低相关:一项前瞻性观察研究。重症监护。2010;14(4):R127。
Corpeno R, Dworkin B, Cacciani N, Salah H, Bergman HM, Ravara B,等。机械通气致大鼠膈肌收缩功能障碍的时间过程分析。中国生物医学工程杂志,2014;29(4):529 - 529。
李勇,李俊,李志强,李志强。机械通气患者膈肌变薄的研究。胸部。2012;142(6):1455 - 60。
Vassilakopoulos T, Zakynthinos S, Roussos C.长凳到床边的回顾:断奶失败——我们是否应该用控制机械通气让呼吸肌休息?危重症护理。2006;10(1):204。
Powers S, Wiggs M, Sollanek K, Smuder A.呼吸机诱导的隔膜功能障碍:因果关系。中国生物医学工程学报。2013;30(5):466 - 466。
唐海涛,李志强。呼吸机诱导膈肌功能障碍的信号网络研究。中国生物医学工程杂志,2018;29(4):419 - 419。
Hudson M, Smuder A, Nelson W, Wiggs M, Shimkus K, Fluckey J,等。部分支持通气和线粒体靶向抗氧化剂可防止呼吸机诱导的膈肌蛋白合成减少。科学通报。2015;10(9):e0137693。
Whidden M, Smuder A, Wu M, Hudson M, Nelson W, Powers S.氧化应激是机械通气诱导的隔膜蛋白酶激活所必需的。中国生物医学工程学报。2010;36(5):366 - 366。
Smuder A, Kavazis A, Hudson M, Nelson W, Powers S.氧化通过calpain和caspase-3增强肌原纤维蛋白降解。《游离自由基生物学杂志》2010;49(7):1152-60。
胡ijman P, Beishuizen A, Witt C, de Waard M, Girbes A, Spoelstra-de MA,等。危重患者膈肌纤维无力与泛素-蛋白酶体激活。中国呼吸危重症杂志,2015;19(10):1126-38。
DeRuisseau K, Kavazis A, Deering M, Falk D, Van Gammeren D, Yimlamai T,等。机械通气诱导膈内泛素-蛋白酶体通路的改变。中国生物医学工程学报,2005;29(4):344 - 344。
Smuder A, Sollanek K, Nelson W, Min K, Talbert E, Kavazis A,等。自噬和氧化应激之间的串扰调节机械通气时隔膜中的蛋白质水解。《游离自由基生物医学》2018;115:179-90。
Hussain S, Mofarrahi M, Sigala I, Kim H, Vassilakopoulos T, Maltais F,等。机械通气诱导的膈膜废弃在人类触发自噬。中华呼吸急救杂志。2010;32(11):1377-86。
麦克朗J, Kavazis A, DeRuisseau K, Falk D, Deering M, Lee Y,等。Caspase-3在机械通气诱导萎缩时膈肌核结构域的调节。中华呼吸急救杂志。2007;29(2):344 - 344。
唐海华,李敏,M Budak, N Pietras N, Hittinger S, Vu M,等。机械通气的人膈肌内固有凋亡:与新的Fos/FoxO1/Stat3-Bim轴相关中国科学d辑,2011;25(9):2921-36。
李志强,李志强,李志强,等。机械通气过程中线粒体氧化应激诱导ryanodine受体泄漏。自由基生物医学2020;146:383-91。
Hyatt H, Ozdemir M, Yoshihara T, Nguyen B, Deminice R, Powers S. Calpains在机械通气诱导的膈肌无力和线粒体功能障碍中起重要作用。氧化还原生物学。2021;38:101802。
梁峰,郭美华,李志强,李志强,等。机械通气导致新生羊羔膈肌功能障碍。重症监护。2019;23(1):123。
骨骼肌热休克蛋白70:多种功能和对消瘦性疾病的治疗潜力。《前沿物理》2013;4:30 30。
Smuder A, Morton A, Hall S, Wiggs M, Ahn B, Wawrzyniak N,等。机械通气时运动预处理和热休克素72对膈肌功能的影响。恶病质肌少症肌肉。2019;10(4):767-81。
吉hara T, Deminice R, Hyatt H, Ozdemir M, Nguyen B, Powers S.血管紧张素1-7预防呼吸机诱导的膈功能障碍。中华医学杂志2021;14(4):1512-23。
Zambelli V, Sigurtà A, Rizzi L, Zucca L, Delvecchio P, Bresciani E,等。血管紧张素-(1-7)在呼吸机诱导的膈功能障碍大鼠模型中发挥保护作用。重症监护医学经验2019;7(1):8。
张斌,张志强,张志强,等。加权基因共表达网络分析的总体框架。中华生物医学杂志,2005;4(1):17。
李刘R, G,马H,周X, y王P,赵转录组分析膜片的机械通风控制模型揭示了关键基因参与ventilator-induced膈肌功能障碍。BMC基因组学。2021;22(1):472。
马周X,李,王P G H,刘R,赵y改变表达的小分子核糖核酸的鼠模型中隔膜ventilator-induced隔膜障碍后机械通风控制。BMC基因组学杂志,2021;22(1):671。
李文杰,李志强,李志强,等。Western blot定量分析方法的研究进展。《肛门生物化学》2020;593:113608。
朗菲尔德P,霍瓦特S. WGCNA:加权相关网络分析的R包。生物信息学。2008;9(1):559。
李文杰,李志强,李志强,等。机械通气患者膈纤维快速废用萎缩。中华实用医学杂志,2008;29(3):344 - 344。
第一天,Thompson R. UCHL1 (PGP 9.5):神经元生物标志物和泛素系统蛋白。神经生物学进展。2010;90(3):327-62。
Powis R, Mutsaers C, Wishart T, Hunter G, Wirth B, Gillingwater T. UCHL1水平升高是脊髓性肌萎缩中泛素稳态破坏的代偿反应,并不代表可行的治疗靶点。神经病理学杂志。2014;40(7):873-87。
大隅勇。自噬研究的历史里程碑。细胞科学,2014;24(1):9-23。
王敏,徐勇,张勇,陈勇,常光,安光,等。通过单细胞转录组分析破译自噬调节网络,揭示了自噬在精子发生中的稳态要求。开展。2021;11(10):5010 - 27所示。
二型跨膜丝氨酸蛋白酶的发展与疾病。中国生物化学杂志,2008;40(6-7):1297-316。
穆雷A, Varela F, Hyland T, Schoenbeck A, White J, Tanabe L,等。II型跨膜丝氨酸蛋白酶的磷酸化,TMPRSS13,在肝细胞生长因子激活因子抑制剂-1和-2介导的细胞表面定位。中国生物医学工程学报,2017;29(3):344 - 344。
马志刚,李志刚,王志刚,等。细胞表面锚定丝氨酸蛋白酶TMPRSS13促进乳腺癌进展和化疗耐药性。致癌基因。2020;39(41):6421 - 36。
范文杰,张文杰,张文杰,等。TMPRSS13在结直肠癌中促进细胞存活、侵袭和对药物诱导的凋亡的耐药性。科学通报2020;10(1):13896。
范勇。细胞凋亡诱导的代偿性增殖。细胞已经死了。细胞万岁!细胞生物学杂志,2008;18(10):467-73。
高虹,李艳,李艳。泛素c端水解酶L1对成肌细胞增殖分化的调控作用。中国生物工程学报,2017;26(1):1 - 5。
Hashimoto T, Kato M, Shimomura T, Kitamura N. TMPRSS13是一种II型跨膜丝氨酸蛋白酶,被肝细胞生长因子激活因子抑制剂type 1抑制并激活前肝细胞生长因子。中国生物医学工程学报。2010;26(3):357 - 357。
郭晓明,李志强,李志强,李志强。胱氨酸抑素C在神经退行性疾病中的作用机制。生物科学进展。2011;S3(2): 541-54。
Tavéra C, Leung-Tack J, Prévot D, Gensac M, Martinez J, Fulcrand P,等。大鼠肾小球系膜细胞分泌胱氨酸抑素C:体外促生长活性的自分泌环。生物化学学报。1992;32(3):1082-8。
Pirttilä T, Lukasiuk K, Håkansson K, Grubb A, Abrahamson M, Pitkänen A.胱抑素C调节小鼠癫痫持续状态后的神经退行性变和神经发生。神经生物学杂志,2005;20(2):241-53。
确认
作者感谢长治医学院中心实验室韩鹏勇的协助。
资金
本文由山西省自然科学基金项目(No. 201901D111332)资助。
作者信息
作者及隶属关系
贡献
所有作者都参与了研究设计、研究解释、数据分析和手稿审查。DZ设计了协议。DZ, WY, QN进行实验。XJ进行数据分析。DZ撰写了手稿。DD对手稿进行了批判性的修改。作者对文章做出了贡献,并批准了提交的版本。
相应的作者
道德声明
伦理批准并同意参与
所有实验步骤均符合《实验动物护理和使用指南》(华盛顿特区,1996年),并获得长治医学院伦理委员会的伦理批准(批准2019/3/13)。
发表同意书
不适用。
相互竞争的利益
作者声明,他们没有已知的相互竞争的经济利益或个人关系,可能会影响本文报道的工作。
额外的信息
出版商的注意
伟德体育在线施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可协议中,除非在材料的信用额度中另有说明。如果材料未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。如欲查看本牌照的副本,请浏览http://creativecommons.org/licenses/by/4.0/.创作共用公共领域奉献弃权书(http://creativecommons.org/publicdomain/zero/1.0/)适用于本条所提供的资料,除非在资料的信用额度中另有说明。
关于本文
引用本文
张,D,郝,W,牛,Q。et al。共同差异表达的轮毂基因参与对抗呼吸机诱导的膈功能障碍的内源性保护机制。骨骼肌12, 21(2022)。https://doi.org/10.1186/s13395-022-00304-w
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/s13395-022-00304-w
关键字
- 隔膜功能障碍
- 机械通风
- 内生保护机制
- 加权基因共表达网络分析
- 共差异表达的枢纽基因