肌管分析仪功能
用户可以使用这款应用逐步进行分析。指导手册,所有结果的详细定义和示例分析可以在GitHub存储库中找到[19].该应用程序的输出保存在与输入图像相同的文件夹中,包括在分析的不同步骤中保存为png的几张图像,以及一个Excel文件,每个分析步骤都有单独的选项卡。所有输出文件都以输入图像命名,后缀指定哪个函数产生输出。分析是模块化的,这意味着可以重新访问每个步骤,而不必重做之前的所有步骤,并且可以跳过某些步骤或在稍后阶段执行。
在分析之前,必须选择由JPEG或PNG图像组成的图像集。有三种通道可用:蓝色用于Hoechst(核),红色用于MyHC蛋白(肌管),绿色可选用于标记某种标记阳性的核(即MYOD,成肌细胞转录因子,在这种情况下)。
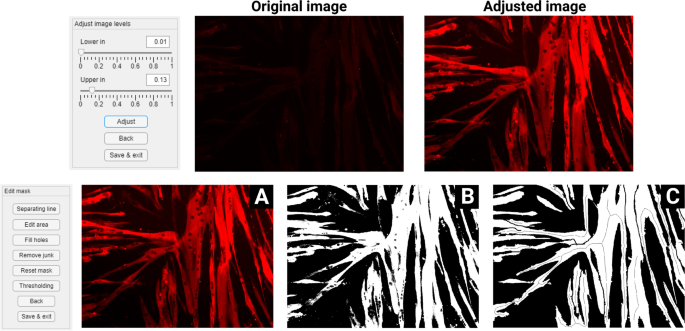
“调整水平”功能利用图像直方图上的强度窗口操作[20.].每个图像的直方图可以调整,使图像中的结构可见,增加对比度,减少背景染色(图。1).这可以减少曝光时间,从而避免在成像过程中漂白细胞。输入强度范围由用户指定,该范围内的像素分布在图像的整个可能的强度范围内(例如,0-1)。调整后的图像保存为PNG文件,用于分析的所有后续步骤。重复使用该功能将覆盖先前调整的图像。
实现了“编辑掩膜”功能,以制作一个二值图像,表明红色通道的哪些部分是肌管,哪些部分不是。图像分割是使用阈值手动完成的,因为像素强度取决于蛋白质的不同表达水平以及用于成像的设备和设置。生成的二值图像可以使用各种编辑工具进行编辑[1],并优先于正确的分析。可以在图像上绘制区域来添加/删除部分肌管,可以绘制线条来分离/连接肌管,可以删除垃圾(< 1000像素的白色物体)并填充洞(不接触图像边界的黑色像素集)。面膜保存为PNG文件,其中每个单独的肌管都用不同的颜色表示。这种手动掩膜编辑对于指示单独的肌管并使用以下函数评估所有参数是至关重要的。
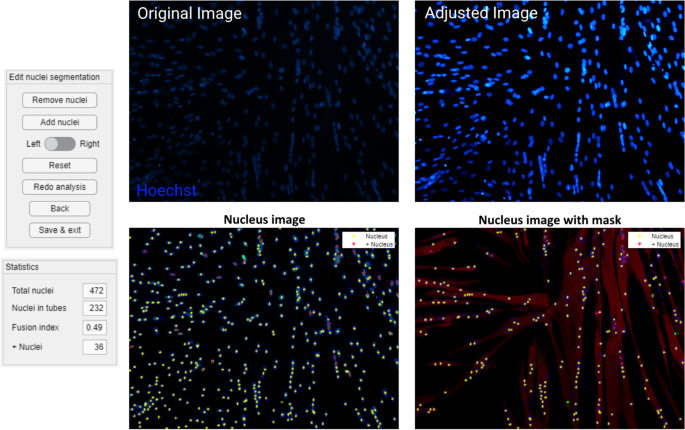
“指示核”函数提供了核中心的初始指示,基于从蓝色通道分割出来的物体的质心(Hoechst的核染色,图。2),并要求用户输入在所有分析中应用的像素大小,以便使用不同显微镜和放大倍数制成的图像。这种分割使用一个半径接近平均核的圆形滤波器作为分水岭分割的起点[21],它提供用于初始质心指示的对象。通过距离变换[22],对图像集中的松散核进行常规分水岭分割。用这种方法得到的椭圆状物体的大小直径和大小直径均为平均值,并根据所应用的像素大小进行缩放,得到的平均核直径约为10 μm。通过可用的编辑功能,可以在程序中添加或删除质心,包括单个蓝色(Hoechst)通道图像和结合蓝色和红色(MyHC)通道的图像。在前面的函数中创建的掩膜允许标记myhc阳性肌管内的核,以便可以计算融合指数,并像前面提到的那样手动调整。绿色通道图像(如果选中)也使用固定强度阈值进行分割,并且程序表明所得到的掩膜内的核对于所使用的标记物是阳性的(图2)。3.).融合指数和其他统计数据(核总数、肌管中核数、标记核总数、肌管中标记核数)与所有单个核的坐标一起保存到Excel输出文件中。
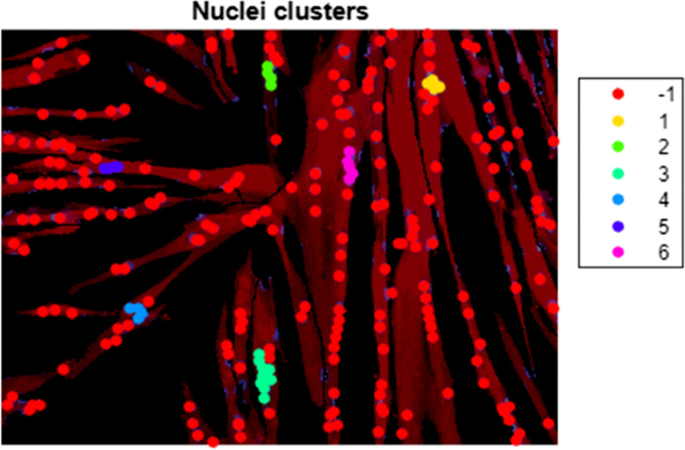
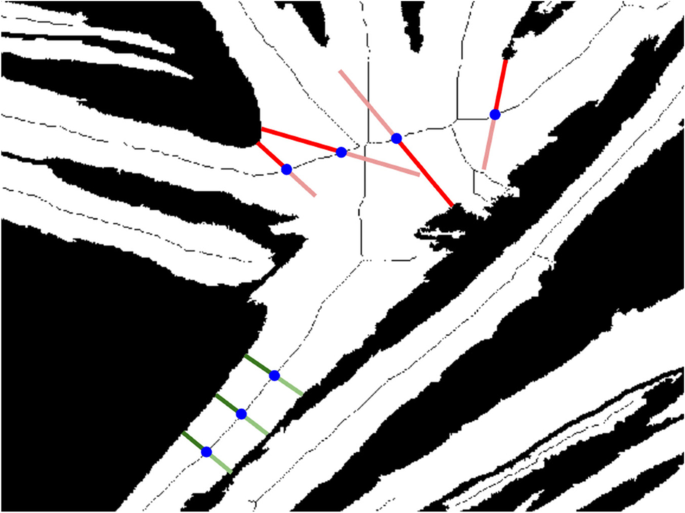
“聚类核”函数旨在量化核的聚类特征。该函数使用在前一个函数中获得的核坐标来聚类核(图2)。3.),然后对检测到的群集进行趋势线分析。趋势线是用正交回归计算的,由这个计算产生的RMSE被用作线性的度量。核聚类被任意定义为至少四个核的一组,聚类由聚类分层聚类算法执行[23].聚类算法首先将每个核视为一个单独的聚类,并寻找两个最近的聚类,即两个元素之间距离最短的聚类。然后,该算法合并这些聚类并重复,直到两个聚类之间的最短距离超过固定阈值。这个阈值是通过将核直径和核之间允许的最大边到边距离相加来设置的。在本研究中,该值设置为14 μm,允许现有集群中的核边缘与待加入集群的核边缘之间的最大距离为4 μm。一个星系团内原子核之间的边到边距离可以更高,只要另一个原子核在这个最大距离内。在运行聚类算法之前,可以更改允许的最大距离以及核直径。集群的描述性参数和回归输出被保存到Excel输出文件中的单独选项卡中。图3中所示的集群图保存为PNG文件,并包括一个颜色图例,以分别显示所有集群,红色表示不属于特定集群的核(标记为“−1”)。
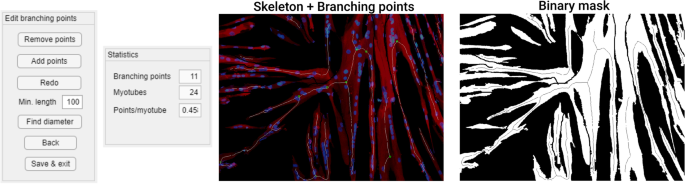
“分支点”函数根据MATLAB内置函数“bwskel”获得的肌管骨架中的分支点提供肌管中分支点的初始指示(图2)。4).分支点可以使用编辑功能添加或删除。“分支点”功能还可以选择进行直径测量。用于测量的点指示在包含掩模的距离变换的单独图像上。转换后像素的值包含到最近的黑色像素的距离,这意味着肌管中间的像素包含该点的肌管半径。用户可以选择一组像素,对于每个像素,将属于肌管骨架的最近像素的值加倍,以获得直径的估计值。使用肌管骨架像素提供了直径的最佳估计,同时也消除了由于不精确选择造成的误差。点的选择很重要,因为在肌管交叉和一些肌管特征的情况下,距离的测量将不再垂直于肌管的长度,如图所示。5.描述性参数(分支点的数量、肌管覆盖、肌管的数量、每个肌管的点)、分支点坐标和直径测量被保存到Excel输出文件中的单独选项卡中。用于直径测量的图像和带有单独肌管标签的掩膜版本保存为单独的PNG文件(图2)。6).
肌肉显微活检数据收集
肌肉显微活检的收集方案,以及细胞培养、免疫荧光染色和成像的程序已在前面描述[6].卫星细胞是从小鼠的显微活检样本中提取的内侧腓肠肌5例CP患者和3例年龄匹配的TD儿童,年龄均在4 ~ 9岁之间(平均TD: 5.51±1.46岁,CP: 7.88±0.99岁)。所有入选患者均被诊断为痉挛性双侧脑瘫,大运动功能分类系统级别为II或III级。因此,通过保持之前描述的相同条件,本研究基于人类卫星细胞分化,以60000个细胞/cm播种2在第6天用4%的多聚甲醛(伊士曼柯达)固定。免疫荧光图像使用Eclipse Ti显微镜(尼康)获得,代表井。细胞核为蓝色,使用Hoechst (1:3000, Thermofisher Scientific),肌管为红色,使用抗肌球蛋白重链抗体(MyHC,小鼠,1:20,Hybridoma Bank)。应用程序执行的所有分析都遵循附加文件中描述的指导方针进行1.
实验装置
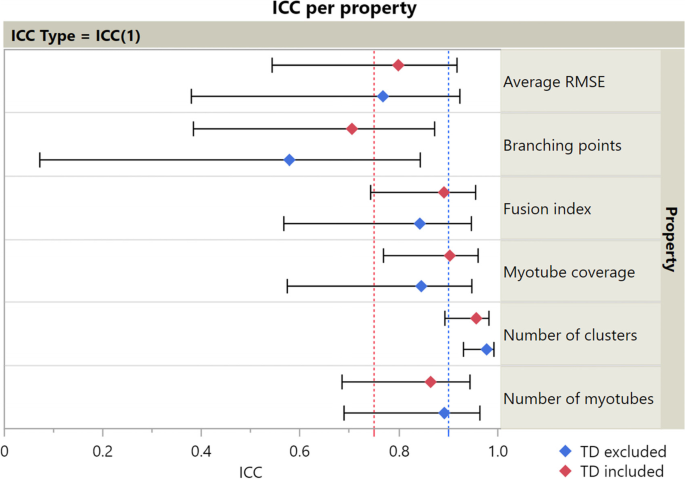
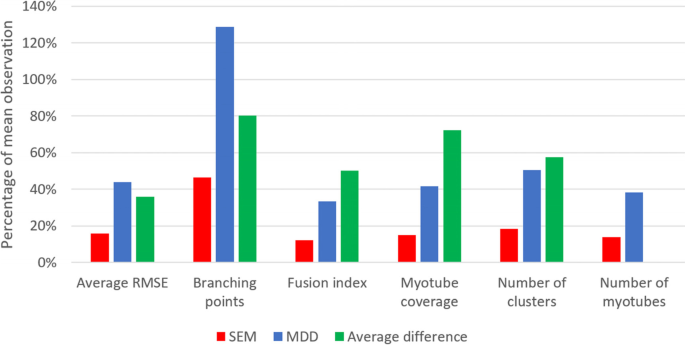
一个由19个图像集组成的数据集,每个图像集由核(使用Hoechst)和肌管(MyHC)的免疫荧光染色图像组成,用于测试新应用程序的可行性,并定义与核和肌管特性相关的一系列结果参数的评分者间信度和已知组效度。使用类内相关系数(ICCs)和测量标准误差(sem)定义评分者之间的信度。从TD样本卫星单元获得6组图像,从CP样本卫星单元获得13组图像。以这种方式细分数据集,当考虑整个数据集时,icc大于~ 0.6时,icc的幂为> 90%,而当只考虑CP样本时,icc大于0.7 [24].CP数据集的范围更广,因为由于患者的异质性,预计icc较低。所有图像集均由两位细胞生物学家分析,他们专门从事细胞培养分析,使用新开发的Myotube分析仪。为了定义评级者之间的可靠性,使用自定义的MATLAB脚本计算ICCs, sem和相应的置信区间,并在[25,26,27].最小可检测差异(mdd)计算为\ (\ mathrm {SEM} * 1.96 *大概{2}\ \)[28].已知组效度是通过比较CP儿童和TD数据的结果参数来定义的。对于每一组,定义了中位数和四分位间范围。为了测试TD和CP之间的假设差异是否由新的核和肌管参数量化,使用一个分析仪的测量结果来比较组间差异,使用未配对的双尾分析t以及。采用JMP (SAS)进行统计学分析,显著性水平为95%。其中,符号“*”表示ap小于0.05,“**”表示p< 0.01, ***表示p< 0.001。对于每个参数,我们还检查了观察到的显著差异是否超过了mdd。对于特定参数,如果平均差值大于MDD,则表明TD和CP之间的差值在至少95%的情况下(当使用相同样本量时)应该是可检测到的。如果没有,差异可能不足以从评分者之间的方差中区分出来,并且在不到95%的情况下会被检测到。平均差异小于扫描电镜表明,它将几乎难以区别于评分者之间的方差。为了全面描述Myotube Analyzer工具的半自动方法的特点和潜在的附加价值,我们还探讨了其与全手动方法在参数融合指数、簇数、肌管和核数方面的一致性。这种方法间分析是在相同的19张图像数据集上进行的,该数据集用于定义评级者间的可靠性,也基于可靠性指标ICC和SEM。对于这种方法间的分析,全手动和半自动方法总是由同一评分员执行。
参数定义
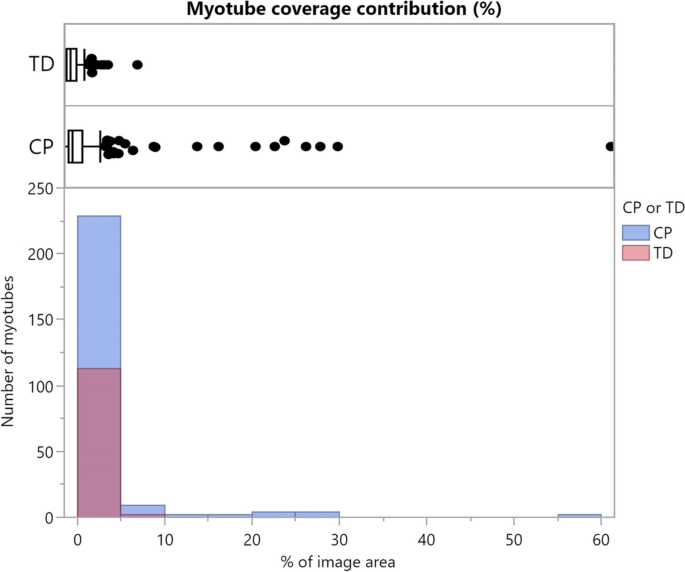
表格1包含每个结果参数定义的概述。所有参数的计算都在Myotube分析仪中实现。RMSE值和肌管覆盖率也分别调查了所有个体集群和肌管。