摘要
背景
尽管最近加强的免疫抑制方案降低了肾移植的临床急性排斥反应的发生率,但亚临床急性排斥反应和边缘性变化仍然存在问题。本研究旨在评估抗排斥治疗对早期亚临床急性排斥反应和边缘性变化的影响。
方法
本研究共纳入269例肾移植术后接受3个月和1年协议活检的肾移植患者,根据3个月病理结果分为检查结果正常的肾移植患者(A组)和检查结果≥交界性改变的肾移植患者(B组)。术后1年评估病理变化、移植物功能和移植物存活情况。
结果
3个月的活检结果显示166例患者(A组)正常,103例患者(B组)出现交界性改变和亚临床急性排斥反应。n= 108)的患者在1年内保持正常,而30.1% (n= 50)恶化到≥临界变化。B组52.4% (n= 54)例患者恢复正常。在亚临床急性排斥反应患者中,25.0% (n= 5)尽管接受抗排斥治疗,1年后仍维持亚临床急性排斥反应。平均估计肾小球滤过率从60.4±24.5下降到58.3±19.0 mL/min/1.73 m2A组为57.2±28.2 ~ 53.7±20.3 mL/min/1.73 m2B组(p= 0.417)。A组移植3、5、7年存活率分别为99.4%、99.4%、97.6%,B组分别为100.0%、98.6%、98.6% (p= 0.709)。
结论
亚临床急性排斥反应很可能复发。然而,在移植后早期干预亚临床急性排斥反应可能有助于防止随后的组织学改变。
简介
免疫抑制的最新进展降低了移植后急性排斥反应(AR)的发生率;然而,增强现实技术仍然存在问题。研究表明,临床过敏性鼻炎发生率已下降至< 20% [1活检证实的AR发生在约25%的患者中[2,3.].移植后1年内的亚临床AR (SAR)对移植物结局有负面影响,未治疗的SAR与慢性病理发展相关[4].
先前的一项研究证实了在移植后早期治疗SAR的有效性[5].然而,“边缘性变化”(BL)是一种模棱两可的诊断,对BL的分类较为困难。Nankivell等人[6]报道了无间质炎症(i0)的BL不应作为有间质炎症(≥i1)的BL进行治疗,因为作者发现形态正常外观的BL与无间质炎症的BL之间的结局没有差异。因此,很难将BL作为一种AR来对待[7],而BL的治疗仍不清楚[6,8,9,10].
我们在肾移植后3个月和1年分别进行了配对活检。本研究基于移植后3个月的活检方案,评估移植后1年内的形态学变化和干预措施的疗效。
方法
患者及临床资料
从2006年8月到2016年8月,共有363例患者在我们中心接受了活体亲属捐赠者的肾移植。1).所有供体均为成年人(>为20岁),与受者的关系为父母161例,配偶67例,兄弟姐妹27例,子女5例,祖父母3例,三级亲属6例。363例患者中有332例在移植后3个月和1年进行了配对活检。我们分析了配对活检的病理结果与抗排斥治疗干预之间的关系。排除标准为移植后3个月内进行抗排斥治疗的临床AR (n= 41),移植前已有预先形成的供者特异性抗体(DSA) (n= 18),移植前血浆置换治疗局灶性节段性肾小球硬化(n= 4)。
最终纳入269例患者。根据3个月协议活检时的组织学改变将患者分为两组:检查结果正常(NR)的患者(A组)和≥BL改变的患者(B组)。BL患者又分为两组:接受抗排斥治疗(BL-t,n= 33)和未接受治疗的观察组(BL-o,n= 50)。SAR被定义为经活检证实的AR(图。1).我们评估了移植后3个月至1年之间的形态学变化,并基于移植后3个月的协议活检评估了干预SAR和BL的疗效。
免疫抑制疗法
对于所有患者,维持免疫抑制剂包括钙调神经磷酸酶抑制剂(CNI)[环孢素(CYA)或他克莫司(TAC)],抗增殖剂(霉酚酸酯或硫唑嘌呤),以及甲基强的松龙从20到4mg逐渐减少剂量。TAC剂量调整为术后1个月维持8 - 12 ng/mL的低谷值,术后1 - 3个月维持7 - 10 ng/mL。移植后3个月,TAC剂量调整至5 - 7 ng/mL。调整CYA剂量,使其曲线下面积(AUC)为0 - 4小时,目标值为3500 - 4500 ng·h/mL,直到移植后1个月,AUC为2500 - 3500 ng·h/mL,直到移植后3个月,低谷值为100 - 150 ng/mL。霉酚酸酯的剂量为25 ~ 30 mg/kg,但未测量AUC。接受abo兼容移植的患者在移植后第0天和第4天接受抗cd25单克隆抗体诱导治疗。abo不相容移植患者根据抗a /B IgG滴度行1 ~ 3次血浆置换,并于术前10天和1天给予抗cd20单克隆抗体。成人受体的目标滴度在1:64以内,儿童受体的目标滴度在1:8以内。当诊断为巨细胞病毒(CMV)感染时,免疫抑制药物的减少是短暂的,并在CMV感染恢复后恢复。
数据收集
我们回顾性收集了以下医学信息:受体和供体的人口统计学数据、免疫抑制剂、缺血时间、初始排尿时间、巨细胞病毒感染和移植物存活。从移植到观察的最后一天,我们对所有患者进行了随访。CMV感染定义为存在CMV抗原血症。CMV感染的预防性治疗是不可用的;只进行先发制人的治疗。所有标本均由至少两名病理学家和一名医生复查,并根据班夫分类使用公认的标准进行评分[11].通过估计肾小球滤过率(eGFR)评估肾功能。对于< 19岁的儿科患者,使用五阶公式[12],对于成年患者(≥19岁),使用日本肾病学会公式(公式194)计算eGFR [13].该研究方案符合《赫尔辛基宣言》,并由东宝大学大森医学中心伦理委员会批准(批准号M18207)。
SAR和BL的治疗
静脉注射甲基强的松龙(250-500 mg/天,3-5天)和/或去精瓜林(3-5 mg/kg, 5-7天)作为抗排斥治疗。A组患者均未接受上述抗排斥治疗。B组所有SAR患者均接受抗排斥治疗。然而,BL患者的抗排斥治疗是由其主治医师考虑其病理严重程度和临床病程自行决定的。
统计分析
所有值都以中位数[四分位间距(IQR)]、平均值和标准偏差或百分比表示。分类变量采用卡方检验或Fisher精确检验进行分析。连续变量比较采用非配对t检验、配对t检验和双向方差分析。中位数比较采用Wilcoxon秩和检验。采用logistic回归分析单因素和多因素相关性。采用Kaplan-Meier法和log-rank检验评估移植物存活。差异被认为有统计学意义p< 0.05。数据分析使用JMP Pro软件,版本13 (SAS研究所,Cary, NC, USA)。
结果
病人的背景
研究了269例患者移植后3个月活检时的形态学变化(A组,n= 166;B组,n= 103)1).B组有83例出现BL, 20例出现SAR。BL分为BL和抗排斥治疗(BL-t,n= 33)和BL,观察和未抗排斥治疗(BL-o,n= 50)。AR还包括13例1a级,2例1b级,4例2a级,1例2b级。A组接受TAC的患者数量明显高于B组(分别为54.2% vs. 39.8%;p= 0.022)。移植后3个月内CMV感染发生率B组明显高于A组(分别为50.5% vs. 28.3%;p< 0.001)。A组和B组CMV感染患者中分别有61.7%和66.7%的患者减少了免疫抑制剂(p= 0.608)。移植前CMV血清型状态(R−/D−、R−/D+、R+/D−和R+/D+) A组分别为7.9%、21.2%、4.2%和66.7%,B组分别为3.2%、27.4%、5.2%和64.2% (p= 0.341)(表中数据未显示)。
移植后3个月和1年活检的病理结果
形态变化的发生率见表2.移植后3个月和1年,NR患者的发生率分别为61.7%和60.2%,BL患者的发生率分别为30.9%和32.7%,SAR患者的发生率分别为7.4%和7.1%。n= 108)的患者在移植后1年仍出现NR,而34.9% (n= 58)进展至≥BL。B组为41.0% (n= 34)移植后3个月出现BL的患者1年后仍出现BL, 51.8% (n在BL-t亚组中,有57.6%的患者形态改善为NR,而在BL-o亚组中,这一比例仅为48.0%。移植后1年,BL-o亚组的NR率低于其他组。在有SAR的患者中,25.0%的患者在接受抗排斥治疗后移植1年后仍出现SAR。然而,55.0% (n= 11)在移植后1年恢复到NR。根据我们的免疫抑制方案,CNI治疗在3个月时根据AUC或谷值进行调整。A组121例(72.9%)患者行CNI复位,B组67例(65.0%)患者行CNI复位。n= 36;BL-t,n= 23;特别行政区,n= 8)。A组5例(3.0%)患者CNI升高,B组10例(9.7%)患者CNI升高(BL-o)。n= 2;BL-t,n= 1;特别行政区,n= 7)。
BL和SAR患者移植后3个月至1年小管间质炎症评分的变化
表格3.根据小管炎显示BL和SAR患者的组织学改变(t)和间质炎症(i)评分。三组在两个时间点上有显著差异(t分数,p< 0.001;我的分数,p= 0.003)。在移植后3个月的活检中,SAR组的t评分显著高于BL-o和BL-t亚组(分别为1.95±0.76 vs. 1.16±0.37和1.18±0.39;所有p< 0.001)。移植后1年,BL-o、BL-t和SAR组的t评分显著低于移植后3个月(p< 0.001)。在间质炎症方面,移植后3个月,SAR组的i评分显著高于BL-o和BL-t亚组(分别为1.40±0.82 vs. 0.68±0.47和0.97±0.47;p< 0.001和p= 0.028)。移植后1年,BL-o和BL-t亚组的i评分显著降低(p< 0.001)。移植后3个月的病理严重程度和移植后1年的病理改善情况见表4.在BL组(n= 83),移植后1年这些病理表现在t1与t2-3、i0与i1之间无差异(表24).
在BL-o和BL-t亚组的比较中,受体和供体的人口统计学资料、免疫抑制剂、冷缺血时间、初始排尿时间、3个月内CMV感染均无差异。然而,供体-受体人白细胞抗原失配(HLA-DR失配)(BL-o, 0.84±0.62;BL-t, 1.12±0.60;p= 0.043)和热缺血时间[BL-o, 4 min (IQR, 3-5);BL-t, 3 min (IQR, 3 - 4);p= 0.012],差异有统计学意义。分析BL组病理改变为NR的单因素和多因素相关性。我们的单因素分析显示,BL治疗干预不影响NR的病理改变[优势比(OR), 1.47;95%可信区间(CI), 0.61-3.56;p= 0.394], HLA-DR失配(OR, 1.47;95% ci, 0.72-3.01;p= 0.279),或热缺血时间(or, 1.05;95% ci, 0.77-1.41;p= 0.772)。在多因素分析中,干预对BL (OR, 1.26;95% ci, 0.48-3.36;p= 0.623), HLA-DR失配(OR, 1.51;95% ci, 0.72-3.21;p= 0.274),热缺血时间(OR, 1.02;95% ci, 0.77-1.36;p= 0.870)也与NR的病理改变无关。
移植物功能和移植物存活率
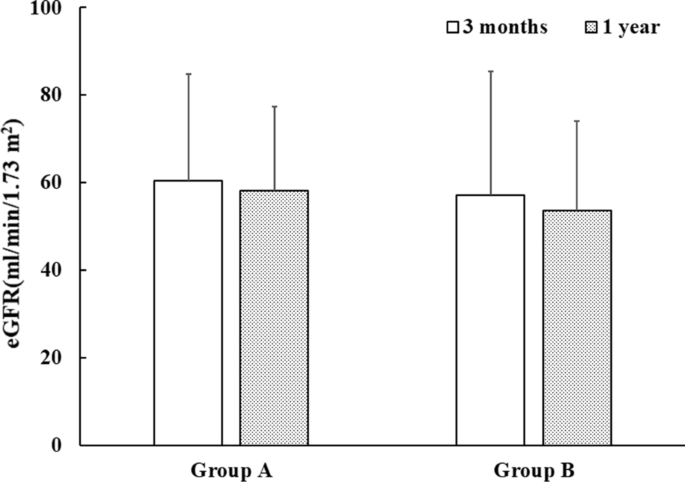
eGFR由60.4±24.5下降至58.3±19.0 mL/min/1.73 m2(p= 0.042), A组为57.2±28.2 ~ 53.7±20.3 mL/min/1.73 m2(pB组< 0.01)。2).然而,eGFR在两组之间没有显示出顺序差异(p= 0.417)。移植后3个月和1年,BL-o亚组的eGFR数值低于BL-t亚组(55.9±21.1 vs. 62.0±40.6 mL/min/1.73 m)253.2±18.1比56.9±26.6 mL/min/1.73 m2分别;p= 0.438)。A组移植3、5、7年存活率分别为99.4%、99.4%、97.6%,B组分别为100.0%、98.6%、98.6% (p= 0.709)5).3例发生移植物丢失(A组1例,B组2例),所有患者移植物丢失的原因均为慢性同种异体移植物肾病。在B组,blt亚组的移植物存活率分别为100%、100%和100%;BL-o亚组为100%、97.1%、97.1%;以及SAR子组中的100%,100%和100%。
讨论
本研究根据早期协议活检的病理结果揭示了早期干预的重要性。移植后3个月和1年BL和SAR的总发病率相似。而且,随后的病理改变更容易与前一病理改变相同。抗排斥治疗在改善随后的组织学改变方面显示出优势。
与我们的结果一致,Kee等人。[2]报告在12.5%和34.1%的常规活检中检出AR和BL (n= 88)。早期SAR的发生可能有多种原因,包括HLA不匹配、使用的免疫抑制剂类型、免疫抑制不足、感染、移植物功能延迟和供体年龄[14,15,16].蔡等人。[16]报道了在活体肾移植中,随着HLA-DR错配数量的增加,SAR的发病率也随之增加。他们研究了304名接受移植的患者,发现在移植后2周活检中检测到的SAR患者中HLA-DR错配的数量明显更高(OR, 2.39) [16].在我们的研究中,在移植后3个月,≥BL的患者HLA-A/B和HLA-DR错配的数量更可能高于NR患者。免疫抑制剂的选择对预防SAR也很重要。我们的研究还表明,TAC治疗与移植后3个月组织学上NR发生率明显高于≥BL相关。马图等人[17]研究了3365名肾移植受者,发现与TAC相比,CYA治疗增加了AR的风险(风险比,1.57;p= 0.007) [17].
AR已知是CMV的间接影响[18].既往研究表明,移植后1个月内CMV感染是AR的危险因素(风险比,1.6;p= 0.020) [19].另一份报告重点研究了106名移植前CMV血清阳性的受者的SAR与CMV疾病或CMV感染之间的关系[20.].CMV疾病是AR的危险因素(危险比,3.0;p= 0.014),但无症状CMV感染(p= 0.987)。相反,我们的研究表明,移植后3个月BL和SAR的受体更有可能在移植后3个月内表现出CMV抗原血症阳性。虽然SAR/BL组与正常组CMV感染后免疫抑制药物减量率无明显差异(61.7% vs. 66.7%),p= 0.608),我们推测CMV感染后免疫抑制的减轻可能会影响3个月协议活检时SAR或BL的发生。为了解决与CMV感染相关的早期SAR和BL,预防CMV感染可能起到预防CMV感染和减少早期SAR和BL的作用。
移植后1年内SAR发生率与移植物存活相关[3.].撒迦利亚等人[21]发现晚期活检(12-24个月)诊断的SAR和BL与eGFR下降显著相关。蔡等人。[16]报道了NR、BL和未治疗SAR患者的10年移植物生存率分别为96.2%、93.2%和62.3%。即使在没有症状的情况下,活体组织活检在检测移植物中未被识别的形态变化方面具有优势。Kurtkoti等人[5]进行了一项前瞻性随机研究,比较移植后1个月和3个月接受和未接受活检的患者,作者发现接受活检的患者在6个月时血清肌酐浓度较低(1.28±0.33 vs. 1.55±0.39 mg/dL,p< 0.001)和12个月(1.20±0.33和1.52±0.41 mg / dL,p< 0.001)。利用常规活检早期发现移植后形态变化似乎很重要,它有助于早期治疗和预防BL或SAR,以避免移植结果受损。
既往报道已揭示了经活检证实的SAR的治疗效果[4,22].Miyagi等人[22]的研究发现,高剂量类固醇脉冲治疗早期SAR可有效抑制移植后1年间质纤维化的发展。虽然SAR影响慢性评分,但它不能反映移植后短期内的血清肌酐水平[22].拉什等人。4]表明,与接受治疗的SAR和BL相比,未经治疗的SAR和BL与早期慢性病理和晚期移植物功能障碍的发展相关。移植后2年,接受治疗的SAR + BL组的血清肌酐水平明显低于未治疗组(分别为133±14 vs. 188±22µmol/L;p= 0.05)。因此,作者建议对SAR进行包括BL在内的抗排斥治疗,以改善长期病理和移植物预后[4].
BL的治疗方法仍然存在争议。关于BL的最佳治疗方法尚未达成共识[8]因为BL是一种模糊的诊断,很难作为一种排异反应来治疗[7].麦克雷等人。[9]报道了在指征活检中检出间质性炎症的小管炎(BLt1i0)预后与正常组织学改变相似,对目前BL的诊断阈值提出了质疑。在BL类别中,间质性炎症的小管炎(BLt1i1)与无间质性炎症的小管炎(BLt1i0)预后不同;与BLt1i0相比,BLt1i1更可能与移植物功能恶化和移植物衰竭相关。这一结果表明BLt1i1在组织学上与AR相似。在本研究中,发生严重间质炎症的BL患者更有可能接受抗排斥治疗。在移植后1年,BL-o组的i评分和t评分均下降,但均高于BL-t组。blt组的抗排斥治疗似乎有效;然而,这些疗法是否适用于BL-o组尚不清楚,需要进一步研究。
本研究的主要局限性是观察期较短,单个中心的患者数量较少。如上所述,BL的治疗不是随机的。在3个月的BL患者中,接受治疗的患者间质炎症比未接受治疗的患者更多。此外,没有预定义的抗排斥治疗方案,包括甲基强的松龙和/或去氧精瓜林。因此,根据BL的亚分类级别和每个患者的临床情况进行治疗。本研究没有分析DSA,因为我们无法收集所有病例的DSA。因此,由于缺乏DSA结果,无法确定早期组织学改变与DSA之间的任何关联。值得注意的是,在1年的时间里,移植物存活率高,移植物功能基本稳定,未发生临床ar相关事件。因此,移植物预后的比较仅显示出微小的差异。
总之,通过协议活检发现早期组织学改变,并根据这些改变进行干预,可能有助于改善随后的组织学改变。但是SAR(包括BL)更容易复发,对于有这些组织学改变的患者需要仔细观察,以改善移植物的预后。
数据和材料的可用性
本文中使用的数据可从通讯作者处获得。
缩写
- 基于“增大化现实”技术:
-
急性排斥反应
- AUC:
-
曲线下面积
- 提单:
-
边缘的变化
- 置信区间:
-
置信区间
- 巨细胞病毒:
-
巨细胞病毒
- 有限公司:
-
钙调磷酸酶抑制剂
- 自保”:
-
环孢霉素
- DSA:
-
供体特异性抗体
- 表皮生长因子受体:
-
估计肾小球滤过率
- HLA-DR不匹配:
-
供体-受体人白细胞抗原不匹配
- 差:
-
四分位范围
- 或者:
-
优势比
- 特别行政区:
-
亚临床急性排斥反应
- TAC:
-
他克莫司
参考文献
Bakr MA, Nagib AM, Gheith OA, Hamdy AF, Refaie AF, Donia AF,等。优化活体肾移植受者的免疫抑制方案。临床移植杂志,2017;15(增刊1):16-23。https://doi.org/10.6002/ect.mesot2016.l46.
Kee TY, Chapman JR, O 'Connell PJ, Fung CL, Allen RD, Kable K,等。肾移植活检诊断亚临床排斥反应的治疗。移植。2006;82(1):36-42。https://doi.org/10.1097/01.tp.0000225783.86950.c2.
酒井,小口,田松,石堂,等。肾移植的移植活检。肾脏学(Carlton)。2018; 23(2): 38-44。https://doi.org/10.1111/nep.13282.
刘志强,刘志强,张志强,等。早期亚临床排斥反应治疗的有益效果:一项随机研究。中国生物医学杂志,1998;9(11):2129-34。https://doi.org/10.1681/ASN.V9112129.
张志强,张志强,张志强,等。1个月和3个月移植肾活检的应用:一项随机对照研究。中国生物医学工程学报。2008;8(2):317-23。https://doi.org/10.1111/j.1600-6143.2007.02049.x.
李志刚,李志刚,李志刚。无间质炎症的小管炎是否代表T细胞介导的急性排斥反应?中华医学杂志,2019;19(1):132-44。https://doi.org/10.1111/ajt.14888.
张志刚,张志刚,张志刚,张志刚,张志刚,等。活组织检查具有“边缘性排斥反应”的性质和消除这一类别的前景。中国生物医学工程学报,2012;12(1):191-201。https://doi.org/10.1111/j.1600-6143.2011.03784.x.
Meehan SM, Siegel CT, Aronson AJ, Bartosh SM, Thistlethwaite JR, Woodle ES,等。在同种异体肾移植活检中,未按班夫标准处理的交界浸润与急性排斥反应的关系。中国生物医学杂志,1999;10(8):1806 - 1402。https://doi.org/10.1681/ASN.V1081806.
McRae M, Bouchard-Boivin F, Beland S, Noel R, Cote I, Lapointe I,等。当前诊断阈值与先前诊断阈值对在适应症活检中诊断为T细胞介导排斥反应可疑的边缘性改变患者结局的影响移植。2018;102(12):2120 - 5。https://doi.org/10.1097/TP.0000000000002327.
闵思,朴玉生,安生,朴涛,朴德昌,金明生,等。亚临床交界性改变引起的慢性同种异体移植物损伤:来自肾移植系列活检的证据。中华外科杂志,2012;33(6):343-51。https://doi.org/10.4174/jkss.2012.83.6.343.
Racusen LC, Halloran PF, Solez K. Banff 2003年会议报告:新的诊断见解和标准。中华医学杂志,2004;4(10):1562-6。https://doi.org/10.1111/j.1600-6143.2004.00585.x.
植村O,永井T,石仓K,伊藤S,畑屋H,后藤Y,等。以肌酐为基础的方程来估计日本儿童和青少年慢性肾病的肾小球滤过率。临床临床经验。2014;18(4):626-33。https://doi.org/10.1007/s10157-013-0856-y.
松尾S,今井E,堀尾M,安田Y,富田K,新田K,等。修正了日本血清肌酐估计GFR的方程。中华肾脏病杂志2009;53(6):982-92。https://doi.org/10.1053/j.ajkd.2008.12.034.
亚临床排斥反应的意义和协议活检的价值。中华医学杂志,2006;6(9):2006 - 12。https://doi.org/10.1111/j.1600-6143.2006.01436.x.
吉廖提P,洛法罗D,利昂F,帕帕利亚T,参议员M,格列柯R,等。用低剂量静脉注射类固醇治疗早期亚临床排斥反应与移植物生存损害无关:单中心13年的经验中华肾内科杂志,2016;29(3):443-9。https://doi.org/10.1007/s40620-015-0206-0.
崔斌,申明杰,申世杰,金玉生,崔玉杰,金玉生,等。活体肾移植早期活检的临床意义:单一中心的十年经验。中华医学杂志,2005;5(6):1354-60。https://doi.org/10.1111/j.1600-6143.2005.00830.x.
急性排斥反应与晚期肾移植衰竭:危险因素与预后。《肾内科杂志》2004;19增刊3:iii38-42。doi:https://doi.org/10.1093/ndt/gfh1013
Kotton CN。巨细胞病毒:预防、诊断和治疗。Am J Transpl. 2013;13增刊3:24-40;测试:https://doi.org/10.1111/ajt.12006
张志强,张志强,张志强,等。巨细胞病毒感染和疾病对同种异体肾移植受者排斥反应的影响中国生物医学工程学报,2002;2(9):850-6。https://doi.org/10.1034/j.1600-6143.2002.20907.x.
山中K, Kyo M, Okumi M,加藤T,角田Y,一丸N,等。异体肾交界性改变时间质炎症对移植物存活的影响。肾脏学(Carlton)。,85 2014; 19(24): 17 - 20。https://doi.org/10.1111/nep.12242.
张志强,张志强,张志强,张志强,等。根据组织学表型,1年后进行的系列活检可用于预测长期移植肾功能。临床移植杂志,2018;16(4):391-400。https://doi.org/10.6002/ect.2016.0323.
Miyagi M, Ishikawa Y, Mizuiri S, Aikawa A, Ohara T, Hasegawa A.早期异体肾活检亚临床排斥反应对慢性异体肾移植功能障碍的意义。临床杂志2005;19(4):456-65。https://doi.org/10.1111/j.1399-0012.2005.00303.x.
确认
我们感谢肾内科(东宝大学医学院,东京)的工作人员进行临床管理,感谢外科病理科(东宝大学医学院)的Kazutoshi Shibuya收集组织病理学数据。我们还要感谢来自Edanz的Angela Morben, DVM, ELS。https://jp.edanz.com/ac),以编辑本手稿的初稿。
资金
不适用。
作者信息
作者及隶属关系
贡献
KS撰写了手稿。MM是共同导师,设计和编辑了手稿。HO、NT、TM参与样品制备,参与病理诊断。YI, TK, YH, SS和KS讨论了结果,并对最终的手稿做出了贡献。所有作者都阅读并批准了最终的手稿。
相应的作者
道德声明
伦理批准并同意参与
该研究方案符合《赫尔辛基宣言》的规定,并得到东宝大学大森医学中心伦理委员会的批准(批准号M18207)。
发表同意书
不适用。
相互竞争的利益
作者宣称他们之间没有利益冲突。
额外的信息
出版商的注意
伟德体育在线施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可协议中,除非在材料的信用额度中另有说明。如果材料未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。如欲查看本牌照的副本,请浏览http://creativecommons.org/licenses/by/4.0/.创作共用公共领域奉献弃权书(http://creativecommons.org/publicdomain/zero/1.0/)适用于本条所提供的资料,除非在资料的信用额度中另有说明。
关于本文
引用本文
樱林K,村松M,板桥Y。et al。抗排斥疗法对肾移植活检早期亚临床急性排斥反应的影响。Ren代替Ther8, 19(2022)。https://doi.org/10.1186/s41100-022-00407-6
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/s41100-022-00407-6
关键字
- 协议活组织检查
- 肾移植
- 亚临床急性排斥反应