摘要
背景
衰老已被证明会带来一些结构性和功能性的肺部变化,尤其是COPD。然而,衰老是否会影响SAD (COPD的一种可能前兆)尚未得到很好的表征。
客观的
我们旨在从计算机断层扫描、脉冲振荡和肺活量测量的角度全面评估衰老与SAD之间的关系。
方法
我们纳入了来自ECOPD的1859名参与者,并使用线性关联检验来评估不同年龄亚组的SAD患病率,并使用多元回归模型来确定年龄对SAD风险和严重程度的影响。然后,我们在这些受试者中重复了按气流限制分层的分析。
结果
无论定义方法如何,SAD的患病率随着年龄的增长而增加。在对其他混杂因素进行校正后,每10岁年龄的增加与ct定义的SAD风险(OR 2.57, 95% CI 2.13至3.10)和空气滞留严重程度的增加(β 2.09, 95% CI−0.06至4.25)显著相关-856年),气道抗(β−0.02,95% CI为−0.04至−0.01 X5;β 0.30, 95% CI 0.13 ~ 0.47;β 1.75, 95% CI 0.85至2.66 (Fres),以及呼气流量率的下降(β−3.95,95% CI−6.19至−1.71 (MMEF%)预测;β−5.42,95% CI为−7.88 ~−2.9550%预测)的SAD。所有这些关联通常在IOS或肺活量测定所定义的SAD中维持。对气流限制进行分层后,进一步发现年龄对LAA的影响-856年是几乎所有亚组中最显著的。
结论
年龄的增长与SAD的患病率、风险的增加以及严重程度的恶化显著相关。CT可能是评估与衰老相关的SAD更为理想的方法。衰老在SAD发病中的分子机制有待进一步探讨。
试验登记中国临床试验注册中心ChiCTR1900024643。2019年7月19日注册
简介
众所周知,随着年龄的增长,肺会发生一些结构和功能上的变化。例如,在健康的老年人中,肺泡增大、支气管增厚增加、气体变化表面积减小、肺泡附着丧失被描述为“老年性肺气肿”[1].此外,肺老化也与空气滞留增加有关[2],残余容积增加,肺活量降低[3.],呼气流量率下降[4].同样,这些生理异常也出现在慢性阻塞性肺病(COPD)中[5],这已被广泛认为是一种与年龄有关的疾病。
小气道是指管腔直径小于2毫米的外周气道[6].小气道功能障碍(SAD)主要表现为小气道壁增厚,末端细支气管截面积减小[7],肺活量下降,残余容积增加[8].一些病理结果强调小气道的大量丧失先于肺气肿和COPD的病理证据[7].SAD也越来越多地被视为COPD发展的前兆。这让我们提出了一个科学问题,即SAD是否也像COPD一样与衰老相关。鉴于此,一封写给《欧洲呼气杂志》编辑的信显示,年龄的增长与包括PRM在内的图像异常水平升高有关性功能和人口、难民和移民事务局Emph[9].Martinez等人发现,在没有气流阻塞的美国受试者中,无论呼吸道症状如何,年龄增长与计算机断层扫描(CT)确定的功能性小气道异常有关[10].Lee等人的一项研究也报道,仅在82名无症状的韩国人中,ct定义的空气滞留的患病率随着年龄的增长而增加[2].然而,这些初步的探索只是从CT的角度来关注美国人或韩国人。衰老与SAD之间的综合联系从图像,脉冲振荡(IOS)和中国的肺量测量仍然没有被确定。
对于发现小气道异常的困难,SAD诊断没有金标准。目前推荐和可行的衡量和定义SAD的标准主要是CT、IOS和肺活量测定[11].因此,我们从所有这些不同的衡量标准来综合评估衰老对SAD的影响。从各个角度识别SAD的年龄相关变化,将为我们更好地理解SAD,并对定义早期肺部疾病有直接意义。
我们的研究有三个主要目标。首先,我们的目的是全面评估年龄与CT、IOS和肺活量测定方法定义的SAD患病率和风险的关系。其次,我们评估了年龄对各种SAD标记所显示的SAD严重程度的影响。第三,我们比较了哪些标记物是揭示SAD年龄相关改变的最敏感指标,从而确定可能的最佳诊断方法。
材料与方法
研究参与者
本研究使用的数据来自早期慢性阻塞性肺疾病(ECOPD)研究的横断面分析(试验注册:中国临床试验注册中心ChiCTR1900024643)。ECOPD是一项前瞻性观察队列研究。第一个参与者于2019年7月入学。基线登记于2021年8月结束。有关基本原理、设计、纳入和排除标准的细节已在先前的其他地方说明[12].简而言之,在中国广东省自愿招募了大约2000名年龄在40-80岁之间的参与者。这些参与者包括大约1000名COPD患者和其他无COPD患者。COPD定义为支气管扩张剂使用后第一秒的用力呼气量(FEV)1)/用力肺活量< 0.7 [13].所有参与者在基线时均完成了标准呼吸流行病学问卷、肺活量测定、高分辨率CT、IOS等测试。每年都会对他们进行跟踪调查。本研究集中于具有合格问卷、CT、IOS和肺活量测定(N = 1859)的受试者。我们从所有这些不同的方法来评估衰老与SAD的关系。此外,考虑到气流限制对肺活量测定法定义的SAD的重大影响以及ECOPD登记的特点,我们在1859名相同的受试者中重复了所有分析,这些受试者按气流限制(定义为FEV)分层1/ fvc < 0.7。ECOPD研究由广州医科大学第一附属医院伦理委员会批准(No.2018-53),并获得所有参与者的书面知情同意。
问卷调查
标准呼吸道流行病学问卷,由国际BOLD研究修订而成[14],并已在中国以前的COPD研究中使用[15,16],在我们的研究中由训练有素的调查人员进行。我们提取了有关COPD的人口统计学和危险因素的信息。此外,我们还计算了修改后的医学研究理事会和COPD评估测试[17].我们将已知的家庭年收入分为三个层次(低:< 10000元人民币;中:1 - 10万元;高:> 10万元人民币)。教育程度分为小学及以下、初中及高中、大学及以上。除这两个参数外,其他变量的定义与前面描述的相同[12].
CT图像分析
高分辨率CT由我们的专业研究人员进行。我们使用多排CT扫描仪(Siemens Definition AS Plus 128-切片机和United-imaging uCT 760 128-切片机)来获取图像。CT方案和质量控制的完整细节已在前面概述[12].CT图像定量分析采用胸部成像平台(https://www.chestimagingplatform.org)使用半自动3D切片机4.11软件(https://www.slicer.org) [18].肺气肿用全吸气时小于-950 HU的低衰减单位百分比(LAA-950年),以及使用在完全失效时小于-856 HU的低衰减单元百分比(LAA-856年) [19].此外,我们还记录了残气量(RV)和总肺活量(TLC)等参数。ct定义的SAD的严重程度由LAA等参数表示-950年,LAA-856年,RV和TLC。有LAA的人-856年> 20%在本研究中被认为是SAD [20.].
脉冲高频指示
我们按照欧洲呼吸学会指南执行IOS (MasterScreen IOS, Hochberg,德国)[21].在用药前进行IOS,并进行肺量测定,观察强制呼气本身对气道张力的影响[22].所有数据均由专家审核,以达到高质量。我们记录了以下IOS参数:5hz电阻(R5), 20hz电阻(R20), R5和R20之间的差值(R5 - R20), 5hz电抗(X5),电抗面积(AX),谐振频率(Fres)。其中,R5-R20反映小气道或外周气道的阻力。其值> 0.07 Ka/L/s表示SAD [23].通过所有这些记录的气道阻力和抗抗参数来指示ios定义的SAD的严重程度。
肺量测定法
我们使用传统的肺活量计(Carefusion MasterScreen Pneumo,德国)进行了肺活量测定。所有参与者在支气管扩张剂(硫酸沙丁胺醇气雾剂,400 μg, 20分钟后)下进行肺功能测试。手术操作和质量控制标准均参照美国胸科学会和欧洲呼吸学会[24,25].预测的最大呼气中流量百分比(MMEF%),预测的用力肺活量的50%和75%的用力呼气流量(FEF %)50%预测和FEF75%预测)均取自FEV总和最大的最佳曲线1和FVC。如果支气管扩张剂后MMEF %预测,则定义为SAD50%预测或FEF75%的预测(三个中的任意两个)< 65% [26].呼吸量测定法定义的SAD的严重程度由这三个呼气中末流速参数表示。
统计分析
详细信息可以在补充材料的统计分析部分找到。
结果
参与者特征
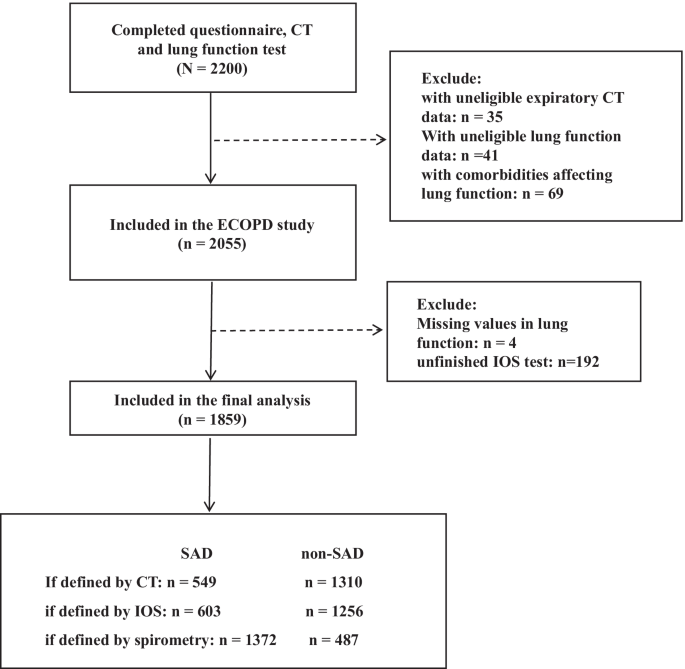
截至2021年8月,2200名参与者完成了问卷、CT和肺活量检查。经资格评估后,341名受试者被排除在外。排除的具体情况见图。1.其余1859名参与者纳入最终分析,并从不同角度(CT、IOS和肺活量测定)进行评估。然后,按气流限制分层后,在这些受试者中重复所有分析。分层的细节在附加文件中列出1:图S1。
表格1显示我们队列的平均年龄为61岁,男性占总受试者的74%。分层后,与非阻塞性亚组相比,气流限制亚组的个体更可能是年龄较大、男性、体重过轻;有更多的吸烟或职业暴露,更严重的呼吸道症状(无感冒),更多的合并症,更多的吸烟者住在家里,更多的父母有呼吸道疾病史;有较大比例的人受教育程度低或中等,家庭年收入低或中等而恶化;健康状况较差(mMRC和CAT得分较高)。此外,梗阻性亚组肺功能较非梗阻性亚组更差,气道阻力和气道阻力更大,CT图像异常更严重。
SAD的患病率和风险随着年龄的增长而增加
随年龄增长的SAD患病率和风险见表2而且3.,分别。无论SAD定义方法如何,SAD患病率与年龄增长之间存在显著的线性趋势(ct定义的SAD、ios定义的SAD和肺活量测定法定义的SAD的趋势P均< 0.001)。但在不同的测量方法中,患病率差异很大(49岁或更年轻的受试者,CT的患病率为2.5,肺活量测量的患病率为43.3;50-59岁受试者的CT评分为14.0,肺功能评分为61.1;60-69岁受试者的CT评分为36.3,肺活量测试为82.1;70岁及以上受试者的CT评分为57.3,肺功能评分为93.2)。此外,在调整可能的混杂因素后,年龄每增加10年与SAD风险显著相关(OR 2.57, 95% CI 2.13至3.10,对于ct定义的SAD P < 0.001;OR 1.79, 95% CI 1.54 ~ 2.08, ios定义的SAD P < 0.001;OR 2.38, 95% CI 2.01至2.80,对于肺活量测定法定义的SAD, P < 0.001)。当气流限制分层时,所有这些相似的关联(附加文件1:表S1和表S2)也被保留,除了阻塞性组中肺活量测定定义的SAD,因为其极高的患病率(830/832),这可能是由于MMEF%预测值和FEF的值提取密切相关50%预测或FEF75%预测,FEV1/ FVC。
SAD标记物与年龄的关系
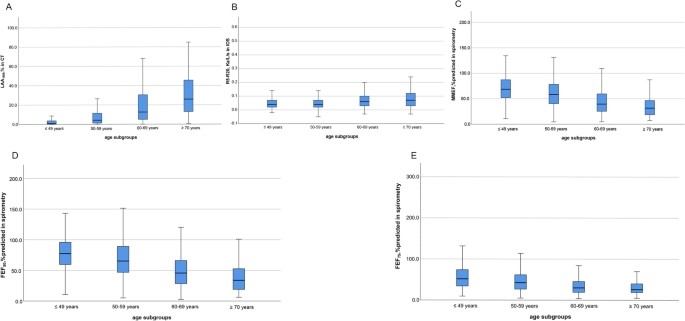
总体而言,年龄较大的受试者倾向于有更多的空气滞留(更高的LAA)-856年),气道阻力(较高的R5-R20),以及较低的呼气中末流速(预测的MMEF%较低,FEF50%预测和FEF75%预测)(图2).此外,分层后,阻塞性受试者SAD标志物所显示的SAD严重程度比非阻塞性受试者更严重。初步可以直观地看到LAA的线性趋势-856年在CT上比其他标记物更明显(附加文件1:图S2)。
年龄对SAD严重程度的影响
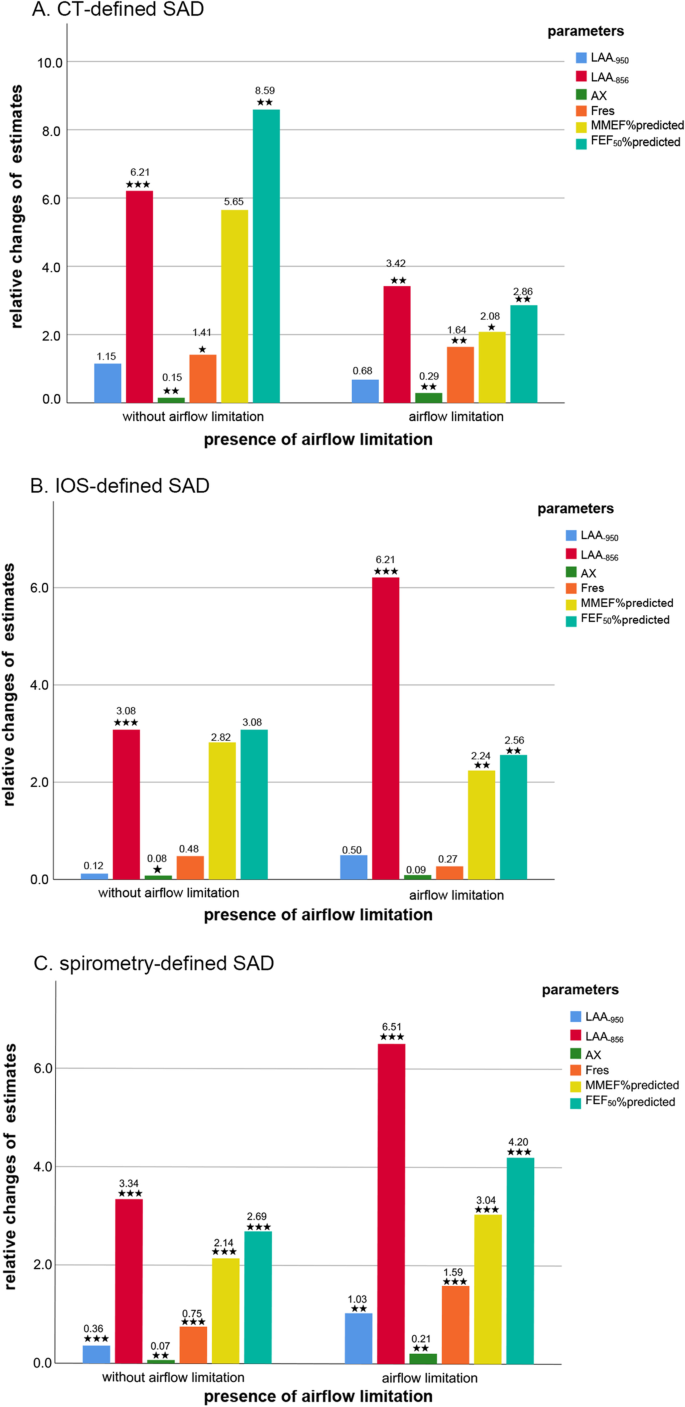
我们在多元模型中分析了年龄对SAD严重程度的影响,并对上述混杂因素进行了调整。我们发现年龄增加(每增加10年)与LAA增加2.09%显著相关-856年(95% CI 0.06−4.29,P = 0.057临界意义),0.02 Ka / L / s X5下降(95% CI 0.04−−0.01,P = 0.002), 0.30 Ka / L AX下降(95%可信区间0.13到0.47,P < 0.001), 1.75 Hz耐火的增加(95%可信区间0.85到2.66,P < 0.001), MMEF %预计减少3.95% (95% CI 6.19−−1.71,P = 0.001),和FEF50%predicted减少5.42% (95% CI 7.88−−2.95,P < 0.001)悲伤的学科评估CT(表4).上述相似的关联在IOS或肺活量测定法定义的SAD中仍然存在5而且6分别)。即使通过气流限制分层,重复分析也没有改变我们在所有亚组中的结果(附加文件1:表S3, S4, S5, S6, S7和S8)。令我们惊讶的是,在所有指标中,对SAD严重程度贡献最大的参数几乎指向LAA-856年,一个用于测量空气滞留程度的指标,在气流限制分层和定义方法的所有亚组中(图。3.).年龄对LAA无显著影响-950年通常用于评估肺气肿。然而,情况并非总是如此。LAA之间的关系-950年在无气流限制的SAD受试者中(β 0.36, 95% CI 0.21至0.52,P < 0.001;β 1.03, 95% CI 0.36至1.70,对于气流受限的SAD受试者P = 0.003)(补充文件1:表S7、S8和图S3)。此外,年龄对AX或Fres的影响在各亚组中均显著远超对R5-R20的影响。虽然R5-R20倾向于代表外周小电阻,更常用于定义SAD。
年龄对有和没有气流限制的SAD受试者SAD严重程度的相对影响(由CT、IOS和肺活量测定参数的标记指示)。注意:面板一个为CT诊断的SAD。面板B为IOS定义的SAD。面板C为肺活量测定法定义的SAD。从多元回归模型的非标准化β估计中提取估计的相对变化,并将其转化为绝对值。这些变化是由每10年增加的年龄引起的。* P值< 0.05,* * P值< 0.01,* * * P值< 0.001。缩略语的定义见表1
讨论
在我们的研究中,我们发现了几个新的发现。首先,年龄与SAD的患病率、风险的增加和严重程度的加重显著相关。其次,老化对SAD严重程度的最大影响是LAA的空气捕获-856年提示CT可能是准确检测SAD的最佳诊断方法。第三,衰老对AX和Fres的影响比R5-R20更明显。
之前的几项研究已经报道了SAD的患病率。然而,患病率差异很大,从1990-1991年海湾战争期间的退伍军人的6.7%不等[27]至医生诊断为哮喘患者的53.8% [28].差异可能是由于使用不同的肺活量测定诊断标准和不同的目标人群。其中,Xiao等人报道的SAD在中国人中最具代表性。[26他们表明,总体患病率为46.9%,从20-29岁的21.5%增加到70岁或以上的74.7%。在我们的研究中,SAD的患病率是相似的,尽管他们使用的诊断标准是支气管扩张剂前的肺功能测试。这种差异可能是由于招募的目标人数为1000名COPD患者和1000名非COPD参与者(COPD患者约占总受试者的一半),这导致了比Xiao等人报道的普通人群中更高的SAD患病率。[26].
我们进一步探讨了CT和IOS诊断SAD的患病率。令人惊讶的是,CT或IOS诊断的患病率随着年龄的增长而增加,远低于肺活量仪诊断的患病率。这可能是由于检测不同亚型SAD的各种测量方法的特点。在对SAD可能的风险因素进行调整后,衰老仍然与SAD风险显著相关。这可能表明,我们不能简单地将年龄视为一个综合的词。例如,环境有毒因素和危害暴露(如香烟、生物量和污染暴露)随着年龄的增长而增加[28].我们不能简单地认为SAD的肺老化变化可能是环境因素积累的直接结果,年龄间接介导,而完全忽略了年龄本身的影响。相比之下,我们在研究中的发现也提醒我们更多地关注年龄本身在肺结构和功能变化中的作用。至于衰老对SAD的潜在机制,确切的真相仍然未知。Brandenberger等人发现,可能的答案可能来自各种类型的肺部驻留细胞和与衰老相关的免疫系统[29].
我们研究中最重要的发现之一是,年龄的增长与空气滞留(LAA)严重程度的增加有关-856年)而不是肺气肿(LAA-950年)用于CT或IOS定义的SAD。这与Martinez等人在无梗阻或呼吸障碍的受试者中发现的情况相似。他描述了PRM金融服务管理局每十年显著增长2.7%,但PRMEMPH增加无显著性(P = 0.34) [10].我们合理地推测了这种现象的可能解释。已证实,在老年性肺中,肺气肿发生前会出现气隙扩大[30.].此外,还有一篇复习胸部Journal还得出结论,正常老化肺的形态学变化包括肺泡增大,但没有壁破坏和远端导管扩张[31].更令人信服的是,McDonough等人确实使用显微ct在肺气肿破坏发生前发现了小的传导气道异常[7].这种现象也可以用PRM来区分性功能即使在高分辨率CT上[32].虽然PRM的概念有一点不同性功能和LAA-856年,都在一定程度上表现为小气道功能障碍。
此外,与以往研究不同的是,我们还通过IOS和肺活量测定来评估年龄对SAD严重程度的影响。通过对3种方法中各种SAD标记物的比较,LAA-856年CT检查是识别SAD年龄相关改变最敏感的指标。在此之前,关于哪种方法(CT、IOS和肺活量测量)是最可靠和可用的SAD测量方法一直存在长期的争论[11,33].我们的研究为评估SAD时CT方法的首选提供了一些证据。与CT和IOS定义的SAD不同,年龄对肺气肿指数(LAA)有显著影响-950年)如果SAD是由肺活量测定法定义的,那么SAD的严重程度。它也可能反过来证明CT可以在更早的阶段(肺气肿构造出现之前)识别SAD。
据我们所知,IOS中的R5-R20标准是定义哮喘患者SAD的常见标准[34].现在有研究直接照搬这一标准来评估COPD中的SAD,没有证据,也忽略了IOS上其他参数的值。我们发现,在以社区为基础的人群中,AX或Fres比R5-R20对每10年增加的SAD严重程度的贡献更大。这与之前的一些研究是一致的。例如,在有症状的肺功能保留患者中检测SAD时,AX和Fres比R5-R20具有更大的诊断能力(更大的AUC值)[35,36].因此,在一般人群或COPD人群中直接使用R5-R20诊断SAD可能是不合理的。对于非哮喘患者的SAD,应重视AX或Fres,它们可能具有更大的潜在价值。但它们背后的截断值、机制和实际应用需要在未来进一步验证。
我们的研究是第一个通过CT、IOS和肺活量测量全面评估衰老与SAD之间关系的研究,样本量相对较大。我们的发现不仅证实了SAD确实是一种与衰老相关的异常,而且表明CT可能是未来研究中评估SAD的首选措施。此外,建议在研究IOS试验对COPD SAD的检测价值时,应更重视AX或Fres标志物,而不是R5-R20。
我们的研究也受到一些限制。首先,SAD由LAA定义-856年而不是PRM性功能这可能在诊断功能性SAD方面更有效。但这一微小的差异并不影响我们与先前发现一致的结论。其次,我们的研究只是一个横断面研究。缺乏纵向数据阻碍了我们纵向扩展年龄进展对SAD的影响,并验证LAA是否有效-856年在长期和个人内部评估中保持最敏感。但我们已经尽力调整所有可能导致SAD的危险因素,尽量减少个体间的差异。第三,在50岁以下的受试者中,CT检测到SAD的患病率需要谨慎解释,不仅因为人数相对较少,而且因为这组受试者的年龄主要集中在40-50岁(在这157名受试者中,40-50岁的受试者约占93%)。因此,这些结果可能不适用于40岁以下的年轻人群。这可能是由于我们的队列在入组时主要招募了40-80岁的受试者,这也是目前肺部健康检查的推荐筛查年龄。此外,大多数50岁以下的受试者可能比随机样本更健康,也更不愿意参与此类研究。尽管有这个缺点,但它确实反映了需要健康检查的人口的真实特征。最后,ECOPD的参与者是志愿者,招募的目标人数约为1000名COPD患者和1000名非COPD患者,不能完全代表一般人群,导致SAD的患病率略高。然而,为了使我们的结果更加有力,我们重复了这些被试中按气流限制分层的所有分析,并进一步阐述了在气流限制影响之外老化与SAD之间的关系。
结论
年龄增长与SAD的患病率、风险和严重程度的增加显著相关,其中LAA的影响最大-856年在CT。这些发现不仅表明在未来的研究中强调年龄对早期肺部疾病的影响是必要的,而且表明CT可能是检测SAD年龄相关变化的最优手段。此外,不同年龄SAD人群的AX和Fres特征为今后使用IOS评估SAD时考虑AX或Fres参数值提供了新的思路。未来的研究需要明确早期肺部疾病如SAD中衰老的分子机制,以及CT或AX和IOS中的Fres在检测SAD中的实际应用。
数据和材料的可用性
本研究中使用和分析的数据集可根据合理要求从通讯作者处获得。
缩写
- 悲伤:
-
小气道功能障碍
- CT:
-
计算机断层扫描
- IOS:
-
脉冲高频指示
- 慢性阻塞性肺病:
-
慢性阻塞性肺疾病
- ECOPD:
-
早期COPD
- FEV1:
-
用力呼气量在第一秒
- FEV1%的预测:
-
FEV的比值1到它的预测值
- FEV1/ FVC:
-
FEV的比值1到用力呼气量
- MMEF %预测:
-
最大呼气中流量百分比预测
- FEF50, %预测和FEF75%的预测:
-
用力呼气流量在50%和75%的用力肺活量的百分比预测
- LAA) - - -950:
-
全激发CT显示肺低衰减区,衰减值低于-950 Hounsfield单位
- LAA-856年:
-
全止期CT显示肺低衰减区,衰减值低于-856 Hounsfield单位
- 房车:
-
残余体积
- 薄层色谱:
-
总肺活量
- R5:
-
5hz电阻
- R20:
-
20hz时的电阻
- R5-R20:
-
从R5到R20的差异
- X5:
-
5赫兹的电抗
- AX:
-
电抗的区域
- 耐火的:
-
共振频率
- 置信区间:
-
置信区间
- 人口、难民和移民事务局:
-
参数响应图
参考文献
慢性阻塞性肺疾病(COPD)与老年?中国生物医学工程学报,2011;29(2):344 - 344。
李伟强,钟世善,杨怡,李勇,高怡,朴兆明。无症状受试者肺部薄层CT空气捕集与衰老和吸烟的相关性。放射学。2000;214:831-6。
正常人残肺容量和肺活量的年龄差异。格容托尔。1960;15:155-60。
Rodriguez-Roisin R, Burgos F, Roca J, Barbera Á, Marrades RM, Wagner PD。与衰老有关的呼吸功能的生理变化。中国科学院学报(自然科学版),1999;
伊藤K,巴恩斯PJ。慢性阻塞性肺病是一种加速肺部衰老的疾病。胸部。2009;135(1):173 - 80。
李普沃斯B,马诺哈兰A,安德森w打开安静区:小气道哮喘表型。中国呼吸医学杂志,2014;2(6):497-506。
McDonough JE, Yuan R, Suzuki M, Seyednejad N, Elliott WM, Sanchez PG,等。慢性阻塞性肺疾病的小气道阻塞与肺气肿。中华实用医学杂志,2011;29(4):344 - 344。
McNulty W, Usmani OS。评估小气道功能障碍的技术。中华口腔医学杂志,2014;
鲍德维因IM, Postma DS, Telenga ED, Hacken NHT, Timens W, Oudkerk M,等。衰老和吸烟对使用参数响应映射的肺计算机断层扫描的影响。中国生物医学工程学报,2015;29(4):344 - 344。
马丁内斯CH,迪亚兹AA,梅尔德鲁姆C,柯蒂斯JL,库珀CB,皮罗奇C,等。SPIROMICS中有和没有气流阻塞的受试者的年龄和小气道成像异常。中国呼吸急救杂志。2017;19(4):464-72。
李颖,李晓霞,袁丽玲,王海林,庞明。慢性阻塞性肺疾病患者小气道功能的评价及其应用(综述)。中华外科杂志,2021;22(6):1386。
吴峰,周勇,彭杰,邓智,文霞,王智,等。中国广东省早期慢性阻塞性肺疾病(ECOPD)研究的基本原理和设计:一项前瞻性观察队列研究中华外科杂志,2015;13(12):695 - 695。
Agusti A, Vogelmeier C, Papi A, Beasley R, Pavord I, Anzueto A,等。慢性阻塞性肺病诊断、管理和预防全球战略:2021年报告。https://goldcopd.org/2021-gold-reports/.2021年7月1日访问。
Buist AS, Vollmer WM, Sullivan SD, Weiss KB, Lee TA, Menezes AM,等。阻塞性肺病倡议(BOLD)的负担:基本原理和设计。慢性阻塞性肺病。2005; 2:277 - 83。
钟楠,王超,姚伟,陈鹏,康杰,黄松,等。中国慢性阻塞性肺疾病的患病率:一项基于人群的大型调查中华呼吸急救杂志。2007;32(8):753-60。
周勇,胡刚,王东,王松,王勇,刘忠,等。中国广东省基于社区的慢性阻塞性肺疾病(COPD)预防和管理综合干预:聚类随机对照试验BMJ。2010; 341: c6387。
Jones PW, Harding G, Berry P, Wiklund I, Chen WH, Kline LN。COPD评估测试的开发和首次验证。中国生物医学工程学报,2009;34(3):648-54。
Fedorov A, Beichel R, kalpthy - cramer J, Finet J, Fillion-Robin JC, Pujol S,等。三维切片机作为定量成像网络的图像计算平台。磁共振成像。2012;30(9):1323-41。
Labaki WW, Martinez CH, Martinez FJ, Galban CJ, Ross BD, Washko GR,等。胸部计算机断层扫描在慢性阻塞性肺疾病患者评估和治疗中的作用中国呼吸急救杂志。2017;26(11):1372-9。
Regan EA, Lynch DA, Curran-Everett D, Curtis JL, Austin JH, Grenier PA,等。肺功能测定正常的吸烟者的临床和放射学疾病。中国医学杂志,2015;29(4):529 - 529。
欧斯蒂文E,麦克劳德D,洛里诺H,法雷R,汉托斯Z, Desager K,等。强制振荡技术在临床实践中的应用:方法论、建议和未来发展。中国地质大学学报(自然科学版),2003;22(6):1026-41。
Williamson PA, Clearie K, Menzies D, Vaidyanathan S, Lipworth BJ。用肺泡一氧化氮和脉冲振荡测量法评估哮喘和COPD的小气道疾病。肺。2011;189(2):121 - 9。
彭杰,吴峰,田辉,杨辉,郑勇,邓智,等。脉冲振荡法检测小气道功能障碍的临床特点及危险因素。呼吸医学。2021;190:106681。
李文杰,李志强,李志强,等。肺功能测试的一般注意事项。中国生物医学工程学报,2005;26(1):153-61。
李文杰,李志强,李志强,等。肺活量测定的标准化。中国生物医学工程学报,2005;26(2):319-38。
肖东,陈忠,吴松,黄凯,徐娟,杨林,等。在中国,小气道功能障碍的患病率和危险因素,以及与吸烟的关系:来自全国横断面研究的发现。中国呼吸医学杂志,2020;8(11):1081-93。
Karlinsky JB, Blanchard M, Alpern R, Eisen SA, Kang H, Murphy FM。第一次海湾战争退伍军人的呼吸道症状和肺功能异常2004; 164:2488-91。
Boudewijns EA, Babu GR, Salvi S, Sheikh A, van Schayck OC。慢性阻塞性肺疾病:老年疾病?中华健康杂志,2018;8(2):020306。
肺衰老机制的研究。中国生物医学工程学报,2017;36(3):469-80。
Verbeken EK, Cauberghs M, Mertens I, Clement J, Lauweryns JM, Van de woestijne KP。老年性肺。与正常和肺气肿肺的比较。2.功能方面。胸部。1992;101(3):800 - 9。
陈旧性肺与慢性阻塞性肺疾病:异同。中华外科杂志2009;6(7):570-2。
Galban CJ, Han MK, Boes JL, Chughtai KA, Meyer CR, Johnson TD,等。基于计算机断层扫描的生物标志物为COPD表型和疾病进展的诊断提供了独特的特征。中华外科杂志,2012;18(11):1711-5。
Scichilone N, Contoli M, Paleari D, Pirina P, Rossi A, Sanguinetti CM,等。评估和进入小气道;对哮喘管理的启示。中国药物学杂志,2013;26(2):172-9。
杨晓明,张晓明,张晓明,等。小儿哮喘小气道功能障碍的临床研究。中国临床免疫杂志。2021;21(2):128-34。
李丽丽,闫涛,杨娟,李永强,付丽霞,兰丽,等。脉冲振荡法检测慢性呼吸道症状和保留肺功能受试者的小气道功能障碍呼吸科学,2021;22(1):68。
赵海燕,萧耀华,苏建春,李玉春,高宏,彭德伟。有症状的保留肺功能患者小气道功能障碍的脉冲振荡测量。中华过敏临床免疫杂志,2020;8(1):229-35。
确认
我们感谢ECOPD研究的所有参与者。此外,我们也感谢田和神、赖文军、魏绍丹、凌晓鹏(广州医科大学第一附属医院,国家呼吸疾病临床研究中心,广州呼吸健康研究所,呼吸疾病国家重点实验室)对收集数据的帮助。
资金
本研究由广东省珠江人才计划地方创新科研团队项目(No. 2017BT01S155)、自然重点研发计划(No. 2016YFC1304101)、国家自然科学基金(No. 81970045)、广东省中山医学发展基金(No. ZNSA-2020003、ZNSA-2020012、ZNSA-2020013)、广东省自然科学基金(No. 2018A0303130227)资助。广州市科技计划项目(No. 201904010071)、呼吸疾病国家重点实验室自主项目(No. 201904010071);sklrd - qn - 201913)。
作者信息
作者及隶属关系
贡献
CQD:构思思路,收集资料,分析资料,解读,起草稿件,最终修改稿件。研究设计,数据分析,最终稿件修改。FW, JQP:数据收集,数据分析,最终稿件修改。HJY, YLZ, LFL, NNZ, XW, SX, ZSD, JWX, PYH, KNZ, XHW:数据收集和最终手稿修改。PXR, YMZ:研究构想和设计,解释和最终手稿修订。所有作者都同意对工作的各个方面负责。所有作者都阅读并批准了最终的手稿。
相应的作者
道德声明
伦理批准并同意参与
ECOPD的研究是按照《赫尔辛基宣言》的准则和条例进行的。ECOPD研究(试验注册:中国临床试验注册中心ChiCTR190002464)的所有参与者均给予书面知情同意,该研究得到广州医科大学第一附属医院伦理委员会(No. 2018-53)的批准。
发表同意书
不适用。
相互竞争的利益
所有作者都声明他们没有实际或潜在的相互竞争的经济或非经济利益。
额外的信息
出版商的注意
伟德体育在线施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
补充信息
附加文件1:表S1。
CT、IOS和肺活量测定在有和没有气流限制的受试者中定义的SAD患病率随年龄的变化。表S2。有和没有气流限制的受试者年龄和SAD风险的多变量二元逻辑回归分析。表S3。ct定义的SAD受试者中年龄对无气流限制的SAD严重程度的多重调整贡献(n = 81)。表S4。在ct定义的气流受限的SAD受试者中,年龄对SAD严重程度的多重调整贡献(n = 468)。表S5。在未受气流限制的ios定义的SAD受试者中,年龄对SAD严重程度的多重调整贡献(n = 207)。表S6。在ios定义的患有气流受限的SAD受试者中,年龄对SAD严重程度的多重调整贡献(n = 396)。表S7。在呼吸量测定法定义的无气流限制的SAD受试者中,年龄对SAD严重程度的多重调整贡献(n = 542)。表S8。在呼吸受限患者中,年龄对SAD严重程度的多重调整贡献(n = 830)。图S1。通过气流限制和定义方法对1859名受试者进行分层的流程图。图S2。通过CT、IOS和肺活量仪标记显示的小气道异常在有和没有气流限制的受试者年龄分层中的分布。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可协议中,除非在材料的信用额度中另有说明。如果材料未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。如欲查看本牌照的副本,请浏览http://creativecommons.org/licenses/by/4.0/.创作共用公共领域奉献弃权书(http://creativecommons.org/publicdomain/zero/1.0/)适用于本条所提供的资料,除非在资料的信用额度中另有说明。
关于本文
引用本文
戴,C,吴,F,王,Z。et al。小气道功能障碍与衰老之间的关联:来自ECOPD队列的横断面分析。和物23, 229(2022)。https://doi.org/10.1186/s12931-022-02148-w
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/s12931-022-02148-w
关键字
- 小气道功能障碍
- 老化
- 计算机断层扫描
- 脉冲高频指示
- 肺量测定法