摘要
背景
酵母菌属是一种常见的原生寄生虫,寄生于人和动物的胃肠道。而越来越多的报告描述了两者之间的联系酵母菌属而健康个体的肠道微生物群,只有少数研究调查了两者之间的关系酵母菌属以及腹泻患者的肠道菌群。
方法
的特定子类型(ST7)的影响酵母菌属对腹泻患者肠道菌群组成进行了研究16 s核糖体RNA (rRNA)基因测序和生物信息学分析。
结果
与无腹泻患者相比酵母菌属腹泻患者感染酵母菌属ST7的细菌多样性较低。Beta多样性分析显示,st7感染和st7感染之间的细菌群落结构存在显著差异酵母菌属无病人。的比例肠杆菌科而且埃希氏杆菌属-志贺氏杆菌在st7感染患者中显著富集。相比之下,丰富的拟杆菌而且Parabacteroides更普遍的是酵母菌属无病人。
结论
这项研究的结果首次揭示了感染酵母菌属ST7与腹泻患者的细菌多样性降低和微生物结构改变有关。我们对临床腹泻患者的研究也是第一次加强了ST7是一种致病性亚型的概念酵母菌属.
图形抽象

背景
酵母菌属是一种基因多样化的单细胞寄生虫,寄生在人类和多种动物的肠腔内[1].存在酵母菌属已涉及无症状和有症状的宿主[2].临床特征归因于酵母菌属包括恶心、厌食、腹痛、胀气及急性或慢性腹泻[3.].酵母菌属已被报道为免疫抑制人群腹泻的原因,如肾移植受者[4].也有人认为酵母菌属与肠易激综合症(IBS)及炎症性肠病(IBD)有关[5].然而,酵母菌属与IBD患者相比,在健康受试者中更常见,且无症状酵母菌属携带者往往有更高的肠道细菌多样性,这表明酵母菌属定殖对宿主肠道菌群产生有益影响[6,7,8].
是否酵母菌属是一种病原体还是一种共生的人体肠道尚未明确确定。考虑到巨大的基因变异酵母菌属亚型,研究其影响是很重要的酵母菌属关于子类型级别的主机运行状况[9].一些研究表明,不同的亚型对宿主肠道菌群产生不同的影响[8,10].例如,在一个实验鼠模型中,酵母菌属7亚型(ST7)感染与该属有益菌减少有关乳酸菌而且双歧杆菌属[11],而亚型4 (ST4)感染通过调节肠道细菌组成和免疫反应,促进了实验诱导的结肠炎的更快恢复[12].亚型3 (ST3)的存在与有益细菌种类呈正相关,如属普氏菌,Methanobrevibacter而且瘤胃球菌属,来自意大利的病人[13].
近年来积累的证据揭示了两者之间的正相关酵母菌属携带和不同的细菌组成。这些研究大多集中于健康受试者,只有少数研究在亚型水平上区分了相关性[9].在我们之前的调查中,我们已经证明了这一点酵母菌属腹泻患者的主要亚型为ST7 [14],但据我们所知,还没有研究调查ST7感染与肠道菌群之间的关系。我们进行了研究报告,以更好地了解之间的联系酵母菌属以及腹泻患者的肠道菌群。为此,我们通过生物信息学分析肠道菌群的V3-V4区域16 s核糖体RNA (rRNA)基因14酵母菌属st7感染腹泻患者14例酵母菌属-腹泻控制阴性。我们的发现为临床意义提供了有价值的见解酵母菌属ST7。
方法
研究人群
本研究所使用的粪便样本是新加坡国立大学医院所保存的粪便样本的一部分,这些粪便样本是从病人那里收集的,以供以前的研究使用[14].本研究共使用28份粪便样本(男性9份,女性19份)。患者的平均年龄为71岁(范围:42-91岁)1:表S1)。研究设计和方案得到了国家医疗保健集团领域特定审查委员会的批准。
DNA提取和酵母菌属子类型识别
根据制造商的说明,使用Qiagen DNA stool Mini Kit (Qiagen, Hilden, Germany)从粪便样本中提取基因组DNA。存在酵母菌属建立和亚型鉴定如前所述[14].简单地说,DNA样本扩增使用引物BhRDr (5 ' -GAG CTT TTT AAC TGC AAC AAC G-3 ')和RD5 (5 ' -ATC TGG TTG ATC CTG CCA GTA-3 ') [15].PCR产物(约600 bp)随后根据制造商说明书(Qiagen)使用QIAquick®PCR纯化试剂盒进行清理,并送往商业实验室进行测序(Axil Scientific Pte Ltd., Singapore, Singapore)。酵母菌属通过BLAST搜索(http://blast.ncbi.nlm.nih.gov/Blast.cgi).
16 s核糖体rna序列
使用Qubit®dsDNA HS检测试剂盒(赛默飞世尔科学公司,沃尔瑟姆,马萨诸塞州,美国)监测DNA浓度。测序文库使用MetaVX文库制备试剂盒(Genewiz, South Plainfield, NJ, USA)构建。简单地说,20 - 30ng的DNA被用来产生扩增子,覆盖的V3-V4的高变区16 s细菌的rRNA基因。使用正向引物“CCTACGGRRBGCASCAGKVRVGAAT”和反向引物“GGACTACNVGGGTWTCTAATCC”。PCR循环在25µl的反应体积中进行,其中包含2.5µl TransStart缓冲液,2µl dNTPs,各引物各1µl, 0.5µl TransStart Taq DNA聚合酶和20 ng模板DNA。循环条件为:94℃变性3 min, 95℃5 s, 57℃退火90 s, 72℃延伸10 s, 24个循环,72℃最终延伸5 min。通过限环PCR将索引接头添加到扩增子的末端。最后,用磁珠净化文库。浓度测定使用微孔板阅读器(Infinite 200 Pro;Tecan Group Ltd, Männedorf, Switzerland),通过1.5%琼脂糖凝胶电泳确认预期的片段大小约为600 bp。下一代测序是在实验室的Illumina Novaseq平台(Illumina, Inc, San Diego, CA, USA)上进行的。根据制造商的说明进行了自动聚类生成和250对端双读测序。
生物信息学和微生物群多样性分析
过滤阳性和阴性reads的配对测序,然后使用QIIME2 DADA2插件去噪和去除嵌合体,以获得扩增子序列变体(asv) [16].使用核糖体数据库项目(RDP)分类器将分类分类分配到ASV表中,RDP分类器是在Silva v138数据库上训练的贝叶斯算法拟合分类器[17].根据ASV分析的结果,每个样品都可以得到α多样性指数、物种丰富度和物种均匀度,分别用Shannon指数和Simpson指数来反映细菌丰富度和均匀度。用观察到的asv和Chao1丰富度估计来估计细菌丰富度。基于Bray-Curtis差异构建主坐标分析(PCoA)图,分析不同类群间群落结构的差异。热图用于显示组之间的不同类群。通过线性判别分析效应量(LEfSe)分析,发现不同组间丰度差异显著的细菌类群P-value < 0.05,线性判别分析评分> 2 (https://huttenhower.sph.harvard.edu/galaxy/).利用中心对数变换数据,ALDEx2在R中进行细菌差异丰度分析[18].
统计分析
使用R-4.0.3软件(R统计计算基金会,维也纳,奥地利)和GraphPad Prism 8软件(GraphPad软件公司,圣地亚哥,CA,美国)进行统计分析。α多样性采用Mann-Whitney-Wilcoxon (MWW)检验,β多样性采用置换多元方差分析(PERMANOVA),相对丰度采用Wilcoxon秩和检验。
结果
序列数据评估
Illumina Novaseq的高通量测序16 srRNA基因共产生4,557,937个配对reads,其中3,701,427个高质量reads被选择用于生物信息学分析。每个样品的平均reads数为132,193±12,066。利用稀疏度曲线反映测序深度,并从采样结果间接评价物种丰富度。我们的数据显示获得了足够的测序深度,st7感染患者的asv数量似乎低于未感染的患者(附加文件)2:图S1)。
酵母菌属ST7感染与肠道细菌菌群α多样性降低有关
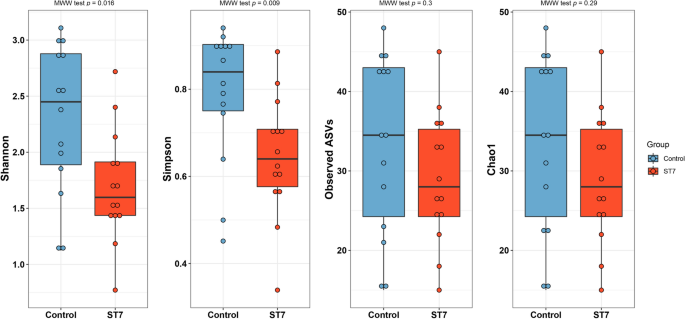
用Shannon、Simpson和Chao1指数和观察到的asv 4个指标来反映肠道细菌群落的alpha多样性。反映细菌丰富度和均匀度的Shannon和Simpson多样性指数均显示,st7感染患者的肠道细菌群落多样性低于对照组酵母菌属未感染受试者(MWW试验,P< 0.05)(图1).用观察到的ASVs和Chao1指数反映肠道细菌群落的丰富度。虽然st7感染患者的细菌丰富度较低,但与st7感染患者相比,差异不显著酵母菌属未感染受试者(MWW试验,P> 0.05)(图1).
之间的关系酵母菌属ST7感染和肠道微生物组β多样性
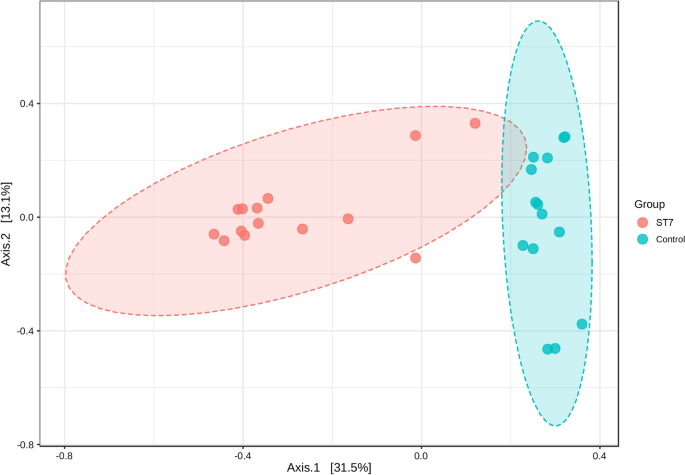
Bray-Curtis不相似指数,用于评估两种细菌群落结构的差异酵母菌属采用PCoA和PERMANOVA对st7感染和未感染患者进行分析。PCoA图显示样本的聚类依赖于酵母菌属患者ST7感染情况;PC坐标1(31.5%)和PC坐标2(13.1%)的得分解释了数据方差的44.6%(图2)。2).PERMANOVA分析显示感染组与非感染组的细菌群落结构差异有统计学意义(F-value = 9.4615,R2= 0.26681,P< 0.001)。
的影响酵母菌属肠道菌群ST7感染
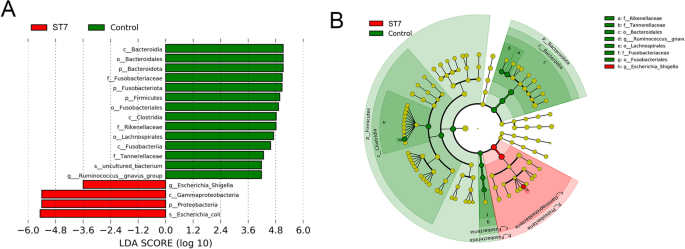
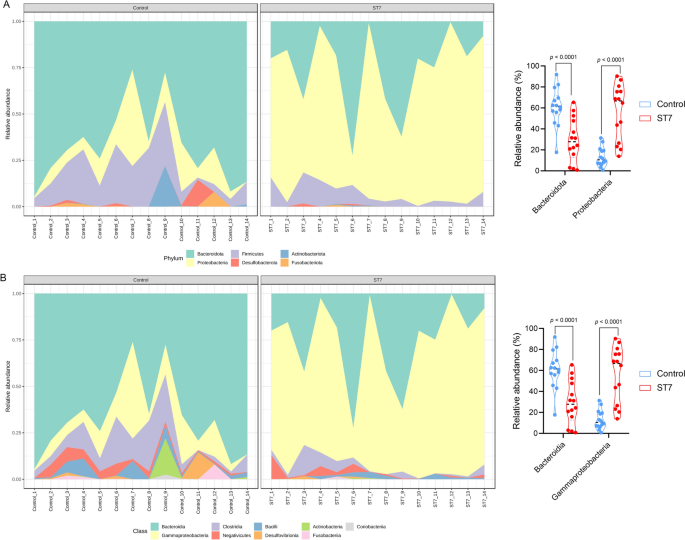
利用LEfSe分析鉴定了在细菌中丰度存在显著差异的细菌类群酵母菌属st7感染和非感染患者。变形菌门(门),Gammaproteobacteria(类),Escherichia-Shigella(属)和大肠杆菌(种)在st7感染患者中富集(图7)。3.a, b).同样,细菌成分分析表明,门变形菌门与st7感染患者相比,酵母菌属非感染者,而门Bacteroidota在st7感染患者中较少(Wilcoxon检验,P< 0.0001;无花果。4a).在类水平上,我们观察到的丰度较高Gammaproteobacteria和较低水平的Bacteroidia在st7感染患者(Wilcoxon试验,P< 0.0001;无花果。4b).关于菌序分布,细菌性的在酵母菌属游离患者的比例较高Enterobacterales在st7感染的受试者中观察到(Wilcoxon检验,P< 0.0001,附加文件3.:图S2)。同样,的上升趋势肠杆菌科在st7感染患者中,类杆菌在st7感染患者中较低(Wilcoxon检验,P< 0.0001;额外的文件3.:图S2)。热图显示了st7感染组和未感染组在属水平上粪便微生物群中属的相对丰度(附加文件)4:图S3)。的比例Escherichia-Shigella感染了酵母菌属ST7比in酵母菌属自由个人(附加文件4:图S3)。相比之下,的水平拟杆菌而且Parabacteroides在酵母菌属免费患者(附加文件4:图S3)。使用ALDEx2包对细菌asv进行差异丰度分析酵母菌属ST7感染与4个细菌类群显著相关,即Escherichia-Shigella,Escherichia-Shigella“机密”字样,大肠杆菌而且Phascolarctobacterium(附加文件5:图S4)。
讨论
尽管许多早期研究报告说酵母菌属与急性或慢性消化系统疾病有关,其临床意义和致病性尚不清楚。酵母菌属在无症状和有症状的患者中都可以发现,而只有少数研究调查了酵母菌属胃肠道疾病。我们的研究是第一个调查和报道罕见的影响酵母菌属ST7对胃肠道疾病患者肠道细菌群落的影响。
ST7的致病性已在体外和体内实验中确定[9,19].例如,ST7感染诱导免疫球蛋白A (IgA)降解,破坏结肠上皮细胞系的上皮屏障[20.,21].ST7感染还增加了由丝裂原激活蛋白激酶(MAPKs)介导的小鼠巨噬细胞中促炎细胞因子的释放,如白细胞介素(IL)-6、IL-1β和肿瘤坏死因子α (TNFα),并增强了脂多糖(LPS)介导的NF-κB通路激活的作用[22,23].此外,ST7感染也引起小鼠模型的结肠病理改变[11].我们前期研究显示ST7是腹泻患者的主要亚型,提示其对人类潜在的致病性[14].本研究进一步研究了ST7感染与腹泻患者肠道微生物群的关系。我们观察到,st7感染患者的细菌多样性下降,而“有害”细菌的丰度更高Escherichia-Shigella.
有几项研究调查了酵母菌属肠道细菌菌群的定殖和多样性[7,10,24,25,26,27].微生物多样性被认为是健康肠道的潜在生物标志物,更高的多样性意味着肠道生态系统的稳定性和弹性[28].在一系列与下消化道炎症相关的消化系统疾病中,如IBD和IBS,已观察到肠道微生物群多样性的减少[29,30.].迄今为止进行的大多数研究都表明酵母菌属定殖与肠道微生物群落的细菌多样性较高有关[25,26,27].然而,相比之下,在目前的研究中我们发现的存在酵母菌属ST7与较低的细菌多样性相关。缺乏关于。的资料酵母菌属因为ST7在人类中是一种相对罕见的亚型,大多数微生物组研究都是基于健康个体,而ST7通常是在有症状的个体中报道[14,31].
之前的研究也表明酵母菌属有更高丰度的厚壁菌门而较少的丰度变形菌门,相比之下酵母菌属自由个人[27,32].在门的水平上,变形菌门在健康人类的肠道中有低丰度,和扩张变形菌门通常与维持肠道微生物群落平衡的能力受损有关,而这反过来又是生态失调和疾病风险的潜在诊断特征[33].此外,埃希氏杆菌属-志贺氏杆菌类群,属于门变形菌门和家人肠杆菌科,是全球引起肠胃炎最重要的肠道病原体之一[34].已经确定肠杆菌科丰度与胃肠或全身炎症呈正相关[35],以及更丰富的肠杆菌科常见于IBD患者[36].酵母菌属发现-定殖患者表现出较低的比例肠杆菌科在不同的研究中[7,26],表明酵母菌属定植与健康的肠道菌群有关。令人惊讶的是,我们的数据显示了更丰富的肠杆菌科提示ST7感染与肠道炎症相关。这些结果也强调了……的重要性酵母菌属微生物区系研究中的亚型。
两者之间的联系酵母菌属而且拟杆菌已在几项研究中详细阐述[8,32,37,38].属种拟杆菌通常为互惠或共生,是哺乳动物胃肠道微生物群的最重要组成部分[39].它们在能量吸收、碳水化合物降解和宿主肠道健康的过程中发挥着复杂的作用[39,40].一些研究暗示拟杆菌在胃肠道慢性炎症的发展过程中[41,42),而拟杆菌亦为人体肠道内短链脂肪酸的主要生产者,对维持免疫系统的稳定至关重要[43,44].在健康个体中,酵母菌属据报道,定殖可降低的比例拟杆菌[37而在…中不那么流行拟杆菌肠型样本[8].类似的,角色Parabacteroides关于宿主健康的问题也很复杂。丰富Parabacteroides在一名溃疡性结肠炎患者中,发现物种与疾病活动性密切相关[45],同时也确定了物种的来源Parabacteroides可以减轻大肠杆菌lps诱导体外产生IL-8,提示其可能具有抗炎能力[46].有趣的是,我们的数据还显示ST7感染降低了的丰度拟杆菌而且Parabacteroides种在腹泻患者中,但有病原学作用拟杆菌而且Parabacteroides在未来的研究中需要更多的阐明。
值得注意的是,本研究仅显示了腹泻患者中ST7及其与微生物多样性的关系;其他亚型与腹泻患者相关的数据仍然有限。另一个令人困惑的因素是,一些腹泻患者的检测结果呈阳性Clostridioides固执的,这是导致菌群失衡的潜在因素;然而,我们没有区分其对肠道微生物群落的影响酵母菌属ST7由于本研究纳入的患者数量较少。未来的研究应该包括更多的样本和亚型,以比较特定亚型对肠道微生物群落和宿主健康的影响。
结论
目前的研究首次报告了酵母菌属ST7感染与腹泻患者肠道细菌群落多样性和丰富度降低有关。此外,酵母菌属st7感染患者的“有害”细菌比例较高(变形菌门)在人体肠道中。我们的数据表明酵母菌属ST7可与微生物群的多个成员相互作用,如埃希氏杆菌属-志贺氏杆菌群体,来引起这些负面的改变。这些发现强调了分层的重要性酵母菌属感染分为亚型,可能为临床囊胚症的治疗提供新的指导方针。
数据和材料的可用性
本文粪便菌群的原始序列数据被上传到NCBI的序列阅读档案(sequence Read Archive, SRA)数据库,项目ID为PRJNA850541 (https://www.ncbi.nlm.nih.gov/bioproject/PRJNA850541).
缩写
- asv:
-
扩增子序列变体
- 炎症性肠病:
-
炎症性肠病
- 肠易激综合症:
-
肠易激综合症
- IgA:
-
免疫球蛋白的
- LEfSe:
-
线性判别分析效应大小
- MAPKs:
-
丝裂原激活蛋白激酶
- MWW:
-
Mann-Whitney-Wilcoxon
- 努哈:
-
国立大学医院
- PCoA:
-
主坐标分析
- PERMANOVA:
-
置换多元方差分析
- RDP:
-
核糖体数据库程序
- 圣:
-
子类型
参考文献
Tan KS。对分类、鉴定和临床相关性的新见解酵母菌属spp.临床微生物学Rev. 2008; 21:639-65。
Stensvold CR, Tan KSW, Clark CG。酵母菌属。寄生虫学,2020;36:315-6。
Sohail MR, Fischer PR。酵母菌属hominis和旅行者。旅行医学感染杂志2005;3:33-8。
饶k, Sekar U, Iraivan KT, Abraham G, Soundararajan P。酵母菌属hominis-肾移植受者腹泻的新原因。印度医学杂志。2003;51:719-21。
Rostami A, Riahi SM, Haghighi A, Saber V, Armon B, Seyyedtabaei SJ。的作用酵母菌属sp.和双核内变形虫属fragilis肠易激综合征:系统回顾和荟萃分析。寄生虫Res. 2017; 116:2361-71。
Rossen NG, Bart A, Verhaar N, van nod E, Kootte R, de Groot PF,等。低流行率酵母菌属在活动性溃疡性结肠炎患者中。中国临床微生物学杂志,2015;34(4):339 - 344。
Audebert C, Even G, Cian A, Loywick A, Merlin S, viscgliosi E,等。肠道原生动物的定植酵母菌属与人类肠道细菌菌群的多样性增加有关。科学通报2016;6:25255。
王杰,李志刚,王志刚,李志刚,等。的群体水平分析酵母菌属人类肠道菌群的亚型流行和变异。肠道。2019;68:1180-9。
邓琳,沃伊切赫,加斯科因NRJ,彭刚,谭光文。之间相互作用的新见解酵母菌属肠道菌群和宿主免疫力。公共科学学报。2021;17:e1009253。
Forsell J, Bengtsson-Palme J, Angelin M, Johansson A, Evengård B, Granlund M酵母菌属以及瑞典旅行者的肠道菌群。BMC微生物学杂志,2017;17:231。
亚森佳,梁烨,彭长武,张勇,谭广雄。致病细菌之间的相互作用酵母菌属亚型和肠道菌群:体外和体内研究。微生物。2019;7。
邓玲,Wojciech L, Png CW, Koh EY, Aung TT, Kioh DYQ,等。用酵母菌属在dss诱导的结肠炎小鼠模型中,ST4与保护性免疫反应和肠道微生物组的调节有关。中国生物医学工程学报(英文版);
Gabrielli S, Furzi F, Fontanelli Sulekova L, Taliani G, Mattiucci S酵母菌属来自意大利的患者的-亚型显示ST3与健康的肠道菌群有关。寄生虫流行病控制,2020;9:e00134。
邓丽,戴华,彭刚,李建伟,谭冠雄。囊胚病的患病率和分子分型艰难梭状芽胞杆菌感染,新加坡。寄生虫载体。2021;14:277。
Scicluna SM, Tawari B, Clark CG。DNA条形码酵母菌属.原生生物。2006;157:77 - 85。
杨晓明,杨晓明,杨晓明,杨晓明。基于Illumina扩增子数据的高分辨率样本推断。Nat Methods. 2016; 13:581-3。
Quast C, Pruesse E, Yilmaz P, Gerken J, Schweer T, Yarza P,等。SILVA核糖体RNA基因数据库项目:改进的数据处理和基于网络的工具。核酸科学,2013;41:D590-6。
Fernandes AD, Reid JN, Macklaim JM, McMurrough TA, Edgell DR, Gloor GB。统一高通量测序数据集的分析:通过成分数据分析来表征RNA-seq、16S rRNA基因测序和选择性生长实验。微生物。2014;2:15。
Aykur M, Camyar A, Türk BG, Sin AZ, Dagci H.与子型和等位基因的相关性评价酵母菌属伴有慢性自发性荨麻疹。热带学报2022;231:106455。https://doi.org/10.1016/j.actatropica.2022.106455.
普希亚,范提林甘A,陆杰,谭克辉。人分泌性免疫球蛋白A的降解酵母菌属.寄生虫学报,2005;97:386-9。
Yason JA, Ajjampur SSR, Tan KSW。酵母菌属分离株B对抗菌肽LL-37表现出多种耐药模式。《感染Immun》2016;84:2220-32。
Teo JD, Macary PA, Tan KS。的多效性酵母菌属人单核细胞系中配体特异性toll样受体信号通路和NF-κB激活的sp4和7亚型。PloS ONE。2014; 9: e89036。
林晓霞,彭志强,张志强,焦华,李明,等。有丝裂原激活蛋白激酶对巨噬细胞促炎细胞因子表达的差异调节对肠道寄生虫感染的响应。感染Immun 2014; 82:4789-801。
Kodio A, Coulibaly D, Koné AK, Konaté S, Doumbo S, Guindo A,等。酵母菌属定植与健康马里儿童肠道细菌群落多样性增加和改变有关。微生物。2019;7:649https://doi.org/10.3390/microorganisms7120649.
Even G, Lokmer A, Rodrigues J, Audebert C, visvisgliosi E, Ségurel L,等。与定殖相关的人类肠道微生物群的变化酵母菌属sp.和痢疾主要见于非工业化人口。前端细胞感染微生物。2021;11:533528。
金美善,李玉杰,金tj,元宜俊。肠道原生动物定殖的肠道微生物组概况酵母菌属在韩国人群中。微生物。2021;34。https://doi.org/10.3390/microorganisms10010034.
Stensvold CR, Sørland BA, Berg R, Andersen LO, van der Giezen M, Bowtell JL,等。粪便菌群多样性分析酵母菌属艾滋病患者和酵母菌属消极的人。微生物。2022;10:326。https://doi.org/10.3390/microorganisms10020326.
李文杰,李志强,李志强,等。人体微生物群的研究进展。基因组医学。2016;8:51。
龚东,龚霞,王玲,于霞,董强。炎症性肠病中微生物多样性降低的参与。胃肠病学研究。2016;2016:6951091。
孙丁,兰格尔一世,富恩特斯,海坎普-德容一世,Hultgren-Hörnquist E,德沃斯WM,等。感染后肠易激综合征患者粪便和粘膜微生物组成的改变与黏膜淋巴细胞表型和心理困扰相关。中国医药科学。2015;41:342-51。
Stensvold CR, Lewis HC, Hammerum AM, Porsbo LJ, Nielsen SS, Olsen KE,等。酵母菌属:揭示一种常见但被忽视的寄生虫的潜在危险因素和临床意义。流行病学,2009;137:1655-63。
张晓明,张晓明,张晓明,杨晓明,Cacciò张晓明酵母菌属它是人类肠道微生物群的常见成员。中国科学,2017;11:2848-63。
申NR,何永涛,裴俊伟。变形菌门:肠道菌群失调的微生物特征。生物技术,2015;33:496-503。
Devanga Ragupathi NK, Muthuirulandi Sethuvel DP, Inbanathan FY, Veeraraghavan B.大肠杆菌而且志贺氏杆菌血清组:挑战和策略。新微生物新感染,2017;21:58-62。
刘娟,王敏,陈伟,马军,彭勇,张敏,等。儿科重症监护室脓毒症患者肠道菌群分类组成的改变。前方儿科。2021;9:645060。
翟志,张峰,曹睿,倪霞,辛志,邓杰,等。天蚕素A通过调节C57BL/6小鼠dss诱导的IBD肠道菌群来缓解炎症。前沿微生物。2019;10:1595。
Andersen LO, Bonde I, Nielsen HB, Stensvold CR.回顾性宏基因组学研究方法酵母菌属.中国生物医学工程学报,2015;https://doi.org/10.1093/femsec/fiv072.
O 'Brien Andersen L, Karim AB, Roager HM, Vigsnæs LK, Krogfelt KA, Licht TR,等。qPCR揭示人体常见肠道寄生虫与细菌的相关性。中国临床微生物学杂志,2016;35:1427-31。
Wexler嗯。拟杆菌:好的,坏的,以及事实真相。临床微生物学,2007;20:593-621。
Bornet E, Westermann AJ。矛盾的作用拟杆菌在肠道感染中。趋势微生物。2022;30:104-8。
Vieira-Silva S, Falony G, Darzi Y, Lima-Mendez G, Garcia Yunta R, Okuda S,等。物种-功能关系塑造了人类肠道微生物群的生态特性。生物工程学报。2016;1:16088。
Bamias G, Okazawa A, Rivera-Nieves J, Arseneau KO, De La Rue SA, Pizarro TT,等。共生菌会加剧肠道炎症,但对小鼠回肠炎的发展不是必需的。中华免疫杂志2007;178:1809-18。
清水J,久保田T,高田E,高井K,藤原N,有光N,等。在复发性多软骨炎患者中,肠内产生丙酸的细菌可能与产生il10的调节性T细胞的扭曲反应有关。PLoS ONE。2018; 13: e0203657。
Zafar H, Saier MH Jr. Gut拟杆菌健康和疾病中的物种。肠道微生物检查,2021;13:1-20。
野村K,石川D,冈原K,伊藤S,羽贺K,高桥M,等。拟杆菌门在溃疡性结肠炎中,物种与疾病活动性相关。中华临床医学杂志2021;10:1749。
Hiippala K Kainulainen V, Suutarinen M, Heini T, Bowers JR, Jasso-Selles D,等。抗炎和上皮增强的分离拟杆菌而且Parabacteroides来自健康的粪便捐赠者营养。2020;12:935。
确认
我们感谢高怡玲博士和戴惠仪博士在样本采集和DNA提取过程中的协助。我们也感谢Png Chin Wen博士对生物信息学分析的评论。这项工作得到了MOE Tier-1拨款(R-571-000-037-114)的支持。
资金
这项工作由MOE Tier-1赠款(R-571-000-037-114)和NUSMed内部赠款(NUHSRO/2022/071/NUSMed/Microbiome)资助。
作者信息
作者及隶属关系
贡献
KT和JL构思并设计了这项研究。实验由LD进行,数据由LD进行分析,所有作者均已阅读并认可最终稿件。
相应的作者
道德声明
伦理批准并同意参与
这项研究得到了国家医疗保健集团领域特定审查委员会(NHG DSRB)的批准(参考编号:2017/01110)。在收集粪便样本之前,从患者那里获得书面知情同意。
发表同意书
不适用。
相互竞争的利益
作者宣称他们之间没有利益冲突。
额外的信息
出版商的注意
伟德体育在线施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
补充信息
附加文件1:表S1。
本研究中使用的样本。
附加文件2:图S1。
稀疏曲线。的x-轴显示每个样本的读取数y-axis表示asv的数量。图中的每条曲线代表一个不同的样本,同一组中的样本用统一的颜色表示。ASVs:扩增子序列变体。
附加文件3:图S2。一个
肠道菌群的有序分布酵母菌属st7感染患者和非st7感染患者酵母菌属控制(左)。两组之间两种不同顺序的相对丰度(右)。b肠道菌群的分布酵母菌属st7感染患者和非st7感染患者酵母菌属对照(左),根据家庭。两组之间两个不同家族的相对丰度(右)。Wilcoxon秩和检验。
附加文件4:图S3。
ST7感染相关分类标记的热图。
附加文件5:图S4。
肠道细菌组成与存在的关系酵母菌属ST7。ASV折叠变化与中位数丰度的关系(左),ASV折叠变化与条件之间的关系(右)。红色标记表示有显著变化的asv (Wilcoxon秩检验)。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可协议中,除非在材料的信用额度中另有说明。如果材料未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。如欲查看本牌照的副本,请浏览http://creativecommons.org/licenses/by/4.0/.创作共用公共领域奉献弃权书(http://creativecommons.org/publicdomain/zero/1.0/)适用于本条所提供的资料,除非在资料的信用额度中另有说明。
关于本文
引用本文
邓丽丽,李俊杰,谭家胜酵母菌属ST7与腹泻患者细菌多样性降低和肠道微生物组谱改变有关。寄生虫向量15, 312(2022)。https://doi.org/10.1186/s13071-022-05435-z
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/s13071-022-05435-z
关键字
- 酵母菌属
- ST7
- 肠道微生物组
- 细菌多样性
- 致病性