摘要
突触是神经元之间交流的场所,是构成所有动物认知和行为的神经回路的基础。化学突触是突触前神经元和突触后目标之间的特殊非对称连接,在复杂信号网络的控制下,通过一系列不同的细胞和亚细胞事件形成。一旦建立,突触通过调节突触囊泡的组织和融合促进神经传递,并且还必须保留经历塑性变化的能力。近年来,突触基因已涉及广泛的神经发育障碍;这些疾病所带来的个人和社会负担,以及缺乏有效的治疗方法,促使人们继续研究基础突触生物学。神经系统的特性和功能在动物门中是非常保守的,许多关于脊椎动物中枢神经系统突触的见解都来自于对无脊椎动物模型的研究。一个突出的模型突触是黑腹果蝇幼虫神经肌肉交界处,它与脊椎动物大脑和脊柱的谷氨酸突触有着惊人的相似之处;这种苍蝇的其他优点还包括它的简单性和实验的多功能性,以及它作为模式生物长达一个世纪的历史。在这里,我们调查了突触发生的主要事件的发现,包括目标规范,形态发生,以及突触特化的组装和成熟,重点是在该研究所进行的工作果蝇神经肌肉接头。
背景
人脑中大约有1000亿个神经元[1,2它们通过数万亿个突触连接在一起[3.,4].因此,理解突触发生——突触连接发育和成熟的过程,使神经元形成构成知觉、认知和行为基础的回路——仍然是一项艰巨的任务。化学突触是连接突触前神经元和突触后目标的特殊的非对称连接,很少有例外。5,6].在人类中,突触的形成主要始于胚胎发育时期[7].突触发生遵循轴突寻路的过程,轴突尖端的一种被称为生长锥的运动结构通过响应一系列细胞外引导线索,在复杂和动态的环境中导航,与适当的目标进行物理接触[4,8,9].一旦轴突到达目的地,突触的形成就会通过细胞粘附分子(CAMs)、底物粘附分子(SAMs)以及突触前和突触后区室之间的双向信号等各种粘附作用开始。5,7].随着突触的成熟,突触前轴突通过突触囊泡(SV)的膜融合来组装有效的神经递质释放机制。Ca的流入触发SV的释放2+离子通过电压门控通道,并发生在被称为活性区(AZ)的特殊区域[7,10,11,12,13,14].同时,突触后区室可能是另一种神经元或另一种细胞类型的树突,在与突触前释放位点精确对齐的特定区域内积累神经递质受体[15,16,17].
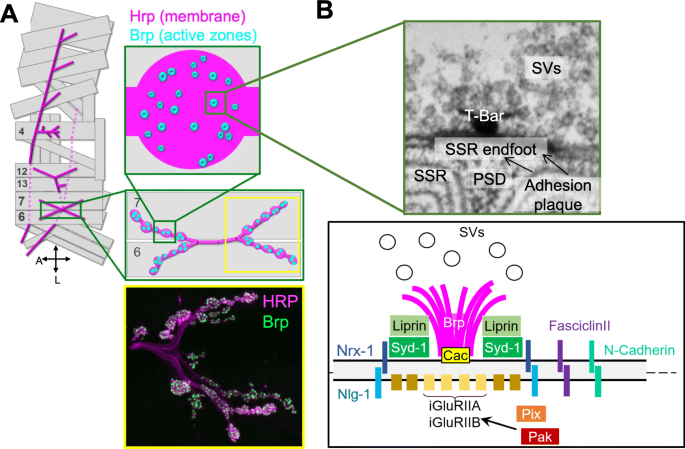
尽管理解脊椎动物中枢神经系统(CNS)的谷氨酸突触可以说是神经科学的首要目标之一,但蠕虫和苍蝇的PNS突触,如神经肌肉连接处(NMJ),是特别合适的模型,因为它们易于控制,而且在结构和化学上与脊椎动物中枢神经系统的突触具有惊人的相似性。对兴奋性谷氨酸突触的深刻见解,特别是已经从研究中出现果蝇幼虫NMJ(图;1) [18,19,20.,21,22].在果蝇中,NMJ是一个模式化的结构,通过解剖很容易接近,也可以通过半透明的幼虫角质层进行非侵入性成像。更广泛地说,果蝇NMJ可以通过复杂的基因突变、筛选、表达和编辑策略进行操作,并适用于先进的生化、电生理学、超微结构和光成像技术。在突触发生过程中果蝇,保守的信号通路,如骨形态发生蛋白[23,24], Wnt/Wingless (Wg) [25,26,27]、成纤维细胞生长因子[28],以及白细胞共同抗原相关受体蛋白酪氨酸磷酸酶(LAR-RPTP) [29,30.,31,32协调细胞和分子事件的复杂相互作用。
突触发生不是一个单一的事件,而是一个动态的过程。虽然突触发生最激烈的时期发生在胚胎期和出生后早期,但神经系统的发育持续整个青春期,甚至持续到人类生命的第三个十年[33].这些变化不仅包括新突触的增加,还包括它们的“修剪”或移除;据估计,人类新生儿前额叶皮层内的突触有一半在成年时被移除[33].重要的是,结构可塑性形成了学习和记忆的基础,反映了突触不仅对基线发育线索作出反应的能力,而且对急性外部刺激作出反应的能力[6,34,35].神经元的这种显著特性是基于相互的双向信号,以及突触前和突触后隔室的精确编排的组装和功能[6,34,35],强调把突触作为一个整体来理解的重要性。
Synaptic规范:找到正确的目标
当轴突生长锥与其目标发生物理接触时,各种CAMs就会协调正确的突触前和突触后伙伴的规范和对齐[7,36,37,38].CAMs在突触发育过程中发挥作用,除了在物理粘附中发挥作用外,还作为跨突触信号分子发挥作用,并参与SV组织、受体聚类以及结构和功能可塑性等过程[36,37,38].CAM相互作用的关键保守调控因子包括跨突触结合的Eph受体酪氨酸激酶及其配体ephrin,它们都可以在突触前或突触后的隔室中表达,并促进双向通信,以调节突触的形态发生和可塑性[39,40].CAM可分为两类:一类是与同类型的另一分子进行嗜同性相互作用,另一类是与不同CAM或与细胞外基质(ECM)中的底物粘附分子(SAMs)进行嗜异性相互作用[36,41].cam不一定局限于单一的绑定模式。例如,SynCAM [42,43,44]和II型经典钙粘蛋白[45]在体内同时显示亲同性和亲异性结合,而I型经典钙粘蛋白在体外显示两种形式的结合[46,47],但在体内只观察到嗜同性相互作用[48].
传统的亲同性cam包括NCAM/CD56 [49,50]和相关的果蝇束蛋白II (FasII) [51,52,53];DSCAM [54,55];SynCAM [42,43,44];以及I型和II型经典钙粘蛋白[56,57,58,59].在同质性CAMs中,I型cadherin cadherin - n / cadherin 2 (CadN)在中枢神经系统中表达最高,研究最好。CadN定位于突触间隙[60]并与突触前az相邻[61]并根据活动重新分配[62].除了提供黏附连接,cadn还参与神经传递[63],突触前短期可塑性[64],树突棘形态发生[65,66],枝晶的活性依赖塑性和稳定性[67,68],以及长期增强作用[69,70].其他同亲性CAMs也具有类似的多样化功能,包括神经元形态发生[71,72,73,74],自我平衡[75]和活动依赖性可塑性[50,53],突触结构的组织[42,76],以及长期增强作用[49,77].
突触上的嗜异相互作用是由CAMs介导的,如Neurexins和Neuroligins [78,79,80,81], Teneurins [82,83),而果蝇Dprs和DIPs [84,85].高度保守的Neurexins和Neuroligins可能是所有突触cam中最具特征的。Neurexins包括三个脊椎动物成员和一个苍蝇同源物Neurexin-1 (Nrx-1),而脊椎动物neuroigins 1-4各有一个对应的成员果蝇同源物(Nlg1-4) [78,80];在不同类群中都存在Neurexin和Neuroligin的其他同源物。Neurexins和Neuroligins都是专门的突触,在体外表达均足以诱导突触分化[86,87].Neurexins或Neuroligins的缺失会导致多个系统中突触形成和功能的严重甚至致命缺陷[88,89,90,91,92],反映了它们在促进生物体突触前和突触后成分之间形成稳定连接方面的核心作用[88,93,94,95,96,97,98].工作在果蝇NMJ表明Nrx-1-Nlg1的突触后靶点包括神经递质受体[93]和调节肌动蛋白细胞骨架动力学的WAVE调节复合物[99];nrx -1- nrg1的下游突触前靶点包括核心AZ组分[93]和BMP通路受体及效应器[94].Nrx-1- nlg1复合物介导相互作用的双向性质的进一步证据包括发现突触前AZ成分Syd-1直接结合Nrx-1,通过Nrx-1- nlg1调节GluRs的组成和聚类[93];这说明了核心AZ机制可以组织突触后对应物的一种机制。此外,肌肉Nlg1的缺失导致突触前形态和AZ组装的缺陷,这表明突触后装置可以调节释放位点的互惠机制[93].有趣的是,Nlg1还调控BMP通路受体Wit/Tkv亚基和Mad [94],以逆行的方式,进一步强调了Nrx-1-Nlg1功能的双向特性。
值得注意的是果蝇运动神经元也表达一种称为Neurexin IV (Nrx-IV)的蛋白质[One hundred.更恰当地归类为涉及人类自闭症谱系障碍的接触蛋白相关蛋白(CASPR)/paranodin/CNTNAP受体家族的同源物[101,102].尽管从c端到跨膜肽和膜近端LamG重复序列的结构相似,但Nrx家族树的这个CASPR/CNTNAP分支有一个更少的LamG结构域和两个额外的细胞外结构域(FIB基序和n端DISC结构域)。Nrx-IV在果蝇中最为人所知的是其在神经胶质细胞之间形成的隔膜连接中的重要作用,从而在中枢神经系统和血淋巴之间创建一个不渗透的屏障[103].然而,Nrx-IV也在多种情况下参与胶质-神经元相互作用[104,105,106].有趣的是,在这篇综述中,Nrx-IV发挥了意想不到的作用果蝇突触生物学,因为突触前Nrx-IV表达水平的改变导致异常的NMJ形态和AZ密度synaptic形态[107].Nrx-IV的这些功能被认为是微(mi) RNA miR-34的下游,miR-34协调突触前和突触后的突触发生[108].到目前为止,还不清楚Nrx-IV的这种作用是由突触后Nlg介导的,还是之前发现的Nrx-IV受体/共受体介导的。
与CadN和NCAM/FasII或Neurexins和Neuroligins等cam的数十年工作相比,Tenurins和Dprs/DIPs的重要性是相对最近才认识到的。高度保守的Teneurins包括四个脊椎动物成员,其中一个秀丽隐杆线虫元素和2果蝇成员(82].脊椎动物Teneurins在视觉系统partner匹配和细胞特异性中的作用最为突出[109].在果蝇NMJ中,突触前的10 -a和突触后的10 -m形成一种异亲性复合物,调节突触规范、神经元形态、突触结构和神经传递[110].值得注意的是神经元的损失10和肌肉ten-m不仅在它们各自的隔室中产生缺陷,而且在相反的细胞中也产生缺陷:10表型包括突触后光谱蛋白和突触下网(SSR)的减少,而ten-m表型包括突触前MTs、sv和T-bar形态的中断[110].这些发现表明,Teneurins,连同Neurexin和Neuroligins,可以在顺行和逆行方向介导突触间隙的通信。
CAMs的跨突触结合和下游输出,与其他信号信号线索和与ECM的相互作用一致,协调突触前和突触后伙伴之间的膜接触。飞虫NMJ的膨胀通过Wnt/Wg- [111]和依赖bmp的[112,113增加新的钮扣。可能的bouton添加模式包括不对称出芽,类似于酵母细胞分裂;对称钮扣划分;或由轴突轴从头形成[114].除了增加bouton外,消除或修剪bouton对优化突触结构和防止过度生长也很重要[18,19].在突触扩展过程中也观察到中间结构,如突触前“碎片”和丝状足状突触体,尽管与boutons不同,这些结构只是非常短暂地观察到[18,19,111,115].这些序列的形态过程,包括钮扣的增加,然后扩展到完全大小,必要时,剪枝,由基线和/或活动依赖的信号信号调节,以实现突触的大小和结构,以促进适当的连接和强度。
突触前AZ组装的快速启动
在I型幼虫的形态发生过程中(Ib型和Is型;参阅[116,117]以详细讨论突触和钮扣类型),膜的初始生长先于功能和结构突触组件的募集。为了支持这一点,大量的光成像实验在果蝇已经揭示了新生的钮扣最初缺乏突触前和突触后的特化[111,118,119].随后对果蝇的相关时间流逝光和超微结构研究表明,这些不成熟的“幽灵”扣是高度瞬态的,因为AZ前体和SV对接在几分钟内就可以看到。突触后特化形成较慢,但有些成分需要数小时才能到达并完全积累[120,121].在切断的轴突中仍然可以观察到这些钮扣的添加和成熟过程,尽管频率低于完整的轴突,这表明在缺乏蛋白质合成的情况下,局部机制足以支持至少某种程度的突触扩展[119].
AZ组分的积累产生了致密的蛋白质基质,其中至少有5种在多个分类群中广泛保守:RIM/Unc-10、Munc13/Unc13、边缘结合蛋白(RBP)、Liprin-α/SYD-2和ELKS/CAST/ERC/Bruchpilot (Brp) [11,12].最近的数据表明,虽然AZ蛋白Syd-1以前被认为是无脊椎动物独有的[122,123,124],最新研究发现小鼠中存在一种名为MSYD1A的同源基因[125].然而,当用超微结构分辨率观察这些成分时,形态在突触和生物体之间有所不同(综述[11,13].例如,果蝇NMJs在较大粘连斑块的中心显示t形结构,其特征为电子致密膜形态和一组重复的膜-膜交叉桥(图2)。1).在脊椎动物中,一种网格状排列的金字塔状密集投影已在CNS [126],感觉突触显示“带状”投影[127],其结构范围可从扁平结构到球形结构[128].尽管存在这些形态差异,但积累的证据表明,这些密集的投射在突触前的功能和组织中具有基本相似的作用;这些作用之一是SVs通过细丝与这些投影的物理捆绑,正如在小鼠中观察到的那样[129],青蛙[130]和苍蝇[131].
尽管轴突隔室内存在局部组装机制[119],一般来说,AZ的发育依赖于AZ成分以及SV前体(SVPs)和其他物质的运输,通过细胞体的远程机动运输[132,133,134,135,136],尽管扩散等机制也可能对[137,138].关于在发布站点如何将AZ和SV组件组织成功能结构,存在几个模型。体外研究表明,被称为短笛/巴松管运输囊泡(PTVs)的特化密集核心囊泡(DCVs)可能以一种单一/定量的方式传输组件,这样每个PTV包含一个预先组装的AZ“包”[139,140].有人提出,AZ和SV材料以1-2个ptv和5-6个svp的集合体共同运输,这些集合体在交付时可以非常迅速地形成一个功能AZ [141,142,143,144,145].然而,ptv和现成可用az包的存在尚未通过体内研究得到最终证实[146,147],到目前为止,还没有证据表明在ptv中含有预先组装好的az果蝇NMJ或其他无脊椎动物突触,尽管有趣的是,溶酶体相关囊泡(PLVs)已被发现运输sv和az在果蝇运动神经元轴突[148].
AZ早期组装:SYD-1、LIPRIN-Α、UNC-13
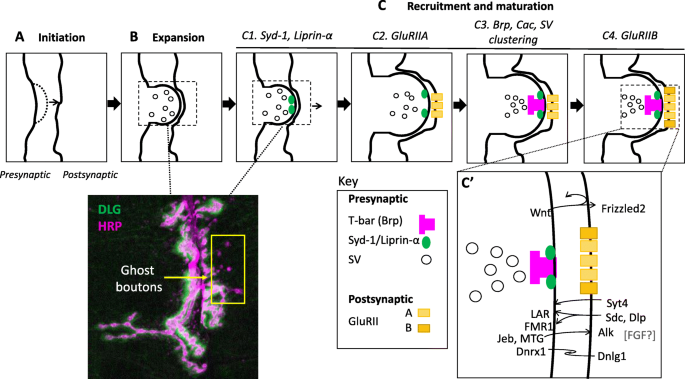
与上述预组装AZ模型相反,无脊椎动物体内研究表明,虽然AZ组装发生得非常快,但仍可以区分一系列步骤(图2)。2c) (146].为了支持分级可用分区组装,在此基础上进行了大量的研究秀丽隐杆线虫而且果蝇表明两个最早被招募到突触前az的成分是支架蛋白Syd-1/ Syd-1和lipin -α/SYD-2 (synapse -d的有效性)93,122,123,124,149,150,151,152,153,154];果蝇的证据表明,这些成分可能比其他AZ蛋白早几个小时[122,149].在蠕虫和苍蝇中,Syd-1和Liprin-α在驱动AZ早期组装过程中具有密切的空间和功能关系[122,124]以及SV组织[152,154].在苍蝇中,损失syd-1而且liprin -α导致NMJ尺寸减小,AZ尺寸增大,分别由光镜和电子显微镜观察到[120,122,表明AZ组织存在潜在缺陷。此外,两者的损失syd-1或liprin -α在果蝇导致神经传递减少[120,122].
钮扣生长和突触成熟概述。钮扣的增加是由膜生长引起的(一个),然后扩大规模(b).(上)在几分钟内,随着Syd-1和Liprin-α等早期成分的积累,AZ前体形成。(下)α-Dlg标记的I型NMJ突触后SSR和突触前区α-HRP的免疫染色。缺乏突触后结构的未成熟钮扣(幽灵钮扣)被指出(Ci).成熟发生在突触前和突触后特化的剩余成分被招募时,包括gluriia型受体(人民共和国);Brp, Cac和SVs (Ciii);和gluriib型受体(文明).插图(c’)显示双向跨突触通路,这对突触发育非常重要。主要通路包括经典和非经典的Wnt和BMP信号,同时也描述了由Syt4、LAR、FMR1、Jeb和MTG介导的通路。FGF途径也有报道,但途径的细节,如方向性,还没有定义
Syd-1支架蛋白定位于突触前末梢的点状簇,在蠕虫中似乎是神经系统特异性的[123,124,155],以及在苍蝇中[122].早期研究证实,Syd-1具有PDZ、C2和rhogtpase - activation protein (GAP)-like结构域[155],尽管Syd-1的RhoGAP活性一直存在争议,直到最近才发现它是ELKS/Brp聚类所必需的[153].Syd-1可能是最早集中在新生AZ的AZ成分之一,因为Syd-1位于Liprin-α in的上游秀丽隐杆线虫(123,124和在果蝇,其中需要Syd-1才能正常积累Liprin-α [122].Syd-1还通过直接结合Nrx-1与Nrx-1- nlg跨突触黏附复合物相互作用,调节突触后受体聚类[93].到目前为止,还没有明确的哺乳动物Syd-1同源物被确定,尽管基于部分序列相似性和在SV对接和突触传递中的类似作用,小鼠MSYD1A被认为是可能的同源物[125].
与Syd-1相反,Liprin家族成员Liprin-α在后生动物中高度保守,人和动物之间有~ 50%的相似性秀丽隐杆线虫同源,除神经系统外,在许多组织中广泛表达[121,156].Liprin-α在突触前区室中已被很好地表征,有趣的是,也被发现具有高度丰富的突触后表达,可能表明突触后作用[121,156].在结构上,Liprin-α包含一个N-terminal卷曲线圈区域,它介导同源和异质多聚化,以及一个c端Liprin同源(LH)区域,包含三个SAM(不育-α-motif)结构域[120,157,158].特别是LH区域的SAM结构域,被认为介导Liprin-α与Syd-1和至少12个其他参与突触发育和/或功能的蛋白质的相互作用[121,156].事实上,Liprin-α最初是通过它与lar - rpps成员的相互作用被发现的,包括脊椎动物LAR, PTPδ和PTPσ [157,158];虽然这些最初的观察是在非神经元细胞的局灶性粘连上,但对LAR和Liprin-α的研究一直专注于它们在神经系统中的不同功能。特别是LAR在轴突引导、神经突延伸以及突触组装、形成和可塑性方面起着关键作用[29,30.].Liprin家族蛋白还包括Liprin-β,它和Liprin-α一样,是促进果蝇NMJ突触扩张所必需的,Liprin-γ/KazrinE,它在NMJ中拮抗Liprin-β的功能[151].然而,与Liprin-α相比,Liprin-β和Liprin-γ的作用在很大程度上仍然未知,它们是否在AZ中发挥作用仍有待观察。
最近的一项研究果蝇研究表明,神经递质释放的中枢调节因子Unc13的两种蝇类亚型之一Unc13A可能与Syd-1和Liprin-α共同募集[103].Unc13是在秀丽隐杆线虫(104],后续研究证实了其在SV对接、启动和融合中的作用[159,160].Unc13启动SNARE/SM机制进行胞吐[105,161]并调节释放动力学[103].通过调控SV释放,Unc13还参与多种形式的可塑性,包括短期增强和长期增强和抑制[106,162].超分辨率显微镜揭示了这两个果蝇同位型Unc13A和Unc13B相对于其他核心成分和Ca具有不同的定位模式2+这表明不同的亚型可能通过独立的途径调节和优化SV释放[103].有趣的是,随着AZ组装和成熟的进展,从Unc13A募集到Unc13B募集的转变让人联想到突触后区室中不同受体亚单位以顺序方式募集的模型(有关这一过程的更多细节,请参阅“突触后细胞基质”一节;图2 cii-iv) [93],可能反映了单个分子异构体在突触成熟的不同阶段的不同作用。
下游AZ组件:rim、rim- bp和BRP
Syd-1和Liprin-α募集后[122,123,124,149],而Unc13A亚型[103],其余AZ组件本地化,包括Unc13B、RIM/Unc-10、RIM- bp、ELKS/Brp。与Unc-13一样,RIM (Rab3 -我实习米分子)首次被发现是SV释放和神经传递的调节因子[163,164],后来发现从自抑制同二聚体复合物中单体化Unc-13促进SV引物[165,166,167].RIM还在短期和长期可塑性方面发挥作用[168,169]和Ca2+到AZ的通道本地化[167,170,171,172].特别是Ca的调控2+通过与RIM- bp的相互作用来调节173,174].RIM和RIM- bp支架蛋白一起形成与Ca相互作用的复合物2+渠道(172,175].中进一步证明了rim - bp的重要性果蝇,突变在哪里rim-bp导致Ca2+通道聚类以及Brp分布、AZ超微结构和突触释放的中断[176].
除了Unc-13、RIM和RIM- bp外,支架ELKS/Brp的积累也伴随着Syd-1和Liprin-α的AZ组装,这一过程可以在新钮扣形成后的几分钟内开始[119]但这可能需要数小时才能完成[149].工作果蝇为Brp在AZ的功能提供了令人信服的线索。果蝇Brp以两种异构体表达,这两种异构体在突触上都是必需的[177].免疫荧光显示,Brp在运动神经元的突触前末端形成独特的点状结构[178,179以及其他神经元,如R8光感受器[180].在活荧光研究中,一种非功能性截断Brp-short结构[149,181]常被用作突触前AZ的标记物,以取代可在过表达时聚集的全长Brp [179].重要的是,Brp是AZ的基本结构成分,被认为是电子显微镜可见的电子密度t条的主要成分(图2)。3.) [149], Brp的丢失导致t型条的完全消除[178,179].超分辨率激发发射耗竭(STED)显微镜显示Brp点实际上是甜甜圈状结构,代表附着在突触释放位点膜上的漏斗状Brp复合物的上半部分[149,178],这两个果蝇Brp异构体以圆形模式交替[177].将直接随机光学重建显微镜(dSTORM)超分辨率与电生理学相结合的进一步研究表明,成熟的AZs由大约137个杆状Brp蛋白组成,组织成大约15个七聚体结构,而适当的神经传递依赖于这种多聚体结构的化学计量学和组织的精确维持[182].Brp除了作为AZ的关键结构成分外,还被认为通过控制SVs的易释放池(RRP)的大小来调节突触释放[177].Brp也是短期塑性的必要条件,Ca2+通道聚类[178],与观察到的相一致果蝇Ca2+声道亚基不和谐音(Cac)同时被招募到AZ [149].
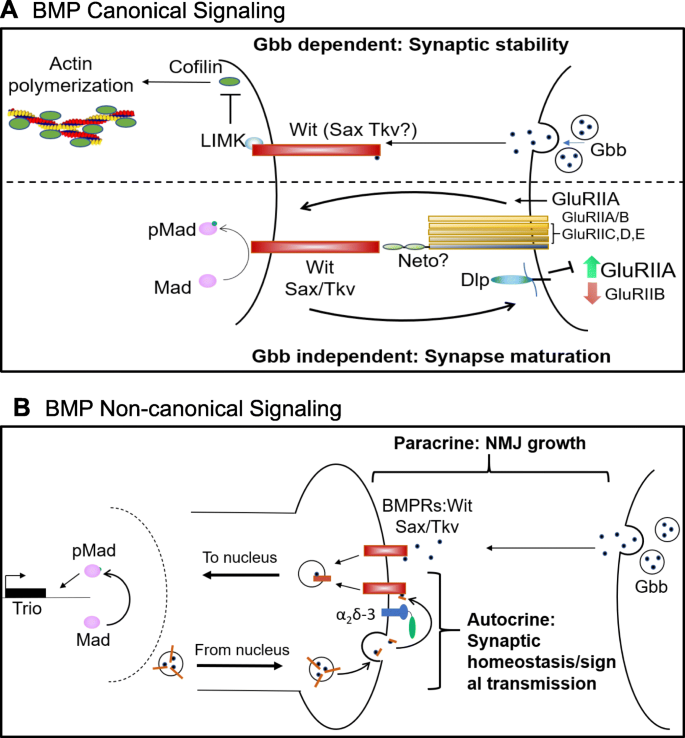
BMP规范和非规范信号在NMJ。一个BMP规范信号包括旁分泌、逆行机制,肌肉源性Gbb通过突触释放,激活BMPRs Wit和Sax/Tkv触发内化。内化的Gbb被运输到神经元核,在那里它激活Mad的磷酸化到pMad,从而激活Trio-GEF的转录,促进NMJ的整体生长。第二种自分泌典型途径包括cpy结合的Gbb从被α隔离的神经元释放2δ-3,钙通道亚单位。然后,神经元衍生的Gbb结合BMPRs并引起类似于旁分泌典型通路的转录变化,以调节突触稳态和信号传递。bBMP非典型信号通路包括Gbb依赖和独立的信号通路。Gbb依赖的非规范信号包括Gbb在与Wit结合的地方逆行释放。LIMK作为Wit效应剂抑制Cofilin,通常通过丝切断促进肌动蛋白动力学。在Gbb独立的非规范机制中,含有iGluRs的GluRIIA与局部突触前pMad形成正反馈环路。该机制依赖于Wit和Sax/Tkv,但不依赖于转录,并被Dlp (Glypican)抑制。
本文中关于AZ的组成、体系结构和功能的讨论只涉及这个高度复杂和重要结构的大量工作中的一小部分。突触前AZ的细胞壁包含许多其他蛋白质,包括:短笛/法夫和巴松支架;Ras超家族gtpase,如Rab3和Rac1,以及它们各自的gap和鸟嘌呤核苷酸交换因子(gef);细胞膜运输机制,如SNARE蛋白、突触素和突触tagmin;三方Cask/Mint1/Veli配合物;发育信号通路;细胞骨架网络[11,12,183,184,185].此外,尽管在整个领域取得了重大进展,但关于阿斯利康的许多问题仍然存在。正在进行的和未来的研究将涉及的主题包括AZ的精确超微结构/纳米结构,AZ如何参与短期和长期的可塑性,以及AZ如何感知和调节突触的稳定性和完整性[11,12].
突触后细胞突
与突触前末端相反,突触前末端总是神经元[7],突触后靶细胞通常是神经元细胞,但也可以是其他类型的细胞,如胶质细胞[186,187,188,189,190或效应器官,如果蝇NMJ。早期对哺乳动物兴奋性突触的树突棘的超微结构研究发现了一种被称为突触后密度(PSD)的三维细胞内结构,该结构位于脊柱膜的正下方[191,192,193].树突棘PSD和其他突触后细胞类型中的类似细胞室结构[13],富含多种蛋白质类型,包括神经递质受体以及支架、信号和细胞骨架分子[15,16,17].谷氨酸受体(GluR)是最常见的受体类型,存在于脊椎动物中枢神经系统和无脊椎动物NMJ中占主导地位的兴奋性谷氨酸能突触[194,195].GluRs包括离子型GluRs (iGluRs),这是一种丰富的亚型,其中受体本身形成一个离子通道孔,以介导毫秒级的快速突触传输;这与代谢性GluRs (mGluRs)相反,后者通过次级信使激活离子通道,而且作用较慢,出现频率较低[194,195].iGluRs可进一步细分为AMPA-、NMDA-和kainate型受体,其中AMPA和NMDA受体最为常见[194].在果蝇NMJ中,只有AMPA/kainate受体在基因组测序的基础上被鉴定[195,196].然而,最近的研究表明,果蝇NMJ上的iGluR可能不同于经典的脊椎动物iGluR亚型,因为它们显示出不同的结构和神经递质结合特性[197].
在果蝇NMJ、iGluRs是由GluRIII/GluRIIC、GlURIID和GluRIIE三个不变亚基以及GluRIIA或GluRIIB中的一个组成的异质四聚体[198,199,200,201,202,203].将iGluRs招募到突触后细胞室需要基本的保守辅助亚基Neto [204,205,206,207,208并被认为发生在突触前AZ成分Syd-1和Liprin-α到达之后,但在Brp和Cac募集之前(图2)。2c) (149].GluRIIA和GluRIIB的单通道特性不同,它们分别负责大的和小的谷氨酸门控电流[203,209].在果蝇NMJ中,适当的iGluR亚基组成和GluRIIA/GluRIIB平衡是由Neto调节的,可能是通过Pak的招募[206),果蝇p21活化激酶(PAK)的同源物[210,211].含有GluRIIA和GluRIIB亚基的iGluRs的比例进一步由突触前AZ蛋白Syd-1通过与Nrx-1-Nlg1复合物的相互作用调节[93]和通过非规范的、smad依赖的BMP通路[212].GluRIIA与GluRIIB亚基的比例在突触的整个生命周期中发生变化,年轻的突触优先合并GluRIIA,随着突触的成熟,GluRIIB也会合并[181].GluRIIA募集被认为是突触形成的重要驱动力,它与GluR四聚体的结合几乎是不可逆的[181,209,213];后一种特性,以及GluRIIA合并在GluRIIB之前的倾向,可能解释了GluRs的同心排列,其中富含GluRIIB的受体在富含GluRIIA的核心周围形成一个环(图2)。2c) (93].适当的亚单位募集的时间序列,以及GluRIIA-和gluriib相关受体的相对空间排列,被认为不仅对于突触的起始发生是必要的,而且对于随后的稳定和成熟也是必要的[93].
除了神经递质受体外,突触后细胞室中还富含在突触成熟和稳定中发挥进一步作用的其他因子。除了上述在iGluR组成中的作用外,Pak还调节突触后支架大圆盘(Dlg)的水平,肌肉超微结构,以及SSR的形成,SSR是包围突触前钮扣的管状-板层膜褶皱的突触后系统[214,215,216,217]被描述为在结构和功能上等同于树突棘的果蝇NMJ [218].SSR扩展的另一个值得注意的调节因子是Syndapin (Synd),它是F-BAR膜雕刻蛋白家族的成员[219,220],似乎只出现在突触后,它可能通过调节肌肉肌动蛋白细胞骨架来介导SSR的发展[221,222].SSR的发展还需要更多的肌动蛋白调节蛋白集中在突触后的细胞突中,包括hu-li tai shao (Hts)/内收蛋白,一种肌动蛋白盖帽蛋白[223,224,225]和Enabled (Ena) [226],促进线性F-actin的组装;SSR形态发生的其他关键细胞骨架调控因子包括突触前和突触后的Spectrin [227,228]和突触前锚蛋白[229,230].最后,含有PDZ结构域的脊椎动物PSD-95/SAP90蛋白Dlg属于PDZ蛋白膜相关鸟苷基激酶(MAGUKs)家族[15,16],促进激振子K的聚类+离子通道[231]和FasII的[232].Dlg对于含gluriib受体的聚类也是必要的[233],而脊椎动物PSD-95调节NMDA受体的聚类[234].虽然Dlg在突触后SSR中最为丰富,但在突触前AZ中也存在较低的水平[235],与lipin -α的分布相似[121,156].
一些传统上主要与突触前或突触后作用相关的因素,包括Dlg和Liprin-α,也显示相反的定位,尽管丰度降低,这表明需要在新的环境中重新考虑这些因素。Dlg呈现出一个类似于Liprin-α的突触前池,已被证明可以促进Cac的AZ定位,并对突触释放概率和短期可塑性产生影响[236].lipin -α,主要作为一种突触前AZ蛋白被研究,显示出压倒性的突触后分布[121,156].突触后Liprin-α与PSD中的pdz结构域蛋白GRIP相互作用,也受Ca的调控2+/钙调蛋白依赖性蛋白激酶II (CaMKII) [237].在这些研究之外,突触后Liprin-α的作用,包括在果蝇NMJ在很大程度上是一个谜,可能会为未来的研究提供肥沃的土壤。考虑其他常规突触前蛋白的可能的突触后表达也是有趣的,如Syd-1,它似乎显示出一些突触后染色[122].
隔室间的跨突触通信
尽管突触前区室和突触后区室之间存在差异,但有效的双向通信对于整个突触的协调组装、成熟和功能至关重要(图2)。2c”).跨突触通信的关键协调者包括信号转导通路,包括作为顺行信号的主要驱动因素的Wnt/Wg通路[25,26,27],而BMP通路是逆行信号的主要贡献者[24].这些信号通路控制着神经发育的许多不同方面,包括生长、信号传递、突触成熟、AZ组装和稳态。有趣的是,这些功能是由信号通路控制的,这些信号通路具有许多相似的生长和下游因子,并且能够在发育过程中根据需要区分这些功能。本节将详细介绍信号的不同类别和子类别,并描述发展中的NMJ如何能够区分它们。
在果蝇NMJ中,Wg同时参与顺行和自分泌信号。Wg从突触前末端分泌,并结合嵌入突触后膜的Frizzled2 (Fz2)受体。Fz2的激活触发受体的内化和切割,允许c端片段(Fz2- c)进入突触后核,在那里它有助于基因表达的变化,从而积极调节突触的扩展和可塑性[27,238].逆行的Wg信号传导受到几种细胞外因子的负调控,包括细胞外基质金属蛋白酶(MMPs)和脱羧酯酶Notum,它们分别裂解HSPG共受体和Wg,以限制信号传导[239].突触前的Wg配体也介导一个分散的典型通路,调节突触前的细胞骨架。神经来源的Wg使糖原合成酶激酶3 (GSK3)/Shaggy失活,后者通过与Map 1B同源物Futsch相互作用调节微管动力学[240,241,242].
BMP信号在NMJ中控制神经元发育的许多方面,包括生长、突触传递和突触稳态。许多BMP信号的这些功能不是同时发生的,但使用许多相同的因素来引起这些反应。那么细胞是如何解开这些信号功能来实现正常发育的呢?最近令人兴奋的发现补充了过去的研究,表明我们如何开始根据信号的差异来区分这些功能。果蝇同时利用典型和非典型的BMP信号。在典型的BMP通路中,玻璃底船配体(Gbb)与BMP7同源,由肌肉分泌,并与四聚体复合物结合,其中包含II型受体Wishful Thinking (Wit)和I型受体thickvein (Tkv)和Saxophone (Sax)。这种相互作用介导转录因子Smad/Mothers的磷酸化对抗十肢瘫痪(Mad) [243,244,245],从而影响转录,导致依赖活性的生长或突触聚类[113].典型BMP信号也可能通过与Rho-GEF三人组的相互作用调节肌动蛋白;人们认为逆行BMP通路调节突触前三联蛋白的转录水平以限制突触生长[246].
虽然前面的典型BMP描述代表了一种顺行、跨突触机制,但第二个典型BMP通路涉及一种自分泌信号机制,其中依赖活动的刺激指导突触加强和成熟[247].当活动依赖刺激促进运动神经元释放和重吸收Gbb,触发局部持续的BMP反应时,就会发生自分泌信号。最近,钙通道亚基(α2δ-3)被发现与神经元衍生的Gbb发生物理相互作用,并被要求限制Gbb可以加强突触的作用范围[248].
旁分泌和自分泌BMP典型信号均利用Gbb与Wit结合引起信号级联,允许pMAD调节转录。那么,运动神经元如何区分这两种信号来调节两种可分离的功能(钮扣生长和突触(AZ)密度)?每种类型信号的时间需求部分解释了其可分离性,因为肌肉衍生的生长信号主要是在早期阶段(L1)需要的,而持续的神经元衍生信号则是在后期阶段需要的,以细化和加强突触[248].此外,与Gbb相互作用的因素也可以分离功能。Crimpy (Cmpy)与Gbb发生物理相互作用,促进Gbb招募到密集的核心囊泡(DCVs),在那里它可以从Cmpy外畴的神经元末梢释放[249].缺乏Cmpy会导致过度生长,这可能是因为没有Cmpy,神经元会将自分泌BMP信号误解为肌肉源性BMP信号,而肌肉源性BMP信号通常控制整体生长。
一些非典型的BMP通路也被识别出来,并根据它们是否利用Gbb进行划分。非典型的Gbb依赖信号通路控制bouton的生长,当肌肉分泌Gbb并与神经元Wit相互作用激活LIM Kinase1 (LIMK1)时发生。LIMK1通过促进肌动蛋白聚合调控活性依赖的钮扣形成[112,250].非典型的gbb独立信号通路促进谷氨酸受体异四聚体中GluRIIA亚基的稳定性。gbb独立的非典型信号通路涉及一个正反馈回路,GluRIIA在其中促进局部突触前pMad库在az的积累。pMad反过来比GluRIIB优先聚集和稳定额外的GluRIIA亚基[212].重要的是,这种BMP信号利用了与典型BMP信号不同的通路,因为当核pMad作为转录调节因子时,突触pMad的积累不会导致NMJ过度生长。此外,虽然这种正反馈机制确实需要Wit和Sax,但它不使用LimK,从而区别于非规范的依赖于gbb的BMP信号。如果这个通路不通过像Gbb这样的扩散因子进行交流,那么跨突触的交流是如何实现的呢?正如Sulkowski等人所指出的,突触间隙为~200A, GluR四聚体和BMP受体(BMPRs)分别延伸~135A和~ 55A进入突触间隙。GluR辅助蛋白Neto增加了GluR四聚体的跨度,这表明它可以作为跨突触链接,尽管需要对这个模型进行仔细的测试。
除了Wnt/Wg和BMP,在果蝇NMJ中还描述了许多其他重要的信号转导途径。多项研究已经证实Synaptotagmin 4 (Syt4)在逆行信号传导中的作用[251,252]和LAR(白细胞共同抗原相关)[31,120].而Syt1,另一个突触表达果蝇synaptotagmin亚型,与突触前sv有关[253], Syt4是严格意义上的突触后Ca2+调节突触前SV融合和响应突触后Ca的活动依赖结构可塑性的传感器2+涌入(251,252].突触信号也受到硫酸肝素蛋白聚糖(HSPGs)的调控,如Dallylike (Dlp)和Syndecan (Sdc),其影响包括Wnt/Wg和BMP在内的多种途径[254,255].Dlp在GluRIIA和突触前pMad之间的正反馈回路中起负制动作用,而pMad本身被章鱼胺(果蝇的非肾上腺素类似物)的存在所抑制[256].此外,Dlp和Sdc调节RPTP LAR,影响突触前神经元形态和AZ组装[31,120].一个悬而未决的问题是,这些HSPGs与LAR的相互作用是否来自直接的物理结合,或者是否涉及另一种机制,如因子的分泌。此外,HSPGs对LAR和BMP信号的影响,以及Rho-GEF Trio在这两个LAR下游的观察[257,258]及BMP [246],增加了两种路径之间的交叉对话的可能性。最近发现Dlp和Sdc也通过细胞内脆性X智力迟钝1 (FMR1)蛋白以逆行方式起作用,以便与Wnt和果冻胃间变性淋巴瘤激酶(Jeb-Alk)信号通路结合[259].Jeb-Alk通路本身是一种顺行跨突触信号通路,可调节突触前形态和神经传递[260]在Mind-The-Gap (MTG)的控制下,MTG是一种突触前分泌的分子,可以调节突触间隙的细胞外环境[19,261,262,263].
有趣的是果蝇据报道,FGF受体无情(Htl)和窒息(Btl)与脊髓肌萎缩相关(SMA)蛋白生存运动神经元(SMN)相互作用,以调节NMJ的形态发生,这与FGF在脊椎动物突触中的作用一致[28,264,265].肌肉表达的Htl本身是突触前形态所必需的,尽管实现这一目标的精确跨突触机制仍有待定义[28];尽管如此,观察到两个SMN [266]和Htl [28]与突触后SSR共定位,提高了SMN在肌肉中FGF信号下游发挥作用的可能性。这种相互作用是有趣的,因为SMN似乎也在突触前BMP效应蛋白Mad和Dad的下游发挥作用[266],表明突触SMN可能对突触前和突触后区室的不同输入作出反应。事实上,已知突触两侧都需要SMN来支持正常的NMJ发育和生长[28,266,267,268]形成NMJ结构和功能的多个分子的特性[226,235,269,270,271,272].
上述通信机制中涉及的许多分子和通路在调节钮子形态发生和AZ组装方面都具有明确的作用,这提高了这两个过程耦合的可能性。事实上,与众多Wg、BMP和LAR通路成分相关的形态学和AZ表型与AZ组装与突触前末端大小(由bouton数决定)之间的反比关系一致。例如,在LAR通路中,这种相关性对LAR受体本身以及Liprin-α都是正确的[120], HSPG配体Dlp [273], Abelson激酶(Abl) [274]、Rho-GEF三人组[153,275]和f -肌动蛋白组装分子Ena [269].Syd-1及其下游效应子Nrx-1和Nlg1的AZ与NMJ大小呈负相关;虽然Syd1和Nrx-1-Nlg尚未被证实为LAR相互作用体,但它们可能通过Syd-1和Liprin-α的相互作用与LAR通路结合。93,122].虽然因果关系和潜在机制尚未得出结论,但积累的证据表明,bouton生长和AZ组装的调节机制并不是独立的。形态发生和AZ形成的协调可以确保有限的生物材料池的适当分配;这与AZ的化学计量和稳态重塑动态调整突触强度的发现是一致的[276].因此,对于这些过程的协调,一个可以想象的解释是,限制AZ的大小可以确保所有的钮扣都有释放位点,即使膜的膨胀仍在继续。
数据和材料的可用性
不适用。
缩写
- Abl:
-
阿贝尔森
- 筛选:
-
间变性淋巴瘤激酶
- AMPA:
-
α-amino-3-hydroxy-5-methyl-4-isoxazolepropionic酸
- 阿兹:
-
活跃区
- 骨形态发生蛋白:
-
骨形态发生蛋白
- Brp:
-
Bruchpilot
- 瓶:
-
上气不接下气
- Cac:
-
不和谐
- 凸轮:
-
酶分子
- CaMKII:
-
Ca2+/钙调素依赖性蛋白激酶II
- CASPR:
-
Contactin-associated蛋白质
- 演员:
-
与活性区相关的结构蛋白
- 中枢神经系统:
-
中枢神经系统
- 爸爸:
-
女儿们反对十肢瘫痪
- 直流电压:
-
致密的核囊泡
- 下降:
-
Dpr相互作用蛋白
- 了解:
-
光盘大
Dlp
Dallylike蛋白质
- Dpr:
-
长鼻反应不良
- Nlg:
-
果蝇Neuroligin
- Nrx-1:
-
果蝇Neurexin
- DSCAM:
-
唐氏综合症细胞粘附分子
- dSTORM:
-
直接随机光学重建显微术
- 麋鹿:
-
富含E、L、K和S氨基酸的蛋白质
- Ena:
-
启用
- ECM:
-
细胞外基质
- 伦理委员会:
-
ELKS/ rab6交互/CAST家族成员
- FGF:
-
成纤维细胞生长因子
- FMR1:
-
脆性X智力迟钝1蛋白
- GABA:
-
氨基丁酸
- 差距:
-
GTPase-activating蛋白质
- Gbb:
-
玻璃底船
- GEF:
-
鸟嘌呤核苷酸交换因子
- GluR:
-
谷氨酸受体
- GSK3:
-
糖原合成酶激酶3
- HSPG:
-
硫酸肝素蛋白聚糖
- Htl:
-
无情的
- 高温超导:
-
胡里太少
- iGluR:
-
Ionotropic GluR
- 杰布:
-
吉利
- 政治:
-
白细胞共同抗原相关
- LIMK1:
-
LIM Kinase1
- Liprin:
-
LAR-interacting蛋白质
- 韩:
-
Liprin同源性
- 疯了:
-
母亲们反对十肢瘫痪
- MAGUK:
-
膜相关的鸟苷基激酶
- 微型飞机:
-
特立独行的
- mGluR:
-
Metabotropic GluR
- MTG:
-
当心缺口
- Munc / Unc:
-
哺乳动物不协调或不协调的
- 门冬氨酸:
-
n -甲基-
- NMJ:
-
神经肌肉接头
- PAK / PAK:
-
p21-activated激酶
- PDZ:
-
PSD蛋白,DLG,闭塞带蛋白-1蛋白
- pn:
-
周围神经系统
- PSD:
-
突触后密度
- PTV:
-
短笛/巴松管运输囊泡
- 边缘:
-
Rab相互作用分子
- RIM-BP:
-
RIM-binding蛋白质
- RPTP:
-
受体蛋白酪氨酸磷酸酶
- RRP:
-
易于释放池
- 山姆:
-
无菌-α主题
- 山姆:
-
底物粘附分子
- Sax:
-
萨克斯风
- 提交:
-
Syndecan
- SM:
-
Sec1 / Munc18-like
- SMA:
-
脊髓性肌肉萎缩相关
- SMN:
-
存活运动神经元
- 陷阱:
-
可溶性n -乙基马来酰亚胺敏感因子激活蛋白受体
- 苏维埃社会主义共和国:
-
突触下网
- 、:
-
受激辐射耗竭
- SV:
-
突触囊泡
- 高级副总裁:
-
SV前体
- 悉德:
-
Synapse-defective
- Syt:
-
Synaptotagmin
- 十:
-
Teneurin
- TGF -β:
-
转化生长因子β
- Tkv:
-
Thickveins
- 智慧:
-
一厢情愿的想法
- Wnt /工作组:
-
无翼= 1 /无翼
参考文献
Saleeba C,邓普西B, Le S, Goodchild A, McMullan S.一个学生的神经电路跟踪指南。前沿神经科学2019;13:1-19。
人脑的数量:线性放大的灵长类大脑。神经科学。2009;3:31。
Colon-Ramos哒。神经回路发育中的突触形成。中国生物医学工程学报。2009;37(9):344 - 344。
Comer JD, Alvarez S, Butler SJ, Kaltschmidt JA。发育中的脊髓的共轴突引导:从卡哈尔到现在。神经科学进展。2019;14(1):1 - 16。
贾福生,李鹏,沈坤。神经科学中的细胞生物学:突触前形成的细胞和分子机制。中国生物医学工程学报,2013;23(1):329 - 329。
杰塞尔TM,坎德尔ER。突触传递:一种双向的和自我修改的细胞-细胞通信形式。细胞。1993;72(1):行。
Sudhof TC。为了理解突触的形成。神经元。2018;100(2):276 - 93。
Cammarata总经理,Bearce EA, Lowery LA。生长锥中的细胞骨架社交网络:+TIPs如何介导微管-肌动蛋白交联驱动轴突生长和引导。细胞骨架。2016;73(9):461 - 76。
Lowery LA, Van Vactor D.尖端之旅:理解生长锥的机制。中国生物医学工程学报。2009;10(5):332-43。
金勇,郭建林。突触前分化的分子机制。细胞发育生物学,2008;24:237-62。
阿克曼F,韦茨CL,加纳CC.无脊椎动物和脊椎动物突触前活跃区。EMBO报告2015;16(8):923-38。
Sudhof TC。突触前活跃区。神经元。2012;75(1):11-25。
翟荣国,贝伦。突触前神经末梢活跃区的结构。生理机能。2004;19(5):262 - 70。
艾曼,李文杰。果蝇活动区:从分子到行为。神经科学Res. 2018;127:14 - 24https://doi.org/10.1016/j.neures.2017.11.015.
盛敏,金东。突触的突触后组织。中国生物医学工程学报。2011;3(12):a005678。
Scannevin RH, Huganir RL。兴奋性突触的突触后组织和调节。神经科学2000;1(2):133-41。
盛敏,金俊杰。突触后信号和可塑性机制。科学(80-)。2002, 298(5594): 776 - 80。
Van Vactor D, Sigrist SJ。果蝇突触前形态发生、活动区组织和结构可塑性。Curr Opin neurobiology, 2017; 43:119-29[引于2020年2月10日]。可以从:http://www.ncbi.nlm.nih.gov/pubmed/28388491.
李志强,李志强,李志强。脑间隙突触前分泌对突触外基质-整合素界面和突触后环境的影响。计算机科学进展。2009;38(3):554-71。
柯林斯CA, DiAntonio A.突触发展:来自果蝇的见解。神经生物学杂志,2007;17(1):35-42。
高坂H,大泽S, Itakura Y, Fushiki A, Nose A.果蝇幼虫运动回路的发育。开发增长差异。2012;54(3):408-19。
柯夏卡H,盖廷PA,鼻子a。苍蝇幼虫运动的神经回路。中国医药杂志,2017;23(12):1722-33。
Keshishian H, Kim YS。协调发展和功能:果蝇神经系统中的逆行BMP信号。神经科学,2004;27(3):143-7。
巴亚特V,贾斯瓦尔M,贝伦HJ。在果蝇神经肌肉连接处的BMP信号通路及其与神经退行性疾病的联系。神经生物学杂志,2011;21(1):182-8。
Speese SD, Budnik V. Wnts:在突触上崭露头角。神经科学,2007;30(6):268-75。
王志强,王志强,王志强,等。Wnt信号通路在神经肌肉连接点发育中的作用。中国生物医学工程学报。2012;4(6):1-22。
Packard M, Koo ES, Gorczyca M, Sharpe J, Cumberledge S, Budnik V.果蝇Wnt,无翼,为突触前和突触后分化提供了必要的信号。细胞。2002;111(3):319 - 30。
森A, Yokokura T, Kankel MW, Dimlich DN, Manent J, Sanyal S,等。果蝇脊髓性肌萎缩的建模将Smn与FGF信号通路联系起来。中国生物医学工程学报。2011;29(3):489 - 497。
韩佳,全S,严建伟,高杰。突现突触组织者:LAR-RPTPs及其同伴。中国生物医学工程学报。2016;324:39-65。
Um JW, Ko J. ar - rptps:形成突触发育的突触粘附分子。细胞生物学杂志,2013;23(10):465-75。
Johnson KG, Tenney AP, Ghose A, Duckworth AM, Higashi ME, Parfitt K,等。HSPGs Syndecan和Dallylike结合受体磷酸酶LAR,对突触发育有明显影响。神经元。2006;49(4):517 - 31所示。
杜娜,胡思克,M,胡根拉德,贾沃斯基,朴,等。兴奋性突触发育和维持中的LAR受体蛋白酪氨酸磷酸酶。神经科学。2005;8(4):458-67。
裴丹杰,朱达林,Šimić G,雷辛先生,尤林斯,胡晓明,等。人类前额叶皮层的突触棘异常稚嫩。中国科学(d辑),2011,26(3):349 - 349。
坎德尔ER。记忆存储的分子生物学:基因和突触之间的对话。科学(80-)。2001, 294(5544): 1030 - 8。
蔡柏利,ER坎德尔,KM哈里斯。突触可塑性和记忆巩固的结构成分。中国生物医学工程学报。2015;7(7):1-29。
Thalhammer A, Cingolani LA。细胞黏附与突触可塑性。神经药理学。2014;78:23-30。
贾佐格鲁,李春华,李志强。细胞粘附,突触的主干:“脊椎动物”和“无脊椎动物”的视角。中国生物医学工程学报。2009;1(4):a003079。
突触黏附:记忆的基石?神经元。1998;20(6):1059 - 62。
丽高,叶NY突触发育和可塑性:ephrin/Eph受体信号通路的作用。神经生物学杂志。2009;19(3):275-83。
李国强,李国强。Eph/ephrin信号通路在细胞-细胞和细胞-基质粘附中的作用。前沿科学,2012;17(2):473-97。
孙明民,谢伟。果蝇突触发育与功能的细胞粘附分子。中国科学:生命科学,2012;35(1):20-6。
Biederer T, Sara Y, Mozhayeva M, Atasoy D,刘x, kalavalali ET,等。SynCAM,一种驱动突触组装的突触粘附分子。科学(80-)。2002, 297(5586): 1525 - 31所示。
Fogel AI, Akins MR, Krupp AJ, Stagi M, Stein V, Biederer T. SynCAMs通过嗜异黏附组织突触。神经科学杂志,2007;27(46):12516-30。
孙晓峰,陈晓峰,陈晓峰,等。突触细胞黏附分子通过调节轴突-轴突接触参与感觉轴突寻路。中国生物医学工程学报,2014;29(4):344 - 344。
Brasch J, Katsamba PS, Harrison OJ, Ahlsén G, Troyanovsky RB, Indra I,等。II型钙粘蛋白的同质性和异质性相互作用确定了细胞粘附行为的特异性组。Cell Rep. 2018;23(6): 1840-52。
Ounkomol C, Yamada S, Heinrich V.对AFM悬臂上排列的功能化微球的单细胞粘附试验证实了异亲性E-和n -钙粘蛋白结合。中国生物工程学报,2010;29(3):344 - 344。
陈志伟,陈志伟,陈志伟。钙粘蛋白黏附的研究进展。中国科学院学报(自然科学版),2006;29(3):344 - 344。
巴苏R,泰勒先生,威廉姆斯我。突触特异性中的经典钙粘蛋白。中国生物医学工程学报,2015;9(3):193-201。
Lüthi A, Laurent JP, Figurovt A, Mullert D, Schachnert M.海马长期增强与神经细胞黏附分子L1和NCAM。大自然。1994;372(6508):777 - 9。
王春华,王志强,王志强,王志强,等。PSA-NCAM是活动诱导的突触可塑性所必需的。神经元。1996;17(3):413 - 22所示。
舒斯特CM,戴维斯GW,费特RD,古德曼CS。突触可塑性的结构和功能成分的遗传解剖。I.束素II控制突触的稳定和生长。神经元。1996;17(4):641 - 54。
戴维斯GW,舒斯特CM,古德曼CS。控制靶选择机制的遗传分析:靶源性束素II调节突触形成模式。神经元。1997;19(3):561 - 73。
Beumer K, Matthies HJG, Bradshaw A, Broadie K.整合素通过CaM激酶ii依赖通路调节DLG/FAS2,在胚胎后发育期间介导突触的细化和稳定。发展。2002;129(14):3381 - 91。
Agarwala KL, Ganesh S, Amano K, Suzuki T, Yamakawa K. DSCAM,哺乳动物中高度保守的基因,在分化小鼠大脑中表达。生物化学与生物物理学报,2001;29(3):377 - 382。
唐氏综合征细胞黏附分子DSCAM介导的细胞间黏附。Mol Brain res 2000;79(1-2): 118-26。
铃木,武一。钙粘蛋白在神经元形态发生和功能中的作用。开发增长差异。2008;50(增刊1):S119-30。
平野,吴一。钙粘蛋白在脑形态发生和布线中的作用。中国生物医学工程学报(自然科学版),2012;26(2):597-634。
Brigidi GS, Bamji SX。钙粘蛋白-连环蛋白在突触处的黏附复合物。神经生物学杂志,2011;21(2):208-14。
王晓明,陈晓明,王晓明,等。钙粘蛋白与连环蛋白在树突和突触形态发生中的作用。中国生物医学工程学报,2015;9(3):202-13。
杨晓明,王晓明,王晓明。鸡视顶盖发育过程中黏附分子的表达。神经科学杂志,1995;15(6):4556-71。
Uchida N, Honjo Y, Johnson KR, Wheelock MJ, Takeichi M.连环蛋白/钙粘蛋白粘附系统定位于突触连接边界的递质释放区。中国生物医学工程学报,1996;26(3):344 - 344。
张志刚,张志刚,张志刚,张志刚,等。在海马神经元中,n -钙粘蛋白在短暂的突触刺激后从突触外围重新定位到突触中心。公共科学学报,2013;8(11):1-12。
李志刚,李志刚,李志刚。突触后N-钙粘蛋白和β-连环蛋白对突触前效应的影响。神经科学,2012;15(1):81-9。
Jüngling K, Eulenburg V, Moore R, Kemler R, Lessmann V, Gottmann K. N-cadherin跨突触调节胚胎干细胞来源神经元谷氨酸突触的短期可塑性。神经科学杂志,2006;26(26):6968-78。
Togashi H, Abe K, Mizoguchi A, Takaoka K, Chisaka O, Takeichi M. Cadherin调控树突棘形态发生。神经元。2002;35(1):77 - 89。
阿部K, Chisaka O, Van Roy F, Takeichi M. α n -连环蛋白控制树突棘和突触接触的稳定性。神经科学,2004;7(4):357-63。
Mendez P, De Roo M, Poglia L, Klauser P, Muller D. N-cadherin介导可塑性诱导的长期脊柱稳定。中国生物医学工程学报,2010;29(3):339 - 339。
冈村K,田中H,八田Y, Saeki Y,田口A,平冈Y,等。钙粘蛋白活性是活动诱导脊柱重塑所必需的。中国生物医学工程学报,2004;26(5):529 - 529。
Bozdagi O, Bin WX, Nikitczuk JS, Anderson TR, Bloss EB, Radice GL,等。成熟海马CA1突触协调长期增强和树突棘增大的持续性需要n -钙粘蛋白。神经科学杂志,2010;30(30):9984-9。
吴志刚,王珊珊,王志刚,王志刚。在LTP后期,突触点的数量增加:n -钙粘蛋白被合成,募集到突触位点,并需要增强。神经元。2000;28(1):245 - 59。
Ashley J, Packard M, Ataman B, Budnik V. fasiclin II通过淀粉样前体蛋白和脚手架蛋白dX11/mint信号新突触的形成。中华神经科学杂志,2005;25(25):5943-55。
于海辉,杨建军,王军,黄艳,李涛。果蝇内畴多样性及其在神经元形态发生中的作用。神经科学杂志,2009;29(6):1904-14。
王洁,李春杰,李涛,梁ih,李春杰,李涛。果蝇的姐妹分支分化和抑制轴突异位分岔是必需的。神经元。2002;33(4):559 - 71。
Hutchinson KM, Vonhoff F, Duch C. Dscam1是果蝇运动神经元中正常树突生长和分支所必需的,而不是树突间距。神经科学杂志,2014;34(5):1924-31。
Spring AM, Brusich DJ, Frank CA. c端Src激酶在果蝇神经肌肉连接处开启稳态突触可塑性并调节fasiclin II的表达。公共科学图书馆。2016;12(2):1-31。
高虹,李志刚,李志刚。细胞粘附分子fasiclin2对突触后分子组装的体内诱导作用。中国生物医学工程学报,2007;29(6):339 - 339。
梅福德M,巴兹莱A,凯勒F,夏彻S,坎德尔ER。海兔中ncam相关黏附分子与长期突触可塑性的调制。科学(80-)。1992, 256(5057): 638 - 44。
谢伟,李志刚,李志刚。神经蛋白与神经蛋白的研究进展。Mol神经生物学,2011;44(3):426-40。
张志刚,张志刚。神经素信号在突触发育中的作用。神经生物学杂志,2007;17(1):43-52。
Bottos A, Rissone A, Bussolino F, Arese M.神经蛋白和神经蛋白:神经系统外的突触。中国生物医学工程学报(自然科学版),2011;
Sudhof TC。神经蛋白和神经蛋白将突触功能与认知疾病联系起来。大自然。2008;455(7215):903 - 11所示。
莫斯卡TJ。在Teneurin轨道上:一种新的突触组织分子出现。前细胞神经科学2015;9:1-14。
塔克RP, Chiquet-Ehrismann R. Teneurins:发育过程中参与细胞间信号传递的一个保守的跨膜蛋白家族。中国生物医学工程学报。2006;29(2):344 - 344。
Zinn K, Özkan E.神经免疫球蛋白超家族相互作用网络。《神经生物学杂志》2017;45:99-105。
果蝇突触对中dpri - dip的匹配表达。飞(奥斯丁)。2017; 11(1): 19-26。
Graf ER, Zhang X, Jin SX, Linhoff MW, Craig AM。神经素通过神经原素诱导GABA和谷氨酸的突触后特化分化。细胞。2004;119(7):1013 - 26所示。
Scheiffele P, Fan J, Choih J, Fetter R, Serafini T.神经素在非神经元细胞中表达触发接触轴突的突触前发育。细胞。2000;101(6):657 - 69。
瓦罗奎,阿穆尼,罗森,莫曼,M,戈特曼,等。神经原素决定突触的成熟和功能。51神经元。2006;(6):741 - 54。
李J, Ashley J, Budnik V, Bhat MA。果蝇Neurexin在突触后密度、突触生长和突触传递的适当活性区对应中的关键作用。55神经元。2007;(5):741 - 55。
陈凯,刘志刚,于思生,陈凯。果蝇神经肌肉连接处神经肽的研究进展。公共科学图书馆,2010;5(6):e11115。
Etherton MR, Blaiss CA, Powell CM, Südhof TC。小鼠神经素1α缺失引起与认知障碍相一致的相关电生理和行为变化。中国科学:自然科学(英文版),2009;
陈丽丽,蒋敏,张波,欧高策,Südhof TC。所有Neurexins的条件删除定义了Neurexins基本突触组织者功能的多样性。神经元。2017;94 (3):611 - 625. - e4。
李文杰,李文杰,李文杰,等。Syd-1与Neurexin的合作使突触前和突触后的组装同步。神经科学,2012;15(9):1219-26。
Banerjee S, Venkatesan A, Bhat MANeurexin, neuroroginin和wishful thinking协调神经肌肉连接处的突触细胞结构和生长。中国生物医学工程学报,2017;
张志刚,张志刚,张志刚。神经原素对兴奋性和抑制性突触形成的控制。科学(80-)。2005, 307(5713): 1324 - 8。
Chubykin AA, Atasoy D, Etherton MR, Brose N, Kavalali ET, Gibson JR,等。神经胶质素-1和神经胶质素-2对兴奋性和抑制性突触的活性依赖验证。神经元。2007年,54(6):919 - 31所示。
陈永春,林永强,Banerjee S, Venken K,李娟,Ismat A,等。果蝇神经素2在突触前和突触后对适当的突触分化和突触传递是必需的。神经科学杂志,2012;32(45):16018-30。
Banovic D, Khorramshahi O, Owald D, Wichmann C, Riedt T, Fouquet W,等。果蝇神经素1促进谷氨酸神经肌肉连接处的生长和突触后分化。神经元。2010;66(5):724 - 38。
邢刚,李敏,孙勇,芮敏,庄勇,吕华,等。在果蝇神经肌肉连接处,neurexin - neuroroligin 1通过WAVE调节复合物调节突触形态和功能。Elife。2018;7:1-23。
鲍姆加特纳,利特尔顿,布洛迪,巴哈特,马,哈贝克,兰格尔,贾,等。果蝇神经素是隔膜连接和血液神经屏障形成和功能所必需的。细胞。1996;87(6):1059 - 68。
李文杰,李文杰,李志强,李志强。Neurexin IV, caspr和paranodin - Neurexin家族的新成员:轴突和神经胶质的相遇。神经科学,1998;21(10):444-9。
佩莱斯,M纳提夫,M拉斯蒂格,M格鲁梅特,J席林,马丁内斯R,等。一种新型接触蛋白相关跨膜受体的鉴定,该受体具有涉及蛋白质-蛋白质相互作用的多个结构域。中国科学d辑,1997;16(5):978-88。
Böhme MA, Beis C, red - alla S, Reynolds E, Mampell MM, Grasskamp AT,等。活性区支架通过不同的Unc13亚型积累来调节Ca2+通道-囊泡耦合。神经科学,2016;19(10):1311-20。
Maruyama IN, Brenner S.一种由植物unc-13基因编码的浮波酯/二酰基甘油结合蛋白秀丽隐杆线虫.自然科学进展,2001;29(3):377 - 382。
赖勇,崔武武,李海杰,李灿,Altas B,等。Munc13和Munc18启动突触囊泡的分子机制。神经元。2017;95 (3):591 - 607. - e10。
罗森蒙德C,西格勒A,奥古斯丁一世,瑞姆K,布泽N,李JS。Munc13亚型对囊泡启动和短期可塑性的差异控制。神经元。2002;33(3):411 - 24。
Zweier C, de Jong EK, Zweier M, Orrico A, Ousager LB, Collins AL,等。CNTNAP2和NRXN1在常染色体隐性pitt - hopkins样智力障碍中发生突变,并决定果蝇中一种常见突触蛋白的水平。王志强,王志强。2009;35(5):366 - 366。
McNeill EM, Warinner C, Alkins S, Taylor A, Heggeness H, DeLuca TF,等。保守的microRNA miR-34通过突触前和突触后细胞中不同机制的协调调节突触发生。网络学报。2020;11(1):1092。
Leamey CA, Sawatari A. teneurins:视觉地形生成中的新玩家。中国生物医学工程学报(英文版);2014;
刘志刚,刘志刚,刘志刚,刘志刚。神经肌肉突触中神经神经素信号通路的研究进展。大自然。2012;484(7393):237 - 41。
张志刚,张志刚,张志刚,张志刚,等。突触结构和功能的快速活动依赖修改需要双向Wnt信号。神经元。2008;57:705-18。
Piccioli ZD, Littleton JT。逆行的BMP信号通过突触前LIM激酶对木非林的调节调节快速活性依赖的突触生长。神经科学杂志,2014;34(12):4371-81。
Berke B, Wittnam J, McNeill E, Van Vactor DL, Keshishian H.突触的BMP逆行信号:突触成熟和活动依赖可塑性的允许信号。中华神经科学杂志,2013;33(45):17937-50。
Zito K, Parnas D, Fetter RD, Isacoff EY, Goodman CS。观察突触生长:果蝇突触生长的非侵入性共聚焦成像。神经元。1999;22(4):719 - 29。
Fuentes-Medel Y, Logan MA, Ashley J, Ataman B, Budnik V, Freeman MR.胶质细胞和肌肉通过吞噬不稳定的突触钮扣和脱落突触前碎片来雕刻神经肌肉树突。公共科学图书馆。2009;7(8):e1000184。
杨晓东,李志强,李志强。果蝇幼虫肌细胞谷氨酸能突触的形态特征。中华神经科学杂志,1989;9(2):710-25。
黄斌,千叶。果蝇幼虫神经肌肉突触的单细胞分析。生物工程学报,2001;29(1):55-70。
张志刚,张志刚,张志刚,张志刚,等。果蝇卷曲-2在突触发育过程中的核运输需要PDZ蛋白dGRIP。中国科学(d辑),2006;26(3):344 - 344。
Vasin A, Zueva L, Torrez C, Volfson D, Littleton JT, Bykhovskaia M. Synapsin调节果蝇神经肌肉连接处突触钮扣的活动依赖性生长。神经科学杂志,2014;34(32):10554-63。
考夫曼N, DeProto J, Ranjan R, Wan H, Van Vactor D.果蝇liprina和受体磷酸酶Dlar控制突触形态发生。神经元。2002;34(1):27-38。
Miller K, Chou VT, Van Vactor D. Liprin-α与突触细胞基质的组装。在:神经科学和生物行为心理学参考模块。巴塞尔:爱思唯尔;2017.1 - 8页。
李文杰,李志强,李志强,等。Syd-1同源物调节果蝇突触前和突触后的成熟。中国生物医学工程学报,2010;29(4):369 - 369。
戴Y, Taru H, Deken SL, Grill B, Ackley B, Nonet ML,等。SYD-2 Liprin-α通过ELKS组织突触前活性区形成。自然神经科学;2006; 9(12): 1479 - 87。
潘维,张志刚,张志刚,张志刚,等。突触前成分的层次组装已被定义秀丽隐杆线虫突触。神经科学。2006;9(12):1488-98。
Wentzel C, Sommer JE, Nair R, Stiefvater A, Sibarita JB, Scheiffele P. MSYD1A,一种哺乳动物突触缺陷-1蛋白,调节突触源信号和囊泡对接。神经元。2013;78(6):1012 - 23所示。
黄建科,王勇,田中华,张伟,等。突触前粒子网:超微结构、组成、溶解和重建。神经元。2001;32(1):63 - 77。
Chakrabarti R, Wichmann C.在神经元和带状突触组织释放的纳米机器。国际分子化学杂志,2019;20(9):23-32。
结构提示功能:突触带作为胞外纳米机器的案例。BioEssays。2001; 23(9): 831 - 40。
穆雷桑V,莱亚斯A,施纳普BJ。运动蛋白KIF3A是脊椎动物光感受器突触前带的一个组成部分。神经科学杂志,1999;19(3):1027-37。
Harlow ML, Ress D, Stoschek A, Marshall RM, McMahan UJ。青蛙神经肌肉连接处的活跃区物质结构。自然。2001;409(6819):479 - 84。
王晓明,杨晓明,杨晓明,Franzén杨晓明。果蝇神经肌肉连接处突触前细胞质投影的研究进展。中国生物医学工程杂志,2010;32(3):389-94。
王晓明,王晓明,王晓明。突触前成分的传递与轴突转运。神经生物学杂志,2008;18(5):495-503。
沈凯。轴突与树突的传输。神经生物学杂志,2014;27:65 5 - 70。
Pack-Chung E, Kurshan PT, Dickman DK, Schwarz TL.果蝇突触Bouton形成和突触囊泡运输所需的驱动蛋白。神经科学。2007;10(8):980-9。
Pilling AD Horiuchi D Lively CM Saxton WM驱动蛋白-1和动力蛋白是果蝇运动轴突中线粒体快速运输的主要马达。Mol Biol Cell, 2006;17(4): 2057-68。
赫德DD,萨克斯顿WM。运动蛋白突变通过破坏果蝇的快速轴突运输引起运动神经元疾病表型。遗传学。1996;144(3):1075 - 85。
何谓慢轴突运输?科学通报,2008;29(3):344 - 344。
杨晓明,张晓明。神经发育过程中大分子分子的扩散转运。中华神经科学杂志,1992;12(1):77-85。
Shapira M,翟RG, Dresbach T, Bresler T, Torres VI, Gundelfinger ED,等。短笛-大管运输囊泡突触前活性区的单一组装。神经元。2003;38(2):237 - 52。
翟RG, Vardinon-Friedman H, case - langhoff C, Becker B, Gundelfinger ED, Ziv NE,等。组装突触前活动区:一个活跃的前体囊泡的特征。神经元。2001;29(1):131 - 43。
Tao-Cheng JH。预组装多囊泡转运聚集体中活性区和突触囊泡蛋白的超微结构定位。神经科学。2007;150(3):575 - 84。
李志强,李志强。突触前组装的细胞和分子机制。神经科学,2004;5(5):385-99。
王志刚,王志刚。脊椎动物突触发生机制的研究。神经科学,2005;28(1):251-74。
Bury LAD, Sabo SL.突触形成前突触囊泡和活性区蛋白的协调运输。神经科学进展。2011;6(1):1 - 14。
叶武,霍琳,马德,冯伟,沈凯。突触前蛋白捕获与解离的平衡控制着突触的空间分布。神经元。2013;78(6):994 - 1011。
李斌,沈凯。多巴胺能神经元生长锥后突触前物质的快速组装是由轴突运输的精确调节介导的。Cell Rep. 2018;24(10): 2709-22。
Petzoldt AG, Lützkendorf J, Sigrist SJ。突触前活性区支架的组装和可塑性控制机制。《神经生物学杂志》2016;39:69-76。
Vukoja A, Rey U, Petzoldt AG, Ott C, Vollweiter D, Quentin C,等。突触前生物发生需要溶酶体相关囊泡的轴突运输。神经元。2018;99 (6):1216 - 1232. - e7。
Fouquet W, Owald D, Wichmann C, Mertel S, Depner H, Dyba M,等。果蝇活跃区组装的成熟。中国生物医学工程学报,2009;36(1):339 - 339。
甄敏,金勇。脂蛋白SYD-2调控突触前末端分化秀丽隐杆线虫.大自然。1999;401(6751):371 - 5。
阿斯蒂加拉加S, Hofmeyer K, Farajian R, Treisman JE。三种果蝇唇蛋白相互作用控制突触的形成。神经科学杂志,2010;30(46):15358-68。
张海燕,张志刚,张志刚,张志刚。秀丽隐杆线虫胆碱能神经肌肉连接点的突触前密集投影通过SYD-2/Liprin和UNC-10/ rimm依赖的相互作用将突触小泡定位在活动区。神经科学杂志,2011;31(12):4388-96。
旋手MA,瓦拉DA,赫尔曼TG。果蝇syd-1具有rhogap活性,这是bruchpilot/elks突触前聚类所必需的,但neurexin-1没有。遗传学。2018;208(2):705 - 16。
李玲,田旭,朱敏,宝格丽D, Böhme MA, Goettfert F,等。果蝇Syd-1、Liprin-α和蛋白磷酸酶2A B’亚基Wrd以线性途径发挥作用,以防止远端轴突突触物质的异位积累。神经科学杂志,2014;34(25):8474-87。
Hallam SJ, Goncharov A, McEwen J, Baran R, Jin Y. SYD-1是一种具有PDZ, C2和rhogap样结构域的突触前蛋白秀丽隐杆线虫.神经科学,2002;5(11):1137-46。
Spangler SA, Hoogenraad CC. liprina蛋白:突触成熟的支架分子。生物化学学报,2007;35(p5): 1278-82。
Serra-Pagès C, Medley QG, Tang M, Hart A, Streuli M. Liprins, LAR跨膜蛋白-酪氨酸磷酸酶相互作用蛋白家族。中国生物医学工程学报,1998;29(3):344 - 344。
Serra-Pagès C, Kedersha NL, Fazikas L, Medley Q, Debant A, Streuli M. LAR跨膜蛋白酪氨酸磷酸酶和卷曲线圈LAR相互作用蛋白共定位于局灶粘连。中国科学(d辑),1995;14(12):2827-38。
张志刚,张志刚,张志刚。的哺乳动物同源物秀丽隐杆线虫unc-13基因定义了新的c2结构域蛋白家族。中国生物医学工程学报,2001;29(4):553 - 553。
Augustin I, Rosenmund C, Südhof TC, Brose N. Munc13-1是谷氨酸能突触囊泡融合能力的关键。自然。1999;400(6743):457 - 61。
un13排列SNAREs和Superprimes突触囊泡。神经元。2017;95(3):473 - 5。
徐娟,Camacho M,徐勇,Esser V,刘旭,Trimbuch T,等。从Munc13-1 C1C2BMUN的晶体结构了解神经递质释放和突触前可塑性的机制。Elife。2017;6:e22567。
王勇,M冈本,F Schmitz, K Hofmann, Südhof TC。Rim可能是rab3调节突触-囊泡融合的效应因子。大自然。1997;388(6642):593 - 8。
Mittelstaedt, Alvaréz-Baron E, Schoch S. RIM蛋白及其在突触功能中的作用。中国生物医学工程学报。2010;36(6):599-606。
陆杰,马丘斯M,杜鲁波娃I,戴H, Südhof TC, Tomchick DR,等。Munc13-1同型二聚体到Munc13-1 /RIM异型二聚体开关的结构基础。公共科学图书馆。2006;4(7):1159-72。
邓琳,Kaeser PS,徐伟,Südhof TC。RIM蛋白通过逆转munc13的自抑制同二聚体激活囊泡启动。神经元。2011;69(2):317 - 31所示。
Kaeser P.将突触囊泡推过RIM。细胞生物学杂志,2011;1(3):106-10。
Castillo PE, Schoch S, Schmitz F, Südhof TC, Malenka RC。RIM1α是突触前长期增强所必需的。大自然。2002;415(6869):327 - 30。
肖奇,潘文杰,王勇,等。RIM1α形成一种蛋白质支架,调节活跃区神经递质的释放。大自然。2002;415(6869):321 - 6。
Graf ER, Valakh V, Wright CM,吴超,刘震,张永青,等。RIM促进了果蝇神经肌肉连接处活跃区域钙通道的积累。神经科学杂志,2012;32(47):16586-96。
Han Y, Babai N, Kaeser P, Südhof TC, Schneggenburger R. RIM1和RIM2冗余决定后脑突触ca2 +通道密度和易于释放池大小。中华神经医学杂志,2015;29(1):344 - 344。
Kaeser PS,邓琳,王勇,Dulubova I,刘霞,Rizo J,等。RIM蛋白通过直接的pdz域相互作用将Ca2+通道连接到突触前活性区。细胞。2011;144(2):282 - 95。
RIM-BP基因的结构和进化:一个新家族成员的鉴定。基因。2007;403(1 - 2):70 - 9。
王勇,杉田,Südhof TC。神经元C2结构域蛋白的RIM/NIM家族:与Rab3和一类新的Src同源3结构域蛋白的相互作用。中国生物医学工程学报,2000;26(2):344 - 344。
Hibino H, Pironkova R, Onwumere O, Vologodskaia M, Hudspeth AJ, Lesage F. RIM结合蛋白(RBPs)将rab3相互作用分子(RIMs)偶联到电压门控Ca2+通道。神经元。2002;34(3):411 - 23所示。
刘克西,Siebert M, Mertel S, Knoche E, Wegener S, Wichmann C,等。边缘结合蛋白是活性区域的中心部分,对神经递质释放至关重要。科学。2011;334(6062):1565 - 9。
马科维,李志强,李志强,等。Bruchpilot细胞阵型决定了突触囊泡可释放池的大小。中国生物医学工程学报,2013;26(4):369 - 369。
王志强,王志强,王志强,等。Bruchpilot促进活性区组装,Ca2+通道聚集和囊泡释放。科学(80-)。2006, 312(5776): 1051 - 4。
Wagh DA, Rasse TM, Asan E, Hofbauer A, Schwenkert I, Dürrbeck H,等。与ELKS/CAST同源的Bruchpilot蛋白是果蝇突触活性区的结构完整性和功能所必需的。神经元。2006;49:833-44。
Sugie A, Hakeda-Suzuki S, Suzuki E, Silies M, Shimozono M, Möhl C,等。果蝇光感受器突触前活性区的分子重构。神经元。20156;86(3):711 - 25所示。
胡晓明,陈晓明,陈晓明,陈晓明,等。体内谷氨酸受体组成的活性依赖位点特异性变化。神经科学,2008;11(6):659-66。
张晓东,张晓东,张晓东,等。定量超分辨率成像的Bruchpilot区分活跃区状态。Nat Commun. 2014;5:4650。
Sudhof TC。突触囊泡循环。神经科学,2004;27:509-47。
将RG, Kaeser PS. ELKS活性区蛋白作为多任务分泌支架。开放生物学,2018;8(2):170258。
凯撒PS,雷格尔WG。容易释放的突触囊泡池。中国神经医学杂志,2017;43(1):63-70。
葛伟平,杨晓军,张震,王洪科,沈伟,邓庆东,等。Ca2+−可渗透AMPA受体介导的神经元-胶质突触的长期增强。科学(80-)。2006, 312(5779): 1533 - 7。
Jabs R, Pivneva T, Hüttmann K, Wyczynski A, Nolte C, Kettenmann H,等。突触传递到海马胶质细胞与hGFAP启动子活性。中国生物医学工程学报,2005;29(4):344 - 344。
Bergles DE, Roberts JDB, Somogyi P, Jahr CE。海马体OPCs上的谷氨酸突触。自然。2000;405(1996):187 - 91。
林志刚,林志刚。神经元与神经胶质之间的突触信号。神经胶质。2004;(3):290 - 8。
林世峰,林世峰,林世峰。海马体中gaba能中间神经元和少突胶质细胞前体细胞之间的突触信号。神经科学,2004;7(1):24-32。
突触后密度的信号处理机器。科学(80-)。2000, 290(5492): 750 - 4。
Palay SL.中枢神经系统中的突触。中国生物化学杂志。1956;2(4增刊):193-202。
灰色。大脑皮层的轴-体细胞和轴-树突突触:电子显微镜研究。J Anat. 1959;93(4增刊):420-33。
Scheefhals N, MacGillavry HD。突触后谷氨酸受体的功能组织。中国生物医学工程学报,2018;
果蝇神经肌肉连接处的谷氨酸受体。神经生物学杂志2006;75(06):165-79。
利特尔顿JT。果蝇细胞膜运输和神经递质释放的基因组分析。中国生物医学工程学报,2000;30(2):344 - 344。
韩涛,王志强,王志强黑腹果蝇NMJ谷氨酸受体。中国科学:自然科学(英文版),2015;
郭琴,Schwarz T, Kittel RJ, Schmid A, Rasse TM, Kappei D,等。四种不同的亚基在果蝇神经肌肉连接处表达突触谷氨酸受体是必不可少的。神经科学杂志,2005;25(12):3209-18。
张志强,李志强,王志强,等。一种重要的果蝇谷氨酸受体亚基,在中枢神经和神经肌肉连接处都起作用。神经科学杂志,2005;25(12):3199-208。
许志刚,张志刚,张志刚,张志刚。果蝇肌肉中谷氨酸受体亚基的克隆。科学。2019;254(5028):112 - 4。
谷氨酸受体的优先定位与突触前高释放位点相反。中国生物医学杂志,2004;14(11):924-31。
Petersen SA, Fetter RD, Noordermeer JN, Goodman CS, DiAntonio a .果蝇谷氨酸受体的遗传分析揭示了调节突触前递质释放的逆行信号。神经元。1997;19(6):1237 - 48。
DiAntonio A, Petersen SA, Heckmann M, Goodman CS。谷氨酸受体的表达调节果蝇神经肌肉连接处的数量大小和数量含量。神经科学杂志,1999;19(8):3023-32。
金玉杰,张斌,张晓峰,张晓峰,张晓峰。前域去除使Neto在果蝇神经肌肉交界处稳定谷氨酸受体。公共科学图书馆,2015;11(2):1-26。
金玉军,鲍海华,张波,张波。果蝇在神经肌肉连接处谷氨酸受体聚类中的作用。基因开发,2012;26(9):974-87。
Ramos CI, Igiesuorobo O, Wang Q . Serpe M. neto介导的细胞内相互作用在果蝇神经肌肉连接处形成突触后成分。公共科学图书馆。2015;11(4):1-26。
张伟,St-Gelais F, Grabner CP, Trinidad JC, Sumioka A, moriamoto - tomita M,等。调节红氨酸型谷氨酸受体的跨膜附属亚基。神经元。2009;61(3):385 - 96。
吴d,投手GM, Szilard RK, Sertié A, Kanisek M, Clapcote SJ,等。Neto1是一种新型的cub结构域NMDA受体相互作用蛋白,是突触可塑性和学习所必需的。公共科学图书馆。2009;7(2):0278-300。
Sigrist SJ, Thiel PR, Reiff DF, Schuster CM。突触后谷氨酸受体亚基DGluR-IIA介导果蝇的长期可塑性。神经科学杂志,2002;22(17):7362-72。
赵喆,Manser E. PAK家族激酶。细胞生物学杂志,2012;2(2):59-68。
Civiero L, Greggio E. PAKs在大脑:功能和功能障碍。生物化学学报,2018;1864(2):444-53。
王强,韩涛,王强,李平,等。一种新的,非典型的BMP通路调节果蝇神经肌肉连接处的突触成熟。公共科学图书馆。2016;12(1):1 - 31。
Rasse TM, Fouquet W, Schmid A, Kittel RJ, Mertel S, Sigrist CB,等。体内谷氨酸受体动态组织突触形成。神经科学。2005;8(7):898-905。
曾根,铃木E,星野M,侯D,黑美H,深田M,等。果蝇突触的周围活动区控制着突触的发育。发展。2000;127(19):4157 - 68。
Wan HI, DiAntonio A, Fetter RD, Bergstrom K, Strauss R, Goodman CS。高丝调节果蝇突触生长。神经元。2000;26(2):313 - 29。
帕纳斯D, Haghighi AP, Fetter RD, Kim SW, Goodman CS。rho型鸟嘌呤核苷酸交换因子dPix对突触后结构和蛋白质定位的调控。神经元。2001;32(3):415 - 24。
阿尔宾SD,戴维斯GW。协调结构和功能突触发育:突触后p21激活激酶独立指定谷氨酸受体丰度和突触后形态。神经科学杂志,2004;24(31):6871-9。
Teodoro RO, Pekkurnaz G, Nasser A, Higashi-Kovtun ME, Balakireva M, Mclachlan IG,等。Ral通过外囊的募集介导突触后膜的活动依赖生长。中国生物医学工程学报。2013;32(14):2039-55。
Quan A, Robinson PJ。Syndapin -一种膜重构和内吞的F-BAR蛋白。中国生物医学工程学报,2013;29(4):349 - 349。
Kumar V, Fricke R, Bhar D, red - alla S, Krishnan KS, Bogdan S,等。Syndapin促进果蝇突触后膜系统的形成。Mol Biol Cell, 2009; 20:2254-64http://www.molbiolcell.org/cgi/doi/10.1091/mbc.E08。
Syndapins在受体介导的胞吞作用中整合N-WASP。中国生物医学工程学报。2002;21(22):6083-94。
Oh E, Robinson I. Barfly:在果蝇神经肌肉连接处雕刻膜。神经科学进展。2012;32(1):344 - 344。
王珊珊,杨娟,蔡安,李俊,等。果蝇内收蛋白调节Dlg的磷酸化,并将Dlg靶向到突触和上皮膜。中国生物医学工程学报。2011;36(2):392-403。
王淑华,蔡安,王敏,刘帅,金海,刘波,等。磷调控果蝇内收蛋白是在幼虫神经肌肉连接处与Dlg和PIP2复合物中突触可塑性的决定因素。生物公开,2014;3(12):1196-206。
Pielage J, Bulat V, Zuchero JB, Fetter RD, Davis GW。Hts/内加蛋白控制突触的形成和消除。神经元。2011;69(6):1114 - 31所示。
Loya CM, McNeill EM, Bao H, Zhang B, Van Vactor D. miR-8通过激活肌动蛋白调节因子抑制突触结构。发展。2014;141(9):1864 - 74。
Pielage J, Fetter RD, Davis GW。突触后Spectrin支架定义了果蝇神经肌肉连接处的活性区大小、间距和功效。中国生物医学工程学报,2006;29(3):344 - 344。
Pielage J, Fetter RD, Davis GW。突触前光谱蛋白对突触稳定至关重要。动物学报,2005;15(10):918-28。
Pielage J, Cheng L, Fetter RD, Carlton PM, Sedat JW, Davis GW。突触前巨锚蛋白通过调节突触前微管和跨突触细胞黏附稳定NMJ。神经元。58 2008;(2):195 - 209。
Koch I, Schwarz H, Beuchle D, Goellner B, Langegger M, Aberle H.果蝇锚蛋白2是突触稳定性所必需的。神经元。58 2008;(2):210 - 22所示。
张军,张建平,张建平,等。dlg在体内激振器K+通道突触聚类中的重要作用。神经科学杂志,1997;17(1):152-9。
吴文杰,李志强,李志强,李志强,等。盘状细胞黏附分子束素II的突触聚类及其在突触前结构调节中的作用。神经元。1997;19(4):787 - 99。
陈凯,陈志明,陈志明。果蝇大圆盘(DLG)通过突触前神经支配聚集并调节突触后谷氨酸受体亚基组成。BMC生物学,2005;3:1-13。
饶a,金E,盛M,克雷格AM。培养海马神经元发育过程中兴奋性突触后位点分子组成的异质性。神经科学杂志,1998;18(4):1217-29。
张志刚,张志刚,张志刚,张志刚,等。果蝇肿瘤抑制基因dlg对突触结构和功能的调控。神经元。1996;17(4):627 - 40。
Astorga C, Jorquera RA, Ramírez M, Kohler A, López E, Delgado R,等。突触前DLG通过电压激活Ca2+通道的定位调节突触功能。科学通报2016;6:1-14。
胡根拉德CC, felius - mojer MI, Spangler SA, Milstein AD, Dunah AW, Hung AY,等。钙/钙调素依赖蛋白激酶II降解Liprinα1调控LAR受体酪氨酸磷酸酶分布和树突发育。科学通报。2007;12(4):587-602。
陈娟,张勇,陈娟,陈娟。突触无翼信号通路的研究进展:受体DFrizzled2的分裂和核输入。科学(80-)。2005, 310(5752): 1344 - 7。
杨晓明,周晓明,周晓明。两类基质金属蛋白酶对突触发生的相互调节作用。Dev. 2016;143(1): 75-87[引2020年6月21日]。可以从:https://pubmed.ncbi.nlm.nih.gov/26603384/.
何晓霞,李志强,李志强,等。果蝇神经肌肉连接点发育与突触前信号通路的关系。神经科学杂志,2008;28(43):10875-84。
李志强,李志强,李志强,等。Shaggy是糖原合成酶激酶3的同源物,控制果蝇神经肌肉连接处的生长。神经科学杂志,2004;24(29):6573-7。
Gögel S, Wakefield S, Tear G, Klämbt C, Gordon-Weeks PR.果蝇微管相关蛋白Futsch在MAP 1B的同源GSK3β磷酸化位点被shaggy/Zeste-white 3磷酸化。分子细胞神经科学,2006;33(2):188-99。
麦凯布BD, Marqués G, Haghighi AP, Fetter RD, Crotty ML, harry TE,等。BMP同源物Gbb提供逆行信号,调节果蝇神经肌肉连接处的突触生长。神经元。2003;(2):241 - 54。
阿伯利·H, Haghighi AP, Fetter RD, McCabe BD, Magalhães TR, Goodman CS。一厢情愿的想法编码了一种BMP II型受体,该受体调节果蝇的突触生长。神经元。2002;33(4):545 - 58。
McCabe BD, Hom S, Aberle H, Fetter RD, Marques G, harry TE,等。Highwire调节突触前BMP信号对突触生长至关重要。神经元。2004;41(6):891 - 905。
Ball RW, Warren-Paquin M, Tsurudome K, Liao EH, Elazzouzi F, Cavanagh C,等。逆行BMP信号通过调节运动神经元中三联蛋白的表达来控制nmj的突触生长。神经元。2010年,27岁,66(4):536 - 49。
戈德CP,戴维斯GW。BMP配体Gbb调控独立于突触生长控制的突触稳态表达。神经元。2007;56(1):109-23[引2020年6月21日]。可从:/pmc/articles/PMC2699048/?report=abstract获取。
Hoover KM, Gratz SJ, Qi N, Herrmann KA, Liu Y, Perry-Richardson JJ,等。钙通道亚单位α2δ-3通过活动依赖和自分泌BMP信号通路组织突触。Nat Commun. 2019;10(1)[引2020年6月21日]。可以从:https://pubmed.ncbi.nlm.nih.gov/31811118/.
James RE, Hoover KM,宝格丽D, McLaughlin CN, Wilson CG, Wharton KA等。卷曲能够区分果蝇神经肌肉连接处BMP的突触前和突触后池。Dev Cell. 2014;31(5): 586-98[引2020年6月21日]。可以从:https://pubmed.ncbi.nlm.nih.gov/25453556/.
伊顿文学士,戴维斯GW。LIM Kinase1控制II型BMP受体下游的突触稳定性。神经元。2005;(5):695 - 708。
吉原M,阿道夫森B,加勒KT,利特尔顿JT。Syt 4的逆行信号传导诱导突触前释放和突触特异性生长。科学(80-)。2005, 310(5749): 858 - 63。
Barber CF, Jorquera RA, Melom JE, Littleton JT。synaptotagmin 4对突触可塑性的突触后调节需要C2两个结构域。中国生物医学工程学报,2009;26(2):339 - 339。
吉原M,利特尔顿JT。Synaptotagmin的功能是钙传感器同步神经递质释放。神经元。2002;(5):897 - 908。
李志强,李志强。糖基化突触对跨突触信号通路的调控。神经科学进展。2012;32(1):1 - 21。
Kamimura K, Ueno K, Nakagawa J, Hamada R, Saitoe M, Maeda N. Perlecan在果蝇神经肌肉连接处调控双向Wnt信号。中国生物医学工程学报,2013;29(2):329 - 329。
Kamimura K, Odajima, Ikegawa Y, Maru C, Maeda N. HSPG Glypican通过调节非典型BMP通路调节经验依赖的突触和行为可塑性。2019;28(12): 3144-3156。e4[引2020年6月21日]。可以从:https://pubmed.ncbi.nlm.nih.gov/31533037/.
王晓明,王晓明,王晓明,等。鸟嘌呤核苷酸交换因子在果蝇胚胎轴突发育中的作用。神经元。2000;26(1):93 - 106。
Debant A, Serra-Pagès C, Seipel K, O 'Brien S, Tang M, Park SH,等。该多结构域蛋白结合LAR跨膜酪氨酸磷酸酶,包含一个蛋白激酶结构域,并具有单独的rac特异性和rho特异性鸟嘌呤核苷酸交换因子结构域。中国科学院学报(自然科学版),1996;29(2):366 - 366。
孙丽娟,李志刚,李志刚,李志刚。果蝇脆性X智力低下蛋白对跨突触信号通路的调控作用。中国机械工程。2013;6(6):1400-13。
罗伯夫J,肯特KS,布罗迪K,韦斯JB。果冻肚向间变淋巴瘤激酶的跨突触信号调节神经传递强度和突触结构。神经科学进展。2013;29(3):369 - 369。
Rohrbough J, Rushton E, Woodruff E, Fergestad T, Vigneswaran K, Broadie K.突触后分化需要突触前建立突触间隙细胞外基质。基因开发,2007;21(20):2607-28。
在突触发育过程中,胶质腹配体对Alk受体信号通路的顺行性受大脑间隙的调节。发展。2010;137(20):3523 - 33所示。
李志强,李志强,李志强。内源性凝集素在突触发生中的作用。神经生物学杂志,2012;32(8):1161-79。
Fox MA, Sanes JR, Borza DB, Eswarakumar VP, Fässler R, Hudson BG,等。不同的目标衍生信号组织运动神经末梢的形成、成熟和维持。细胞。2007;129(1):179 - 93。
穆哈V, Müller哈吉。成纤维细胞生长因子(FGF)信号通路的作用及机制黑腹果蝇.国际分子化学杂志,2013;14(3):5920-37。
张海华,丁力希,田田平,杨建平,等。果蝇脊髓肌萎缩的建模。公共科学学报,2008;3(9):e3209。
陈永斌,陈志强,陈志强,陈志强,陈志强,Trülzsch B,陈志强,等。果蝇生存运动神经元基因突变的神经肌肉缺陷。中国科学。2003;12(12):1367-76。
李志强,李志强,李志强,等。减少的SMN蛋白损害脊髓性肌萎缩小鼠模型中神经肌肉连接的成熟。中国科学。2008;17(16):2552-69。
McNeill EM, Thompson C, Berke B, Chou VT, Rusch J, Duckworth A,等。果蝇启用促进突触形态发生和调节活跃区形式和功能。神经科学进展。2020;15(1):4。
李志强,李志强,李志强,李志强,等。miRNA通路控制活性依赖性突触结构的快速变化黑腹果蝇神经肌肉接头。公共科学学报,2013;8(7):e68385。
李志强,李志强,李志强,李志强。果蝇肿瘤抑制基因dlg是正常突触Bouton结构所必需的。神经元。1994;13(4):823 - 35。
关B,哈特曼B, Kho YH, Gorczyca M, Budnik V.果蝇肿瘤抑制基因dlg参与谷氨酸突触的结构可塑性。中国生物医学杂志,1996;6(6):695-706。
范·瓦科特D,沃尔DP,约翰逊KG。硫酸肝素蛋白多糖和神经元连接的出现。神经生物学杂志,2006;16(1):40-51。
林天珧,黄春华,高焕华,刘建国,叶世荣,程春梅,等。Abi与Abl在果蝇轴突发生和突触发生中起相反作用。发展。2009;136(18):3099 - 107。
波森C,伊顿BA,戴维斯GW。形成依赖的突触生长:Dlar信号通过透明调节突触肌动蛋白和动态先驱微管的证据。神经科学杂志,2008;28(44):11111-23。
郭志伟,杨晓明,杨晓明,等。活性区支架的内稳态缩放维持了整体突触强度。中国生物医学工程学报,2019;29(5):529 - 529。
潘迪UB,尼科尔斯CD。人类疾病模型。药物学杂志,2011;29(2):411-36。
李志强,李志强,李志强,李志强。人类疾病相关基因序列的研究进展黑腹果蝇.基因组学报,2001;11(6):1114-25。
确认
我们感谢范·瓦克托实验室成员的有益讨论。我们感谢哈佛医学院电子显微镜设备的Elizabeth Benecchi为图中所示的电子显微镜提供技术支持。3.一个。
资金
这项工作得到了美国国立卫生研究院的支持(F31 NS101756-03 to v.t.c., 5P01NS090994 to S.A.J. and D.V.V.)。
作者信息
作者及隶属关系
贡献
V.T.C.在D.V.V.的监督下撰写了初稿,在同行评议之后,V.T.C.和S.A.J.对手稿的编辑和修订以及概念设计和图形的修订做出了贡献。作者们阅读并批准了最终的手稿。
相应的作者
道德声明
伦理批准并同意参与
不适用。
发表同意书
不适用。
相互竞争的利益
作者宣称他们之间没有利益冲突。
额外的信息
出版商的注意
伟德体育在线施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可协议中,除非在材料的信用额度中另有说明。如果材料未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。如欲查看本牌照的副本,请浏览http://creativecommons.org/licenses/by/4.0/.创作共用公共领域奉献弃权书(http://creativecommons.org/publicdomain/zero/1.0/)适用于本条所提供的资料,除非在资料的信用额度中另有说明。
关于本文
引用本文
周,v.t.,约翰逊,S.A. &范·瓦克托,D.突触发育与成熟果蝇神经肌肉接头。神经系统开发15, 11(2020)。https://doi.org/10.1186/s13064-020-00147-5
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/s13064-020-00147-5
关键字
- 黑腹果蝇
- 突触
- 神经肌肉接头
- 溥敦之外
- 突触可塑性
- 突触前活跃区
- 酶分子
- Trans-synaptic信号