抽象性
后台
高体重风险因素 影响反食性生长因子受体抗体当前研究调查了抗EGFR反体药诱发性拉皮条和直肠癌患者生存概率之间的风险因素关系,以及药取用、减剂量或治疗中断持续治疗的影响
方法论
包括67名非剖析高级或复发直肠癌病人,首次用反EGFR抗体药处理
结果
高体重病人生存时间和异常拉皮类(++67.2kg)比低体重病人长得多和高得多( < 67.2kg)。此外,退药或减剂量病人的继续治疗时间比不退药或减剂量或停治/免治的病人长得多同时,停止治疗病人的继续治疗时间大大短于提取或减少剂量病人或不提取药量、减少药量或停止治疗病人。
结论
高体重对接受用抗EGFR抗体药治癌药的病人来说是一个新奇预测性因素研究结果显示,高体重病人在接受抗EGFR抗体药时接受癌症药理时,应仔细监控以开发反射疹
后台
随着分子对象代理物的出现,癌症药物处理最近取得了重大进展。特别是使用分子对象处理癌症药法帮助癌症患者延长生存时间一号,2..分子对象代理物具体面向与癌症细胞扩散、转移和渗透相关联的分子,产生副作用不同于传统癌症药物处理法,其特征为恶心/呕吐、食欲消退、口炎和近距离抑制[3,4..
此外,据报告接受癌症药物治疗的病人的痛苦程度有所改变。5HT创用3受体神经素1受体对立器以及抗仿药指南的建立减少了恶心和呕吐的发生,Carelle等2002年调查所报告的精神和社会焦虑症,包括对家庭、伙伴和社会的影响,是接受癌症治疗的病人常见结果5..此外,癌症药物处理大都从住院转向门诊,允许数名病人工作时接受治疗。因此,Nozawa等人2013年调查显示外部物理症状,包括毛发损耗、水肿和eczema在患者求解中排名高6..然而,制定消除这些效果的措施证明具有挑战性。
特别是,以EGFR为对象的抗生长因子抗体药可引起各种皮肤失序开发,如词形拉皮、干皮和paronichia7,8,因为EGFR用正常皮肤表示由这些药引起的皮肤失序不仅会因外观变化引起心理压力,而且还会影响病人QOL九九..此外,考虑到反EGFR药物造成的皮肤失常程度与生存概率相关一号,2切需适当控制皮肤失序以避免治疗中断开发有效方法预测病人在用抗EGFR抗体药治疗前皮肤失常的严重程度将促进及时实施预防或早期措施
各种风险因素描述异形拉皮以抗EGFR抗体药cetuximab处理的染色性癌症男或青年患者发展2-3级拉皮[10..此外,我们先前报告高体重是开发反EGFR抗体药[11..体重对生存概率的影响尚不清楚因此,本研究回溯性调查反EGFR反体药理和生存概率期间产生异常拉皮片的风险因素之间的关系反EGFR反体药提取、减剂量或停止治疗对继续治疗概率的影响研究结果可能有助于实施预防或早期措施,预防皮肤失常,然后对预期会经历皮肤失常并进而控制皮肤失序并推广继续治疗的病人使用反EGFR抗体药并延长癌症患者生存率
方法论
目标病人
无法解析高级或复发CRC病人2014年1月至2018年12月首次接受EGFR抗体药片(cetuximab或panitumab)作为Iwate医科院癌症化疗的电子医疗记录皮肤病患者,包括psorlipat或acti这项研究包括先前注册的一项研究的病人,该项研究确定高体重为反EGFR抗体治疗期间产生异常拉皮片的风险因素[11..与前次研究一样,目标病人按体重分类,这是开发异常皮疹的风险因素。这项研究是根据《赫尔辛基宣言》和经Iwate医科大学道德委员会批准后进行的(MH2021107批准号)。本研究不干预并使用二级数据源故无需病人表示知情同意
标准处理
这项研究所审查的不可解析高级或复发CRC病人标准处理方法包括cetuximab/panitumab+FOLFOXI级LV+blos5-FU+注入5-FU+L-OHP理疗I级LV+blos5-FU+注入5-FU+CPT-11
每种疗程表如下:Cmab+FOLFOX理疗法(Cmab,400 mg/m2初始剂量后为250 mg/m2第1天8分I级-LV200 mg/m2第一天bolus5-FU,400 mg/m2第一天注入5-FU,24mg/m2第一至二日L-OHP85 mg/m2第一天2周/周期)Pmab+FOLFOX理疗I级-LV200 mg/m2第一天bolus5-FU,400 mg/m2第一天注入5-FU,24mg/m2第一至二日L-OHP85 mg/m2第一天2周/周期)Cmab+FOLFIRI理疗2初始剂量后为250 mg/m2第1天8分I级-LV200 mg/m2第一天bolus5-FU,400 mg/m2第一天注入5-FU,24mg/m2第一至二日CPT-11,150 mg/m2第一天2周/周期)和Pmab+FOLFIRI理疗I级-LV200 mg/m2第一天bolus5-FU,400 mg/m2第一天注入5-FU,24mg/m2第一至二日CPT-11,150 mg/m2第一天周期2周)
调查项目和方法
调查项目包括基本病人信息(性别、年龄、癌症阶段、高度、体重、医学历史、化疗历史和伴生药学)、血液生化测试(aline氨基转移ases这些数据取自电子医疗或药理指令记录
皮肤失常评价
aneiformrash信息从电子医疗记录中采集,这是使用反EGFR抗体药处理期间观察到的特征。从处理启动到完成阶段收集的皮肤失序等级数据是根据癌症化疗中常用的不良事件常用术语标准评价的此外,考虑到逆差通常在EGFR管理后1个月内开发12药管后1个月评价反射疹启动状态从开始处理到完成收集药物提取、减少剂量或停止处理的信息
评估治疗持续概率和生存概率
治疗持续概率定义为从开始使用反EGFR抗体药处理到改变原型的周期生存概率定义为从癌症诊断日到因任何理由死亡或停机日的周期
统计分析
算法测试 学生测试t级测试Fisher精确测试用于分析按体重分类的每组病人特征Probentity评分匹配法还用于适应病人背景偏差,根据体重划分病人分为两组kaplan-Meier方法(log-short测试)用于比较按体重分类的每组生存概率并发曼-惠特尼U级测试用来比较按体重分类的每组反射分级并构造接收器操作特征曲线以设定最优截值,目标病人划分为两类
奇差测试单向分析法用于分析每个组的病人特征,分类方式为反EGFR抗体药是否存在提取、减少剂量或停止处理Tukey诚实重大差分测试用于分析单向ANOVA后多重比较kaplan-Meier法(log-short测试)用于比较每个组别继续治疗概率,分类为反EGFR抗体药是否存在提取、减少剂量或停止处理sss统计动词28(IBM, Armonk,NY)用于所有统计分析并产生结果公元前值 < 0.05被认为具有统计意义
结果
目标病人
研究期间,67名非解剖高级或复发CRC病人首次接受抗EGFR抗体药作为癌症化疗没有一个报告皮肤病,如psorlipat或atuti表格显示67名病人的特点一号.此外,18名和49名病人分别接受cetuximab和panitumab抗EGFR抗体药处理法有10名病人的Cmab+FOLFOX理疗,8名病人的Cmab+FOLFOX理疗,26名病人的Pmab+FOLFERI理疗,23名病人的Pmab+FOLFOX理疗所有病人使用异效润滑剂,37个病人使用单环素支持抗EGFR抗体药引起的异常疹
异常崩溃风险因素对生存的影响
目标病人分类二组,按体重取出,作为风险因子取自前次报告11..表显示按体重分类的每组病人特征2.按体重划分,目标病人分类为低体重类( < 67.2kg)和高体重类(+++67.2kg)比较每一因子结果表明,高体重病人中男性比女性高,高高度远比低体重病人高。抗EGFR抗体药类异常拉皮片辅助护理适应性评分匹配后,有14名高体重病人和14名低体重病人,两者在性或高度等病人背景特征方面没有差别
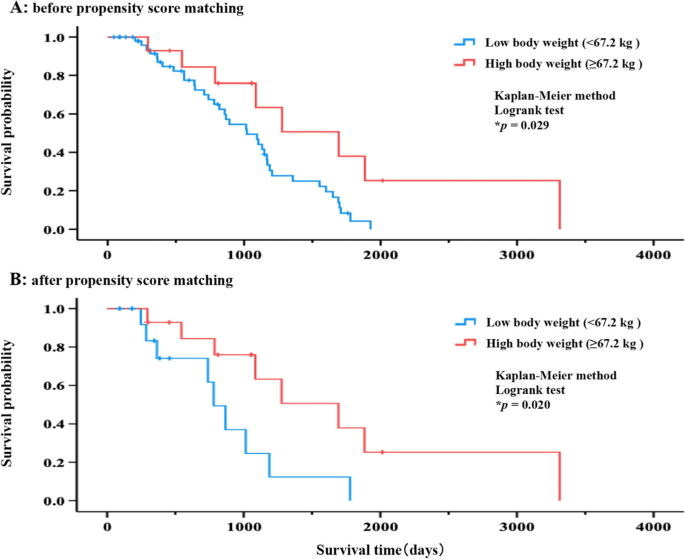
其后比较按体重分类的每组生存概率高体重病人的中值生存时间比低体重病人长得多(1693天[95%置信区间,CI910-2476]对1020天[95%CI738-1302,p=0.029)(图12)。一号A).类似地,在惯性评分匹配后,高体重病人生存时间比低体重病人长得多(体积低)(公元前=0.020一号)体重低和体重高的病人生存时间中位数分别为781天(95%CI,612-950)和1693天(95%CI,910-2476)(图12)。一号)
体重和异常拉皮级关系
表表显示根据体重分类的每组反射分数对比结果3.目标病人分类为低或高体重组,并按组比较每个因子高体重病人的阴性拉皮片等级比低体重病人高得多。
反EGFR反药提取、减少剂量或处理中断对继续治疗概率的影响
表中显示按是否存在反EGFR反药提取、减少剂量或停止治疗分类的每组病人特征4.目标病人分类为不提取药剂、减少剂量或停止治疗取药或减剂量或停止处理以比较每一因子结果表明,与不提取药量、减少药量或停止治疗药量相比(TukeyHSD测试,TUKEHSD公元前=0.018此外,戒毒或减剂量病人和停治病人的体重比不戒毒、减剂量或停治病人的体重高得多(TukeyHSD测试,公元前=0.007公元前=0.006)因此,三大类在性别、身高和体重方面有差异然而,在百合物使用状态方面没有观察到差异。
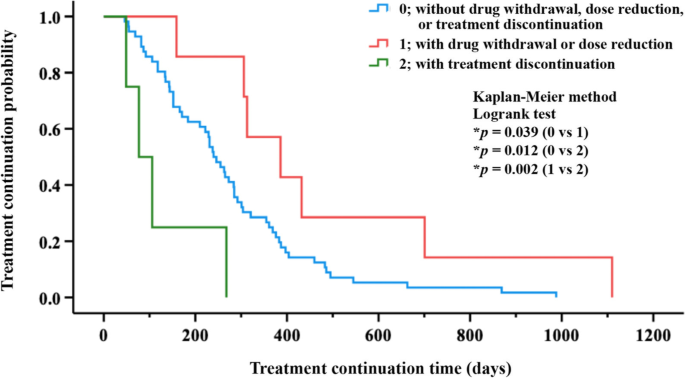
取用或缺用反EGFR反体药、减用剂量或停止处理中位生存时间不提取药物,不减少药量或停止治疗取药或减剂量分别为77天(95%CI,21-133),240天(95%CI,204-276)和386天(95%CI,199-573)。此外,退药或减剂量病人的继续治疗时间比不提取药、减剂量或停治或停治的病人长得多(图16)。2)同时,停止治疗病人的继续治疗时间大大短于提取或减少剂量或不提取药量、减少药量或停止治疗的病人(图二)。2)
讨论
本项研究回溯性调查反EGFR抗体药和生存概率引起的异常拉皮险与药取用、减少剂量或治疗中断对治疗持续概率的影响之间的关系第一,我们调查人体重量-异形疹风险因素-生存效果高体重病人生存时间(++67.2kg)比低体重病人生存时间长得多( < 67.2kg!微博一号A和1B)并发现体重高的病人比体重低的病人高得多(表表)3)上期研究报告高逆差级与高生存概率相关一号,2..研究显示,反EGFR抗体药引起的异常拉皮求生概率在这个病人群中更高
高体积指数(BMI)的病人据报高转水损耗[TEWL]13service屏障函数索引表示高TEWL表示皮肤屏障功能减值在当前研究中,随着体重增加,BMI总体增长,导致高体重病人BMI值高得多(27.7++0.92)比低体重病人BMI值高得多(21.2+++0.33)t级测试公元前< 0.001)因此,这些高体重病人的皮肤屏障功能可能已经下降,有可能增加他们因反EGFR抗体药引起的皮肤失常感考虑到本研究的回溯性,TEWL值没有测量未来研究中将进一步调查。
此外,我们还调查反EGFR反体药提取、减少剂量或停止治疗对继续治疗概率的影响结果表明,退药或减剂量病人的继续治疗时间比不提取药、减剂量或停止治疗或停止治疗的病人长得多(图16)。2)停止治疗病人的继续治疗时间远短于提取或减少剂量或不提取药量、减少药量或停止治疗的病人(图二)。2)此外,戒毒或减少剂量或停止治疗的病人体重比不戒毒、减少剂量或停止治疗的病人体重高得多(表)(表)。4)结果表明,戒毒或减少剂量的病人和停止治疗的病人都可能因体重增加而产生严重的腹形疹子。再者,不控制皮肤症状可能导致停止治疗并缩短继续治疗时间对比之下,通过提取或减少剂量成功控制皮肤症状可能导致避免停止治疗并延长持续治疗时间
除反EGFR抗体药外,bevizumab14,15抗血管内向细胞生长因子抗体药和regrafenib16多因子抑制器 对非剖析高级或复用CRC的病人标准处理regorafenib特征侧作用手脚皮肤反应各种研究报告人工脚皮肤反应等级与生存时间之间的关系17,18号和预测因素影响生存时间18号..具体地说,二二二研究用Regorafenib处理的向北CRC的病人报告,二级手脚皮肤反应的病人生存时间比0级脚反应的病人长[17..此外,在多向性CRC大预期Regorafenib研究中,报告长生存与早期(28天)人工脚皮肤反应和性能良好状态(0比1)相关18号..研究结果可能与主动生活方式表现良好并影响生存时间的个人手脚皮肤反应增加相关18号..此外,在前次研究中,大体表面积(++1.6m2)被确定为影响生存时间的预测性因素然而,提交人没有进一步解释这一点。同时,在当前研究中,在使用反EGFR抗体药后无法调查特定癌症药(如regrafenib)的影响未来需要更详细的研究此外,考虑到单体医疗设施小病人群,这里描述的结果必须在更大多中心未来研究中进一步验证
结论
研究结果显示,高体重病人在接受抗EGFR抗体药时接受癌症药理时,应仔细监控以开发阴道疹
提供数据和资料
本研究中生成或分析的所有数据都包含在手稿中
缩写
- EGFR:
-
防渗透生长因子受体
- CRC:
-
直肠癌
- mab:
-
Cetuximab
- Pmab:
-
Panitumab
- CTCAE:
-
常见术语反向事件标准
引用
JonkerDJ、O'CallaghanCJ、KarapetisCS、ZalcbergJR、TuD、AuHJ等Cetuximab治直肠癌NEnglJMD2007;357:2040–8.https://doi.org/10.1056/NEJMoa071834.
Van Cutsem E, PeetersM,SienaS,HumbletY,HendliszA,NeynsB等开放标签阶段三测试全景+最佳支持性护理JClinOncol2007;25:1658–64.https://doi.org/10.1200/JCO.2006.08.1620.
CoatesA类、AbrahamS类、KayeSB类、SowerbuttsT类、FrewinC类、FoxRM等接收端病人感知癌症化疗的副作用欧氏癌症ClinOncol1983年;19:203-8https://doi.org/10.1016/0277-5379(83)90418-2.
布尔-德内特M公司、德维特R公司、施密茨PI公司、DjontoJ公司、vBeurdenV公司、StoperG公司等病人感知化疗的副作用:5HT3对立者的影响BRJ癌症1997;76:1055–61.https://doi.org/10.1038/bjc.1997.507.
CarelleNiotoEBellangeraJ改变病人对癌症化疗副作用的感知癌症2002/95:155-63https://doi.org/10.1002/cncr.10630.
诺泽克市、Shimizu市、Kakimoto市、MizotaY市、山本S市、TakahashiY市等量化评估癌症患者外观变化和相关危难心理剖析2013年;22:2140-7https://doi.org/10.1002/pon.3268.
Tahara M,ShiraoK,BokuN,山口K,KomatsuY,InabaY等多中心二级Cetuximab加inotecJpnJClinOncol2008年:38:762-9https://doi.org/10.1093/jjco/hyn102.
慕洛K、佳野T、道台K、白井K、TakiuchiH、HamamotoY等二级全景单治JpnJClinOncol2009年;39:321-6https://doi.org/10.1093/jjco/hyp016.
Lacouture me、MitchellEP、PiperdiB、PillaiMV、ShererH、IannottiN等皮肤毒理评估协议Petitumab二级开放标签随机测试评估先发制人皮肤毒理学对皮肤毒理学和染色性癌症患者生活质量的影响JClinOncol2010/28:1351-7https://doi.org/10.1200/JCO.2008.21.7828.
StingzingS公司、KapaunC公司、LaubenderRP公司、JungA公司、NeumannJ公司、ModestDP公司等Cetuximab皮肤毒性预测值与上层剖析癌症病人及其与上层生长因子感应感应器感应路径参数相关联:由德国AIOCRC研究组随机测试产生intJ癌症2013;132:236–45.https://doi.org/10.1002/ijc.27654.
TakahashiH,AsakaJ,TairabuneT,UjiieH,松浦拉Y,NiheiS等分析抑制生长因子受体抗药并检验避免方法引起的皮肤失常JClin药理2021;46:1404–11.https://doi.org/10.1111/jcpt.13475.
Van CutsemE上皮生长因子受体抑制器使用挑战肿瘤学2006年11:1010-7https://doi.org/10.1634/theoncologist.11-9-1010.
LfflerH,AramakiJU,EffendyI体质指数对皮肤易感性皮肤反射技术2002年8:19-22https://doi.org/10.1046/j.0909-752x.
FuchsCS公司、MarshallJ公司、MitchellE公司、WierzbickiR公司、GanjuV公司、JefferyM公司等随机控制测试ironotcan加注入物、bolus或口服froprimiJClinOncol2007;25:4779–86.https://doi.org/10.1200/JCO.2007.11.3357.
SaltzLB公司、ClarkeS公司、Diaz-RubioE公司、ScheithauerW公司、FigerA公司、WongR公司等evacizumab结合基于oxaliplatin化疗作为转移式染色体癌症第一线治疗:随机三级研究JClinOncol2008年26:2013-9https://doi.org/10.1200/JCO.2007.14.9930.
Groeme A、Van Cutsem E、SienaS、FalconeA、YchouM等Regorafenib单片处理前经处理色素癌:国际多中心随机测试柳叶刀2013;381:303–12.https://doi.org/10.1016/S0140-6736(12)61900-X.
里歇尔曼LPSLETLLGRegorafenib患者抗angiro-naive和化疗-阻抗高级直肠癌:二二B测试结果肿瘤学2019;24:1180-7https://doi.org/10.1634/theoncologist.2019-0067.
山口K公司、小松Y公司、SatohT公司、UetakeH公司、YoshinoT公司、NishidaT公司等大规模未来观察研究 regorafenib肿瘤学2019;24:e450-7https://doi.org/10.1634/theoncologist.2018-0377.
Acknowledgements
作者感谢学习参与者的参与和Iwate医科大学教职员工的帮助。
供资问题
这项工作得到了日本科学促进会KAKERKNHI支持,Agent-ActiveKojimachi,Chiyoda-ku,东京,日本
作者信息
作者和附属关系
交文
高桥广治、太云友子、小木Ujie、浅田纯一和工藤都参与了本项研究的构思设计广桥、YaegashiYukiko、Saito和Satoru Nihei参与数据采集、分析和判解所有作者都批判性地修改手稿,评论草稿并核准最终版本
对应作者
道德申报
道德核准并同意参赛
这项研究是根据《赫尔辛基宣言》和经Iwate医科大学道德委员会批准后进行的(MH2021107批准号)。本研究不干预并使用二级数据源因此,无需病人表示知情同意。
协议发布
不适用
竞技兴趣
作者声明他们没有竞技兴趣
附加信息
发布器注解
伟德体育在线Springer自然对发布地图和机构附属关系中的司法请求保持中立
权限和权限
开放存取文章依据创用CC4.0国际许可使用,允许使用、分享、改编、分发和复制任何介质或格式,只要你适当信任原创作者和源码提供链接并显示是否修改图片或其他第三方素材均载入文章Creative公共许可中,除非素材信用栏中另有表示素材未载入文章Creative公共许可中, 法定规则不允许使用或超出许可使用范围时, 需直接从版权持有者处获取许可 。查看许可副本访问http://creativecommons.org/licenses/by/4.0/.创用公共域免责http://creativecommons.org/publicdomain/zero/1.0/)适用于本条提供的数据,除非信用线对数据另有说明。
关于此文章
点上此文章
高桥市et al.风险因子诱发反渗透生长因子受体抗体药求生存效果:回溯观察研究J药房保健Sci822(2022)https://doi.org/10.1186/s40780-022-00253-y
接收:
接受:
发布:
多尔市:https://doi.org/10.1186/s40780-022-00253-y
关键字
- 直肠癌
- 反EGFR抗体药
- 逆差拉皮
- 高体权
- 生存性