抽象性
后台
Imune检查站蛋白质(ICP)是免疫系统的核心因子组,据报告它表达度与恶性肿瘤患者预测相关,许多抑制器显示为治疗目标另一方面,比较方案可溶解形式循环血液诱发系统免疫抑制在这次研究中,我们调查了可溶式CD80(sCD80)与软组织肿瘤患者的临床病理参数之间的关系。
方法论
共有119名主软组织肿瘤患者注册参加这项研究sCD80水平用酶免疫测定
结果
良性(34)和软组织沙马(85)病人之间 sCD80水平没有重大差别STS高sCD80群比低sCD80群5年使用日志测试低5年(OS高超404pg/ml,低+404pg/ml,MS高超531pg/ml,低+531pg/ml)。多变量Cox比例危险分析高sCD80组与低sCD80组相比,5MS和5OS大相径庭
结论
归根结底,sCD80可能对STS系统免疫环境产生消极影响,并有可能作为治疗目标
后台
软组织sacoma(STS)是一种稀有多式肿瘤组一号..STS发病率小于十万例癌症的六分之六,表示成人所有癌症病例为1-2%一号..尽管最近STS诊断和治疗有所进展,但开发相容性病人的死亡率较高。因此,许多研究试图定义预测STS病人预测的不同因素年长和深度、疏松度高和广度STS报告为预测性因素,与低预测相联2,3,4..此外,编译一种免疫脱机机制抑制对肿瘤的免疫响应已知会对其预测产生重大效果Imune检查站蛋白质(ICP)是免疫系统的核心因子组,据报告该素度与恶性肿瘤患者预测相关,许多抑制物显示为治疗目标5..C.Perisano等PD1/PD-L1表达式免疫心理学评价60名受高等级sacomas影响的成人病人PD1淋巴细胞渗透和PD-L1高阶表达法6..
反之,一种可溶化化化ICP循环血液诱导系统免疫抑制7..PD-L1型可溶式与癌症关联报告,如肾细胞癌、肝细胞癌、食道癌、肺癌、胃癌、直肠癌和淋巴马[8,九九,10,11,12,13,14..高端 sPD-L1与癌症病人预测加重有重要关系,包括STS15..研究中,我们调查了可溶式CD80(sCD80)之间的关系,DCD80是抑制系统CTLA-4中软组织肿瘤患者血液和病理参数的关系
材料方法
病人类
共有119名接受治疗的病人接受回溯性审查,包括34名软组织肿瘤病人和85名2002至2016年STS病人,并注册参加这项研究局部复发或转介前医院不适当剖分或首次访问时相距偏移的病人排除于本研究范围外这项研究得到了Mie大学医学院伦理学委员会的批准。由人类参与者参与的所有学习程序都符合Mie大学道德委员会的道德标准以及1975年《赫尔辛基宣言》。组织病理诊断和组织学等级由独立病理学家验证
sCD80测量
所有病人的血液样本均在初步处理前采集所有样本均以-80度存储,直至测量后千分之离心g级15分钟sCD80级使用Human CD80ELISA Kit(B7-1)(英国剑桥Abcam)。最小可检测水平sCD80为31pg/m可检测级别下值分配0pg/ml
统计分析
统计分析使用Mann-WhitneyU测试或Kruskal-Wallis量化数据测试比较血清sCD80水平和各种临床参数接收器操作特征曲线分析为评价检测复发性、转移性或因疾病死亡的阈值ROC曲线通过绘制y轴敏感度和x轴虚阳率(1特性)生成,并评估曲线下区域局部免复发求存时间定义从初始处理到临床记录本地复发日期免元存取定义为从初始处理到临床记录远程转移日期的时间总体生存定义从初始处理到肿瘤致死日期的时间kaplan-Meier生存图和日志排序测试用于评估LRFS、MFS和OS的差异免疫性测试结果与sCD80测试结果之间的关联由kappa系数测试评价Cox比例危险分析用于调整预测因素中的不平衡性公元前< 0.05被认为重要EZR软件程序用于统计分析
结果
特征学习群
表汇总研究群的临床和病理特征一号.
年龄大相径庭 健康自愿者 良性肿瘤患者 STS患者sCD80水平在健康志愿者、有良性肿瘤的病人和STS病人之间没有重大差别34良性肿瘤的直方诊断为12个脂类、14个树本色子、3个树本色子、2个元巨型细胞肿瘤、1个树本色子和1个其他肿瘤,85个STS中为38个lieosarcomas(WLSSs)、5个Syvalsarcomas(SSs)、4个恶性外围神经层肿瘤(MPNSTs)和其他5个表2)所有良性肿瘤患者都接受肿瘤剖析,85个STS患者接受治疗(57个病人全剖析,23个病人边切剖析,3个病人内部剖析和2个病人离子波射治)(表2)3)超过60岁的男性患者和有恶性肿瘤历史的男性患者的SCD80水平较高,但良方和STS患者的sCD80水平差别最大(表80水平)(一号)
特征STS群
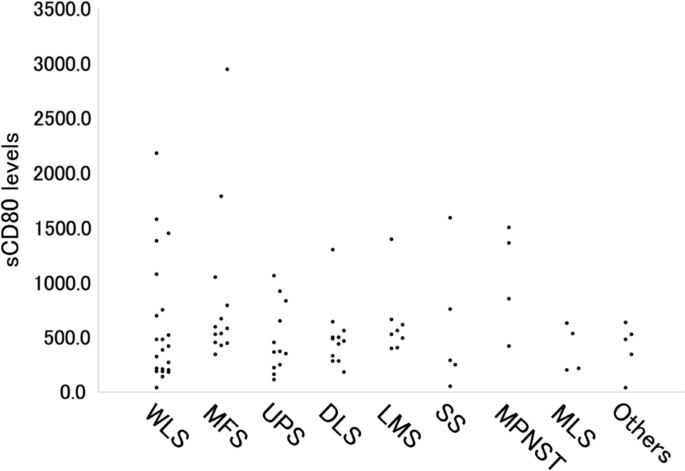
STS病人的临床和病理特征见表3.sCD80水平有显著差异sCD80平均值(标准偏差)如下:MPNST 1033.6(495.5)pg/mMFS856.2(734.0)pg/mUPS476.7(314.0)pg/mSS 586.1(616.9)pg/mWLS604.5(571.6)pg/mDLS497.0(284.7)pg/mMLS394.2(218.1)pg/mLMS 631.5pg/m等403.9pg/m一号)ACCSTS分类显示26名病人分类为I级,15人分类为II级,44人分类为III级sCD80平均富集度较高阶段比低级高,但差别不大。
STS组复发、转移和疾病死亡
恶性病人平均跟踪为40个月(范围从0.6至208个月不等)。研究期间23名病人复发,36名病人复发,25名病人因病死亡
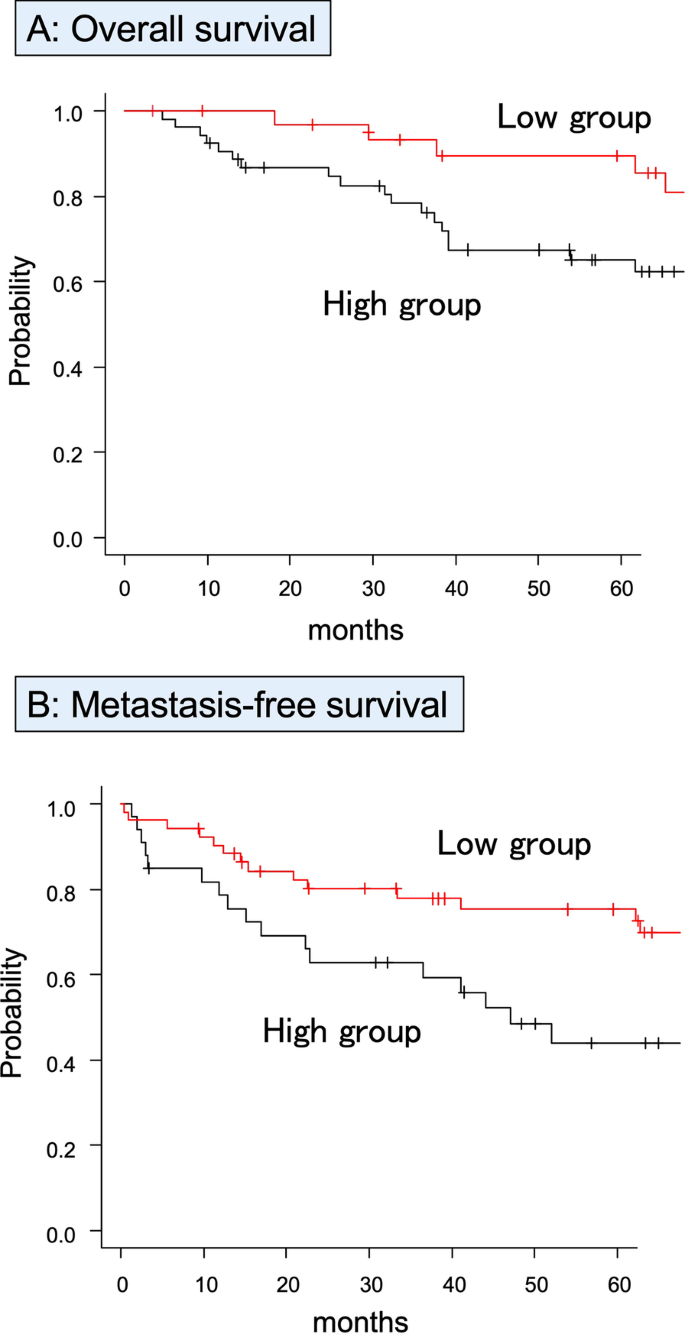
sCD80诊断精度确认相容性、DOD和复发性,ROC分析通过评价曲线下区域完成AUC识别DD、Deptes和复发程序分别为0.641(95%CI0.514-0.767)、0.625(95%CI0.49-0.761)和0.50(95%CI0.362-0.639)(图一)。2A-C.根据ROC分析,5OS截取值404pg/ml划分群分低类(++404pg/ml)和高类(>404pg/ml)sCD80高组比低组低5OS3低SCD8089.5%高SCD8065.0%公元前=0.015sCD80划分二组5MFS使用531pg/ml截值划分组531pg/ml高组大都低5MFS3低SCD80:75.3%,高SCD80:44.0%公元前=0.016
以同样方式将sCD80划分为2组5LRFS,并进行了ROC分析AUC0.5检测复发,未评价进一步分析
sCD80高级STS
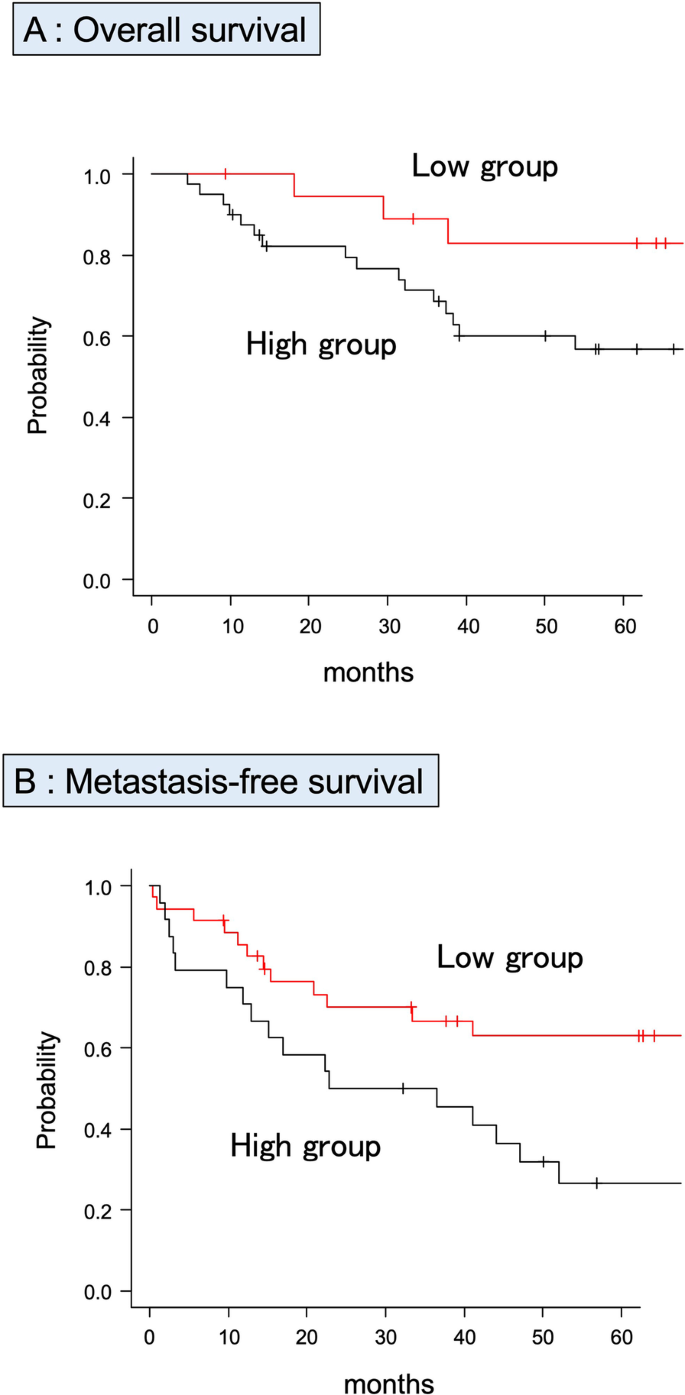
并检视SCD80值与剩余59名病人生存关系中值sCD80值为496.4pg/ml(平均值=611.0,范围=48.8-2947.4)研究期间,20名病人复发,36名病人复发,25名病人因病死亡类似上文,SCD80划分二组5OS和5MFS,截取值分别为404和5314高低sCD80组分图5A,B)5LRFS结果排除是因为AUC5LRFS低值(AUC0.525)4C)级
高群比低群差5OS值(低sCD80:83.0%,高sCD8056.3%,公元前=0.062高组5MFS低得多(低sCD80:62.9%,高sCD80:26.5%,公元前=0.022图25A,B)sCD80多变式Cox比例危险分析显示5MFS有显著差异(HR:2.397,95%CI 1.143-5.027;公元前=0.0214)
讨论
癌症细胞为了避免攻击免疫性,积极使用规管T细胞、骨髓抑制细胞和ICP的免疫抑制功能
原创性比较方案用来抑制T细胞过度激活而不是攻击自身,但在致癌过程中,癌症细胞被用来避免免疫系统攻击并扩散当前,各种免疫检查站分子及其链条识别反CTLA4抗体获批后,它正成为多类癌症新标准处理方法,如黑瘤和非小细胞肺癌16..还有一些报告显示在STS病人中对检查站抑制器进行临床试验,并有报告显示二级测试抗CTLA4抑制器Ipilimumab17..研究中受治病人的代名词评语高表示CT抗原,但没有临床利益或抗CT抗生素响应证据后一阶段实验中,nivolumab和ipilimumab综合理疗响应率比nivolumab单方理疗高(16%) (5%)。指CTLA-418号..
研究重点是CD80,这是一个抑制者igand为CTLA4CD80是一个转模glycotein, 共振器表达于激活单细胞表层、B细胞和T细胞19号,20码..据报CD80还表现为肿瘤细胞和球状上皮细胞21号,22号..
双B7子分子CD80(B7-1)和CD86(B7-2)定位为共振分子,在T细胞激活中起最大作用CD80/86通过绑定CD28激活T细胞,反之,CTLA4表示激活T细胞和Treg细胞与CD80/CD86绑定比CD28强并抑制T细胞激活此外,CTLA4从APC(反基因显示单元)中去除CD80/CD86,从而抑制共振信号并抑制T细胞激活19号..
近日中可解析化ICP吸引注意力高循环可溶性PD-L1与多恶性肿瘤预测不良有显著关联[STS一号,九九,10,11,12,13,14,15..PD-L1可溶解功能抑制系统免疫响应,治疗目标从手机PD-L1扩展至手机循环可溶解PD-L123号..在这次研究中,我们分析可溶解CD80与STS病人预测之间的关系,提出可溶解CD80可能影响STS免疫系统假设
有三个报告sCD80源头:在细胞膜上取CD8024码CD80单片从细胞释放25码并分式CD8017..数样变异中,转模域的删除形式在细胞膜上释放不稳定性,结果产生sCD80
功能学上 SCD80对肿瘤行为双词效果报告在一个方面,sCD80抑制T细胞激活,优先绑定CTLA419号高水平sCD80对患血癌和前列腺癌者预测差25码..反之,sCD80抑制T细胞激活26诱导细胞扩散27号并禁止PD-L1/PD1中介免疫抑制28码..在这次研究中,我们成功证明高sCD80与短生存和无损生存相关sCD80可能抑制STS中的免疫系统至今已经进行了7次Galiximab临床试验,a-CD80抗体https://clinicaltrials.gov)淋巴病临床实验中,据报告49%的病人显示经Galiximab使用后肿瘤体积下降,没有四级不良事件或与治疗有关的死亡29..高sCD80值预测差,因此即使在STS区域也有可能预期gliximab效果
约束
这项研究有一些局限性病人数少STS稀有癌症,多组肿瘤STS发病率不到十万分之六,表示所有癌症成人为1-2%30码..因此难以采集样本,并可能难以判定其截取值研究中截取值由ROC曲线决定更多样本可能给我们更正确截值sCD80并判定STS中截值sCD80水平可成为STS病人的实用预测标志
提供数据和资料
不适用
缩写
- 比较方案:
-
imune检查站蛋白质
- sCD80:
-
可溶式CD80
- STS:
-
软组织sacoma
- MS:
-
免元生存
- OS:
-
整体生存
- sPD-L1:
-
可溶式PD-L1
- ROC:
-
接收者操作特征
- AUC:
-
区域曲线下
- LRFS:
-
本地免复发生存
- WLS:
-
Well-differentiated liposarcoma
- DLS:
-
偏差双脂瘤
- MLS:
-
Myxoid润滑镜
- MFS:
-
Myxofibrosarcoma
- UPS:
-
无差别心性sacoma
- LMSs:
-
Leiomyosorma
- SS:
-
异性沙马
- MPNST:
-
恶性外围神经层肿瘤
- DOD:
-
死病
引用
BourcierK公司、LeCesneA公司、TselikasL公司等软组织sacoma基础知识心电图插播2019;42(9):1255–61.
SasakiH公司、长野S公司、科米亚S公司等验证不同营养评估工具预测软组织旋翼细胞患者预测养分学2018;10(6):765
OguraK Higashi软组织沙卡统计:日本骨软组织肿瘤寄存器报告癌症2009;115:5243–50.
Stojadinovica、leungDH、hoosA等分析2 084局部成人软组织沙马微值安苏格2002;235(3):424–34.
JulianAM,BhagirathbhaiD,AixaES等下一代癌症免疫检查站理疗:新动态与挑战J Hematoloncol2018;11(1):39
PerisanoC,VitielloR,SgambatoA等PD1和PD-L1高等级成人肢体表达法评价:免疫法可能产生的影响BiolRegul自动机代理2020年;344Supplication3:289-94
GangC、AlexanderCH、WeiZ等ExsomalPD-L1帮助免疫抑制并关联反PD-1响应自然界2018;560(7718):382–286.
FinkelmeierFCanliOTALA等可解决高水平编程死亡解析(spd-L1)识别肝细胞癌患者预测差ourJ癌症2016年;59:152-9
Frigola X,Inman B,LohseC等识别可溶式B7-H1保留抑制免疫活动并关联攻击性肾细胞癌Clin癌症解析2011;17:1915–23.
TakahashiN公司、IwasaS公司、SasakiY公司等srum可编程细胞死亡水平Ligand1作为首次治疗转移性或复发性胃癌的预知因子J癌症ResClinOncol2016;142:1727–38.
YoshidaJ、IsikawaT、DoiT等临床悬浮性免疫检查站分子高级食道癌医学Oncol20193660
沈HJYZHAY等可编程死亡和1高表达式外围T细胞淋巴ma:预测生物标志染色学2019;24:392–298.
OkumaY,HosomiY,中原Y等高等素可编程细胞死亡i肺癌2017;104:1-6
TominagaT,AkiyoshiT,YamamotoN等可编程细胞死亡1和可编程细胞死亡iPLOS一号201914e0212978
unihiroA,TomokiN,AkinobuH等可编程死1比PD-L1有效预测软组织sacomas相容和预测SciRep2020年;10:9077
Khans,GerberDE等自免性、检查站抑制法和免疫相关不良事件:审查semin癌症生物2020年;64:93-101
罗伯特GM,AchimJ、Sacha G等实验性研究抗体ivityipilimumab萨科马2013年;168145
d'AngeloSPMMNivolumab或非ipilimumab处理异向sacoma(AllianceA091401):2个开放标签非比较随机测试2柳叶树201919(3)416-426
KakoulidouM公司,GiscombeR公司,Zha人类可溶解CD80通过替代相联生成,并发CD80绑定CD28和CD152影响T细胞激活扫描Jimunol2007/66:529-37
古德、Ao X、Yang Y等可溶性免疫检查站癌症:生产、功能和生物意义Jimunther癌症2018;6:132
丹德图拉SserpaSetal细胞与肿瘤微环境构件之间的分子交互联系建议移动语言癌症新治疗方法的潜在目标癌症医疗2012;1(2):128–40.
GarinEH,ReiserJ,Cara-FuentesG等案例序列:CTLA4-IgG1最小变化疾病和焦点分块硬化皮德尔内弗罗尔2015年;30:469-77
SergioAM、JavierDQ、JoseGV等异常PD-L1对癌症免疫法的临床影响JimunolRes2021883978
加林EH、MuWM、ArthurJ等寄存式CD80最小变化疾病上升,但在焦分球硬化中不上升基德尼Int2010;78(3):296–302.
EsserMT、GrahamDR、CorenLV等CD45、CD80-1、CD86-B7-2和二类大型相容分子分入人体免疫机能丧失病毒类型1病毒和微粒:对病毒病理生成和免疫调控的影响JVirology2001;75(13):6173–82.
Hockbd,StarlingGC,PattonWN等识别循环可解式CD80:染色恶性病人水平路克淋巴2004;45(10):2111–8.
He W、HuZB、LiuF等体外联动可溶性B7分子抗扰活动Acta比奥契姆波尔2006;53(4):807–13.
sturmhoefelk、LeeL、GrayGS等可溶性B7-IgG聚变蛋白癌症解析1999;59(19):4964–72.
Czuczman MS,ThallA,Witzigte等Galithimab第一/二阶段研究反CD80反体复发或复发JClinOncol2005;23(19):4390–8.
BourcierK公司、LeCesneA公司、TselikasL公司等软组织sacoma基础知识心电图插播器2019;42(9):1255–61.
Acknowledgements
无
供资问题
不适用
作者信息
作者和附属关系
交文
YM实验、验证、正式分析、调查和可视化,整理数据并写原创手稿KA概念化并监督研究,执行方法学、验证、正式分析、调查和可视化,整理资源,整理数据,编写原创手稿并管理项目KYTTTI实验验证TN验证并整理数据AS写、审查编辑手稿并获取资金所有作者阅读并批准最终手稿
对应作者
道德申报
道德核准并同意参赛
所有实验都按照研究、测试和教育使用动物的跨学科原则和准则进行。研究经作者附属机构道德委员会批准
竞技兴趣
作者声明他们没有竞技兴趣
附加信息
发布器注解
伟德体育在线Springer自然对发布地图和机构附属关系中的司法请求保持中立
权限和权限
开放存取文章依据创用CC4.0国际许可使用,允许使用、分享、改编、分发和复制任何介质或格式,只要你适当信任原创作者和源码提供链接并显示是否修改图片或其他第三方素材均载入文章Creative公共许可中,除非素材信用栏中另有表示素材未载入文章Creative公共许可中, 法定规则不允许使用或超出许可使用范围时, 需直接从版权持有者处获取许可 。查看许可副本访问http://creativecommons.org/licenses/by/4.0/.创用公共域免责http://creativecommons.org/publicdomain/zero/1.0/)适用于本条提供的数据,除非信用线对数据另有说明。
关于此文章
点上此文章
松山市et al.可溶解CD80对软组织肿瘤患者的作用J OrthopSurgRes17404 (2022).https://doi.org/10.1186/s13018-022-03283-2
接收:
接受:
发布:
多尔市:https://doi.org/10.1186/s13018-022-03283-2
关键字
- imune检查站蛋白质
- 可溶解CD80
- 预测