摘要
背景
几种SARS-CoV-2疫苗已显示出对抗Covid-19感染的临床疗效,但不同方案引发的免疫反应仍存在不确定性。对于感染后临床风险增加且免疫衰老可能限制疫苗反应的老年人来说,这是一个特别重要的问题。BNT162b2 mRNA和ChAdOx1腺病毒疫苗是英国计划采用8-12周“延长间隔”部署的首批两种疫苗。
目标
我们分析了131名80岁以上的参与者在第二次“延长间隔”双重疫苗接种BNT162b2 mRNA (n= 54)或ChAdOx1 (n腺病毒疫苗。在第二次疫苗接种后2-3周采集血液样本,并与先前报告的第一次疫苗接种后5周采集的样本配对。采用Elecsys®电化学发光免疫分析法检测抗体反应,采用IFN-γ ELISpot检测细胞反应。
结果
在两次接种任一疫苗后,所有供者均可检测到针对刺突蛋白的抗体反应。4个捐助者有证据表明以前有过自然感染,已知这可以促进疫苗反应。在53例infection-naïve供者中,BNT162b2双疫苗接种后的抗体滴度中位数为4030 U/ml (IQR 1892-8530),而在74例ChAdOx1疫苗接种后的抗体滴度中位数为1405 (IQR 469.5-2543) (p = < 0.0001)。在mRNA受体和ChAdOx1受体中分别观察到30%和49%的尖峰特异性T细胞应答,ChAdOx1疫苗接种者的中位应答分别为14和20点/百万,高1.4倍(p= 0.022)。
结论
双重接种BNT162b2或ChAdOx1可在老年人中诱导较强的体液免疫。mRNA方案的抗体应答是mRNA方案的2.9倍,而腺病毒疫苗的细胞应答是mRNA方案的1.4倍。因此,从两种疫苗平台得出了不同的免疫原性模式。评估这些同源疫苗方案后免疫反应的相对稳定性,以评估疫苗强化的潜在需求,将是有意义的。此外,这些发现表明,异种疫苗平台可能提供进一步优化疫苗反应的机会。
介绍
针对SARS-CoV-2的疫苗已被证明对症状性Covid-19的发展非常有效[1,2,3.]。已经开发了一系列不同的递送刺突蛋白免疫原的方法,包括mRNA,腺病毒和蛋白质平台,并且疫苗的相对免疫原性是开发最佳疫苗方案的重要考虑因素。
目前,预防COVID-19的免疫相关因素尚不确定,尽管刺突特异性抗体反应的大小似乎是疫苗效力的重要决定因素[4,5,6]。在大多数情况下,总刺突特异性免疫反应与中和抗体活性水平相关,后者的决定因素本身可能是疫苗效力的关键因素。相比之下,刺突特异性细胞免疫反应的相对重要性目前尚不确定。T细胞反应在控制呼吸道感染的严重程度方面很重要,值得注意的是,与较轻微的无症状感染相比,SARS-CoV-2疫苗本身在预防严重临床结果方面要有效得多[7]。因此,T细胞对刺突蛋白的反应可能在严重疾病的控制中发挥重要作用。
COVID-19大流行的一个显著特征是老年人的相对脆弱性[8因此,Covid-19疫苗必须在这一人群中表现出高效。这是一个潜在的挑战,因为疫苗诱导的免疫反应在老年人中往往不是最佳的[9]。特别是,老年人接种流感疫苗后的体液反应减少,因此有必要引入一系列新型疫苗平台[10]。这种效应的基础尚不确定,但很可能反映了免疫衰老的影响,免疫系统的功能功效随着年龄的增长而恶化。
提供Covid-19疫苗的另一个变量是第一剂和第二剂疫苗之间的时间间隔。BNT162b2疫苗获得许可,每次给药间隔3周,这种方法已在世界上许多国家采用。相比之下,延长ChAdOx1剂量间隔时间可改善免疫反应,现在通常推荐间隔时间为8至12周。有趣的是,与mRNA平台相比,ChAdOx1疫苗后抗体产生的动力学也被延迟。英国和其他几个国家已经选择采用“延长间隔”疫苗方案,其中BNT162b2或ChAdOx1疫苗的第二剂在第一剂后最多延迟12周。采用这种方法是为了增加单一疫苗接种的人口覆盖率,模型方法和现实世界的临床数据都表明,这种方法在降低人口死亡率方面取得了成功[11]。
有趣的是,在延长了BNT162b2疫苗的接种间隔后,峰值特异性抗体反应的强度增加了三倍,这表明应该考虑延长目前疫苗接种间隔的3周[12]。然而,延长间隔方法也与第二次疫苗接种后细胞免疫应答峰值的幅度降低有关。据我们所知,目前还没有对BNT162b2或ChAdOx1疫苗在延长间隔疫苗方案中使用时的免疫原性进行直接比较。
在这项研究中,我们比较了双重接种BNT162b2或ChAdOx1后老年人的刺突特异性抗体和细胞反应。我们证明mRNA疫苗引起更强的血清学反应,而腺病毒载体驱动更强大的细胞免疫。这些发现对长期疫苗免疫监测和最佳异源疫苗平台的设计具有一系列意义。
方法
研究设计及参与者
131名年龄在80岁及以上、独立生活的参与者被招募参与研究。允许合并并发症。参与者是在2020年12月29日至2021年3月4日期间招募的。当地初级保健网络确定了接种过BNT162b2或ChAdOx1疫苗的80岁及以上的疫苗接种者,他们没有住在住宅或养老院,也没有需要辅助生活。参与者被发送邀请函参加,如果他们想参加,直接与研究团队联系。在与研究小组进行初步接触后,参与者获得了参与者信息表,并通过电话口头表示同意。在第一次采血时间点获得书面同意证实了这一点。获得了西北普雷斯顿研究伦理委员会的伦理批准,结果良好(REC 20\NW\0240),工作在CIA UPH下进行,并根据赫尔辛基宣言和良好临床实践进行。
程序
所有供者均接受了两剂BioNTech/Pfizer公司的BNT162b2或Astra Zeneca公司的ChAdOx1 nCoV-19。54名供者接受了BNT162b2(中位年龄83岁,范围80-96岁),77名供者接受了ChAdOx1(中位年龄83岁,范围80-98岁)。从初级保健记录和邀请信中确定后,还招募了较年轻的健康对照者(29名捐赠者接受了BNT162b2(中位年龄69岁,范围42-79),55名捐赠者接受了ChAdOx1(中位年龄72岁,范围51-79)1)。在第二次疫苗接种后2-3周进行了静脉切开术取样,作为分析的主要时间点。在第一次接种疫苗后5至6周采集的匹配样本也可用于比较评估。样本用于抗体和细胞研究。
罗氏Elecsys®电化学发光免疫分析法(ECLIA)
在英国公共卫生部(PHE) Porton的自动罗氏cobas e801分析仪上使用电化学发光法检测SARS-CoV-2特异性总抗体。按照制造商的建议进行校准和质量控制。采用Roche Elecsys®Anti-SARS-CoV-2 ECLIA (COV2,产品代码:09203079190)检测抗核衣壳蛋白(NP)抗体,采用Roche Elecsys®Anti-SARS-CoV-2 ECLIA (COV2 S,产品代码09289275190)检测抗spike (S)抗体,如前面所述[13]。抗核衣壳结果用截断指数(cut- cut index, COI)值表示,COI值≥1.0视为抗核衣壳抗体阳性。抗尖峰结果以单位/ml (u/ml)表示,在检测的全定量范围内(0.4-2500 u/ml),结果≥0.8 u/ml的样品被认为是抗尖峰抗体阳性。> 2500 u/ml的样品进一步稀释(1:10、1:100、1:1000)至定量范围内。
细胞分析
外周血单个核细胞(PBMCs)从全血样本中分离,使用T-Cell Xtend (Oxford immunnotec)和Ficoll。对回收的细胞进行定量和稀释后,将250,000个PBMC镀入“T-SPOT Discovery SARS-CoV-2”试剂盒(Oxford immunnotec)的每孔中。该方法旨在测量覆盖四种不同SARS-CoV-2抗原蛋白序列的重叠肽池的反应,不受HLA限制,并包括阴性对照和pha刺激的细胞作为阳性对照。从序列中去除与地方性冠状病毒高度同源的肽序列,保留可能与SARS-CoV-1同源的序列。细胞孵育,计数分泌干扰素γ的T细胞。S1池中每百万分之24以上的点被定义为与Oxford immunnote诊断Covid试剂盒一致的阳性结果。
统计分析
使用Kolmogorov-Smirnov分析对数据进行正态性检验。对比分析BNT162b2和chadox1疫苗队列的抗体效价和细胞反应,采用配对样本的Mann-Whitney u检验或Wilcoxon检验。抗体滴度和T细胞反应以中位数和IQR表示。抗体滴度也在补充表中用扫描电镜表示为几何平均值1。所有分析使用Graphpad prism v9.1.0 for Mac (San Diego, California USA)。
结果
在老年供者中,与ChAdOx1相比,双重接种BNT162b2后的刺突特异性抗体应答高2.9倍
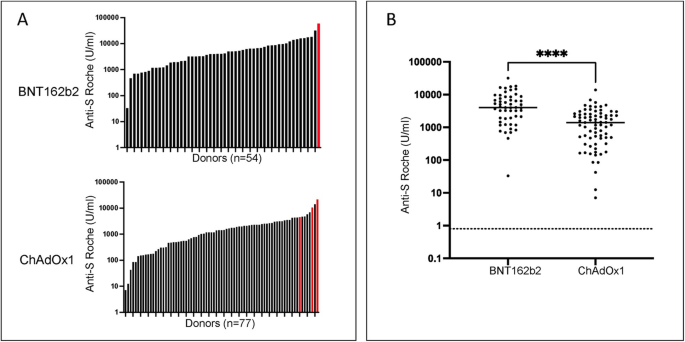
131名年龄在80岁以上、居住在社区的捐赠者被招募到这项研究中。在第二次疫苗接种后2-3周采集血样。采用定量罗氏抗体特异性ELISA法评估抗体特异性反应,所有供者在BNT162b2 (n= 54)或ChAdOx1 (n= 77)种疫苗。1)。然而,接受BNT162b2疫苗接种的供体中位尖峰特异性抗体水平高出2.9倍。具体而言,ChAdOx1疫苗接种BNT162b2 (IQR 1912-8613)后的中位值为4100 u/ml,而ChAdOx1疫苗接种后的中位值为1416 u/ml (IQR 480-2643)。排除了4名血清学证据表明曾感染过SARS-CoV-2的献血者,已知这有力地促进了疫苗反应[14],分别为4030 u/ml和1405 u/ml。
在两次BNT162b2疫苗接种后,尖峰特异性抗体反应的升高反映了对第二种疫苗的增强的增量反应
除了在第二次疫苗接种后采集的血液样本外,我们还获得了在第一次疫苗接种后5-6周采集的匹配患者样本。这些样本的抗体和细胞分析先前有报道,并证明单剂BNT162b2或ChAdOx1疫苗后抗体水平相当[13]。因此,我们接下来继续确定在该队列中接种第二种疫苗后的增量抗体反应模式。
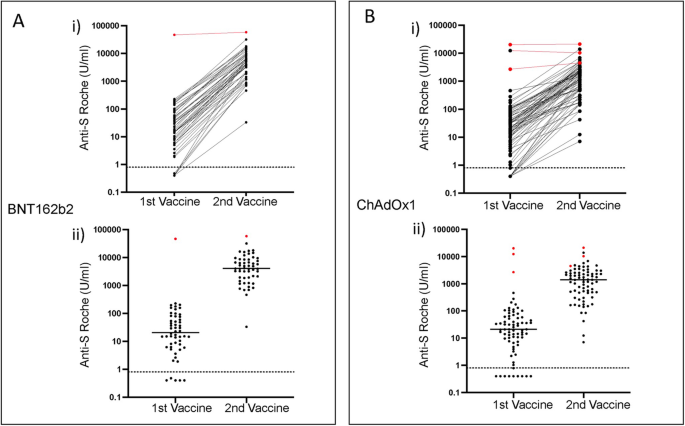
所有BNT162b2疫苗接种者在第一次疫苗接种后抗体水平中位数为21 (IQR为6.2-76.5),在第二次疫苗接种后上升至4100。因此,加强疫苗导致抗体应答增加197倍(图2)。2A)一名献血者有既往SARS-CoV-2感染的血清学证据,这些值分别为47,100和58,800。排除该供体后,可以对53名infection-naïve供体的疫苗应答进行评估,其中第一次和第二次疫苗接种后的抗体应答中位数分别为19 (IQR 6.2-68)和4030 (IQR 1890-8530),增加了214倍(P< 0.0001)。
对于ChAdOx1疫苗接种者,对77名供者提供了配对样本,其中3人有既往感染SARS-CoV-2的血清学证据。在整个队列中,第一种和第二种疫苗之间的抗体水平中位数从21 (IQR 7-60)上升到1416 (IQR 480-2640),增加了67倍p< 0.0001 (Wilcoxon)。2B)。对于先前感染的三名献血者,这些值分别为12,400 (IQR 2680-20,200)和10,350(4,500 - 21,240)。74名既往无感染的献血者的值分别为20 (IQR 6.4-53)和1405 (IQR 470-2540),增加了70倍(p< 0.0001)。
这些数据表明,任何一种疫苗的第二剂都能强烈增强抗体反应。然而,在infection-naïve供体中,BNT162b2疫苗的相对增加量高出三倍,这解释了双重接种后的最终反应更高。
与BNT162b2相比,双重接种ChAdOx1后的刺突特异性细胞反应高1.4倍
我们对该队列中首次接种疫苗后5周免疫应答的中期分析显示,在接种ChAdOx1疫苗后,免疫应答更高[14],然后使用干扰素-γ ELISpot评估双重接种后的相对应答。
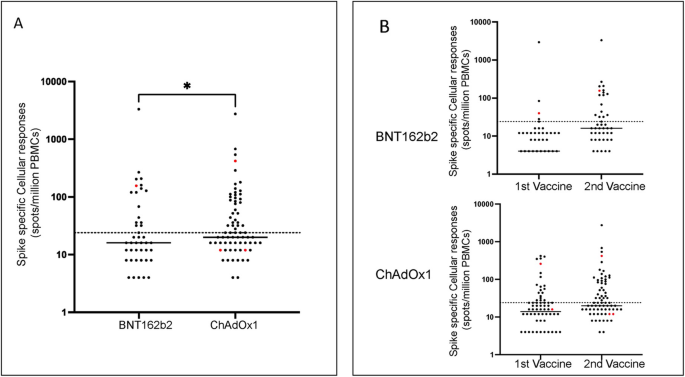
在BNT162b2疫苗接种者中,54名供体中有51名具有配对细胞反应以供分析。在第一次和第二次接种疫苗后,显示细胞反应高于阈值的供体比例分别从9.8%(5/51)上升到33.3%(17/51)。3.A)。排除既往自然感染的单个供者后,中位应答水平增加到每百万PBMC 14个点(P< 0.0001)。3.B)。
对于接种了ChAdOx1疫苗的供者,77名供者中有76名的配对T细胞结果可用。阳性应答比例从第一次接种后的34.2%(26/76)上升到第二次接种后的48.6%(37/76)。3.排除有自然感染证据的献血者后,接种第一次和第二次疫苗后,绝对计数中位数为每百万人20个(p= 0.0014)。3.B)。
这些发现表明,ChAdOx1在老年人中刺激了更强的刺突特异性细胞反应,尽管该疫苗与BNT162b2相比的相对增量优势在第一剂和第二剂疫苗之间从3倍下降到1.4倍。
80岁以上的供者接种双重疫苗后的刺突特异性免疫反应与年轻供者相当
在老年人中,疫苗诱导的免疫反应往往不是最佳的,这可能反映了免疫衰老的影响。因此,我们随后将80岁及以上的捐赠者与42至79岁的捐赠者进行了比较,他们的抗体和细胞反应以类似的方式测量。
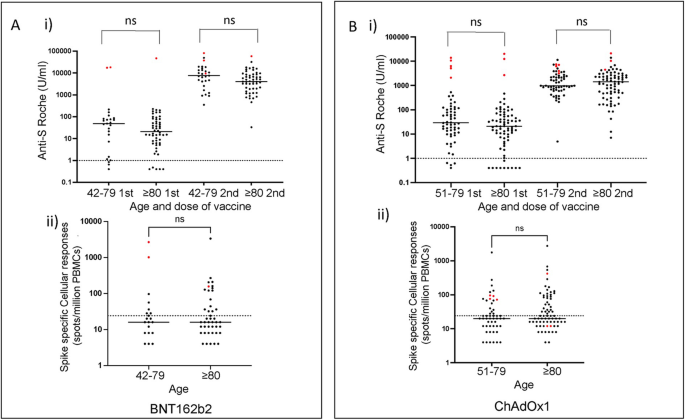
值得注意的是,这两个时间点的免疫反应在两个队列之间具有可比性,老年人的抗体或细胞反应没有明显损伤。在以前没有自然感染的供者中,年轻和老年队列在首次接种BNT162b2疫苗后的抗体应答中位数分别为46和19 (p= 0.57),第二次接种后分别为7026和4030 (p= 0.1)。4A)。ChAdOx1的可比值为25和20 (p= 0.08)、949及1405 (p= 0.96)。4B).这些结果表明,在老年人中,双重接种BNT162b2后,抗体反应有略低的趋势。
在较年轻的队列中,第二次疫苗接种后可进行T细胞测定。在infection-naïve供者中,在老年和年轻队列中,BNT162b2后的中位T细胞反应在两组中均为14个点/百万,而在ChAdOx1后,这些值相等,为20个点/百万。
因此,这些研究结果表明,使用BNT162b2或ChAdOx1进行双同源疫苗接种对于诱导老年人的刺特异性免疫反应非常有效,并且在很大程度上克服了免疫衰老的任何显着影响。
讨论
确定Covid-19疫苗接种的免疫相关因素对于指导在人群中部署最佳疫苗方案至关重要。这一分析对老年人尤其重要,因为他们感染Covid-19的死亡风险明显增加。在本报告中,我们表明双重接种BNT162b2或ChAdOx1疫苗可在老年人中引起不同的免疫反应。这些观察结果提出了一些关于这些差异的潜在基础以及它们如何与临床应用相关的问题。
这项工作的一个显著特征是,在接种两种疫苗后,每个供体都观察到尖峰特异性抗体反应。就这些疫苗在老年人中的免疫原性而言,这是非常令人鼓舞的,并且可能是已观察到的针对Covid-19严重感染的强大临床保护的基础。刺突特异性抗体反应的大小正在成为疫苗效力的免疫相关因素,如果反应能长期维持,那么这些发现预示着对这一群体的保护是好的。
值得注意的是,与接受ChAdOx1疫苗的人相比,接受BNT162b2疫苗的人的抗体反应峰值高出近3倍。我们之前在该队列中的报告显示,在每种疫苗的第一次“启动”剂量后5周,抗体反应相同。因此,第二次剂量后的差异效应表明,第二次剂量的抗体增量增强是区分mRNA和基于腺病毒的平台的关键因素。实际上,BNT162b2疫苗的中位数增量为214,而ChAdOx1疫苗的中位数增量为70。这些发现可能反映了mRNA传递的强体液免疫原性,诱导生发中心反应和尖刺特异性记忆B细胞的发育。重要的是评估这些抗体反应是如何随着时间的推移而发展和维持的,因为研究表明,与BNT162b2相比,接种ChAdOx1疫苗后的免疫反应有所延迟。因此,职称差距可能会随着时间的推移而改变。有人担心,针对腺病毒载体的免疫反应可能会限制这种疫苗的增强程度,但很明显,在第二次注射ChAdOx1后,仍然可以看到强烈的增量反应。
该分析的一个特点是,在接种第二种疫苗后,供体之间抗体反应的相对增加非常相似。这在BNT162b2方案中尤其引人注目,并表明在第一次疫苗接种后对抗体反应的评估是最终反应的有力预测指标。人群中对疫苗的不同反应背后的原因尚不确定,但在第三次加强剂量后,这些特征是否保持将是令人感兴趣的。
与体液免疫相比,双重疫苗接种后,刺特异性细胞反应不那么明显。先前的一份报告显示,单次接种ChAdOx1疫苗后的细胞反应更强,并且在两次接种后仍保持这种优势。ChAdOx1和BNT162b2疫苗分别提高了1.7倍和3.5倍的T细胞应答,因此疫苗之间细胞应答的相对差异从第一种疫苗后的3倍减少到第二种疫苗后的1.4倍。评估加强疫苗接种后是否有任何差异将是有意义的。T细胞反应用干扰素-γ Elispot测定,尽管这是一种标准技术,但在未来的工作中,评估CD4+和CD8+ T细胞亚群和差异细胞因子谱的相对反应将是很重要的。ChAdOx1后细胞反应增强的潜在基础尚不清楚,但可能反映了腺病毒载体表达系统抗原呈递的性质[15]。
差异细胞免疫反应的潜在意义尚不清楚,但可能影响体液免疫的寿命和临床疗效[16]。因此,评估两个队列中抗体反应的时间稳定性并将其与细胞免疫谱相关联将是有意义的。此外,尽管细胞反应可能有助于限制Covid-19感染的严重程度,但基于mrna的疫苗的临床保护率至少与使用ChAdOx1的疫苗一样高。
考虑到两种疫苗免疫反应的不同特征,人们很容易推测,与同源递送相比,组合异种疫苗方案可能提供更好的免疫原性[17]。值得注意的是,与标准间隔同源的BNT162b2疫苗接种相比,ChAdOx1/BNT162b2方案的细胞应答更优越[18]而这种异源疗法介导了增强的细胞启动,同时以4周的疫苗间隔保持强大的体液免疫[19]。等待异种ChAdOx1/BNT162b2联合使用“延迟间隔”疫苗方案的结果将令人感兴趣。
老年人接种流感等疫苗后的免疫反应往往不是最佳的[20.,21],因此有兴趣评估不同年龄组的刺突特异性免疫。有趣的是,在80岁以上的人群和96名42 - 79岁的捐赠者之间,我们没有发现抗体或细胞反应有任何差异。这些发现与老年人接种疫苗后对Covid-19提供的出色临床保护一致,并表明刺突免疫原或新型mRNA和ChAdOx1传递平台的性质似乎能够克服免疫衰老的任何严重影响[22]。然而,在其他研究中也发现了年龄的一些负面影响[23并且通过中和或细胞毒性等检测来评估这些免疫反应的功能质量也很重要。性别对疫苗诱导的免疫反应没有明显的影响,尽管更大规模的人群研究显示男性的抗体反应较低[24]。
我们研究的一个局限性是我们没有研究中供体合并症的详细信息。
总之,“延长间隔”双重接种BNT162b2或ChAdOx1在老年人中引起强烈的刺突特异性免疫反应,这与现实世界的有效性数据一致。这两种疫苗在诱导抗体或细胞反应方面表现出不同的能力,这可能对评估未来的联合治疗方案很重要。
参考文献
Dagan N, Barda N, Kepten E, Miron O, Perchik S, Katz MA,等。BNT162b2 mRNA新冠病毒疫苗在全国大规模疫苗接种环境中的应用中华医学杂志,2013;31(5):393 - 393。https://doi.org/10.1056/NEJMoa2101765。
刘建军,李建军,李建军,等。BNT162b2 mRNA新冠病毒疫苗的安全性和有效性中国生物医学工程学报,2016;33(2):391 - 391。https://doi.org/10.1056/NEJMoa2034577。
Voysey M, Clemens SAC, Madhi SA, Weckx LY, Folegatti PM, Aley PK,等。ChAdOx1 nCoV-19疫苗(AZD1222)抗SARS-CoV-2的安全性和有效性:巴西、南非和英国四项随机对照试验的中期分析柳叶刀》。2021;397(10269):99 - 111。https://doi.org/10.1016/s0140 - 6736 (20) 32661 - 1。
Khoury DS, Cromer D, Reynaldi A, Schlub TE, Wheatley AK, Juno JA,等。中和抗体水平可高度预测对症状性SARS-CoV-2感染的免疫保护。中华医学杂志,2011;27(7):1205 - 1111。https://doi.org/10.1038/s41591-021-01377-8。
冯绍峰,王晓峰,王晓峰,等。预防有症状和无症状SARS-CoV-2感染的相关因素。medRxiv。2021:2021.06.21.21258528。
Earle KA, Ambrosino DM, Fiore-Gartland A, Goldblatt D, Gilbert PB, Siber GR,等。抗体作为COVID-19疫苗保护性关联的证据。medRxiv。2021:2021.03.17.20200246。
刘建军,刘建军,刘建军,等。BNT162b2 mRNA疫苗和ChAdOx1腺病毒载体疫苗对COVID-19死亡率的影响medRxiv。2021:2021.05.14.21257218。
Shahid Z, Kalayanamitra R, McClafferty B, Kepko D, Ramgobin D, Patel R,等。COVID-19与老年人:我们所知道的。中华老年医学杂志,2020;68(5):926 - 99。https://doi.org/10.1111/jgs.16472。
M . ller, M . Moskorz W . Drexler I . Walotka L . Grothmann R .等。Biontech/Pfizer BNT162b2 COVID-19疫苗的年龄依赖性免疫反应临床感染疾病。2021。https://pubmed.ncbi.nlm.nih.gov/33906236/https://pubmed.ncbi.nlm.nih.gov/33906236/。
Wilkinson K, Wei Y, Szwajcer A, Rabbani R, Zarychanski R, Abou-Setta AM,等。老年人大剂量流感疫苗的有效性和安全性:一项系统综述和荟萃分析疫苗。2017;35(21):2775 - 80。https://doi.org/10.1016/j.vaccine.2017.03.092。
刘建军,刘建军,刘建军,等。BNT162b2 mRNA疫苗和ChAdOx1腺病毒载体疫苗对英格兰老年人症状性疾病、住院率和死亡率的早期有效性medRxiv。2021:2021.03.01.21252652。
刘建军,刘建军,刘建军,等。延长间隔接种BNT162b2疫苗可提高老年人抗体产生峰值。medRxiv。2021:2021.05.15.21257017。
Parry HM, Bruton R, Tut G, Ali M, Stephens C, Faustini S,等。老年人单次接种BNT162b2或ChAdOx1可诱导产生相同的抗体,但接种ChAdOx1后细胞反应增强。《柳叶刀》的预印本。2021.https://papers.ssrn.com/sol3/papers.cfm?abstract_id=3825573
杨建军,李建军,李建军,等。先前sars - cov -2感染和未感染的英国医护人员对首次BNT162b2疫苗剂量的t细胞和抗体反应:一项多中心、前瞻性、观察性队列研究。《柳叶刀》的预印本。2021.
Anywaine Z, Whitworth H, Kaleebu P, Praygod G, Shukarev G, Manno D,等。Ad26 2剂异源疫苗接种方案的安全性和免疫原性ZEBOV和MVA-BN-filo埃博拉疫苗:乌干达和坦桑尼亚一项1期随机临床试验的12个月数据中华传染病杂志,2019;22(1):46-56。https://doi.org/10.1093/infdis/jiz070。
Sant AJ, DiPiazza AT, Nayak JL, Rattan A, Richards KA。CD4 T细胞对流感病毒的保护:病毒抗原特异性和功能潜力。中华免疫学杂志,2018;28(1):91-105。https://doi.org/10.1111/imr.12662。
Borobia AM, Carcas AJ, pembrorez Olmeda MT, Castaño L, Jesús Bertrán M, García-Pérez J,等。首次接受ChAdOx1s治疗的受试者中BNT162b2的反应原性和免疫原性:一项随机、适应性、2期试验(CombiVacS)的初步结果《柳叶刀》2021年预印本。
Hillus D, Schwarz T, Tober-Lau P, Hastor H, Thibeault C, Kasper S,等。ChAdOx1-nCoV19和BNT162b2同源和异源启动增强免疫的安全性、反应性和免疫原性:一项前瞻性队列研究medRxiv。2021:2021.05.19.21257334。
刘霞,Shaw RH, Stuart AS, Greenland M, Dinesh T, Provstgaard-Morys S,等。com-COV研究的安全性和免疫原性报告——一项单盲随机非劣效性试验,比较异源和同源启动-增强方案与腺病毒载体和mRNA COVID-19疫苗。《柳叶刀》的预印本。2021.
陈建军,陈建军,陈建军,等。免疫接种对老年人免疫功能的影响。中国生物医学工程学报,2018;40(4):893 - 893。https://doi.org/10.1016/j.smim.2018.10.010。
b细胞对极端年龄人群接种疫苗的反应。免疫学杂志,2009;9(3):185-94。https://doi.org/10.1038/nri2508。
Parry HM, Tut G, Faustini S, Stephens C, Saunders P, Bentley C,等。80岁以上人群接种BNT162b2疫苗可诱导P.1巴西变异体交叉中和的强体液免疫反应《柳叶刀》2021年预印本。
M . ller, M . Moskorz W . Drexler I . Walotka L . Grothmann R .等。Biontech/Pfizer BNT162b2 COVID-19疫苗的年龄依赖性免疫反应medRxiv。2021:2021.03.03.21251066。
魏杰,Stoesser N, Matthews PC, Ayoubkhani D, Studley R,等。英国45965名成年人对SARS-CoV-2疫苗的抗体反应微生物学报。2021。https://doi.org/10.1038/s41564-021-00947-3。
致谢
这项工作得到了由NIHR/UKRI资助的国家核心免疫研究和英国冠状病毒免疫学联盟(UK- cic)的部分支持。
我们感谢Rory Meade医生、Rosie Laugharne医生、Tom Groves医生、Parjit Dhillon医生、Eleanor Brodie医生以及Harborne医疗实践、Northumberland House外科、New Road外科、Lapal医疗实践和Wychbury医疗集团的患者和工作人员。我们还要感谢米莉·曼宁、丹妮尔·萨瑟兰、塔姆辛·德鲁里和亚历克斯·布雷在招聘过程中的帮助。我们感谢Rajinder Jeet和Shahada Rahman Joli提供的静脉切开术服务。
数据和材料的可用性
本研究中使用的去识别数据可在获得伦理权威机构批准并向通讯作者PM (p.moss@bham.ac.uk)。
资金
这项工作得到了由DHSC/UKRI和国家核心研究免疫规划资助的英国冠状病毒免疫学联合会(UK- cic)的部分支持。
作者信息
作者及单位
贡献
HP, RB, PM设计了这项研究。PM, HP, JZ撰写稿件,HP和RB招募参与者。SH, JZ, BH, AO, CS, GT, HP进行了实验。HP, JZ, PM,验证和分析数据。所有作者都可以充分访问数据并批准提交本报告。
相应的作者
道德声明
相互竞争的利益
我们声明没有相互竞争的利益。
额外的信息
出版商的注意
伟德体育在线施普林格·自然对已出版的地图和机构关系中的管辖权要求保持中立。
补充信息
附加文件1:补充表1。
在80岁及以上无既往感染证据的参与者中,抗体反应呈现为接种第一次和第二次疫苗后的几何平均值。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,该协议允许以任何媒介或格式使用、共享、改编、分发和复制,只要您适当地注明原作者和来源,提供知识共享许可协议的链接,并注明是否进行了更改。本文中的图像或其他第三方材料包含在文章的知识共享许可协议中,除非在材料的署名中另有说明。如果材料未包含在文章的知识共享许可中,并且您的预期用途不被法律法规允许或超过允许的用途,您将需要直接获得版权所有者的许可。如欲查阅本许可证副本,请浏览http://creativecommons.org/licenses/by/4.0/。创作共用公共领域免责声明(http://creativecommons.org/publicdomain/zero/1.0/)适用于本文中提供的数据,除非在数据的信用额度中另有说明。
关于本文
引用本文
帕里,H,布鲁顿,R,斯蒂芬斯,C。et al。老年人延长间隔同源双重接种后BNT162b2或ChAdOx1疫苗的差异免疫原性Immun老化18, 34(2021)。https://doi.org/10.1186/s12979-021-00246-9
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/s12979-021-00246-9
关键字
- 疫苗接种
- SARS-CoV-2
- COVID
- 抗体
- 细胞
- 信使核糖核酸
- ChAdOx1
- 荟萃分析