摘要
背景
登革热(DENV)、基孔肯雅热(CHIKV)和寨卡病毒(ZIKV)是在大多数热带和亚热带地区具有重要医学意义的蚊媒病毒。主要通过杀虫剂控制病媒仍然是防止其传播的主要方法。在这里,我们评估了杀虫剂抗药性的概况,并确定了重要的潜在抗药性机制埃及伊蚊而且Ae。蚊从喀麦隆的六个不同地区到军事和民用公共卫生病媒控制行动中常用的杀虫剂。
方法
伊蚊在2020年8月至2021年7月期间,在喀麦隆各地的6个地点采集了蚊子的幼虫或蛹样本,并喂养到下一代G1。Ae。蚊而且Ae。蚊根据世界卫生组织(世卫组织)的建议对G1级成人进行了检测Ae。蚊用实时熔融曲线qPCR分析筛选的G0成人基因型为F1534C、V1016I和V410L伊蚊kdr突变。对已知参与代谢耐药的一些细胞色素p450基因进行了PBO (Piperonyl butyoxide, PBO)检测和实时qPCR。统计分析采用卡方检验和广义线性模型.
结果
观察到对所测试的所有杀虫剂都失去了敏感性。使用0.25%氯菊酯的死亡率在24.27至85.89%之间Ae。蚊从17.35%到68.08%Ae。蚊.0.03%溴氰菊酯的死亡率在23.30%至88.20%之间Ae。蚊69.47 - 84.11%Ae。蚊.我们发现对恶虫威有中等水平的耐药性,死亡率在69.31%至90.26%之间Ae。蚊从86.75%到98.95%Ae。蚊.通过PBO预暴露,我们发现部分或完全恢复了对拟除虫菊酯和恶虫威的敏感性。的基因Cyp9M6F88/87而且Cyp9J10是在Ae。蚊杜阿拉地区对氯菊酯和溴氰菊酯有抗药性的人群。Cyp6P12是高表达的氯菊酯和氯菊酯抗性Ae。蚊样本。检测到F1534C和V1016I突变埃及伊蚊在喀麦隆首次报告了V410L。
结论
这项研究表明Ae。蚊而且Ae。蚊对多种杀虫剂类别具有抗性,涉及多种抗性机制。这些发现可以指导喀麦隆使用杀虫剂控制虫媒病毒媒介。
背景
伊-登革热、基孔肯雅热和寨卡病毒等传播的病毒性疾病在世界各地不同地区,包括非洲的报告越来越多[1].就登革热而言,全世界约有一半人口面临风险,据估计,每年报告的新感染人数为1亿至4亿人[1].病媒控制仍然是预防和抗击传播的基石。使用以杀虫剂为基础的控制战略是应对虫媒病毒疾病暴发的常用方法,目的是迅速降低病媒密度和持续传播[2],通常是在军事行动期间减轻登革热、基孔肯雅热和寨卡病毒威胁的主要战略[3.].然而,杀虫剂的增加使用可能导致选择携带与杀虫剂抗性相关的遗传特征的蚊子。事实上,对公共卫生领域使用的多种杀虫剂的耐药性已经有文献记载埃及伊蚊而且Ae。蚊在世界各地的不同地方[4].
杀虫剂抗性通常通过两种机制实现:解毒增加(代谢抗性)和靶点不敏感(靶点抗性)。通过解毒基因的上调而产生的代谢抗性是一种常见的抗性机制Ae。蚊而且Ae。蚊,主要由三个主要的酶科引起,即单加氧酶(细胞色素P450s)、谷胱甘肽s -转移酶(GSTs)和羧酸酯酶(cos) [5,6].靶位点耐药是由靶基因如乙酰胆碱酯酶(Ace-1),伽马氨基丁酸受体和电压门控钠通道(VGSC)造成击倒阻力(kdr)[5,6].
抗击倒性是拟除虫菊酯和二氯二苯三氯乙烷(DDT)的主要目标位点适应性之一。在Ae。蚊,kdr突变不太普遍,仅检测到4个电压门控钠通道(VGSC)突变影响两个密码子(1532和1534)。在Ae.蚊,许多kdr已有突变的报道[4,7,8].在这些突变中,V1016I、F1534C和V410L突变在拟除虫菊酯耐药性中被广泛研究Ae.蚊来自亚洲、南美洲和少量非洲的人口。在喀麦隆,F1534C和V1016I突变之前曾在Ae。蚊[9,10].V410L是一部小说kdr突变,位于VGSC第6段的I域。这是首次在拟除虫菊酯耐药性中描述Ae.蚊源自巴西里约热内卢里约热内卢的实验室毒株[7,几年后在非洲[11].考虑到该突变已显示出降低钠通道对I型和II型拟除虫菊酯敏感性的潜力,并在与F1534C结合时增加耐药性[12],就必须确定这种突变在自然环境中的当前分布Ae。蚊人口在喀麦隆。这是因为它的存在会大大损害各种拟除虫菊酯杀虫剂的效用,而这些杀虫剂目前是用于伊蚊控制(13,14].此外,一些细胞色素P450基因已被发现在伊蚊田间试验表明,该菌群对拟除虫菊酯具有抗药性,有证据表明其在拟除虫菊酯代谢中的作用CYP9J28,CYP9J10,CYP9J26,Cyp9M6F88/87而且CYP6P12[4,15,16,17,18,19].
我们的目标是量化杀虫剂抗性的概况和涉及的机制Ae。蚊而且Ae。蚊来自横跨喀麦隆南北1000公里的6个城市。在喀麦隆,Ae.蚊是呈现在全国各地的,而分布的呢Ae.蚊仅限于南方,在北纬6度以下[20.,21].我们选择了通常用于公共卫生和军事部队健康保护应用的杀虫剂,以减轻疾病威胁。
方法
蚊类取样及饲养
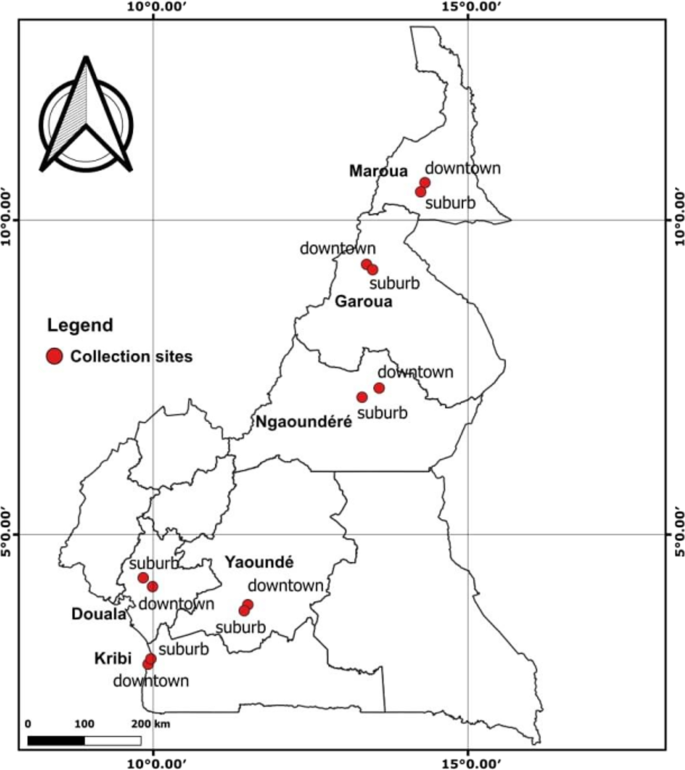
伊蚊样本蚊子幼虫或蛹2020年8月至2021年7月在6个地点在喀麦隆:杜阿拉(N 04°02”729”,E 09年142“N),马鲁阿10°42°37“284”,E 14°18“381”),Garoua (N 09年17°7776年”,13°E 23 288年”),Ngaoundere N 07°35 414年”,E 13°57 365年”,雅温德(N 03 51 993°E 011°27 688“),和Kribi (N 02°56 862”,E 09°54 003”)(图。1).未成熟阶段(野外世代,G0)从不同的潜在幼虫栖息地收集:家养(如罐罐、水箱)、圈养(如旧轮胎、废弃水箱)和自然(如树洞)。在每个地点,从20个阳性幼虫生境收集幼虫或蛹,储存在塑料箱中,转移到昆虫,然后根据地点和土地用途类别(城市和郊区)汇集在一起,饲养到成虫阶段,以分类密钥进行识别[22,23].蚊子被确定为Ae。蚊或Ae。蚊血喂养,繁殖至G1代,用于成虫生物测定。蚊子种群维持在昆虫条件下(温度27±2℃;相对湿度80%±10%),雌性用止血膜供血完成淋病营养周期。本研究使用两株敏感的实验室菌株:病媒控制研究单元(VCRU)菌株Ae。蚊和贝宁实验室染色Ae。蚊.
杀虫剂抗性生物
根据世界卫生组织(世卫组织)议定书,使用3-5天龄的G1代蚊子进行了生物测定。将0.03%和0.05%溴氰菊酯、0.05%甲氰菊酯、0.1%恶虫威和0.25%或0.75%氯菊酯暴露1 h,每管重复4个重复,每个重复20-25只雌性。24 h后记录死亡率;暴露后的活蚊和死蚊分别储存在RNA中或硅胶中。根据世卫组织的建议对死亡率进行解释:死亡率在98%或以上表明易感,死亡率在90至97%之间表明可能存在耐药性,应通过进一步的生物测定加以确认,死亡率低于90%则表明证实存在耐药性[14].
用PBO测定成虫增效剂
为了评估蚊子对杀虫剂的解毒效果,研究了特异性酶抑制剂4%辣龙基丁氧基(PBO),以解决P450s在杀虫剂抗药性中的潜在作用。将3-5天大的雌性成虫预先暴露于ppo浸渍纸1小时,然后立即暴露于所选杀虫剂。24小时后对死亡率进行评分,并与按照世界卫生组织标准使用不含增效剂的每种杀虫剂的结果进行比较[14].
可拆卸的电阻(kdr基因分型结果)
每个城市大约有30只蚊子被分为三种不同的基因型kdr突变:V1016I, V410L和F1534C。使用Livak协议提取每个种群30只蚊子的基因组DNA [24].本研究选择三个kdr突变(F1534C, V1016I和V410L),因为这些突变被描述为与拟除虫菊酯抗性有关Ae。蚊蚊子(4,25].这些突变在非洲也有报道[11,15,26].根据Moyes等的研究,F1534C和V410L与杀虫剂抗性相关,V1016I与其他结合时与杀虫剂抗性相关kdr突变。采用实时熔融曲线定量PCR对V1016I、V410L和F1534C突变进行基因分型[27].每次PCR反应在21.5 μl容积PCR管中进行,PCR管中含有2 μl DNA样品、10 μl SYBR®Green (SuperMix)和1.25 μl每种引物。热循环参数为:95°C持续3分钟,然后40个循环(95°C持续20秒,60°C持续1分钟,72°C持续30秒),最后一个步骤为72°C持续5分钟,95°C持续1分钟,55°C持续30秒,95°C持续30秒。
基因表达
RNA提取和cDNA合成
在这个实验中,使用了三组蚊子:未接触(对照组)来自G1的杀虫剂个体,接触过抗药性测定(抗药性)存活的G1个体,以及敏感(实验室敏感株)的蚊子。每组3个重复,每个蚊种10只。根据制造商的建议,使用PicoPure RNA分离试剂盒(Arcturus®PicoPure RNA提取试剂盒Life Technologies, California, USA)提取RNA。使用“NanoDrop Lite”分光光度计(Thermo Scientific Inc., Wilmington, USA)评估获得的RNA的质量和数量,并保存在−80℃。
根据制造商的说明,使用Superscript III试剂盒(Invitrogen, Carlsbad, CA, USA)合成互补DNA (cDNA)。用QIAquick自旋柱(QIAuick PCR纯化试剂盒,Qiagen)纯化得到的cDNA,并稀释2倍以适应反应的体积。
定量逆转录酶聚合酶链反应
表达分析的候选基因是根据以前参与代谢抗性的影响来选择的[4,17].对每对引物进行标准曲线分析,以检查扩增的特异性和效率。选择4个细胞色素P450候选基因进行分析埃及伊蚊(Cyp9M6F88/87,Cyp9J28a,Cyp9J10,而且Cyp9J32),只有一个答:蚊(Cyp6P12).在体积为20 μl、sybrGreen (Applied Biosystems, Texas, USA) 10 μl、引物(10 μm)各0.6 μl、ddH2O 7.8 μl、CDNA 1 μl的条件下,在95℃反应3 min, 95℃反应10 s, 60℃反应10 s,循环40次。利用2-ΔΔCT方法计算每个候选基因相对于敏感菌株的相对表达量和折叠变化(FC),综合PCR的效率[17],在与管家基因:Aaeg60sL8, RPF7, RSP7和微管蛋白归一化后。所有引物序列和它们的起源显示为答:蚊而且埃及伊蚊在表中1而且2,分别。使用集成到安捷伦品牌TaqMan机器的MxPro软件(MxPro-Mx3005P v4.10, Stratagene, California, USA)。
数据分析
利用广义线性模型(GLM)进行了物种和土地利用类别之间的死亡率比较,该模型具有二项分布和logit链接函数lme4R:统计计算的语言和环境。R统计计算基金会,维也纳,奥地利)。采用卡方检验比较了蚊子预先接触增效剂和未预先接触增效剂后的死亡率。田间样品中各靶基因相对于易感Benin (Ae。蚊)或VCRU (Ae。蚊),根据2−ΔΔCT用管家基因归一化后的PCR效率。该分析使用GraphPad Prism 8.0.2 (GraphPad Software, San Diego, California, USA)进行。P -< 0.05为差异有统计学意义。
结果
杀虫剂抗药性概况埃及伊蚊
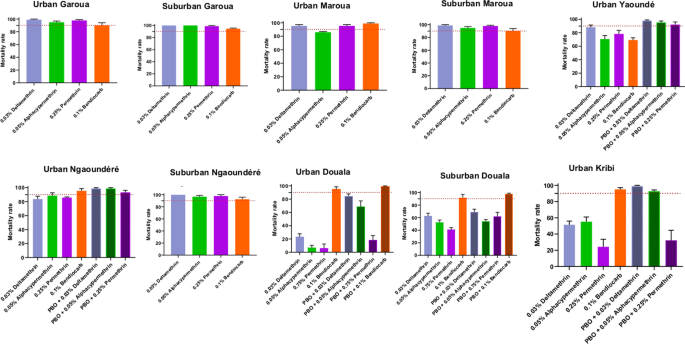
我们总共测试了10个种群Ae。蚊使用四种杀虫剂(图。2).对三种拟除虫菊酯的敏感性因地点而异。对0.25%氯菊酯的抗药性很高,城市Kribi的死亡率为24.27%,城市Ngaoundéré的死亡率为85.89%,城市Maroua可能有抗药性(死亡率为95.43%);郊区Ngaoundéré、城市Garoua、郊区Garoua和郊区Maroua的易感性(死亡率从97.82至98.80%)。值得注意的是,即使使用0.75%的氯菊酯,这是推荐剂量的三倍伊蚊控制,仍然观察到高水平的耐药性。例如,使用0.75%氯菊酯的Douala市区死亡率为5.83%,郊区为40.48%。对于0.03%的溴氰菊酯,在城市Yaoundé、城市Kribi、城市Ngaoundéré、城市和郊区杜阿拉发现了耐药性(死亡率从城市杜阿拉的23.30%到城市Yaoundé的88.20%不等);城郊Maroua可能有耐药性,城郊Ngaoundéré、城郊Garoua、城郊Garoua和城郊Maroua的易感(死亡率从城郊Maroua的98.80%到城郊Ngaoundéré的100%不等)。接受测试的10个人群中有6个对氯氰菊酯具有耐药性(城市Yaoundé、城市克里比、城市Ngaoundéré、城市马鲁阿、城市和杜阿拉城郊);其他三个表现出可能的耐药性(郊区Ngaoundéré,城市Garoua和郊区Maroua),最后一个完全易感(郊区Garoua)。据报告,对恶虫威有中等程度的耐药性,死亡率从Yaoundé城市的69.31%到马鲁阿郊区的90.26%不等。此外,在6个人群中检测到可能的耐药性,死亡率从杜阿拉郊区的91.79%到Ngaoundéré城市的95.50%不等。只有马鲁阿的城市人口易受恶虫威的影响(死亡率为98.91%)。
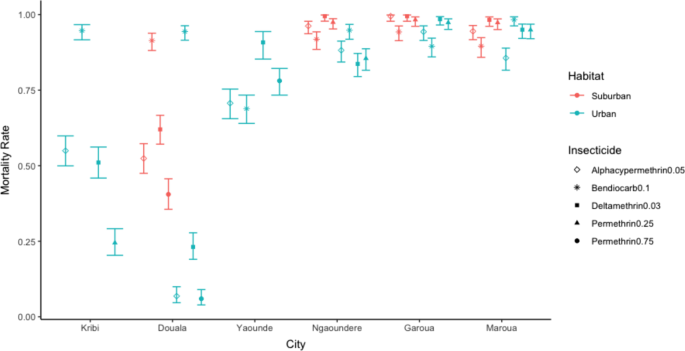
预测中国杀虫剂死亡率的最佳拟合模型Ae。蚊是环境(城市或郊区)、城市和杀虫剂的三重相互作用(附加文件1).在所有城市和杀虫剂的平均水平埃及伊蚊来自城市的人口因杀虫剂致死的死亡率低于来自郊区的人口(P< 0.01)(图3.).在所有城市和环境中,恶虫威造成的死亡率明显高于氯氰菊酯(P< 0.01),溴氰菊酯(P< 0.01)、0.75%氯菊酯(P< 0.01)。然而,这些简单的模式也有例外;在Yaoundé中,恶虫威的死亡率最低,杀虫剂死亡率在Garoua郊区低于城市(图1)。3.).
杀虫剂致死的总死亡率显示出强烈的纬度梯度,北部城市的死亡率较高(图。3.).
杀虫剂抗药性概况白纹伊蚊
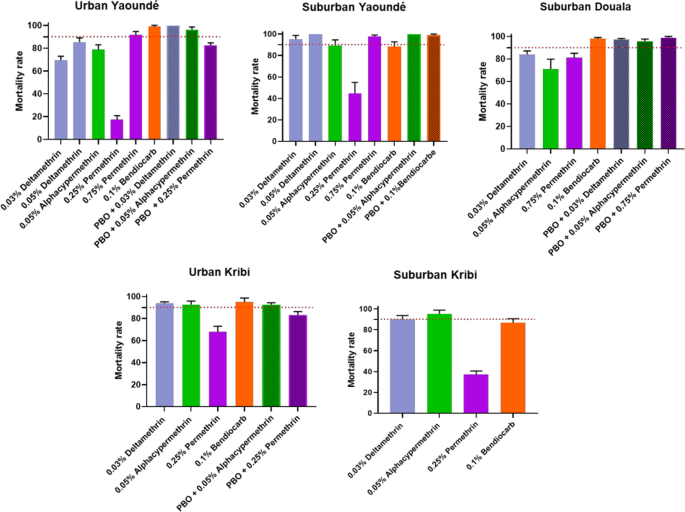
五个Ae。蚊对人口进行了测试(城市Yaoundé,郊区Yaoundé,城市Kribi,郊区Douala和郊区Kribi)。结果如图所示。4.分析表明,所使用的三种拟除虫菊酯存在耐药性或可能耐药性。使用0.25%氯菊酯检测的所有人群均表现出高耐药性,死亡率在17.35%(城市Yaoundé)至81.15%(杜阿拉郊区)之间。当氯菊酯剂量增加到0.75%时,敏感性恢复了一定程度。在城市Yaoundé, 0.25%氯菊酯的死亡率为17.35%,但当使用0.75%氯菊酯时,死亡率增加到91.59%。5个人群中有2个被发现对溴氰菊酯具有抗药性;城市Yaoundé的死亡率为69.47%,郊区Douala的死亡率为84.11%,而其他三个地区(郊区Yaoundé、城市Kribi和郊区Kribi)显示出可能的耐药性。城郊杜阿拉(71.21%)、城郊Yaoundé(78.63%)、城郊Yaoundé(89.40%)对氯氰菊酯抗性;城市克里比和郊区克里比的耐药性分别为92.70%和95.17%。据报告,对恶虫威的耐药性处于中等水平,死亡率从克里比郊区的86.75%到城市的98.95% Yaoundé不等。 Environment was not a statistically significant predictor for resistance inAe。蚊。
在城市中Ae。蚊而且Ae。蚊同侧发生(Douala, Kribi和Yaoundé)Ae。蚊有明显高于Ae。蚊.杀虫剂标准剂量的总平均死亡率分别为54.7%和80.1%Ae。蚊和Ae。蚊来自同域城市(P< 0.02,χ2= 6.61, df = 1)。
协同剂PBO测试
据报道,这两个物种在PBO预暴露后,对杀虫剂(氯菊酯、甲氯菊酯、溴氰菊酯和恶虫威)的敏感性部分或完全恢复(图。2,4).
为Ae。蚊城市人群对氯菊酯的敏感性有所恢复Yaoundé(未接触PBO的死亡率为17.35%,接触PBO后死亡率为82.54%P< 0.001)、杜阿拉郊区(无PBO死亡率为81.15%,暴露PBO后死亡率为99.1%P> 0.05)和城市Kribi(无PBO死亡率为68.08%,暴露PBO后死亡率为83.21%P> 0.1)。对甲氯菊酯的敏感性部分恢复Ae。蚊城市人群Yaoundé(未接触PBO时的死亡率为78.63%,接触PBO后的死亡率为96.36%P> 0.05)、郊区杜阿拉(无PBO死亡率为71.21%,暴露PBO后死亡率为95.94%P> 0.01),以及郊区Yaoundé人群对恶虫威的影响(未接触PBO的死亡率为88.18%,接触PBO后死亡率为98.9%P> 0.25)。据报道,城市Yaoundé对溴氰菊酯的敏感性完全恢复(无PBO的死亡率为69.47%,暴露PBO后死亡率为100%P< 0.005)和对氯氰菊酯郊区Yaoundé 89.40%的死亡率没有PBO和100%的PBO暴露后P> 0.25。
为Ae。蚊样本年代据报道,城市Yaoundé人群对氯菊酯的敏感性部分恢复(未接触PBO的死亡率为78.32%,接触PBO后的死亡率为92.18%P> 0.1)、杜阿拉郊区(无PBO死亡率为40.48%,暴露于PBO后死亡率为62.13%P< 0.01)和城市Ngaoundéré(无PBO死亡率为85.89%,暴露PBO后死亡率为93.25%P> 0.5)。对氯氰菊酯的敏感性有所恢复Ae。蚊城市人群Yaoundé(无PBO死亡率为70.71%,暴露PBO后死亡率为95.45%P> 0.01)、杜阿拉郊区(无PBO死亡率为52.27%,暴露PBO后死亡率为54.27%P> 0.75)和城市Ngaoundéré(未接触PBO的死亡率为88.52%,接触PBO后死亡率为98.80%P> 0.25),对溴氰菊酯在城市人口Yaoundé(88.20%无PBO死亡率和98.03%接触PBO后死亡率P> 0.25)、杜阿拉郊区(无PBO死亡率为62.52%,暴露PBO后死亡率为68.83%P> 0.25)和城市Ngaoundéré(无PBO死亡率为83.77%,暴露PBO后死亡率为98.86%P在Douala郊区人群中,无PBO死亡率为91.61%,接触PBO后死亡率为97.79%P> 0.5)。
基因表达
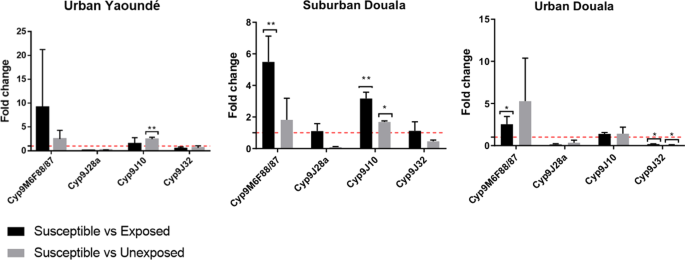
采用qPCR方法,定量检测了4个cytP450基因的表达Ae.蚊(Cyp9M6F88/87,Cyp9J28a,Cyp9J10,而且Cyp9J32).其中,有两种在田间种群中明显过表达,与一种敏感的实验室品系相比(图1)。5).Cyp9M6F88/87在城市Douala抗氯菊酯样本中过表达[(倍数变化(FC) = 2.54±0.90,P= 0.016)]和郊区Douala样本对溴氰菊酯抗性(FC = 5.49±1.64,P= 0.003);而且Cyp9J10郊区杜阿拉(FC = 3.16±0.40,P= 0.013)。
只有一个基因(Cyp6P12)在Ae.蚊人群。与实验室敏感株相比,该基因在城市Douala抗氯菊酯样品中的表达量显著增加(FC = 5.54±0.73,P= 0.001),城市Yaoundé样本对氯氰菊酯耐药(FC = 2.48±0.57,P= 0.034)。然而,在对溴氰菊酯耐药的城市杜阿拉样本中,Cyp6P12与敏感品系相比,表达无显著差异(图。6).
可拆卸的电阻(kdr)基因分型Ae。蚊
在这项研究中,有三个kdr基因型为V1016I、F1534C和V410L。结果见表3.,4而且5.
对于V1016Ikdr基因分型共检测296份样本。其中易感(1016 V/V) 227株(76.69%),杂合子抗性(1016 V/I) 59株(19.93%),纯合子抗性(1016I/I) 10株(3.38%)。等位基因V和I的等位基因频率分别为86.66%和13.34%。
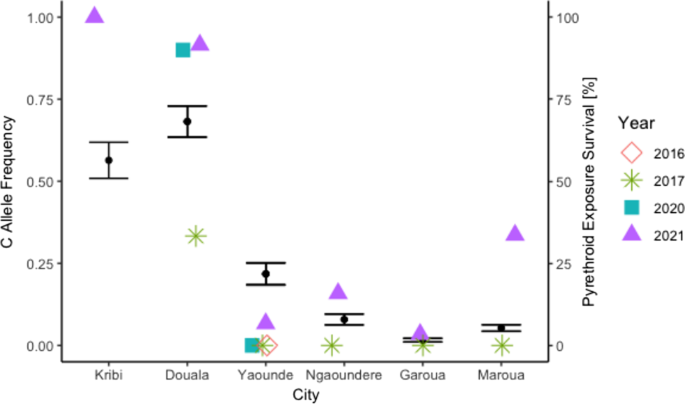
我们检测了296个样本进行F1534C基因分型。其中感感(1534F/F) 170只(57.43%),杂合子耐(1534F/C) 18只(6.08%),纯合子耐(1534C/C) 108只(36.49.05%)。等位基因频率F和C分别为60.47%和39.53%。在研究的5个城市中,C等位基因频率比2017年首次发现的水平有所上升(图1)。7).
我们对299个V410L样本进行了基因分型kdr410 V/V敏感212份(70.91%),410 V/I杂合子耐59份(19.73%),410I/I纯合子耐28份(9.36%)。等位基因V和L的等位基因频率分别为80.77%和19.23%。
讨论
本研究的目的是评价杀虫剂抗药性的概况Ae.蚊而且Ae。蚊在喀麦隆的几个地点收集,并探索潜在的机制。分析结果显示,对所有四种被测试的杀虫剂(溴氰菊酯、甲氯氰菊酯、氯菊酯和恶虫威)都具有抗药性伊蚊物种。而丧失对这些杀虫剂的敏感性伊蚊曾在喀麦隆的一些地区报告过[10,28,29和非洲以外的地区[30.,31,32,33],本研究扩大了喀麦隆杀虫剂抗性评估的空间尺度,同时比较了两个物种。这两种细菌对杀虫剂产生抗药性的原因Ae。蚊而且Ae。蚊尚不清楚杀虫剂的使用对伊蚊在非洲国家是稀缺的[10,15,30.].尽管如此,像F1534C这样具有杀虫剂抗药性的等位基因,随着时间的推移,频率持续增加,表明对更强杀虫剂抗药性的选择性压力。鉴于抗性的选择性压力来源未知,回归易感性似乎不太可能[15,并可能产生操作后果。对所检测的拟除虫菊酯的敏感性降低可能对未来的病媒控制规划构成严重威胁,因为建议将拟除虫菊酯用于成年人的控制伊蚊蚊子,特别是在疾病爆发时[34],通常用于杀虫剂处理过的蚊帐和制服。
埃及伊蚊来自喀麦隆北部的人群比来自南部的人群更容易受到拟除虫菊酯的影响。这表明,对该杀虫剂家族的耐药性尚未在全国蔓延,这些杀虫剂仍可有效控制伊蚊在喀麦隆的一些地方。之前的研究在按蚊在喀麦隆表现出同样的纬度梯度对阻力分布的影响[35].气候是一个潜在的促进机制;而杀虫剂抗性与气候的关系伊蚊在喀麦隆,太阳辐射和湿度是抗性水平的最高预测变量按蚊[35].和我们的研究一样,按蚊来自潮湿热带地区的蚊子通常比来自干燥干旱气候的蚊子具有更高的抵抗力。
拟除虫菊酯耐药性在城市环境中更为频繁,这反映了按蚊喀麦隆的蚊子[36].这可能是在城市环境中更密集地使用杀虫剂处理过的蚊帐和家用杀虫剂(例如蚊香)的结果。然而,这两个Ae。蚊而且Ae。蚊在喀麦隆主要在户外和白天进食,因此不太可能遇到驱虫蚊帐[37,38].土地使用也可以通过确定幼虫栖息地类型的可用性来影响抗性Ae。蚊在轮胎和水容器中发育的幼虫对杀虫剂的抗性水平可能不同[15].
在未接触PBO的情况下,部分或完全恢复对检测的所有杀虫剂的敏感性Ae。蚊而且Ae。蚊被观察到。其他几个非洲国家也出现了类似的结果[10,15,28,29,33],以及非洲以外的地区[16,17].这些结果表明,P450基因在对拟除虫菊酯(溴氰菊酯、甲氯氰菊酯和氯菊酯)和氨基甲酸酯(恶虫威)的抗性中发挥了重要作用。这些观察结果被基因的过表达所证实Cyp9M6F88/87而且Cyp9J10在某些Ae。蚊人口和Cyp6P12在Ae。蚊人口在喀麦隆。这些基因在代谢抗性中的作用先前已得到证实[16,17,18,19,39].
三种可能kdr本研究对涉及拟除虫菊酯抗性的突变进行了基因分型:F1534C、V1016I和V410L伊蚊蚊子(11,40,41,42].这三个kdr以前在非洲也报道过突变[15,42,43,44],但此前在喀麦隆只发现了F1534C和V1016I [9,10].这项研究首次揭示了V410L突变的存在Ae。蚊在喀麦隆。2017年,巴西首次报道了这种突变[7],而它在非洲的第一个证据是2020年在安哥拉发现的[11].V410L单独会产生较低水平的杀虫剂抗性,但当它与V1016I或F1534C同时出现时,会产生较高水平的抗性[7,11].与安哥拉的频率相比,V410L的频率是中等的,支持了这种突变的新引入假说。F1534C和V1016Ikdr基因突变很常见Ae.蚊并在全球范围内发行[4].V1016I和V410L频率中等,而F1534C频率较高,在Ae。蚊自2017年首次在喀麦隆观察到这种突变以来,该病毒在该国的人口中广泛传播。这一结果支持了先前在喀麦隆观察到的F1534C突变在该国的引入和逐渐传播[10].广义上说,检测kdr突变在非洲比过去观察到的更为频繁[45].面对对拟除虫菊酯的抗药性,这三个人kdr突变可能对病媒控制措施产生影响。
该研究的主要局限性是我们没有评估所观察到的表型抗性与大肠杆菌感染之间是否存在关联kdr突变检测。
结论
我们的研究显示,对四种杀虫剂失去敏感性:溴氰菊酯、甲氯氰菊酯、氯菊酯和恶虫威Ae。蚊而且Ae。蚊.这些杀虫剂最有可能用于疫情应对中的蚊虫控制和降低部署军事人员的疾病风险,而这项研究表明,这些缓解战略的效果有限。敏感性损失程度因城市、土地利用类型和物种而异。我们的研究结果表明,抗性涉及多种机制,这可能影响植物的策略伊蚊包括在喀麦隆首次检测到V410L突变。需要进行进一步调查,包括测试新型杀虫剂,以帮助制定有效战略,控制喀麦隆的虫媒病毒媒介。
数据和材料的可用性
在本研究过程中产生的所有相关数据都包含在手稿中。
缩写
- 背景:
-
脱氧核糖核酸
- kdr:
-
可拆卸的阻力
- RNA:
-
核糖核酸
- 恶唑:
-
胡椒基丁醚
- 聚合酶链反应:
-
聚合酶链反应
- VGSC:
-
电压门控钠离子通道
- 人:
-
世界卫生组织
参考文献
Bhatt S, Gething PW, Brady OJ, Messina JP, Farlow AW, Moyes CL等。登革热的全球分布和负担。大自然。2013;496:504-7。
Wilson AL, Courtenay O, Kelly-Hope LA, Scott TW, Takken W, Torr SJ,等。病媒控制对控制和消除病媒传播疾病的重要性。《公共科学图书馆热带气象杂志》2020;14:e0007831。
Harwood JF, Farooq M, Richardson AG, Doud CW, Putnam JL, Szumlas DE,等。探索新的热雾和超低体积技术,以改善登革热病媒的室内控制,埃及伊蚊(双翅目蚊科)。中华医学昆虫杂志2014;51:45 - 54。
Moyes CL, Vontas J, Martins AJ, Ng LC, Koou SY, Dusfour I,等。主要杀虫剂抗药性的当代现状伊蚊感染人类的虫媒病毒载体科学通报:2017;11:e0005625。
王晓燕,王晓燕,王晓燕,等。蚊虫抗药性的分子基础。《生物化学与分子生物学》2004;34:653-65。
佩里T,巴特汉姆P,达本PJ。杀虫活性和抗药性生物学。《生物化学与分子生物学》2011;41:411-22。
Haddi K, Tomé HV, Du Y, Valbon WR, Nomura Y, Martins GF,等。检测到一种新的拟除虫菊酯抗性突变(V410L)在钠通道埃及伊蚊:这是控制蚊子的一个潜在挑战。Sci众议员2017;7:46549。
Kosinski K, Lee Y, Romero-Weaver A, Chen T-Y, Collier T, Wang X,等。在电压门控钠通道基因中发现了两个新的单核苷酸多态性埃及伊蚊蚊子从佛罗里达。J Fl蚊防协会2022;69:8。
Djiappi-Tchamen B, Nana-Ndjangwo MS, Mavridis K, Talipouo A, Nchoutpouen E, Makoudjou I,等。植物抗虫基因分析埃及伊蚊而且白纹伊蚊来自喀麦隆的蚊子种群。基因。2021;12:828。
Yougang AP, Kamgang B, Bahun TAW, Tedjou AN, Nguiffo-Nguete D, Njiokou F,等。首次检测到F1534C击倒抗性突变埃及伊蚊(双翅目:库蚊科),产于喀麦隆。《贫困》2020;9:1-12。
艾尔斯CF,塞克萨斯G,博雷戈S,马奎斯C,蒙泰罗I,马奎斯CS,等。V410L敲除抗性突变发生在岛屿和大陆群体埃及伊蚊在西非和中非。《公共科学图书馆热带气象杂志》2020;14:e0008216。
Saavedra-Rodriguez K, Maloof FV, Campbell CL, Garcia-Rejon J, Lenhart A, Penilla P,等。拟除虫菊酯抗性vgsc中IS6、IIS6和IIIS6结构域突变的平行进化埃及伊蚊来自墨西哥。Sci众议员2018;8:6747。
Macoris Mde L, Andrighetti MT, Wanderley DM, Ribolla PE。杀虫剂抗药性对田间防治的影响埃及伊蚊在圣保罗州2014; 47:573-8。
WHO:昆虫学监测伊蚊寨卡病毒背景下的spp.:昆虫学家的临时指南。世界卫生组织,2016年。https://apps.who.int/iris/handle/10665/204624.2021年9月21日访问。
巴多洛A, Sombié A, Pignatelli PM, Sanon A, Yaméogo F, wanggrawa DW,等。中国的杀虫剂抗性水平和机制埃及伊蚊瓦加杜古及其周边地区的人口布基纳法索《公共科学图书馆热带卫生公报》2019;13:e0007439。
Ishak IH, Kamgang B, Ibrahim SS, Riveron JM, Irving H, Wondji CS。马来西亚登革热病媒人群对拟除虫菊酯的耐药性埃及伊蚊是由细胞色素P450基因的CYP9家族介导的。科学通报:2017;11:e0005302。
Ishak IH, Riveron JM, Ibrahim SS, Stott R, Longbottom J, Irving H,等。细胞色素P450基因CYP6P12使无kdr的马来西亚登革热病媒人群对拟除虫菊酯产生耐药性白纹伊蚊.Sci众议员2016;6:24707。
葛井S,小形O, Itokawa K, Shono T, Ng LC, Kobayashi M,等。登革热蚊媒对拟除虫菊酯的耐药性机制,埃及伊蚊:靶点不敏感、渗透和代谢。科学通报,2014;8:e2948。
史密斯LB, Tyagi R, Kasai S, Scott JG。cypp介导的氯菊酯抗性埃及伊蚊还有反监管的证据。科学通报:2018;12:e0006933。
Kamgang B, Happi JY, Boisier P, Njiokou F, Herve JP, Simard F, Paupy C.登革热和基孔肯雅病毒媒介的地理和生态分布埃及伊蚊而且白纹伊蚊喀麦隆的三个主要城镇。医学兽医昆虫学。2010;24:32 - 41。
Tedjou AN, Kamgang B, Yougang AP, Njiokou F, Wondji CS。的最新地理分布和流行情况埃及伊蚊而且白纹伊蚊(双翅目:库蚊科),喀麦隆的两种主要虫媒病毒载体。科学通报2019;13:e0007137。
爱德华兹弗兰克-威廉姆斯。埃塞俄比亚地区的蚊子。嗨。成虫和蛹。伦敦,大英博物馆(自然历史);1941.
南部非洲的蚊子:库蚊科和毒蚊科。Hartebeespoort: Ekogilde出版商;1996.
Livak KJ。的序列的组织和映射黑腹果蝇在精子发生过程中转录的X和Y染色体。遗传学。1984;107:611-34。
Saavedra-Rodriguez K, Urdaneta-Marquez L, Rajatileka S, Moulton M, Flores A, Fernandez-Salas I,等。在拉丁美洲与拟除虫菊酯抗性相关的电压门控钠通道基因突变埃及伊蚊.分子生物学杂志2007;16:785-98。
史密斯LB, Kasai S, Scott JG。拟除虫菊酯抗性的埃及伊蚊而且白纹伊蚊:人类疾病的重要蚊媒。生物化学与化学。2016;133:1-12。
Schmittgen TD, Livak KJ。用比较C - T法分析实时PCR数据。Nat Protoc。2008;3:1101。
Kamgang B, Yougang AP, Tchoupo M, Riveron JM, Wondji C.两种主要虫媒病毒媒介的时间分布和抗药性概况埃及伊蚊而且伊蚊albopictu它位于喀麦隆首都Yaoundé。Parasit向量。2017;10:469。
Yougang AP, Kamgang B, Tedjou AN, Wilson-Bahun TA, Njiokou F, Wondji CS。杀虫剂抗药性的全国概况白纹伊蚊(双翅目:库蚊科)。PLoS ONE。2020; 15: e0234572。
植物对杀虫剂的抗性及解毒酶活性白纹伊蚊阿萨姆邦索尼特普尔地区的人口。印度Int J Mosq Res. 2014; 1:35-41。
Ishak IH, Jaal Z, Ranson H, Wondji CS。登革热病媒中杀虫剂抗性和击倒抗性的对比模式埃及伊蚊而且白纹伊蚊从马来西亚。Parasit向量。2015;8:181。
Marcombe S, Fustec B, Cattel J, Chonephetsarath S, Thammavong P, Phommavanh N,等。虫媒病毒媒介中杀虫剂抗药性的分布和机制埃及伊蚊以及对病媒控制的影响。PLoS nel Trop Dis 2019;13:12。
Kamgang B, Wilson-Bahun TA, Yougang AP, Lenga A, Wondji CS。对比两种主要虫媒病毒载体对I型和II型拟除虫菊酯的抗性模式埃及伊蚊而且白纹伊蚊刚果共和国。《中非无尽贫困》2020;9:1-10。
世卫组织:农药及其应用:用于控制具有公共卫生重要性的病媒和害虫。世界卫生组织,2006年。https://apps.who.int/iris/handle/10665/69223.已于2020年9月18日访问。
汉考克PA, Lynd A, Wiebe A, Devine M, Essandoh J, Watsenga F,等。非洲蚊子疟疾病媒物种中与杀虫剂靶点耐药性有关的基因突变频率的时空趋势建模。BMC医学杂志。2022;20:1-17。
Mandeng SE, Awono-Ambene HP, Bigoga JD, Ekoko WE, Binyang J, Piameu M,等。中国疟疾媒介对溴氰菊酯抗药性的时空发展冈比亚疟蚊来自北喀麦隆的复杂地区。PLoS ONE。2019; 14: e0212024。
Egid BR, Coulibaly M, Dadzie SK, Kamgang B, McCall PJ, Sedda L,等。生态学和行为的回顾埃及伊蚊而且白纹伊蚊以及对病媒控制的影响。寄生虫病媒传播疾病。2022;2:100074。
Kamgang B, Nchoutpouen E, Simard F, Paupy c白纹伊蚊(双翅目:库蚊科)。Parasit向量。2012;兴趣无关。
罗LC,奥尼尔ST,约翰逊EJ,安德森TD。年龄、性别和拟除虫菊酯类抗药状态对埃及伊蚊存活和细胞色素P450基因表达的影响生物化学学报2019;156:96-104。
Kasai S, Ng LC, Lam-Phua SG, Tang CS, Itokawa K, Komagata O,等。首次在主要蚊媒中检测到一种假定的击倒抗性基因。日本白纹伊蚊感染杂志2011;64:217-21。
川田H, Higa Y, Futami K, Muranami Y,川岛E, Osei JH,等。发现来自非洲的电压门控钠通道的点突变埃及伊蚊群体:基因渗入的潜在系统发育原因。科学通报,2016;10:e0004780。
Sombié A, Saiki E, Yaméogo F,樱井T, Shirozu T, Fukumoto S等。F1534C和V1016I kdr的高频率突变及其与拟除虫菊酯抗性的关系埃及伊蚊从Somgande(瓦加杜古)。布基纳法索热带医学卫生,2019;47:2。
Konan LY, Oumbouke WA, Silué UG, Coulibaly IZ, Ziogba J-CT, Guessan RK,等。中国的杀虫剂抗性模式和机制埃及伊蚊(双翅目:库蚊科)阿比让(Côte)的种群显示出对拟除虫菊酯的抗性。医学昆虫杂志。2021;58:1808-1816。
Kudom AA。昆虫学监测以评估潜在的暴发伊蚊蚊媒虫媒病毒和杀虫剂抗药性现状埃及伊蚊从海岸角。加纳热带学报2020;202:105257。
维特曼D, Kamgang B, Badolo A, Moyes CL, Shearer FM, Coulibaly M,等。伊蚊蚊子和伊蚊非洲的虫媒病毒:当前和未来的威胁。国际环境科学与公共卫生,2018;15:220。
Bariami V, Jones CM, Poupardin R, Vontas J, Ranson H.基因扩增、ABC转运蛋白和细胞色素P450s:揭示登革热媒介对拟除虫菊酯抗性的分子基础。埃及伊蚊公共科学图书馆热带病学杂志2012;6:e1692。
Seixas G, Grigoraki L, Weetman D, Vicente JL, Silva AC, Pinto J,等。最近介绍的杀虫剂抗药性是由多种机制介导的埃及伊蚊来自马德拉岛(葡萄牙)。科学通报:2017;11:e0005799。
确认
在此,我们要感谢居住在不同收集点附近的居民和车库业主在现场工作中的合作。有些作者是美国政府的军人。这项工作是作为他们公务的一部分而准备的。U.S.C.§105第17篇规定,本标题下的版权保护不适用于美国政府的任何工作。《美国法典》第17章§101将美国政府工作定义为由美国政府服役人员或雇员作为其官方职责的一部分而准备的工作。本文仅代表作者个人观点,并不代表海军、国防部或美国政府的官方政策或立场。
资金
这项工作由武装部队健康监测司、全球新发感染监测处(GEIS)提供的赠款支持,2020财年资助的ProMIS ID P0076_20_EC和2021财年资助的ProMIS ID P0042_21_N3。
作者信息
作者和联系
贡献
BK, CSW, JH和MM构思和设计了实验。APY、BK、TAWB、CRK和ANT参与蚊虫采集。APY、CRK和TAWB进行生物测定。APY、CRK、MM和TAWB进行了数据分析。APY、CRK、TAWB进行分子分析。APY、MM、JFH、AMK、BK和CSW撰写了论文。所有作者阅读并批准了最终稿件。
相应的作者
道德声明
伦理批准和同意参与
在收集蚊幼虫前,须取得每户或车库业主的户主或代表的口头同意书。
同意出版
不适用。
相互竞争的利益
作者声明他们没有竞争利益。
补充信息
额外的文件1。
逻辑回归的埃及伊蚊不同城市和生境类型的杀虫剂死亡率.郊区生境、杜阿拉市和恶虫威为参照水平。
权利和权限
开放获取本文遵循创作共用署名4.0国际许可协议(Creative Commons Attribution 4.0 International License),该协议允许在任何媒体或格式中使用、分享、改编、分发和复制,只要您给予原作者和来源适当的署名,提供创作共用许可协议的链接,并说明是否有更改。本文中的图片或其他第三方材料包含在文章的创作共用许可中,除非在材料的信用额度中另有说明。如果材料不包含在文章的创作共用许可中,并且您的预期用途不被法律法规允许或超出了允许的用途,您将需要直接从版权所有者那里获得许可。欲查看此许可证的副本,请访问http://creativecommons.org/licenses/by/4.0/.创作共用公共领域奉献放弃书(http://creativecommons.org/publicdomain/zero/1.0/)适用于本文提供的数据,除非在数据的信用额度中另有说明。
关于这篇文章
引用这篇文章
蒙哥马利(M. Montgomery)、哈伍德(j.f.)、尤刚(A.P.)et al。抗虫种群的空间分布埃及伊蚊而且Ae。蚊首次检测到V410L突变Ae。蚊来自喀麦隆。感染说贫困1190(2022)。https://doi.org/10.1186/s40249-022-01013-8
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/s40249-022-01013-8
关键字
- 虫媒病毒
- 埃及伊蚊
- 白纹伊蚊
- 杀虫剂耐药性
- 击倒抗性
- 细胞色素P450单氧酶
- 喀麦隆