摘要
背景
水疱单胺转运蛋白2 (VMAT2)抑制剂可以改善多动运动,是亨廷顿舞蹈病(HD)的有效治疗选择。在四苯那嗪治疗舞蹈病的试验中进行了评估,虽然有效,但由于其药代动力学特性,可能存在耐受性问题。Deutetrabenazine是一种含有氘的新型VMAT2抑制剂,可延长活性代谢物的半衰期并最大限度地减少药物浓度波动。在First-HD试验中,deutetrabenazine对治疗舞蹈病是有效的,并且通常耐受性良好。在没有头对头试验的情况下,我们使用成熟的比较方法,对deutetrabenazine和tetrabenazine治疗hd相关性舞蹈病的耐受性进行了间接治疗比较(ITC),正如在First-HD和TETRA-HD试验中观察到的那样。
方法
来自III期,12周,平行组,临床试验的数据N= 90)和TETRA-HD (N= 84)采用两种基于锚定的方法对二苯四嗪与四苯那嗪的耐受性进行ITC:未调整的ITC进行Bucher比较,调整后的ITC进行匹配间接比较。总不良事件(ae);分析包括轻度、中度和重度ae)、严重ae、特异性ae发生率≥10%以及停药(全因和ae相关)。deutetrabenazine和tetrabenazine的这些结果的风险差异是通过从TETRA-HD中减去适用的安慰剂调整风险来估计的。进行敏感性分析以解决试验之间的差异p-值由z检验获得。
结果
与四苯那嗪相比,在调整和未调整的分析中,二苯那嗪与中度至重度不良事件和神经精神不良事件(包括躁动、静坐症、抑郁、抑郁/躁动性抑郁、嗜睡/嗜睡、失眠和帕金森病)的风险显著降低相关(p< 0.05)。在未调整和调整的分析中,二苯四嗪的剂量减少率或剂量减少/悬浮率明显较低(p< 0.001)。二苯四嗪导致数量上更轻微的不良反应,如腹泻和咳嗽;然而,这些结果没有统计学意义。
结论
这种间接治疗比较表明,对于HD舞蹈病的治疗,与四苯那嗪相比,去氘苯那嗪具有良好的耐受性。
试验注册
ClinicalTrials.govNCT01795859和NCT00219804.
背景
亨廷顿病(HD)是一种以舞蹈病和进行性运动、认知和行为症状为特征的神经退行性疾病[1,2]。美国食品和药物管理局(FDA)唯一批准的治疗舞蹈病相关HD的药物是tetrabenazine,一种囊状单胺转运蛋白2 (VMAT2)抑制剂[3.]。Tetrabenazine在TETRA-HD中进行了评估,在改善舞蹈病的同时,不良事件(AE)的情况引起了对耐受性的担忧[3.,4]。
四苯那嗪是一种新型的VMAT2抑制剂,结构上与四苯那嗪相关,但它含有氘[5,6],一种自然产生的、无毒的氢[7],这与丁苯那嗪相比具有重要的代谢优势,但不会改变其目标药理学。在该化合物中引入氘会减弱药物代谢并延长血浆半衰期,从而导致更均匀的全身暴露(即减少血浆波动)[5,6]。与丁苯那嗪相比,差异化药代动力学特性有可能改善患者的获益-风险概况。在First-HD患者中,deutetrabenazine可显著减少舞蹈病,并且在HD患者中耐受性良好[5]。大多数神经精神不良事件的发生率与安慰剂组相似或低于安慰剂组[5]。
二四苯那嗪和四苯那嗪没有直接比较;然而,由于First-HD和TETRA-HD具有非常相似的研究设计,并且是由同一个研究联盟(亨廷顿研究组)进行的,因此我们使用了成熟的比较有效性模型[8,9]来比较两种药物在调整任何假定的临床差异之前和之后的耐受性。在本分析中,使用未校正分析的Bucher方法对基线特征的交叉试验差异进行校正前后的AE差异进行评估[8],以及用于调整分析的匹配调整间接比较法。考虑到在First-HD中观察到的AE情况,我们假设deutetrabenazine的耐受性比tetrabenazine更有利。
方法
试验的可比性
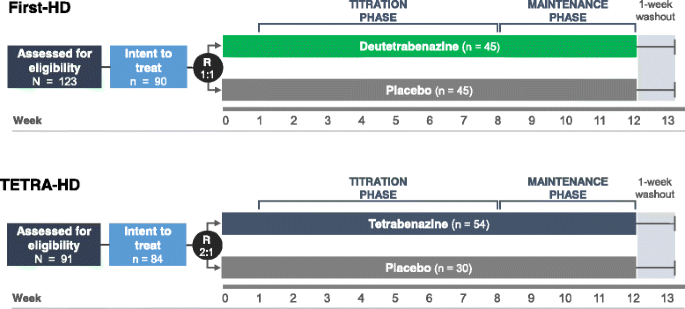
这是一项回顾性研究,使用了先前报道的临床数据。有关First-HD (NCT01795859)及TETRA-HD (NCT00219804)研究方法的详情,可参阅它们各自的初步报告[3.,5]。III期First-HD和TETRA-HD试验在试验设计、伴随用药、患者基线特征和安全性结果定义方面进行了密切比较。在这两项研究中,患者都经历了一致的滴定期、维持期(剂量保持稳定)和1周的洗脱期(图2)。1).两项研究的总治疗期均为12周[3.,5]。关键的首发HD纳入标准包括明显HD (CAG重复长度≥37),筛查和基线时,动态,总功能容量(TFC)评分≥5,TMC评分≥8 [qh]5]。在TETRA-HD中,纳入标准包括显性HD (CAG重复长度≥37),动态,TFC评分>5,总最大舞蹈病(TMC)评分≥10 [3.]。两项试验的排除标准包括致残性抑郁、吞咽困难或构音障碍[3.,5]。两项试验均允许稳定治疗(至少8周)抗抑郁药物[3.,5]。在两项试验中,既往使用丁苯那嗪和目前使用多巴胺D2受体拮抗剂和延长QT间期的药物被排除在外(艾司西酞普兰和西酞普兰允许用于First-HD)。First-HD的筛查失败率较高,这是由于(a)确保患者不服用tetrabenazine,以避免选择对tetrabenazine耐受性良好的患者(注意:First-HD方案允许接受tetrabenazine的患者,但前提是他们在筛查前至少6个月停止),(b)如果吞咽障碍问卷得分高于帕金森病的临界值,则排除患者[10(c)对所有First-HD患者进行独立的功能能力评估。
患者基线特征
确定了First-HD和TETRA-HD队列之间的基线人口统计学和临床差异。根据每个试验的可用样本量,我们对两个试验之间多达三个不同的基线特征进行了多变量调整;年龄、TFC评分、TMC评分。我们认为这些变量与调整最具临床相关性。基于对这两个队列的回顾,我们确定控制年龄、TFC评分和TMC是重要的,因为基线队列差异可能影响药物耐受性,其中年龄的增长[11], TFC的降低和TMC的增加可能预示着更晚期的疾病,发生某些ae的可能性增加。
间接的比较
四苯那嗪的数据来自已发表的临床试验结果和fda批准的处方信息[3.,12]。使用基于锚定的方法,使用来自TETRA-HD的汇总数据和First-HD的患者水平数据对ae进行间接比较。对于未调整的结果,使用Bucher方法比较两个安慰剂对照试验与不同的比较物,并计算两种治疗(即tetrabenazine和deutetrabenazine)的总风险差异[8]。Bucher方法是一种完善且被接受的分析方法,用于跨疾病状态进行间接比较[13- - - - - -16]。
采用匹配调整后的间接比较来评估用去四苯那嗪或tetrabenazine治疗的患者的AE结果,这提供了解释两组患者基线特征差异的能力。这种更复杂的ITC方法结合了倾向评分模型,用于估计治疗效果,考虑预测治疗反应的基线临床协变量。因此,对一项试验中个体患者数据的倾向得分进行加权,使总体与比较试验的总体相似[9]。在此权重调整之后,作为匹配调整间接比较方法的一部分,在调整后的人口中应用bucher类型的比较。在本分析中,对First-HD患者的基线特征进行加权,使其更接近于tetrao - hd患者。
两种方法都提供了对二苯四嗪和四苯那嗪在每个安全结局的试验内风险差异的估计。每个试验的试验内风险差异计算为同一试验中活动组的ae发生率减去安慰剂组的ae发生率。deutetrabenazine和tetrabenazine之间的总风险差异是通过从First-HD各自的试验内风险差异中减去TETRA-HD的试验内风险差异来估计的。所需伤害数(NNH)估计定义为平均每增加1例发生AE的患者需要用tetrabenazine而不是deutetrabenazine治疗的患者数量。NNH估计值计算为总风险差异的倒数。
安全的结果
≥10%的患者发生的任何AE、中度至重度AE、轻度AE、严重AE (SAEs)、停药(全因和AE相关)、剂量减少和特异性AE均被纳入分析。10%的发生率被认为具有临床意义。
敏感性分析
除了先前描述的分析之外,通过调整基线特征(年龄、TFC评分和TMC)的不同组合,进行匹配调整的间接比较,以测试结果的稳健性。此外,ae的编码依据分别为First-HD和TETRA-HD医学词典(MedDRA)和世界卫生组织(WHO)首选术语。对经fda批准的tetrabenazine处方信息中报告的ae进行了检查,并与主要TETRA-HD出版物中报告的ae进行了比较[3.,12]。每当由于两项试验之间潜在的声发射编码差异而导致定义存在歧义时,在分析中使用多个版本的First-HD声发射定义来评估潜在的偏倚。
统计分析
TETRA-HD的基线特征和ae [3.]进行总结,并与First-HD临床研究报告中已有的摘要进行比较。每个试验中各自组的基线特征(即活性组与活性组、安慰剂组与安慰剂组)对分类变量使用卡方分析,对连续变量使用t检验进行比较。P风险差异值采用z检验。所有分析均使用SAS统计软件包的9.2和9.3版本(SAS Institute, Inc.)。
结果
患者比较
虽然在每个临床试验中登记的总体人群之间存在统计学差异,但大多数变量的分布是相似的。入组的First-HD和TETRA-HD患者的平均基线TMC评分分别为12.7和14.9 [3.]。调整前,与四苯那嗪组相比,First-HD组患者的年龄、TFC评分、语言流畅性、符号数字和Stroop单词阅读、行为评估、功能检查表、独立性量表和Barnes akatisia评定量表(BARS)评分均显著高于四苯那嗪组(表1)1).此外,deutetrabenazine组First-HD患者的CAG重复长度以及帕金森病、TMS和统一帕金森病评定量表(UPDRS)的言语评分显著降低。每个试验中的安慰剂组仅在性别、TMC评分和加权前的BARS评分方面存在差异。这些差异在加权后进一步减小。
安全结果比较
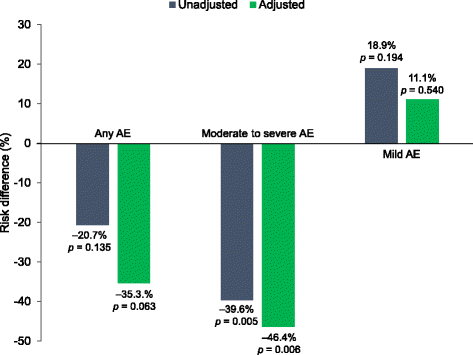
调整前后,与四苯那嗪相比,二苯那嗪的总体不良事件发生率和中度至重度不良事件发生率显著降低(p< 0.001;表格2).这导致与未调整的四苯那嗪相比,二苯那嗪发生中重度ae的风险显著降低(- 39.6%,95% CI: - 67.1, - 12.2%;p= 0.005)和调整(−46.4%,95%置信区间CI: 79.4−−13.3%;p= 0.006)分析。2、表3.).虽然没有统计学意义,但在未调整的患者中,二苯四嗪导致轻度ae的风险增加(18.9%,95% CI: - 9.6%, 47.4%;p= 0.194)和调整(11.1%,95%置信区间CI:−24.4%,46.6%;p= 0.540)分析,特别是咳嗽的发生率更高(调整前)p= 0.062,调整后p= 0.040)腹泻(调整前)p= 0.788,调整后p= 0.951)。与四苯那嗪相比,在调整安慰剂前后,二苯那嗪发生的总剂量减少和因不良事件引起的剂量减少/悬浮的频率显著降低(p所有比较均< 0.001)。
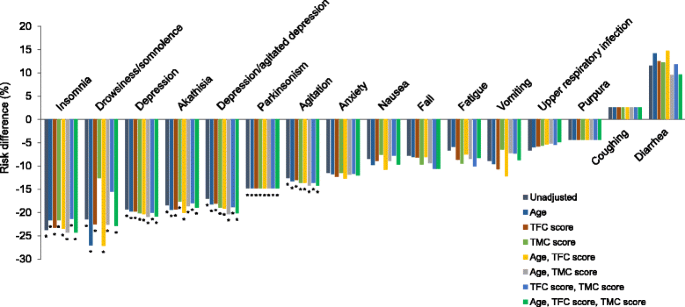
与tetrabenazine相比,Deutetrabenazine的一些个体不良事件发生率显著降低(表1)2).调整前,与四苯那嗪治疗组相比,二苯那嗪治疗组患者的躁动、静坐、焦虑、抑郁、嗜睡/嗜睡、疲劳、失眠和帕金森病的发生率显著降低(p< 0.05)。调整后,除上述不良事件外,二苯四嗪显示抑郁/激动性抑郁、跌倒和恶心的发生率显著降低(p< 0.05)。调整前,躁动风险显著降低(- 12.6%,95% CI: - 23.0, - 2.2%;p= 0.018),静坐不能(−18.5%,95%置信区间CI: 30.5−−6.5%;p= 0.003)、抑郁(−19.3%,95%置信区间CI: 32.0−−6.6%;p= 0.003),抑郁/激动性抑郁(- 17.0%,95% CI: - 30.4, - 3.7%;p= 0.013),睡意/嗜睡(−21.5%,95%置信区间CI: 39.2−−3.7%;p= 0.018)、失眠(−23.7%,95%置信区间CI: 38.7−−8.7%;p= 0.002)和帕金森症(−14.8%,95%置信区间CI: 24.3−−5.3%;p= 0.002),与四苯那嗪治疗相比(图2)。3.、表3.).调整后,与tetrabenazine相比,deutetrabenazine发生以下不良事件的风险仍然显著降低:躁动(- 14.2%,95% CI: - 24.6, - 3.8%;p= 0.007),静坐不能(−18.9%,95%置信区间CI: 32.0−−5.8%;p= 0.005)、抑郁(−20.8,95%置信区间CI: 33.8−−7.8%;p= 0.002),抑郁/激动性抑郁(- 20.2%,95% CI: - 33.9, - 6.5%;p= 0.004),睡意/嗜睡(−22.9%,95%置信区间CI: 44.9−−0.8%;p= 0.042),失眠(- 24.3%,95% CI: - 40.9, - 7.6;p= 0.004),震颤麻痹(−14.8%,95%置信区间CI: 24.3−−5.3%;p= 0.002)。其他不良事件的风险在治疗组之间没有显著差异;然而,除咳嗽和腹泻外,与四苯那嗪相比,二苯那嗪与大多数这些不良事件的数字风险较低有关。为了检验多重比较是否对统计上显著的个体AE发现有影响,我们在0.1水平下进行了Benjamini-Hochberg错误发现率控制程序。在未调整和调整分析中,结果的统计学显著性保持不变。
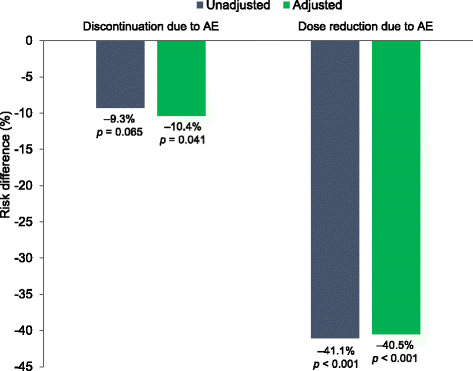
与未调整的tetrabenazine治疗的患者相比,deutetrabenazine治疗的患者剂量减少或剂量减少/暂停的风险显著降低(- 41.1%,95% CI: - 59.1, - 23.1%;p降低< 0.001,为- 41.1%,95% CI: - 60.0, - 22.3%;p< 0.001)和调整(- 40.5%,95% CI: - 62.0, - 19.0%;p剂量减少< 0.001,−41.6%,95% CI:−63.9,−19.3%;p< 0.001的剂量减少/悬浮)分析(图。4、表3.).在未经调整的分析中,与四苯那嗪相比,二苯那嗪因ae而停药的发生率在数值上更低(p= 0.144),在校正分析中,与四苯那嗪相比,二氘四苯那嗪显著降低(p= 0.030)。与调整前的四苯那嗪相比,二苯那嗪因不良反应而停药的风险有降低的趋势(- 9.3%,95% CI: - 19.1, 0.6%;p= 0.065),调整后二苯那嗪患者因ae而停药的比例显著降低(- 10.4%,95% CI: - 20.3, - 0.4%;p= 0.041)。4、表3.).
在未调整分析(NNH = 3, 95% CI: 1,8)和调整分析(NNH = 2, 95% CI: 1,7)中,对于中至重度AE,去甲苯那嗪的NNH值比丁苯那嗪具有统计学上的显著优势。也就是说,调整后,如果有2例患者使用丁苯那嗪而不是去甲苯那嗪治疗,平均会多1例患者发生中至重度AE。同样,在调整和未调整的分析中,与四苯那嗪相比,NNH在以下不良事件上显著有利于二苯那嗪:躁动(未调整的NNH = 8 [95% CI: 4,46];NNH = 7 [95% CI: 4,26]调整后);无运动障碍(NNH = 5 [95% CI: 3,15]);NNH = 5 [95% CI: 3,17]调整后);未调整的抑郁(NNH = 5 [95% CI: 3,15];NNH = 5 [95% CI: 3,13]调整后);抑郁/激动性抑郁(NNH = 6 [95% CI: 3,27],未调整;NNH = 5 [95% CI: 3,15]调整后);嗜睡/嗜睡(NNH = 5 [95% CI: 3,27]); NNH = 4 [95% CI: 2, 119] adjusted); insomnia (NNH = 4 [95% CI: 3, 12] unadjusted; NNH = 4 [95% CI: 2, 13] adjusted); and parkinsonism (NNH = 7 [95% CI: 4, 19] for both). No other AEs analyzed were statistically significant.
敏感性分析
在匹配调整的间接比较中,基线特征的不同组合对调整结果没有显著变化(图2)。3.).基于FDA批准的丁苯那嗪处方信息的结果与基于TETRA-HD出版物的结果相似[3.,12]。由于不良反应引起的抑郁和剂量减少的结果对每个试验使用的不同定义不敏感(表2)3.).
讨论
该比较分析的结果强调,与tetrabenazine相比,在未调整和调整的数据集中,接受deutetrabenazine治疗的患者发生中度至重度ae的风险显著降低,并且由于ae而导致的剂量减少。在调整后的数据集中,停药率也显著降低。这些结果证实了二氘苯那嗪的获益-风险谱的预期改善,可能是由于氘取代和代谢减弱导致的不同药代动力学谱。这一点尤其重要,因为对HD患者使用tetrabenazine的长期评估表明,tetrabenazine耐受性(而不是疗效平台期)往往是剂量限制[17]。
欧洲亨廷顿舞蹈病网络(EHDN) REGISTRY研究报告,接受丁苯那嗪治疗的亨廷顿舞蹈病患者<10% [18]。舞蹈病的临床管理并不统一,HD患者常见的精神合并症(如妄想、行为爆发和精神病)往往需要使用抗精神病药,这也可以改善舞蹈病样的运动。当然,抗精神病药也有明显的副作用,如帕金森病恶化、代谢紊乱(以及其他副作用)和耐受性差,这些都限制了它们的使用。然而,考虑到我们的ITC研究结果,如果在更大的HD人群中也能得到deutetrabenazine耐受性的改善,这可能会增加管理舞蹈病和滴定到更高剂量的选择,从而以更少的剂量限制性不良反应(AEs)最大限度地控制舞蹈病。19]。
我们注意到,与tetrabenazine相比,deutetrabenazine发生几种神经精神不良事件的风险显著降低,包括失眠、嗜睡/嗜睡、抑郁、静坐症、抑郁/躁动性抑郁、帕金森病和躁动。焦虑和疲劳的风险差异也有利于二氘苯那嗪,尽管这些没有达到显著性。所有7个ae,躁动、静坐症、抑郁、抑郁/躁动性抑郁、嗜睡/嗜睡、失眠和帕金森病,在应用本杰明-霍赫伯格矫正后,二苯那嗪治疗仍显著降低。这进一步突出了这些结果的稳健性。在HD中,疾病严重程度通常与精神合并症的进展有关,这可能是继发于疾病过程的[20.]。虽然tetrabenazine是fda批准的唯一一种治疗舞蹈病的药物,但人们担心它会加重神经精神合并症(尤其是抑郁症)[21],在HD患者中经常遇到;然而,治疗过的抑郁症并不是使用它的禁忌症[21,22]。大约40%的HD患者报告有明显的抑郁症状,如低自尊、悲伤、焦虑和自杀意念[23]。最新的美国神经病学学会指南将抑郁症和帕金森症列为与丁苯那嗪相关的最令人担忧的不良反应,并建议对所有患者进行密切监测[22];抑郁症ae已被证明发生在患有或不患有抑郁症的患者中[21]。与tetrabenazine相比,deutetrabenazine发生神经精神不良事件(包括抑郁症和帕金森症)的风险显著降低,这表明deutetrabenazine为患者提供了一种替代治疗选择,可能不太可能诱发或加重神经精神症状。deutetrabenazine发生不良反应的风险较低,可能是由于氢在特定部位被氘取代,从而减弱了代谢,导致更稳定的药代动力学特征。
应该考虑到这种分析的潜在局限性。调整前,在First-HD中,deutetrabenazine组患者的TFC评分较高,CAG重复长度和TMS评分较低,这表明在TETRA-HD中,deutetrabenazine组患者的疾病进展程度低于tetrabenazine组,并且可能具有不同的病程。我们怀疑First-HD组CAG重复长度较低主要是由于招募了tetrabenazine-naïve患者,而不太可能是由于研究中严格的吞咽和功能能力评估标准。该分析调整了First-HD和TETRA-HD患者组之间的重要临床差异。然而,样本量排除了所有临床和人口统计学变量被纳入模型。因此,虽然我们能够调整关键的临床差异(TFC、年龄和TMC),但由于样本量和模型简约性的考虑,我们无法调整一些基线特征,如CAG重复长度和TMS评分。用于选择将哪些变量纳入模型的标准包括与其他变量的共线性,以实现研究组之间差异的稳健调整。与任何间接比较一样,匹配调整间接比较方法不能调整未观察到或未在某一试验中报告的患者特征差异。虽然声发射的定义通常是类似的,但只有当TETRA-HD出版物报道了定义时,它们才能直接进行比较。此外,试验中的样本量一次只允许调整至多三个种群特征; however, the results remained largely unchanged regardless of characteristics included for adjustment.
结论
在调整和未调整的比较中,与tetrabenazine相比,deutetrabenazine显示出明显较低的总体和个体安全性结果率。这对于HD患者尤其重要,他们可能有很高的疾病负担和几种神经精神合并症。First-HD和TETRA-HD具有相似的纳入/排除标准、方案、患者群体、研究终点和干预措施,因此需要有限的调整来匹配基线数据。此外,临床站点在经验和培训方面相似。因此,即使在修改ae的定义、数据来源(主要出版物与fda批准的处方信息)和调整不同基线特征后,敏感性分析的结果也是一致的。这些结果强化了First-HD研究中观察到的良好安全性,这可能归因于氘取代导致的氘四苯那嗪的不同药代动力学特征。综上所述,这些数据表明,deutetrabenazine可能是HD相关舞蹈病患者耐受良好的治疗选择,并且可能允许滴定到最佳治疗剂量,减少因不良反应(AEs)导致的治疗中断。这种优化疗法的潜在好处是可以实现更大的疗效,即舞蹈病的控制,这可能反过来导致功能的改善[5]。需要进一步的临床试验来证实去乌特苯那嗪的长期临床疗效和患者对治疗的坚持。此外,头对头试验将为两种药物的耐受性比较提供最好的证据。
缩写
- AE:
-
不良事件
- 酒吧:
-
巴恩斯无运动障碍评定量表
- 置信区间:
-
置信区间
- EHDN:
-
欧洲亨廷顿舞蹈症网络
- 食品药品监督管理局:
-
美国食品和药物管理局
- 高清:
-
亨廷顿病
- MedDRA:
-
监管活动医学词典
- NNH:
-
需要伤害的人数
- SAE:
-
严重不良事件
- 交通:
-
总功能容量
- 台湾记忆体公司:
-
总最大舞蹈量
- 经颅磁刺激:
-
运动总分
- UHDRS:
-
统一亨廷顿氏病评定量表
- UPDRS:
-
统一帕金森病评定量表
- VMAT2:
-
水疱单胺转运蛋白2
- 人:
-
世界卫生组织
参考文献
Ross CA, Aylward EH, Wild EJ,等。亨廷顿病:自然史、生物标志物和治疗前景。中华神经科杂志,2014;10:20 04 - 16。
沃克FO。亨廷顿氏舞蹈症。中华神经医学杂志,2007;27:143-50。
亨廷顿学习小组。丁苯那嗪抗舞蹈病治疗亨廷顿病:一项随机对照试验。神经学。2006;66:366 - 72。
Jankovic J, Roos RAC。与亨廷顿舞蹈病相关的舞蹈病:治疗还是不治疗?影视学报,2014;29:14 - 8。
亨廷顿研究组,Frank S, Testa CM,等。二氘苯那嗪对亨廷顿病患者舞蹈病的影响:一项随机临床试验。《美国医学协会杂志》上。2016; 316:40-50。
李建军,李建军,李建军,等。四苯那嗪的安全性及药代动力学研究。神经学。2013;80:P07。210.
邵丽丽,何伟。同位素动力学效应在寻找氘化药物中的应用。医药新闻展望,2010;23:398-404。
Bucher HC, Guyatt GH, Griffith LE, Walter SD。随机对照试验荟萃分析中直接和间接治疗比较的结果。中华流行病学杂志。1997;22(3):391 - 391。
谢军,刘建军,刘建军,等。采用匹配调整间接比较的比较效果研究:应用胍法辛缓释或托莫西汀治疗儿童注意缺陷/多动障碍和共病对立违抗性障碍药物流行病学杂志,2012;21(2):130-7。
张志强,张志强。吞咽障碍量表的研究进展。喉镜。2011;121(7):1383 - 7。
Kinirons MT, O 'Mahony MS.药物代谢与衰老。中华临床医学杂志,2004;17(5):544 - 544。
XENAZINE处方信息。Lundbeck, Inc. 2015。p.1-23。
库切拉特M,斯托曼斯I,罗兰德JF。不含防腐剂的拉坦前列素(T2345)治疗开角型青光眼和高眼压的相对疗效和安全性:一项随机临床试验的调整间接比较荟萃分析青光眼杂志,2014;23:69 - 75。
Fenix-Caballero S, alegrei -del Rey EJ, Castano-Lara R, Puigventos-Latorre F, Borrero-Rubio JM, Lopez-Vallejo JF。阿达木单抗、依那西普、英夫利昔单抗和戈利姆单抗治疗银屑病关节炎的疗效和安全性的直接和间接比较。中华临床医学杂志,2013;38(4):391 - 391。
马立民,马立民,马立民,马立民。中重度牛皮癣的生物治疗:间接比较。中华临床医学杂志,2013;38(4):391 - 391。
帕克索、罗匹尼罗和雷沙吉兰在早期帕金森病试验中的不良事件和退出率的间接比较。中华神经科学杂志。2012;32(2):344 - 344。
沈V, Clarence-Smith K, Hunter C, Jankovic J. Tetrabenazine长期开放治疗舞蹈病合并亨廷顿舞蹈病的安全性和有效性及伴随药物的使用。2 .中国地震学杂志。2013;
王晓明,王晓明,王晓明,等。观察亨廷顿舞蹈病:欧洲亨廷顿舞蹈病网络注册。科学进展,2010;2:1184。
减少亨廷顿病舞蹈病的替代方案,一项长期试验(ARC-HD):切换队列第8周的最新结果[摘要]。运动失调,2016;31:(2)。
Epping EA, Kim JI, crawford D,等。前驱亨廷顿舞蹈病的纵向精神症状:十年数据中华医学会精神病学杂志。2016;33(1):184 - 92。
Kenney C, Hunter C, Mejia N, Jankovic J.是否有抑郁症病史是丁苯那嗪治疗的禁忌症?临床神经药物。2006;29:259-64。
Armstrong MJ, Miyasaki JM,美国神经学会循证指南:亨廷顿病舞蹈病的药物治疗:美国神经学会指南制定小组委员会报告。神经学。2012;79:597 - 603。
Paulsen JS, Nehl C, Hoth KF,等。抑郁症和亨廷顿舞蹈症的不同阶段。中华神经病学杂志,2005;17:496-502。
致谢
我们感谢参与两项试验的患者和现场工作人员,以及Arianna Grove博士(由Teva Pharmaceutical Industries资助的变色龙国际通信公司)在编写本报告时提供的编辑协助。
我们也要感谢Ravi Iyer,博士,MBA,梯瓦制药工业公司的员工,他对研究概念和分析的贡献。
统计分析由:美国马萨诸塞州波士顿分析集团公司的Rajeev Ayyagari进行。
资金
这项研究是由以色列的Teva制药工业公司资助的。
数据和材料的可用性
本研究过程中产生或分析的所有相关数据都包含在这篇发表的文章中。
作者的贡献
DOC:稿件准备,重要内容相关的方向和反馈在稿件开发过程中所有相关材料。BC:在整个稿件开发过程中,对所有相关材料进行重要的内容相关指导和反馈。LMD:在整个稿件开发过程中对所有相关材料的重要内容相关方向和反馈。EW:在整个手稿开发过程中,对所有相关材料的重要内容相关方向和反馈。RA:在稿件开发过程中对所有相关材料的重要内容相关方向和反馈。SG:在整个手稿开发过程中,对所有相关材料进行重要的内容相关指导和反馈。DS:在整个手稿开发过程中对所有相关材料的重要内容相关方向和反馈。所有作者都阅读并批准了最终的手稿。
相互竞争的利益
DOC:资助支持:NIH/NINDS, Michael J Fox基金会,美国亨廷顿病协会,Vaccinex, AbbVie, Auspex Pharmaceuticals。咨询费用:梯瓦神经科学,灵北,阿卡迪亚,艾伯维。BC:梯瓦制药公司员工。LMD:梯瓦制药公司的前雇员。EW:分析小组的员工,该小组从梯瓦制药工业公司获得了进行这项研究的咨询费。RA: Analysis Group的员工,该公司从梯瓦制药工业公司获得了本项研究的咨询费。SG:梯瓦制药公司员工。DS:梯瓦制药公司员工。
发表同意书
不适用。
伦理批准并同意参与
不适用。
作者信息
作者及单位
相应的作者
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议(http://creativecommons.org/licenses/by/4.0/),它允许在任何媒体上不受限制地使用、分发和复制,前提是您要适当地注明原作者和来源,提供到知识共享许可协议的链接,并注明是否进行了修改。创作共用公共领域免责声明(http://creativecommons.org/publicdomain/zero/1.0/)适用于本文中提供的数据,除非另有说明。
关于本文
引用本文
克拉森,d.o.,卡罗尔,b.s.,德波尔,L.M.et al。四苯那嗪与四苯那嗪治疗亨廷顿病的间接耐受性比较。[J]克林·莫夫病4, 3(2017)。https://doi.org/10.1186/s40734-017-0051-5
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/s40734-017-0051-5
关键字
- Deutetrabenazine
- 四苯喹嗪
- 亨廷顿病
- 间接治疗比较
- 风险的区别
- 亨廷顿氏舞蹈病
- 舞蹈病
- 安全
- 耐受性
- 运动障碍