摘要
在2005年至2010年期间,美国6至21岁的儿童在自闭症残疾类别下接受特殊教育服务的人数增加了91%,而接受特殊教育服务的儿童总数下降了5%。与普遍发育障碍有关的残疾类别对特殊教育服务的需求继续上升。当基因表达被饮食转录因子改变时,如锌不足或缺乏,或暴露于环境中的有毒物质,如汞或有机磷农药,神经发育会受到不利影响。不同群体之间和群体内部的基因表达模式在地理上是不同的。在北美,对氧磷酶-1的基因变异与自闭症相关,但在意大利没有,表明基因-环境相互作用的区域特异性。在目前的综述中,我们利用一种新的宏观表观遗传方法来比较这两个地理群体之间的饮食和有毒物质接触的变化,以确定导致美国自闭症流行的可能因素。
以自闭症为个案的宏观表观遗传学导论
自闭症是一种发育障碍,由美国精神病学协会(APA)在《精神障碍诊断与统计手册》(DSM)中定义。这种情况被认为是一种广泛性发育障碍(PDD),出现在生命的头3年,影响大脑发育,影响社交和沟通技能。自闭症是由一系列共同的行为定义的,包括但不限于观察到的非语言和口头交流的缺陷,缺乏社会互惠,以及未能发展和维持适当的同伴关系[1].最近的估计表明,31%的自闭症谱系障碍(ASD)儿童也符合注意缺陷/多动障碍(ADHD)的诊断标准,另外24%的ASD儿童表现出ADHD的阈值以下临床症状[2].受这种使人衰弱的疾病影响的儿童人数仍然未知。作为这篇综述的一部分,我们将分析当前的美国。教育部特殊教育的数据来估计从2005年到2010年自闭症患病率的增长。
自闭症的原因也仍然是未知的。D 'Amelioet al。在美国人群的亚群中发现对氧磷酶-1 (PON1)基因变异与自闭症相关,但在意大利没有发现[3.].他们将这种基因变异归因于美国家庭使用有机磷农药(OP)的次数比意大利多。我们认为一个更合理的解释可能在于美国的食品供应。作为调查的一部分,我们还审查和分析了美国农业部(USDA)的食品供应电子表格,以确定哪些食品是美国人最常食用的,以及根据美国农药数据项目报告的哪些食品最常含有OP农药残留。
在这项调查中,我们对自我们发表第一个汞毒性模型以来发表的所有关于自闭症的研究进行了文献综述[4],这解释了汞暴露、营养缺乏和代谢紊乱是如何导致自闭症的。我们评估了所有相关研究,并扩展了我们的汞毒性模型。然后,我们使用扩展模型来比较美国和意大利的人群,以确定哪些因素(如果有的话)可以解释PON1基因变异和两国自闭症患病率的差异。我们提出术语“宏观表观遗传学”来描述研究食物供应及其对身体代谢和基因功能的影响的过程,以及对人群环境暴露的已知情况。
在研究基因和人体之外影响基因表达的更大因素时,我们可以更好地解释一些基因-环境相互作用导致的疾病,如自闭症。许多精神病学专业人士一致认为,基因-环境相互作用研究对于理解自闭症和其他泛自闭症障碍(ASD)类别中普遍存在的发育障碍的病因至关重要。5].科学界如何得出这种理解是解决自闭症患病率上升问题的关键。通过展示宏观表观遗传学方法来确定可能导致美国自闭症流行的因素,我们希望更多的科学家跟随我们的跨学科领导,并将宏观表观遗传学作为一种研究策略。
当前美国自闭症患病率和特殊教育趋势
在20世纪80年代之前,美国自闭症患病率约为0.05% [6].2006年,美国疾病控制与预防中心(CDC)报告称,估计自闭症患病率在所有儿童中已上升至0.6 - 0.7%之间[7].许多科学家和家长认为,美国的自闭症患病率远远高于CDC的统计数据。美国政府科学家和合作者在2007年发表的一篇文章指出,目前有1.1%的3至17岁的美国儿童被诊断患有自闭症谱系障碍[8].
特殊教育数据过去曾被用来估计美国的自闭症流行趋势。[9].在1975年至1995年的出生队列中,1987年至1992年出生的年度队列中,自闭症的增幅最大[9].从1992年到1995年,自闭症患病率逐年增加,但增幅并不明显[9].我们对当前特殊教育数据的回顾表明,从2005年到2010年,在自闭症类别下接受特殊教育服务的6至21岁儿童的数量增加了91%。从2005年到2010年,发育迟缓类儿童的人数增加了38%,在其他健康受损类(OHI)下接受特殊教育和相关服务的儿童人数增加了26%。被诊断为多动症的儿童被纳入了OHI类别。考虑到从2005年到2010年接受特殊教育服务的儿童总数下降了5%,这些增长令人吃惊。表格1提供从数据问责制中心获得并在此检讨期间分析的数据的图形表示形式[10].
由美国疾病控制与预防中心进行的1997年至2008年全国健康访谈调查的数据证实了这些发现,即与自闭症诊断标准相关或共享自闭症诊断标准的自闭症和发育障碍患病率增加[11].无论数据来源如何,与其他国家(如意大利)相比,美国的自闭症患病率明显在上升,在意大利,自闭症患病率估计仅为0.1% [12].由于自闭症患病率因国家、人口和地理位置而异,基因-环境相互作用与饮食因素起作用的可能性越来越明显。环境因素对基因表达的影响主要是通过表观遗传机制介导的,包括脱氧核糖核酸(DNA)甲基化以及组蛋白的甲基化、乙酰化、泛素化和磷酸化。表观遗传调控在神经发育过程中尤为重要[13].
解释自闭症基因-环境相互作用的宏观表观遗传模型
在公共卫生领域,流行病学通过研究基因型、环境暴露和疾病结果如何在人群中发生,可以说是引领了研究基因-环境相互作用的道路[5].然而,这种流行病学方法往往导致相互矛盾的科学结论,因为它的从业者没有考虑到饮食因素之间的相互作用和调节人类代谢和大脑功能的分子和遗传机制[14].尽管存在“营养基因组学”领域的文献,专门研究食物和食物成分对基因表达的影响,但情况一直如此。在确定疾病的公共卫生和社会和/或环境决定因素时,没有营养基因组学研究流行病学似乎是无效的,反之亦然。换句话说,一种更宏观的方法来揭示导致这类神经疾病的环境和遗传因素的全部范围,应该把营养因素作为环境的一个组成部分。通过结合从营养基因组学和流行病学研究中获得的信息,一个宏观表观遗传模型已经被开发出来,来解释一些导致自闭症和注意力缺陷多动障碍的饮食因素与基因-环境的相互作用[4].
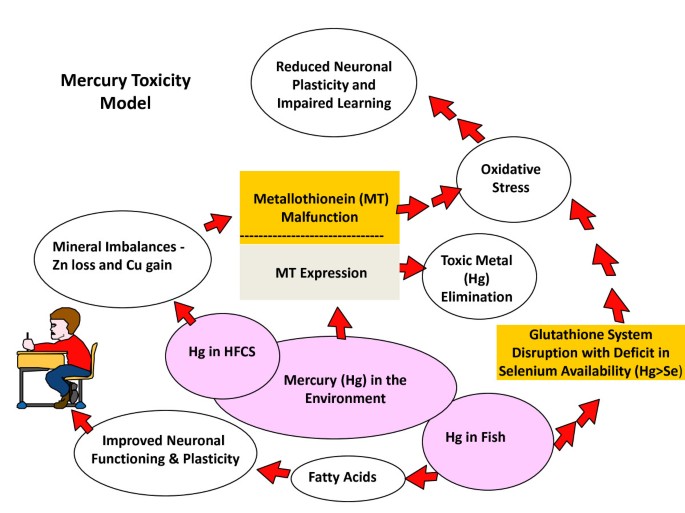
数字1显示了汞毒性模型,该模型从宏观表观遗传学上解释了当基因表达被饮食转录因子(如锌不足或缺乏)或暴露于环境中发现的有毒物质(如重金属汞和铜)所改变时,人类神经发育会受到怎样的不利影响[4].重金属的清除需要金属硫蛋白(MT)基因的表达,该基因合成锌依赖的金属结合蛋白金属硫蛋白[15].随着膳食中锌(Zn)的损失和铜(Cu)的增加,食用高果糖玉米糖浆[16],消除重金属所需的代谢过程在自闭症儿童中受损[4].在高果糖玉米糖浆样品中发现了汞,在某些食用色素中,只要浓度不超过百万分之一,汞的含量是允许的。17,18].汞(Hg)和特定的其他重金属,包括铅(Pb)、铜(Cu)、镉(Cd)、银(Ag)和铋(Bi),能够取代MT蛋白质分子中的锌原子[15].锌的这种“致病”位移会损害MT分子及其吸收重金属并将其带出体外的能力。如果饮食缺乏锌或锌的吸收受损,那么身体可能无法产生足够的MT蛋白来携带和排泄重金属负荷[19,20.].自闭症儿童可能缺锌,常常有MT功能障碍[21- - - - - -23].由于它们排泄有毒重金属的能力减弱,它们的病情严重程度与其有毒金属负担有关[24].这一宏观表观遗传模型提出,在美国,自闭症患病率与高果糖玉米糖浆的摄入和汞的总体暴露有关。4].然而,与食用高果糖玉米糖浆相关的其他饮食因素可能进一步促进美国自闭症的发展
与食用高果糖玉米糖浆有关的其他饮食因素
2009年美国HFCS的人均消费量为每年35.7磅[25].高果糖玉米糖浆年消费量的高峰年份与加州自闭症谱系障碍的增长高峰年份相吻合,加州是唯一报告自闭症谱系障碍病例数量的州,可追溯到20世纪80年代中期[4].汞毒性模型显示,高果糖玉米糖浆的特征最有可能导致自闭症,包括食用高果糖玉米糖浆和加工食品中发现的某些食物色素所产生的锌消耗效应,以及制造过程中有时在高果糖玉米糖浆中发现的低汞浓度可能导致的额外汞接触[4,17].这个模型可以扩展到包括与食用高果糖玉米糖浆相关的其他副作用,这些副作用可能通过PON1基因调节和铅中毒导致自闭症的发展。
美国农业部(USDA)的科学家警告说,当膳食中镁(Mg)的摄入量较低时,食用HFCS会导致钙(Ca)和磷(P)的平衡下降,对人体的宏观矿物质稳态产生不利影响[26].这是一个不幸的发现,因为有证据表明美国人膳食中镁的摄入量很低,他们中的大多数人食用高果糖饮食。2003年,疾病控制与预防中心的科学家报告称,大量美国成年人没有在饮食中摄入足够的镁元素[27].自闭症儿童的血浆镁浓度明显低于正常受试者[28].亚当斯et al。发现与对照组相比,自闭症儿童的红细胞(RBC) Ca、血清和白细胞(WBC) Mg显著减少,RBC铜显著增加[29].最近,美国农业部的科学家报告说,2005年至2006年全国健康和营养检查调查(NHANES)的数据表明,总体而言,近一半的1岁及以上的人膳食中镁摄入量不足[30.].由于大量的美国人在食用高果糖玉米糖浆的同时摄入了不足量的膳食镁,可以预测,大量的美国人可能也在经历钙(Ca)缺乏。
膳食中钙、镁和锌的摄入不足,或因食用高果糖玉米糖浆而损失或置换这些矿物质,可能进一步增强铅(Pb)对儿童认知和行为发展的毒性作用[31].作为NHANES II的一部分,在3000名美国儿童中发现了膳食钙摄入量与血铅浓度之间显著独立的负相关关系[32].血铅水平升高是铅中毒的标志,在一些被诊断为自闭症的儿童中发现了铅中毒,并与多动症的发展有关[33,34].钙或镁的摄入不足,加上高果糖玉米糖浆缺锌的饮食,可能会增加铅中毒导致自闭症和多动症的风险。
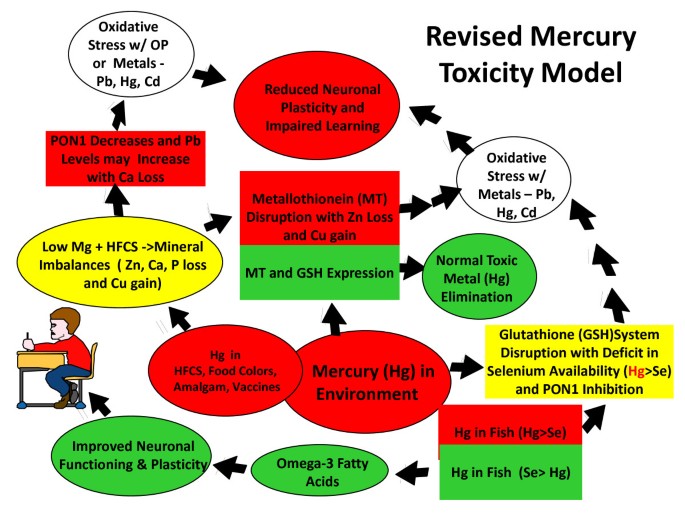
钙或镁摄入不足可能通过影响人血清对氧磷酶-1 (PON1)基因表达进一步促进这些发育障碍。PON1是一种钙依赖酶,负责OP农药的解毒以及水解同型半胱氨酸的硫内酯形式[35,36].PON1在肝脏中合成,并在血液中分泌,与高密度脂蛋白(HDL)结合。PON1的有效性和催化活性在许多ASD儿童中受损,使他们更容易受到有机磷农药残留的毒性影响,有机磷农药残留最常在谷物中发现[37,38].数字2显示了扩展的汞毒性模型,其中包括当膳食中Mg摄入量较低和食用高果糖玉米糖浆导致的铅毒性和PON1活性的变化更多的钙流失(Ca)和磷(P),从而对大矿物稳态产生不利影响。
PON1活性和有机磷暴露在美国
可以断言,在高果糖玉米糖浆的高强度饮食和Mg摄入不足的情况下,PON1活性可能降低,并导致基因易感个体钙损失。尽管还没有人类数据支持这一论断,但在模拟人类代谢综合征时,给大鼠喂食高果糖玉米糖浆饮食时,PON1活性下降[39].PON1活性在人类中得到了广泛的研究,已知有许多因素可以调节或改变PON1的表达,包括但不限于汞暴露、性别和年龄[40,41].年龄发挥着最重要的作用,因为PON1活性在人类出生前非常低,在生命的最初几年逐渐增加[41].在一项研究中,加州大学伯克利分校的科学家发现,许多儿童体内的PON1水平可能在数年内都低于他们母亲的水平,尤其是那些基因型与PON1活性降低有关的儿童[42].科学家们得出结论,这些儿童可能在整个童年时期更容易受到有机磷农药的影响,也更容易患上与氧化应激相关的疾病,如自闭症。42].在另一项研究中,加州大学伯克利分校的科学家发现,当母亲在怀孕期间的对氧磷酶水平较高时,两岁大的儿童不太可能出现PDD症状[43].PON1基因的正常功能和充分表达对产前发育和儿童健康都至关重要,因为在美国,接触有机磷农药是一种常见现象
美国疾病控制与预防中心通过国家生物监测计划(NBP)追踪有机磷农药或其代谢物的暴露情况。报告了总体人口和子群体的暴露数据。虽然大多数美国群体都接触有机磷农药,但6至11岁的儿童接触有机磷农药的比例明显高于成人,因此有机磷农药神经毒性的风险最大[44].哈佛大学的研究人员最近报告称,在儿童经常食用的一些食物中发现有机磷农药残留[45].研究人员担心,儿童有时会接触到单一食品中的多种农药残留。OP农药接触主要发生在食用含有农药残留的食物。
众所周知,接触农药会损害儿童的神经发育,但最近的研究发现,怀孕期间接触农药也会导致儿童智力发育迟缓[46].2008年的一项流行病学研究综述发现,产前和儿童期暴露于OPs会损害神经行为发育[47].怀孕期间尿二烷基磷酸酯(DAP)浓度较高与7岁时儿童认知能力得分较低显著相关。母亲体内DAP浓度最高的五分位数的儿童智商得分比最低的五分位数的儿童低7分[48].脐带血中可测到的有机磷毒死蜱含量最高的一组新生儿,其出生体重比接触最低的一组平均少150克[49].产前接触农药显示出与发育延迟1.5至2年一致的缺陷[49].
饮食是儿童OP接触的主要来源。根据1996年的《食品质量保护法》,美国农业部长受命收集婴儿和儿童经常消费的商品的农药残留数据。美国农业部农药数据计划(PDP)提供符合本法律的残留数据[50].我们回顾了2004年至2008年的PDP数据,确定了最常被发现含有有机磷农药残留的食品。此外,我们从美国农业部获得了人均可用性数据,以确定美国人平均消费的每种食品的数量[25].我们的研究结果表明,小麦和玉米是最可能导致美国儿童接触OP的商品。人均小麦消费量估计为每年约95磅,而人均玉米消费量估计为每年约23磅。玉米的主要用途是生产玉米甜味剂,如高果糖玉米糖浆;但是,PDP并没有收集该商品的农药残留数据。表格2提供此数据审查结果的完整分类。
从表2很明显,消费者在消费同一种商品时,面临着接触多种有机磷农药残留的风险。累积接触将继续发生在美国,那里的农业普遍使用有机磷农药。尽管有机磷农药的使用在其他国家同样普遍,但在不同人群之间存在着遗传变异,这决定了对有机磷农药接触的易感性程度。PON1基因变异在美国人群的亚群中与自闭症相关,但在意大利没有,这可以归因于意大利很少食用高果糖玉米糖浆这一事实,因此减少了PON1调制的条件。
高果糖玉米糖浆的摄入和PON1在美国自闭症中的调节作用
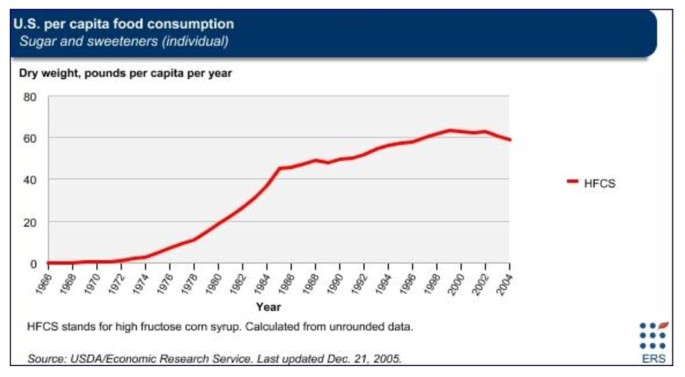
在欧盟27个成员国中,意大利是最初的参与者之一,HFCS被称为“异葡萄糖”,目前意大利人很少食用。另一方面,美国人平均每年摄入35.7磅汞,这可能会增加他们的总体汞接触[17,25].数字3.显示了从20世纪70年代初开始,美国人每年食用高果糖玉米糖浆的人均食品消费量(以磅计),并在整个80年代不断增加,在1999年至2002年期间达到峰值。在我们之前发表的文章中,我们报道了美国高果糖玉米糖浆年消费量的高峰期发生在加州自闭症年增长率达到峰值的同一时期[4].
自1980年以来,美国人每年的HFCS人均消费量超过20磅,而意大利人的HFCS人均消费量可以忽略不计。如前所述,汞(Hg)和果糖都可能调节PON1活性[39- - - - - -41].在美国,过度接触果糖可能主要是通过食用含HFCS的食物,而汞接触也可能通过多种方式发生。对美国和意大利常见汞接触来源的比较可能为PON1基因变异与美国而非意大利的自闭症相关提供进一步的解释。
除HFCS外,无机和单质汞接触的主要来源可能来自食用色素和用汞细胞氯或氯碱产品制成的防腐剂、食用海鲜、牙科汞合金中的汞、疫苗中的硫柳汞,以及根据地理位置的不同吸入汞污染的空气[4,51- - - - - -54].住在燃煤发电厂附近的儿童呼吸的空气中汞含量往往更高,自闭症发病率也更高[55].因为美国和意大利都还没有对燃煤发电厂的汞排放进行监管,这种特殊的汞接触来源不太可能解释这两个国家自闭症患病率的总体差异。在食用海产品、在疫苗中使用汞牙科汞合金、硫柳汞或含汞食品色素和防腐剂方面,意大利与美国之间也没有明显的差别。[56- - - - - -58].我们的模型中唯一剩下的变量是美国人对高果糖玉米糖浆的过度消费,这导致了更多的无机汞和果糖的慢性暴露[4].
无机汞可能与PON1上的半胱氨酸残基相互作用,阻止PON1在肝脏中的激活,并损害身体抵御OP农药和自闭症相关氧化应激源的能力[41].如前所述,PON1负责同型半胱氨酸硫内酯的水解,血浆PON1活性与同型半胱氨酸水平呈负相关[36,59].同型半胱氨酸是氧化应激和甲基化能力受损的代谢生物标志物。最近一项对因纽特人的研究发现PON1活性与汞水平之间存在显著的负相关,与硒水平也存在直接相关[60].随着汞和果糖接触的增加和膳食钙摄入量的减少,人们可以看到ASD儿童PON1活性的降低和同型半胱氨酸水平的升高。
事实上,Pascaet al。最近的报道发现,自闭症儿童的PON1芳酯酶和PON1对氧磷酸酶活性都降低了[61,62].詹姆斯et al。发现自闭症儿童的血浆同型半胱氨酸水平高于对照组,但在服用叶酸和维生素B12后,转甲基化代谢物和谷胱甘肽(GSH)的水平有显著改善[63].帕特尔和柯蒂斯发现,除了每周注射一到三次谷胱甘肽和B12外,如果给患有自闭症和多动症的儿童喂食低果糖、不含食品添加剂和色素的有机饮食,他们在社交、注意力集中、写作、语言和行为等许多方面都有显著改善。64].
在美国,与对照组相比,自闭症儿童的母亲的平均血浆同型半胱氨酸水平也显著增加。65].施密特et al。研究发现,在围孕期服用维生素补充剂的妇女,其孩子患自闭症的风险降低[66].那些在此期间没有服用维生素的妇女更有可能生下患有自闭症的孩子,而当她们在单碳代谢途径中有特定的基因变异时,患自闭症的风险更大。这表明叶酸和其他膳食甲基供体可能改变其儿童基因表达的表观遗传调节,从而降低自闭症的风险[66].
蛋氨酸合成酶将氧化与表观遗传学联系起来
基因表达的表观遗传调控高度依赖于DNA和组蛋白的甲基化,而甲基化能力反过来又依赖于叶酸和维生素b12依赖性的蛋氨酸合成酶的活性,它将同型半胱氨酸转化为蛋氨酸。低蛋氨酸合酶活性降低甲基供体s -腺苷甲硫氨酸(SAM)的水平,同时增加甲基化抑制剂s -腺苷同型半胱氨酸(SAH)的水平[67].因此,SAM与SAH比值变化的综合效应对200多个甲基化反应产生强大影响,包括DNA和组蛋白甲基化[68].
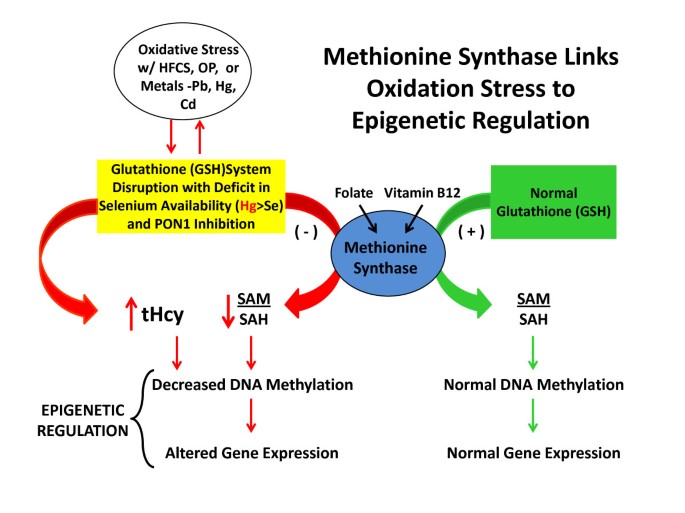
甲硫氨酸合成酶活性受到氧化应激的抑制,其抑制作用导致同型半胱氨酸转移,产生抗氧化的谷胱甘肽(GSH),这是一种重要的适应性反应[69].然而,甲硫氨酸合成酶的氧化抑制通过SAM与SAH比的降低和DNA和组蛋白甲基化的降低导致表观遗传效应。基因表达的表观遗传变化可以诱导对氧化应激的进一步适应性反应。数字4说明了人体在暴露于有机磷农药、重金属和高果糖玉米糖浆等耗钙物质的氧化应激下,这些变化是如何发生的。氧化应激时蛋氨酸合成酶活性降低也会增加同型半胱氨酸硫内酯的形成[70],提高了PON1的重要性。如前所述,PON1对于降低被认为是有害的同型半胱氨酸水平至关重要。血浆同型半胱氨酸(tHcy)水平升高与全基因组DNA低甲基化有关,这种低甲基化可能会代代相传,增加自闭症的风险[71].影响生殖系细胞的表观遗传变化可引起这些跨代效应[72].詹姆斯et al。发现父母与自闭症儿童在甲基化能力和谷胱甘肽依赖性抗氧化/解毒能力方面存在相似的代谢缺陷[71].
多种神经毒素的协同作用
基于以上的讨论,很明显,蛋氨酸合成酶活性在将氧化状态的变化转化为表观遗传效应方面是至关重要的,而这一作用在给予叶酸和维生素B12的自闭症受试者改善的代谢谱中得到了证实[63].这种关系引发了“自闭症的氧化还原/甲基化假说”(氧化还原/甲基化假说),该假说提出,由环境暴露(如汞和农药)引起的氧化损伤可以通过扰乱表观遗传调节引起神经发育障碍[73].本文扩展的大表观遗传汞毒性模型为“自闭症的氧化还原/甲基化假说”提供了额外的支持,同时对氧化应激反馈机制提供了重要的见解,氧化应激反馈机制可能是由于饮食接触毒素导致的营养不良造成的。表现出自闭症行为的孩子的出生可能与他们母亲的产前饮食有关。这些行为的严重程度可因儿童的有毒饮食暴露而进一步加剧,可通过旨在消除这些暴露的饮食改变加以改善。自闭症儿童很可能同时表现出对几种神经毒性物质的表观遗传反应,包括但不限于无机汞、铅、有机磷农药和/或HFCS。这些物质共同作用的综合效应很可能大于这些物质各自作用的综合效应。这种影响可能降低了自闭症儿童的神经可塑性,损害了他们的学习能力。
结论
2005年至2010年,美国6至21岁的儿童在自闭症残疾类别下接受特殊教育服务的人数增加了91%,尽管同期接受特殊教育服务的儿童总体上较少。利用汞毒性模型对美国和意大利的自闭症患病率进行了比较,结果表明,美国自闭症患病率的增加与从鱼类、燃煤电厂、硫柳汞或牙科汞合金中接触到的汞无关,而是与食用高果糖玉米糖浆有关。食用HFCS可能导致矿物质失衡,包括锌、钙和磷的损失和铜的获得,是接触无机汞的潜在来源。由于暴露于有机磷农药和重金属(如铅或汞),这些矿物质失衡在大脑中产生了多种氧化应激途径。食用高果糖玉米糖浆而暴露于无机汞和果糖都可能调节PON1基因表达。随着PON1活性的降低,同型半胱氨酸水平有可能增加,而同型半胱氨酸与全基因组DNA低甲基化有关,可能会从一代延续到下一代,影响神经发育和自闭症患病率。
主要作者信息
在以优异的成绩从美国公共卫生服务局环境卫生官员的职位上退休后,R. Dufault获得了教师执照,教了3.5年的基础特殊教育,在此期间她了解了美国自闭症和多动症儿童是如何接受特殊教育服务的。作为一名志愿者,她目前通过食品成分和健康研究所在线教授表观遗传学课程。
缩写
- 多动症:
-
注意缺陷多动障碍
- Ag:
-
银
- APA:
-
美国精神病学协会
- 自闭症谱系障碍:
-
自闭症谱系障碍
- Bi:
-
铋
- Ca:
-
钙
- Cd:
-
镉
- 疾病预防控制中心:
-
疾病预防控制中心
- 铜:
-
铜
- 衣冠楚楚的:
-
二烷基磷酸
- DSM:
-
精神疾病诊断和统计手册
- 欧盟:
-
欧盟
- 谷胱甘肽:
-
谷胱甘肽
- 高密度脂蛋白:
-
高密度脂蛋白
- 高果糖玉米糖浆:
-
高果糖玉米糖浆
- Hg:
-
汞
- Mg:
-
镁
- MT:
-
金属硫蛋白
- 平衡:
-
国家生物监测计划
- NHANES:
-
全国健康和营养检查调查
- OHI:
-
其他健康受损
- 人事处:
-
有机磷农药
- 病人:
-
磷
- 铅:
-
引领
- PDD:
-
广泛性发育迟缓
- PDP:
-
农药数据程序
- PON1:
-
paraoxonase-1
- 加拿大皇家银行:
-
红细胞
- 长官:
-
S-adenosylhomocysteine
- 山姆:
-
S-adenosylmethionine
- 血浆总高半胱氨酸水平:
-
血浆总同型半胱氨酸
- 农业部:
-
美国农业部
- 白细胞:
-
白细胞
- 锌:
-
锌。
参考文献
美国精神病学协会:《精神障碍诊断和统计手册》,2000年,华盛顿特区:文本修订版(DSM-IV-TR),第4页
Yerys BE, Wallace GL, Sokoloff JL, Shook DA, James JD, Kenworthy L:注意缺陷/多动障碍症状调节自闭症谱系障碍儿童的认知和行为。自闭症杂志,2009,2:322-333。
D'Amelio M, Ricci I, saco R, Liu X, D'Agruma L, Muscarella LA, Guarnieri V, Militerni R, Bravaccio C, Elia M, Schneider C, Melmed R, Trillo S, Pascucci T, Puglisi-Allegra S, Reichelt KL, Macciardi F, Holden JJA, Persico AM:对硫酶基因变异与北美自闭症相关,但在意大利没有:基因-环境相互作用中可能的区域特异性。中华精神病学杂志,2005,10:1006-1016。10.1038 / sj.mp.4001714。
Dufault R, Schnoll R, Lukiw WJ, LeBlanc B, Cornett C, Patrick L, Wallinga D, Gilbert SG, Crider R:汞暴露、营养缺乏和代谢紊乱可能影响儿童的学习。行为学脑功能,2009,5:44-10.1186/1744-9081-5-44。
Caspi A, Moffitt TE:精神病学中的基因-环境相互作用:与神经科学的合力。神经科学杂志,2006,7:583-590。
美国疾病控制和预防中心:勘误:第58卷,第5号。石第10。MMWR。2010, 59: 956-[http://www.cdc.gov/mmwr/preview/mmwrhtml/mm5930a5.htm]
美国疾病控制和预防中心:自闭症谱系障碍的流行——自闭症和发育障碍监测网络,美国,2006年。MMWR。2009, 58: 1-20。
Kogan MD, Blumberg SJ, Schieve LA, Boyle CA, Perrin JM, Chandour RM, Singh GK, Strickland BB, Trevathan E, van Dyck PC:父母报告的美国儿童自闭症谱系障碍诊断的患病率,2007。中华儿科杂志,2009,24(5):369 - 369。10.1542 /家族史- 1522。
Newschaffer CJ, Falb MD, Gurney JG:来自美国特殊教育数据的全国自闭症流行趋势。中华儿科杂志,2005,15:e277-282。10.1542 / peds.2004 - 1958。
数据问责中心:残疾人教育法(IDEA)数据。[http://www.ideadata.org/PartBData.asp]
Boyle CA, Boulet S, Schieve LA, Blumberg SJ, Yeargin-Allsopp M, Visser S, Kogan MD: 1997-2008年美国儿童发育障碍流行趋势。中华儿科杂志,2011,27(4):434 - 442。10.1542 / peds.2010 - 2989。
Iafusco D, Vanelli M, Songini M, Chiari G, Cardella F, Fifi A, Lombardo F, Marinaro A, Melia A, Marsciani A, Vacca A, Prisco F: 1型糖尿病和自闭症的相关性似乎与糖尿病的发病率有关。糖尿病护理。2006,29(8):1985-1986。
Zahir FR, Brown CJ:表观遗传对神经发育的影响:病理生理机制和遗传作用模式。儿科杂志,2011,69:92R-100R。10.1203 / PDR.0b013e318213565e。
Mutch DM, Wahli W, Williamson G:营养基因组学和营养遗传学:营养学的新面孔。中华医学杂志,2005,19:1602-1616。10.1096 / fj.05 - 3911转速。
Coyle P, Philcox JC, Carey LC, Rofe AM:金属硫蛋白:多用途蛋白质。细胞与生命科学,2002,59:627-647。10.1007 / s00018 - 002 - 8454 - 2。
Ivaturi R, Kies C:人体的矿物质平衡受果糖,高果糖玉米糖浆和蔗糖的影响。植物营养学报,1992,42:143-151。10.1007 / BF02196467。
Dufault R, LeBlanc B, Schnoll R, Cornett C, Schweitzer L, Wallinga D, Hightower J, Patrick L, Lukiw WJ:氯碱植物中的汞:测定食品糖中的浓度。环境卫生,2009,8:2-10.1186/1476-069X-8-2。
美国联邦法规。第74部分-经认证的食品色素添加剂清单。[http://ecfr.gpoaccess.gov/cgi/t/text/text-idx?c=ecfr&sid=1070b19eb50e562daa872cfa1755aa09&rgn=div5&view=text&node=21:1.0.1.1.27&idno=21#21:1.0.1.1.27.1.31.9]
Shankar AH, Prasad AS:锌和免疫功能:对感染抵抗力改变的生物学基础。中华医学杂志。1998,38(4):357 - 357。
蔡立雷,张志强,张志强,等:膳食锌缺乏和补足对大鼠小肠和肝脏中金属硫蛋白的免疫定位和浓度的影响。中国生物医学工程学报,2001,31(4):381 - 381。
Yorbik O, Akay C, Sayal A, Cansever A, Sohmen T, Cavdar AO:锌在自闭症儿童中的作用。中华检验医学杂志2004,17:101-107。10.1002 / jtra.20002。
Faber S, Zinn GM, Kern JC, Kingston HM:血浆锌/血清铜比值作为自闭症谱系障碍儿童的生物标志物。生物标志物,2009,14:171-180。10.1080 / 13547500902783747。
Yasuda H, Yoshida K, Yasuda Y, Tsutsui T:婴儿缺锌:与自闭症谱系障碍的关系。科学通报,2011,1:129-
Adams JB, Baral M, Geis E, Mitchell J, Ingram J, Hensley A, Zappia I, Newsmark S, Gehn E, Rubin RA, Mitchell K, Bradstreet J, El-Dahr JM:自闭症的严重程度与有毒金属体负荷和红细胞谷胱甘肽水平有关。毒理学杂志,2009:532640-
美国农业部:经济研究处-数据集。损失调整食品供应:电子表格。[http://www.ers.usda.gov/Data/FoodConsumption/FoodGuideSpreadsheets.htm#sugar]
Milne DB, Nielsen FH:饮食中果糖和镁之间的相互作用对男性的大矿物质稳态产生不利影响。中华医学杂志。2000,19:31-37。
Ford ES, Mokdad AH:美国成年人饮食中镁的摄入量。中国生物医学工程学报,2003,32(4):359 - 359。
Strambi M, Longini M, Hayek J, Berni S, Macucci F, Scalacci E, Vezzosi P:镁在自闭症中的作用。中国生物医学工程学报,2006,29(4):447 - 447。10.1385 / bt: 109:2:097。
Adams JB, Audhya T, McDonough-Means S, Rubin RA, Quig D, Geis E, Gehn E, Loresto M, Mitchell J, Atwood S, Barnhouse S, Lee W:自闭症儿童与神经正常儿童的营养和代谢状况及其与自闭症严重程度的关系。Nutr Metab(伦敦)。2011, 8: 34-10.1186/1743-7075-8-34。
美国农业部:我们在美国吃什么,NHANES 2005-2006。[http://www.ars.usda.gov/SP2UserFiles/Place/12355000/pdf/0506/usual_nutrient_intake_vitD_ca_phos_mg_2005-06.pdf]
营养和金属毒性。中华口腔医学杂志,1997,15(5):561 - 561。
Mahaffey KR, Gartside PS, Glueck CJ: 1至11岁儿童血铅水平和膳食钙摄入量:1976至1980年第二次全国健康和营养检查调查。中华儿科杂志,1986,38(5):557 - 562。
Shannon M, Graef JW:广泛性发育障碍儿童的铅中毒。中华临床毒理学杂志,1996,34:177-181。10.3109 / 15563659609013767。
Eubig PA, Aguiar A, Schantz SL:铅和多氯联苯是注意缺陷/多动障碍的危险因素。环境卫生展望。2010,118:1654-1667。10.1289 / ehp.0901852。
乔斯D,谢伟,Renault F, Rochu D, Schopfer LM, Masson P, Lockridge O:人对氧磷酶(PON1)芳酯酶/有机磷酸酶活性必需残基的鉴定。生物化学,1999,38:2816-2825。10.1021 / bi982281h。
Jakubowski H:对氧磷酶1在同型半胱氨酸硫内酯解毒中的作用。中华临床医学杂志,2010,36(4):447 - 447。10.1007 / 978 - 1 - 60761 - 350 - 3 - _11。
Pasca SP、Dronca E、Nemes B、Kaucsar T、Endreffy E、Iftene F、Benga I、Cornean R、Dronca M:对氧磷酶1在自闭症谱系障碍中的活性和多态性。中华细胞医学杂志2010,14:600-607。
Dufault R, Gilbert SG:粮食中有机磷(OP)农药的影响。在毒理学学会会议上展示的海报,2011年,华盛顿
Ackerman Z, Oron-Herman M, Pappo O, Peleg E, Safadi R, Schmilovitz-Weiss H, Grozovski M:罗格列酮对代谢综合征大鼠肝脏的影响。基础临床药物毒理杂志,2010,107:663-668。10.1111 / j.1742-7843.2010.00553.x。
Costa LG, Giordano G, Furlong CE:对氧磷酶1 (PON1)活性和表达的药理学和膳食调节剂:寻找还在继续。中国生物医学工程学报,2011,31(4):337-344。10.1016 / j.bcp.2010.11.008。
Costa LG, Vitalone A, Cole TB, Furlong CE:对氧磷酶(PON1)活性的调节。中国生物医学工程学报,2005,29(5):541- 551。10.1016 / j.bcp.2004.08.027。
Huen K, Harley K, Bradman A, Eskenazi B, Holland N:墨西哥裔美国母亲和不同基因型和单倍型儿童PON1酶活性的纵向变化。中国药理学杂志,2010,34(4):381 - 381。10.1016 / j.taap.2009.12.031。
Eskenazi B, Huen K, Marks A, Harley KG, Bradman A, Barr DB, Holland N:来自CHAMACOS研究的PON1和接触有机磷农药儿童的神经发育在子宫内.环境卫生展望。2010,118:1775-1781。10.1289 / ehp.1002234。
Barr DB、Bravo R、Weerasekera G、Caltabiano LM、Whitehead RD、Olsson AO、Caudill SP、Schober SE、Pirkle JL、Sampson EJ、Jackson RJ、Needham LL:有机磷农药在美国人群中的磷酸二烷基代谢物浓度。《环境卫生展望》,2004,112:186-200。
Lu C, Schenck FJ, Pearson MA, Wong JW:评估儿童膳食农药接触:在24小时重复样本中直接测量农药残留。环境卫生展望,2010,118:1625-1630。10.1289 / ehp.1002044。
Harari R, Julvez J, Murata K, Barr D, Bellinger DC, Debes F, Grandjean P:产前接触农药的学龄儿童神经行为缺陷和血压升高。环境卫生展望。2010,118:890-896。10.1289 / ehp.0901582。
Jurewicz J, Hanke W:产前和儿童期农药暴露与神经行为发育:流行病学研究综述。国际职业医学与环境卫生杂志。2008,21:121-132。10.2478 / v10001 - 008 - 0014 - z。
Bouchard MF, Chevrier J, Harley KG, Kogut K, Vedar M, Calderon N, Trujillo C, Johnson C, Bradman A, Barr DB, Eskenazi B: 7岁儿童产前接触有机磷农药对智商的影响环境卫生展望,2011,119:1189-1195。10.1289 / ehp.1003185。
Perera FP, Rauh V, Whyatt RM, Tang D, Tsai WY, Bernert JT, Tu YH, Andrews H, Barr DB, Camann DE, Diaz D, Dietrich J, Reyes A, Kinney PL:产前ETS、多环芳烃和农药暴露对出生结局和发育影响的最新研究综述。神经毒理学杂志,2005,26:573-587。10.1016 / j.neuro.2004.07.007。
美国农业部:农业营销服务处。科学与实验室。数据库和年度总结。[http://www.ams.usda.gov/AMSv1.0/ams.fetchTemplateData.do?template=TemplateG&topNav=&leftNav=ScienceandLaboratories&page=PDPDownloadData/Reports&description=Download+PDP+Data/Reports&acct=pestcddataprg]
Mahaffey KR, Clickner RP, Jeffries RA:美国成年女性的血汞浓度因地区而不同:与鱼类消费模式有关(NHANES 1999-2004)。环境卫生展望,2009,117:47-53。
Oskarsson A, Schultz A, Skerfving S, Hallen IP, Ohlin B, Lagerkvist BJ:哺乳妇女食用鱼类和汞合金填料与母乳和血液中总和无机汞的关系。《环境卫生》1996,51:234-241。10.1080 / 00039896.1996.9936021。
美国食品和药物管理局:对疫苗和自闭症问题的持续反应。[http://www.fda.gov/NewsEvents/Testimony/ucm115158.htm]
Windham GC, Zhang L, Gunier R, Croen LA, Grether JK:自闭症谱系障碍与旧金山湾区有害空气污染物分布的关系。《环境卫生展望》,2006,114:1438-1444。10.1289 / ehp.9120。
Palmer RF, Blanchard S, Wood R:环境汞释放点源的邻近性是自闭症患病率的预测因子。卫生场所,2008,15:18-24。
Barbone F, Valent F, Mazej D, Tratnik J, Spiric Z, Prpic I, Sofianou-Katsoulis A, Nakou S, Little D, Mariuz M, Miklavcic A, Neubauer D, Rosolen V, Petrovic O, Parpinel M, Bin M, Tognin V, Carrozzi M, Osredkar J, Horvat M:地中海队列中汞、鱼类摄入与儿童发育的关系第十届汞作为全球污染物国际会议。2011,哈利法克斯,加拿大:FS19-01
欧洲委员会:审查关于汞的共同体战略。最终报告,2010年。[http://ec.europa.eu/environment/chemicals/mercury/pdf/review_mercury_strategy2010.pdf]
Valent F, Pisa F, Mariuz M, Horvat M, Gibicar D, Fajon V, Mazej D, Daris F, Barbone F:胎儿和围产期汞和硒暴露:对意大利Giulkia Friuli Venezia的一组儿童的基线评价。流行病学杂志,2011,35(1):33-42。
Lacinski M, Skorupski W, Cieslinski A, Sokolowska J, Trzeciak WH, Jakubowski H:人对氧磷酶-1 (PON1)蛋白同型半胱氨酸硫乳内酯酶活性的决定因素。中国生物医学工程学报,2004,30(4):381 - 381。
Ayotte P, Carrier A, Ouellet N, Boiteau V, Abdous B, Sidi EAL, Degat MLC, Dewailly E: Nunavik因纽特成人中甲基汞暴露与血浆对氧磷酸酶活性的关系。环境卫生展望,2011,119:1077-1083。10.1289 / ehp.1003296。
Pasca SP、Dronca E、Nemes B、Kaucsar T、Endreffy E、Iftene F、Benga I、Cornean R、Dronca M:对氧磷酶1在自闭症谱系障碍中的活性和多态性。中华细胞医学杂志2010,14:600-607。
Pasca SP、Nemes B、Vlase L、Gagyi CE、Dronca E、Miu AC、Dronca M:自闭症儿童高同型半胱氨酸水平和低血清对氧酸酶1亚酯酶活性。生命科学学报,2006,38(4):344 - 344。10.1016 / j.lfs.2005.09.040。
James SJ, Melnyk S, Fuchs G, Reid T, Jernigan S, Pavliv O, Hubanks A, Gaylor DW:甲基钴胺素联合叶酸治疗自闭症儿童谷胱甘肽氧化还原状态的疗效。中华口腔医学杂志,2009,29(4):394 - 394。
Patel K, Curtis LT:一种治疗自闭症和注意缺陷多动障碍的综合方法:一项前期研究。中华口腔医学杂志,2007,13:1091-1097。10.1089 / acm.2007.0611。
James SJ, Melnyk S, Jernigan S, Lehman S, Seidel L, Gaylor DW, Cleves MA:自闭症儿童母亲叶酸载体基因缺失和DNA低甲基化的功能性多态性。中华神经科学杂志,2010,38(3):359 - 361。
Schmidt RJ, Hansen Rl, Hartiala J, Allayee H, Schmidt LC, Tancredi DJ, Tassone F, Hertz-Picciotto I:产前维生素、一碳代谢基因变异与自闭症风险。流行病学杂志,2011,22:476-485。10.1097 / EDE.0b013e31821d0e30。
Matthews RB, Sheppard C, Goulding C:四氢叶酸亚甲基还原酶和蛋氨酸合成酶:生物化学和分子生物学。中华儿科杂志,1998,32(5):533 - 536。10.1007 / PL00014305。
Petrossian TC, Clarke SG:发现人类甲基转移体。分子细胞蛋白质组学,201,10:M110.00097-
邹刚,Banerjee R:同型半胱氨酸与氧化还原信号通路。抗氧化氧化还原信号。2005,7:547-559。10.1089 / ars.2005.7.547。
Jakubowski H, Perla-Kajan J, Finnell RH, Cabrera RM, Wand H, Gupta S, Kruger WD, Kraus JP, Shih DM:同型半胱氨酸或叶酸代谢的遗传或营养障碍增加小鼠蛋白n -同型半胱氨酸化。中华医学杂志,2009,23:1721-1727。10.1096 / fj.08 - 127548。
杨建军,杨建军,杨建军,等。自闭症儿童父母DNA低甲基化与转甲基化代谢的关系。中华孤独症杂志。2008,38:1966-1975。10.1007 / s10803 - 008 - 0591 - 5。排错在J自闭症发展障碍2008年,38:1976。吉尔·詹姆斯,S[更正为詹姆斯,S吉尔]
格雷罗-博萨尼亚C,斯金纳MK:环境诱导表型和疾病的表观遗传跨代遗传。中华分子生物学杂志,2012,32(4):354 - 354。10.1016 / j.mce.2011.10.004。
戴德华,刘志刚,刘志刚,刘志刚,刘志刚。环境和遗传因素如何共同导致自闭症:一个氧化还原/甲基化假说。神经毒理学。2008,29:190-201。10.1016 / j.neuro.2007.09.010。
确认
作者要感谢博士。Robert Lustig, Blaise LeBlanc和Steven Gilbert对这个手稿和/或其中的概念提供了反馈。该研究项目的资金主要来自对食品成分和健康研究所的捐赠。Lukiw实验室的研究由国家研究资源中心拨款编号P20RR016456、路易斯安那州立大学健康科学中心新奥尔良分校转化研究计划拨款、阿尔茨海默病协会研究者发起的研究拨款IIRG-09-131729以及NIH NIA拨款AG18031和AG038834提供支持。
作者信息
作者和隶属关系
相应的作者
权利与权限
本文由BioMed Central Ltd.授权发布。这是一篇开放获取文章,根据创作共用授权协议(http://creativecommons.org/licenses/by/2.0),它允许在任何媒体上不受限制地使用、分发和复制,只要原著被恰当地引用。
关于本文
引用本文
杜福克,卢昆,w.j.,克里德,R。et al。用宏观表观遗传学的方法来确定美国自闭症流行的原因。中国Epigenet4, 6(2012)。https://doi.org/10.1186/1868-7083-4-6
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/1868-7083-4-6
关键字
- 自闭症
- DNA甲基化
- 环境表观遗传学
- 重金属
- 高果糖玉米糖浆
- PON1
- 山姆
- 锌