摘要
背景
肺移植(LTx)后的生存常常受到闭塞性细支气管炎综合征(BOS)的限制。
方法
对278例接受LTx治疗的受者进行调查。使用的终点是BOS (BOS分级≥2)、死亡或再肺移植(Re-LTx),通过竞争风险回归分析评估。
结果
双LTx (DLTx)受者BOS≥2级的发生率在5年为16±3%,10年为30±4%,20年为37±5%,而单LTx (SLTx)受者相应的BOS≥2级的发生率在5年、10年和20年分别为11±3%、20±4%和24±5% (p> 0。05).主要适应症BOS≥2级发生率由高到低依次为other、PF、CF、COPD、PH、AAT1 (p< 0。05).按主要适应证死亡率由高到低依次为:COPD、PH、AAT1、PF、Other和CF (p< 0。05).
结论
移植类型的BOS分级≥2的发生率没有差异,然而,与SLTx受体相比,DLTx受体显示出更好的生存机会,尽管发生了BOS。BOS发生率最高的是CF、PF、COPD、PH和AAT1受体,但与COPD、PH和AAT1受体相比,CF和PF受体在发生BOS后仍有更好的生存机会。
背景
慢性同种异体肺移植功能障碍(Chronic lung allograft dysfunction, CLAD)仍然是肺移植术后长期成功的主要障碍[1,2,3.]。LTx后的主要死亡原因是CLAD。在LTx后的第一年,很少发生CLAD,但发病率迅速上升,据报道,在最初的五年内,累计发病率高达40%至80% [4,5,6,7]。据报道,移植后早期出现的CLAD比晚发性CLAD预后更差。闭塞性细支气管炎(BO)是肺移植受者肺功能进行性丧失最常见的病理损伤。它被认为是由慢性同种异体移植排斥引起的,其特征是纤维黏液样肉芽组织阻塞小气道。分布呈斑片状,难以经支气管活检发现[3.,7]。由于BO难以在组织学上记录,国际心肺移植学会(ISHLT)于1993年为其生理对应物建立了标准,即闭塞性细支气管炎综合征(BOS)。此诊断需要1 s内用力呼气量(FEV1)永久性下降20%,而不是由于并发过程[8]。自2014年以来,慢性排斥的诊断范围进一步扩大到CLAD,其中包括限制性同种异体移植综合征(RAS)。有小气道病变视觉征象的CT扫描和小气道严重狭窄或完全阻塞的肺活检也可诊断为CLAD [8]。
在瑞典,有两个中心为大约1000万人口进行肺移植,所有这些人都享有国家健康保险。sk
患者及方法
1990年1月至2014年6月期间,278名患者在隆德大学sk
在本研究中,中位年龄为51岁,范围为12-71岁。主要适应症定义为慢性阻塞性肺疾病(COPD) (n67),囊性纤维化(CF) (nα1-抗胰蛋白酶缺乏症(AAT1) (n肺纤维化(PF) (n= 38),肺动脉高压(PH) (n= 39),而被视为“其他”的组别(n= 25),包括支气管扩张、结节病、细支气管肺泡癌、矽肺病和移植物抗宿主病(GVHD)。
7例患者经胸骨正中切口,2例患者经第4肋间隙的翻盖切口(双侧前外侧胸骨横切)行HLTx。SLTx和DLTx按标准方式进行。86例患者经后外侧开胸,7例经翻盖,4例经正中胸骨切开术行SLTx。146例患者通过贝壳切口,17例患者通过正中胸骨切开术,9例患者通过前外侧开胸术。
术前呼吸支持13例(CF 4、PF 5、Re-LTx 3、PH 1),术前ECMO(体外膜氧合)支持12例(CF 6、PF 3、ARDS 1、PH 1、Re-LTx 1)。
术中采用体外循环(ECC)形式的循环支持105例,术中采用ECMO 73例。术中未使用循环支持115例。接收方特征见表1。
慢性同种异体移植物功能障碍
根据ISHLT指南,BOS被定义为FEV下降超过20%1从获得的最高基线,[8,9],其特征是血管周围和间质单核细胞浸润或以致密瘢痕和嗜酸性粒细胞浸润为特征的慢性排斥反应。如果检测到肺功能的快速恶化是慢性同种异体移植物功能障碍的标志,则对TBB进行支气管镜检查,并开始使用脉冲甲泼尼松隆抗排斥治疗,通常与他克莫司或依维莫司联合使用,以替代环孢素。本研究纳入BOS分级≥2的患者进行分析。
统计方法
采用SPSS 19.0版本进行统计计算。(IBM Corp .,纽约州阿蒙克)材料的初级分层分为两组队列。第一组以LTx的主要适应症为基础,分为COPD、AAT1、CF、PH、PF四个指标队列。第二组以LTx类型为基础进行分组:DLTx或SLTx。本研究的目的是分析原发性LTx后BOS(≥2级)的发生情况。在本分析中,死亡作为BOS的竞争风险事件。在竞争风险模型中,我们将BOS≥2级的发生率和死亡作为两个独立的结果进行分析。具体来说,我们使用Gray检验估计并比较了BOS等级≥2和死亡的累积关联函数,Gray(1988)。所有关于竞争风险的计算都是使用R和CMPRSK包(可在http://www.r-project.org)。对于所有的统计分析,ap-value小于0。0.05被认为是显著的。所有统计计算均由瑞典马尔默的Sidesoft AB公司进行。
结果
BOS分级≥2级的累积发病率与死亡
移植类型
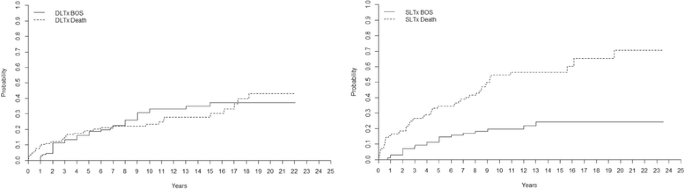
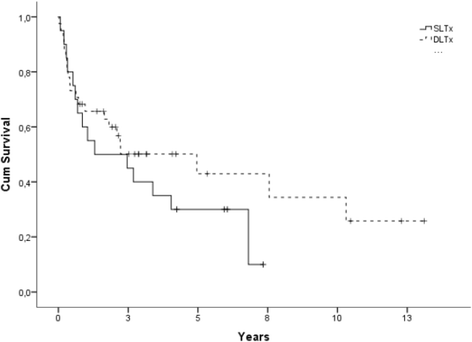
图中按移植类型(DLTx和SLTx)给出了BOS(分级≥2)的发生率(概率百分比±SE)。1。dltx受者的BOS发生率为5年16±3%,10年30±4%,15年35±5%,20年37±5%,而sltx受者的BOS发生率为5年11±3%,10年20±4%,15年24±5%,20年24±5% (p> 0。05).DLTx受者5年死亡率为19±3%,10年死亡率为23±4%,15年死亡率为28±4%,20年死亡率为43±7%,sltx受者5年死亡率为34±5%,10年死亡率为55±6%,15年死亡率为56±6%,20年死亡率为71±8% (p< 0。05).在图中,Kaplan-Meier生存期显示为BOS发生后(≥2级)至随访/死亡。2。生存曲线分为接受过DLTx和SLTx的患者。p> 0。05).
主要适应症
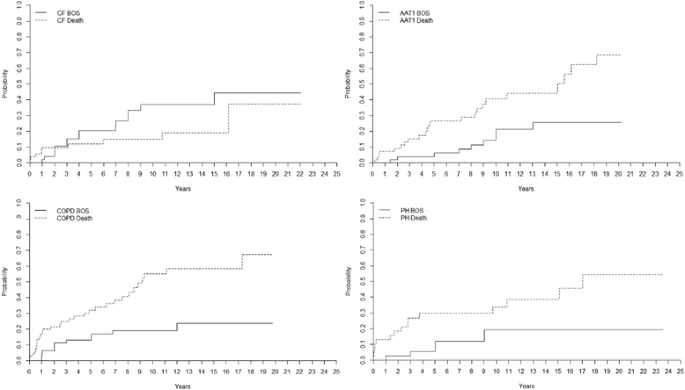
不同诊断组的BOS发生率(≥2级)如图所示。3.。aat1患者的BOS发生率为5年(4±3%),10年(14±6%),15年(26±8%),20年(26±8%)。对于cf患者,5年为20±6%,10年为37±8%,15年为37±8%,20年为44±10%。copd患者5年为13±4%,10年为19±5%,15年为24±7%。在pf患者中,BOS的发生率在5年为25±8%,10年为34±9%,15年为34±9%,20年为34±9%,而ph患者在5年为6±4%,10年为19±7%,15年为19±9%,20年为19±7% (p< 0。05).aat1患者5年死亡率为26±6%,10年死亡率为41±8%,15年死亡率为44±8%,20年死亡率为68±10%。对于cf患者,5年为12±5%,10年为15±5%,15年为19±7%,20年为37±19%。copd患者5年为32±6%,10年为55±8%,15年为58±8%。对于pf患者,5年为26±8%,10年为38±9%,15年为38±9%,20年为52±16%;对于PH患者,5年为30±8%,10年为34±8%,15年为39±9%,20年为54±12% (p< 0。05).
囊性纤维化(CF)、α - 1-抗胰蛋白酶缺乏症(AAT1)、copd和肺动脉高压(PH)组患者肺移植后累积发病率(BOS)和死亡率(LTx)的比较与AAT1受体相比,CF受体发生≥2级BOS的风险明显更高(p< 0。05),但AAT1的死亡率显著高于(p< 0。0.05),说明CF受体可能比AAT1受体更能承受BOS。CF和COPD患者的BOS≥2级发生率相同(p> 0。慢性阻塞性肺疾病(COPD)患者的死亡率(p< 0。0.05),表明CF患者可能比COPD患者更能承受BOS。与PH受体相比,CF受体发生≥2级BOS的风险明显更高。然而,CF和PH受体的死亡率相同,表明CF和PH受体合并BOS的生存机会相同
主要指征与对照组比较
比较两组患者的主要适应证。组“other”描述了一组因支气管扩张、结节病、细支气管肺泡癌、矽肺病、BOS和移植物抗宿主病(GVHD)而接受LTx的异质患者。与慢性阻塞性肺病(COPD)相比,该组的BOS发病率更高。p= 0。007), aat1 (p= 0。001)及PH (p= 0。002)患者。与慢性阻塞性肺病(COPD)相比,这组患者的死亡风险也明显降低。p= 0。037), aat1 (p= 0。281)及PH (p= 0。300)患者。
与AAT1受体相比,CF受体发生BOS的风险更高(p= 0。048),但AAT1的死亡率更高(p= 0。020)。CF和COPD患者发生BOS的发生率相同(p= 0。164),但COPD患者的死亡率更高(p= 0。001)。与PH受体相比,CF受体发生BOS的风险更高(p= 0。055),但CF和PH受体的死亡率相同(p= 0。(图057)。3.)。
年龄与BOS
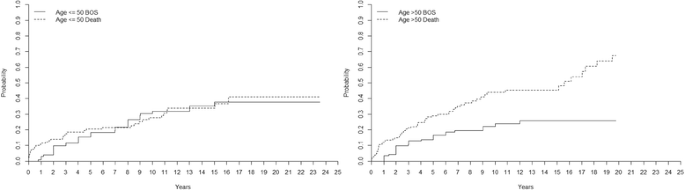
≤50岁患者的BOS(分级≥2)发生率为:5年15±3%,10年30±5%,15年35±5%,20年38±6%。>50岁的患者5年为14±3%,10年为22±4%,15年为26±5% (p= 0。238)。≤50岁患者5年死亡率为20±4%,10年死亡率为28±4%,15年死亡率为34±5%,20年死亡率为41±7%。>50岁患者5年死亡率为29±4%,10年死亡率为44±5%,15年死亡率为45±5% (p= 0。(图019)。4)。
不同的时间段和BOS
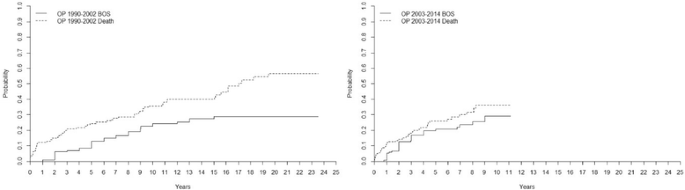
1990-2002年期间,所有受者的BOS(≥2级)发生率在5年为9±3%,10年为23±4%,15年为27±4%,20年为29±4%。同期总死亡率5年24±4%,10年36±4%,15年40±5%,20年57±6%。2003 - 2014年,BOS的发病率分别为2年(8±2%)、4年(17±3%)、6年(21±4%)、8年(24±4%)和10年(29±5%)。同一时期的总死亡率2年为14±3%,4年为22±4%,6年为27±4%,8年为32±,10年为36±5%(图2)。5)。
死亡率
术后12个月前后的死亡原因见表2。“其他原因”组定义为心肌和脑缺血、多器官衰竭以及与患者年龄和健康状况有关的其他原因导致的死亡。
讨论
肺移植是终末期肺病的一种成熟治疗方法[10]。临床肺移植的数量受到器官短缺的限制,这导致人们不断寻找增加器官数量的新方法[11,12,13,14],而肺移植后的生存率主要受CLAD限制。在过去的十年里,肺移植后的生存率有了显著的提高,然而,主要表现为BOS的肺脏损伤仍然是肺移植后发病和死亡的主要原因。虽然一年内发生BOS的风险较低,但在头五年内累积发病率迅速增加[9,15,16]。
BOS的危险因素仍未完全了解[17]。在一些研究中,抗人白细胞抗原(HLA)供体特异性抗体(DSA)与LTx后早期和高级别BOS和死亡相关,但仍存在争议[18,19]。当首次检测到DSA时,使用血浆置换去除抗体或限制抗体介导的损伤的治疗已显示出一定的效果。然而,这种治疗对LTx后临床结果的影响尚不清楚[20.]。细菌和病毒感染也被确定为LTx后BOS的可能诱因[21,22]。虽然BOS通常被认为是不可逆的,但最近的证据表明,一些BOS患者可能对阿奇霉素有反应,其FEV1改善超过10% [22]。此外,最近也报道了另一种形式的慢性排斥反应,限制性同种异体移植综合征(RAS),它不符合BOS的定义,而是以涉及周围肺病理的限制性功能改变为特征,因此引入了更具包容性的术语CLAD [5,23]。
278名受者中BOS≥2级的总累积发生率在移植后5年为15%,10年为26%,15年为30%,20年为32%。BOS的发病率在“其他”组中最高。该组描述了一组异质性的患者,他们因支气管扩张、结节病、细支气管肺泡癌、矽肺病、BOS和移植物抗宿主病(GVHD)而接受LTx,这可能反映了BOS的高发病率。这群人的异质外表使得很难得出任何结论。除“其他”组外,按降序排列,PF受体中BOS发病率最高,其次是CF、COPD、PH和AAT1受体。研究表明,BOS和PF分别表现出相似的疾病特征,病理生理重叠,如上皮细胞损伤和ECM的产生/沉积增加[24]。这一患者群体非常有趣,因为鉴定PF中的生物标志物可能有助于找到早期发现BOS的新方法[25]。死亡率最高的是COPD患者,其次是PH、AAT1、PF和CF患者(按降序排列),这表明与其他主要适应症(如COPD和PH)相比,CF和PF患者在发生BOS的情况下有更好的生存机会。还应该承认,瑞典接受ltx治疗的患者结果可能与其他国家(如美国)不同,因为COPD/CF与间质性肺病的发病率明显更高,再加上瑞典接受ltx治疗的患者更年轻[26]。此外,来自ISHLT的报告显示,与瑞典相比,LTx的间质性肺病发病率几乎是瑞典的两倍。
当我们比较不同患者组(两对)之间的主要适应症时,与COPD、AAT1和PH受体相比,“其他”组发生BOS(分级≥2)的风险明显更高。请记住,这组受者反映了一组异质性的患者,其中一些受者由于BOS和GVHD而接受了LTx,而受者可能在移植时已经产生了免疫反应,可能导致肺移植物发生BOS。
CF受者发生BOS的风险明显高于AAT1受者,但AAT1受者的死亡率明显高于AAT1受者,表明CF受者可能比AAT1受者更能承受BOS的发展。这一发现可能对LTx中支持CF受体的临床意义产生积极影响。此前,由于CF相关的危险因素,如CF相关的关节病以及与细菌/真菌制剂相关的慢性感染,LTx治疗CF的总体生存获益一直存在争议B.cepacia,P.Auriginosa和曲霉属真菌这可能会严重到危及生命[27]。有趣的是,与PH受体相比,CF受体发生BOS的风险明显更高,然而,CF和PH受体的死亡率相同,表明CF和PH受体发生BOS的生存机会相同,尽管有BOS。研究表明,作为病理生理的一部分,PH患者经历了广泛的肺动脉壁重塑,导致内膜的永久性改变[28]。然而,由于闭塞性细支气管炎通常与免疫介导的动脉和静脉病变相关,导致毛细血管前和后的PH,因此在不同的受体中也可见ltx后的PH [29]。从理论上讲,在LTx之前患有PH的患者可能更好地承受这种现象,这说明为什么PH受体尽管有BOS,但生存率并不低于CF。了解这种疾病状态下BOS发展的临床意义可能具有巨大的潜力。然而,由于需要进一步的数据,本研究并未对这一假设进行调查。
CF和COPD患者的BOS发生率相同,但COPD患者的死亡率明显高于COPD患者,表明CF患者可能比COPD患者更能承受BOS的发展。COPD受者在移植时通常比CF患者年龄大,并且COPD患者通常有合并症,如心脏和血管疾病,这可能部分解释了这些结果。我们进行了一项扩展分析,以调查年龄对BOS发展和死亡风险的影响。我们得出结论,年龄对BOS的发展没有影响,但与年龄小于50岁的受者相比,50岁或以上的受者移植后5年的死亡率高9%,移植后10年的风险高16% (p< 0。05).
有趣的是,当我们在整个队列中比较DLTx和SLTx时,我们发现DLTx和SLTx接受者发生≥2级BOS的风险相同。然而,接受DLTx治疗的患者有明显更好的生存机会。这些结果进一步支持了支持DLTx而不是SLTx的临床方案。我们试图分析DLTx和SLTx在COPD等主要适应症中的分布规律,但遗憾的是,分组人数不够大,无法达到统计学评价。我们的研究结果表明,DLTx和SLTx发生BOS的风险相同,但DLTx有更好的生存机会。我们怀疑这些结果可能反映了这样一个事实,即在过去的10-15年里,我们开始对病毒和细菌感染进行早期治疗,在出现排斥反应的第一个迹象时使用更积极的治疗,并且更倾向于DLTx而不是SLTx。在我的诊所,SLTx的频率在2002年达到顶峰,此后明显下降,有利于DLTx。然而,我们的结果并不支持这些假设,因为在不同的时间段内没有发现BOS的风险或死亡率之间的差异。在无花果。5我们展示了1990-2002年和2003-2014年两个不同时间段的结果。
限制
在过去的25年里,移植患者的护理发生了重大变化,这影响了移植年份的存活率等结果变量。多年来,受体纳入标准已经扩大,现在术前ECMO支持或呼吸机支持不再是LTx的禁忌症,代表了复杂的受体客户。与LTx的长期生存有关的几个混杂因素可能在这里发挥作用。这些变量包括受体/供体年龄和总肺活量,以及受体肾功能、氧气需求和同种异体移植物缺血时间。在目前的研究中,被诊断为BOS 1级的患者,在大多数情况下,即使患者被诊断为BOS,也没有得到特定的治疗或改变目前的治疗方案。通过肺活量测定法可以诊断BOS,根据ISHLT, FEV1较基线下降超过20%与BOS分级≥1相关。虽然除了BOS之外,可能影响术后肺功能的混杂因素还有复发性感染或自然衰老过程或其他合并症影响的FEV1下降。还应该承认,与目前的CLAD标准(如表型分为BOS和RAS)相比,对BOS的最佳基线FEV1 < 80%的定义是有争议的。为了区分是否真的有排斥反应(BOS),我们在本分析中将BOS计算为BOS 2级或以上。这当然可以谨慎遵循。
结论
不同移植类型的BOS分级≥2的发生率没有差异,然而,尽管发生BOS的风险相同,与SLTx受体相比,DLTx受体显示出更好的生存机会,这表明接受DLTx的受体比SLTx受体更能承受BOS。这些数据进一步支持临床项目倾向于DLTx而不是SLTx。≥2级BOS发生率最高的是PF、CF、COPD、PH和AAT1受体,其发生率由高到低依次描述了PF受体发生BOS的最高风险。然而,与COPD、PH和AAT1受体相比,CF和PF受体显示出更好的生存机会,尽管发生了BOS。
参考文献
韦勒登,魏西利斯库,等。肺移植术后气道阻塞的部位和性质。[J]中华呼吸与急救杂志,2014;39(3):391 - 391。
Gauthier JM, Hachem RR, Kreisel D.慢性同种异体肺移植功能障碍的研究进展。中华医学杂志,2016;3:185-91。
al - githmi I, Batawil N, Shigemura N,等。肺移植后闭塞性细支气管炎。[J]中华心脏外科杂志,2006;30(3):846 - 851。
范德茂,李建平,李建平,等。慢性同种异体肺移植功能障碍表型的免疫多样性:一项全面的免疫组织化学分析。国际翻译,2017;30:134-43。
Verleden SE, Vanaudenaerde BM, Vos R, Verleden GM.慢性同种异体肺移植功能障碍的表型:一步步接近?中华移植杂志,2016;16:3071-2。
李建军,李建军,李建军,等。肺移植后闭塞性细支气管炎的研究进展。胸部。2016;150:219-25。
王建军,李建军,李建军,等。慢性同种异体肺移植功能障碍:机制的系统回顾。移植。2016;100:1803-14。
李建军,李建军,李建军,等。闭塞性细支气管炎综合征2001:诊断标准的更新。[J]中华心肺移植杂志。2002;21(3):391 - 391。
Verleden GM, Raghu G, Meyer KC,等。慢性同种异体肺移植功能障碍的新分类系统。心肺移植杂志,2014;33:127-33。
Fakhro M, Ingemansson R, Skog I等。瑞典隆德大学医院肺移植术后随访25年:囊性纤维化患者获得较好的治疗效果。中华心血管外科杂志,2016;23:65-73。
Lindstedt S, Pierre L, Ingemansson R.在离体肺灌注过程中,短时间不灌注通气似乎可以减少肺不张而不损害肺。[J] .交通安全学报,2013;2013(3):798 - 798。
林志强,李建军,李建军,等。如何体外修复初排斥供肺用于临床移植有隆德大学医院的临床经验。[J] .交通安全学报,2011;31(2):444 - 444。
Machuca TN, Cypel M.体外肺灌注。[J] .胸外科杂志,2014;6:1054-62。
桑切斯PG, Bittle GJ, Williams K,等。心脏死亡后捐献的停搏前肝素化的体外肺评价。中华外科杂志。2013;25:534 - 541。
Christie JD, Edwards LB, Kucheryavaya AY等。国际心肺移植学会登记:第28届成人肺和心肺移植报告-2011。[J]中华心肺移植杂志,2011;30(3):1104 - 1104。
李建军,李建军,李建军,等。闭塞性细支气管炎综合征和限制性同种异体移植综合征患者肺移植的淋巴表型。移植。2017;101:310-5。
李建军,李建军,李建军,等。微粒:对肺原发性移植物功能障碍的新认识?中国生物医学工程学报,2016;37(2):1101 - 1107。
Westall GP, Paraskeva MA, Snell GI。抗体介入被拒绝。中华外科杂志2015;
张建军,张建军,张建军,等。移植前HLA抗体的存在不影响慢性同种异体肺移植功能障碍的发展或与CLAD相关的死亡。移植。2016;
Safavi S, Robinson DR, Soresi S等。新供体hla特异性抗体预测肺移植后闭塞性细支气管炎综合征的发展。[J]中华心肺移植杂志,2014;33:1273 - 881。
lucraz H, Sharples L, McNeil K,等。供体/受体巨细胞病毒抗体状态不影响肺移植中闭塞性细支气管炎综合征的发生率。[J]心肺移植杂志,2003;22:287-91。
王晓东,王晓东,王晓东,等。阿奇霉素长期治疗闭塞性细支气管炎综合征:分而治之?[J]中华心肺移植杂志。2010;29(3):558 - 568。
李建军,李建军,李建军,等。限制性慢性肺同种异体移植物功能障碍:我们现在在哪里?[J]中华心肺移植杂志,2015;34(4):625 - 630。
特发性肺纤维化中肺损伤和纤维化的新细胞和分子机制。《柳叶刀》杂志。2012;380:680-8。
刘建军,李建军,李建军,等。预后良好的肺移植受者和闭塞性细支气管炎综合征的金属蛋白酶分析。移植。2015;99:1946-52。
Kistler KD, Nalysnyk L, Rotella P, Esser D.肺移植治疗特发性肺纤维化:系统文献综述。中华医学杂志,2014;14:139。
刘建平,刘建平。肺移植术后囊性纤维化患者的呼吸道感染。中华呼吸医学杂志,2014;2:73-82。
Wilkinson M, Langhorne CA, Heath D,等。低氧肺心病10例病理生理分析。中华医学杂志。1988;66:65-85。
张建军,张建军,张建军,等。肺动脉高压与肺移植、闭塞性细支炎和同种异体移植血管重构有关。中华医学杂志。2008;8:391 - 391。
致谢
Lena marde, Leif Eriksson, Jan-Otto Solem和Stig Steen教授。瑞典隆德大学sk
资金
一个也没有。
数据和材料的可用性
由于基于隆德大学sk
作者信息
作者及单位
贡献
MF构思了这项研究,参与了研究的设计,收集了患者数据,分析了数据,并撰写了论文。EB参与其设计,收集患者数据,分析数据,并帮助起草稿件。SL构思研究,参与研究设计,收集患者数据,分析数据,撰写论文。国际扶轮构想了这项研究,参与了它的设计并分析了数据。LA参与了它的设计并帮助绘制了手稿。LH参与了数据的设计和分析。BK参与了数据的设计和分析。RG参与了数据的设计和分析。PW参与了数据的设计和分析。所有作者都阅读并批准了最终的手稿。 The statistical analyzes were performed by Sidesoft AB, Malmo, Sweden.
相应的作者
道德声明
伦理批准并同意参与
本研究按照赫尔辛基宣言进行,并得到隆德大学隆德伦理委员会的批准,参考编号为2016/638。
发表同意书
不适用。
相互竞争的利益
作者宣称他们没有竞争利益。
出版商的注意
伟德体育在线施普林格·自然对已出版的地图和机构关系中的管辖权要求保持中立。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议(http://creativecommons.org/licenses/by/4.0/),它允许在任何媒体上不受限制地使用、分发和复制,前提是您要适当地注明原作者和来源,提供到知识共享许可协议的链接,并注明是否进行了修改。创作共用公共领域免责声明(http://creativecommons.org/publicdomain/zero/1.0/)适用于本文中提供的数据,除非另有说明。
关于本文
引用本文
Fakhro, M., Broberg, E., Algotsson, L.。et al。与单肺移植不同,双肺移植可能对死亡率和闭塞性细支气管炎综合征具有保护作用。J心胸外科12, 100(2017)。https://doi.org/10.1186/s13019-017-0666-5
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/s13019-017-0666-5
关键字
- 肺移植
- 闭塞性细支气管炎
- 移植排斥
- 移植物存活率
- 存活率