摘要
虽然提高在转化谱上进行的兽医临床试验的严谨性和可重复性的必要步骤包括了解该领域的现状,但以前没有对现有的兽医临床试验资源进行广泛的评估。由CTSA One Health Alliance (COHA)试点奖资助,该项目的目标是对北美兽医学院进行一项关于兽医临床试验审查、批准、实施和支持实践的电子调查,以确定利用现有资源和开发新资源的机会,以增强兽医和转化卫生研究的影响。
共有30所院校获邀参与调查,调查回应率为73%。兽医临床研究最常见的资金来源是工业界(33%);然而,应答者报告只有5%(3.7-11.0)的研究是fda监管的。答复者指出,大多数研究(80%);在他们的机构进行的是单点研究。95.5%的机构由IACUC单独或联合医院审查委员会进行研究审查和批准。与临床研究最佳实践相关的劳动力培训在各机构之间存在差异。
确定了通过统一临床研究审查和批准实践来加强基础设施的机会。这自然会导致多地点研究的扩展。根据受访者的反馈,未来的劳动力发展计划可能会集中在开展fda资助的研究、良好临床实践(GCP)、临床研究预算设计、拨款管理、不良事件报告、研究监测和电子数据采集平台使用等方面的培训。
背景
执行良好的兽医临床研究为兽医患者参与者、他们的主人和研究者提供保护,同时确保获得的数据从兽医和转化医学的角度提供最大的利益1,2。了解与兽医临床研究相关的当前基础设施对于制定基准和确定在何处战略性地关注基于需求的举措以发展和改善临床研究前景至关重要。CTSA One Health Alliance (COHA)是一组学术兽医中心,通过nih支持的临床和转化科学奖(CTSA)与当地医学院合作开展转化科学倡议。COHA的一个主要目标是通过兽医临床试验,利用自然动物疾病模型,促进卫生保健的进步,通过促进对病理生理学的了解和对跨物种共有疾病的治疗,使动物和人类都受益3.。虽然了解该领域的现状是提高在转化谱上进行的兽医临床试验的严谨性和可重复性的必要步骤,但以前没有对现有兽医临床试验资源进行广泛的评估。在COHA试点奖的资助下,该项目的目标是对北美兽医学院进行调查,记录兽医临床研究审查、批准、实施和支持方面的现行做法,以确定利用现有资源和开发新资源的机会,从而提高兽医和转化卫生研究的影响。
方法
调查发展过程
在CTSA同一健康联盟(COHA)试点方案的资助下,制定了一项电子调查,以收集有关机构人口统计、临床研究监督方法、基于风险的评估和监测的使用以及质量保证和其他监测做法的详细信息。调查的最终版本采用了质量测量系统(www.qualtrics.com),这是一个基于网络的调查管理软件程序。该调查包括49个问题,通过复选框方法或自由文本简短回答提供结构化的回答选项。对于一些问题,“其他”选项允许受访者提供额外的评论。
在调查开始时获得了所有受访者的知情同意。由于调查只要求与机构流程相关的数据,没有征求个人数据或意见,因此确定不需要大学机构审查委员会(IRB)的审查和批准。2019年11月4日,根据美国兽医学院协会(AAVMC)提供的名单,该调查以电子方式分发给北美大陆的所有兽医学校。调查持续了6周。发出两份电子提醒以鼓励完成调查。一个是在调查窗口的中途发送的,另一个是在调查结束前两天发送的。
分布
这项调查的对象是美国和加拿大的兽医学校/学院和学术兽医医院。电子调查通过电子邮件进行分发,并将调查访问的个性化链接直接发送给每所大学的研究副院长,并将副本发送给大学兽医医院院长和临床试验主任(如适用)。随附的电子邮件解释了调查的目的,并要求收件人提供代表其机构的单一回复。为了本调查的目的,受访者被告知兽医临床研究的定义是“涉及客户拥有的动物的任何前瞻性研究”,术语“兽医临床研究”和“兽医临床试验”可以被认为是可互换的。接受者还被提供了一份列出调查问题的word文档,以便于审查和讨论,并被鼓励与任何对其机构的兽医临床研究组合有最详细了解的人合作或转发调查。
统计分析
调查结束后,使用Qualtrics软件对数据进行分析和描述性统计。分类数据以选择该类别的受访者的总百分比报告,连续数据以中位数和90%置信区间报告。
结果
总体回应和受访者人口统计
共有30所院校获邀参与调查。共收到22所院校的完整回复,整体回应率达73%。没有收到部分调查回复。所有受访者都表示,他们所在的学院/学校、部门或医院将兽医临床研究作为其日常业务的一部分。完成调查的人士,有36.4% (n= 8例,教员(18.2%);n= 4),一名工作人员(18.2%;n= 4)、临床试验办公室主任或同等职位(13.6%;n= 3),兽医学院院长(4.5%;n = 1)或其他(9.1%;n= 2)。在68.2% (n= 15)个案中,院校表示他们是COHA成员,而31.8% (n= 7)我们没有。在那些目前不是COHA成员的机构中,有4家表示他们正在通过与当地学校或医学院合作,积极争取CTSA的资金。
临床研究基础设施
当被问及所在机构目前是否设有兽医临床试验办公室或其他集中的兽医临床研究单位时,59.1%的受访者表示有,40.9%的受访者表示没有。在设有兽医临床试验办公室的院校中,与该办公室相关的全职等效人员总人数中位数为4.3(2.2-6.0)。其中,负责病人护理的中位数全职工作时间为3.5(1.5-4.4),负责行政/管理职责的中位数全职工作时间为1.0(0.5-1.6)。
临床研究经费
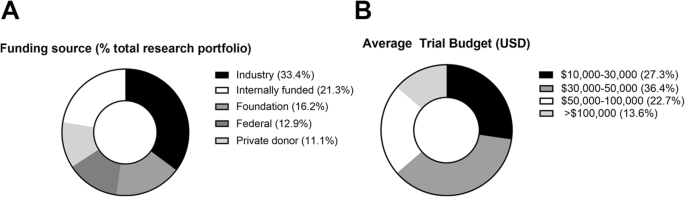
资金来源(占机构临床研究投资组合的百分比)和每个应答机构的平均临床研究总预算详见图。1。兽医临床研究最常见的资金来源是工业界(33.4%;23.2 - -43.5)。其他来源包括由首席研究员“启动”或其他内部资金资助的研究(21.3%;14.0- 28.6%),基金会的外部资金(16.2%;11.1-21.5),联邦补助金(12.9%;7.4-18.5),以及礼物/慈善机构/私人捐赠(11.1%;4.6 - -17.7)。尽管行业赞助的试验数量很多,但应答者报告说,只有5%(3.7% - 11.0%)的试验是由fda监管的。在薪酬补偿方面,受访机构表示,50%(33.3-65.0)的试点机构为全部或部分研究团队提供了某种程度的薪酬支持。最常选择的平均总研究预算(美元)为30,000-50,000美元(36.4%的回复率)。
临床研究的设计和实施
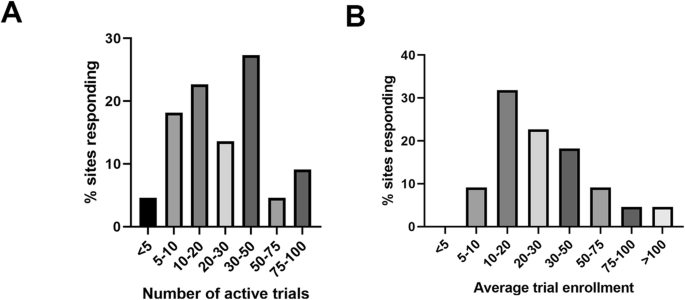
各机构被要求指出其临床研究组合中符合与研究设计和实施相关的各种标准的百分比。数字2详细说明过去三年中各调查机构与平均有效试验数量和平均每个试验患者入组相关的反应。当被要求估计其机构目前正在进行多少项试验时,最常选择的选项是30-50项正在进行的试验(27.3%的回应率),而少数回应机构表示少于5项正在进行的试验(4.5%)或75-100项正在进行的试验(4.5%)。在过去3年中,每次试验最常选择的平均总患者人数为10-20人(31.8%缓解率)或20-30人(22.7%缓解率)。
当被问及他们的机构在过去5年中是否进行了包括使用重组或合成核酸分子(例如基因治疗、重组DNA、疫苗研究)或基于细胞疗法的兽医临床试验时,大多数(63.6%)表示参加了评估客户拥有的动物中重组或合成核酸的研究。在开展结合细胞疗法的研究方面,77.3%的机构表示已经这样做了。
多机构研究参与
在多机构研究参与方面,受访者表示,大多数研究(80%;(65.5-84.4)为单点研究,而只有5%(4.6-13.0)为多点研究,受访者为主要研究机构。当被问及他们是否曾担任涉及私人诊所的研究的主要地点或分包商时,受访者分别有77.3%和22.7%的情况表示“是”。较小数量的机构(22.7%)表示曾作为临床研究的主要地点,而次要地点位于美国以外。此外,18.2%的人表示曾作为次要研究地点,而主要研究地点位于美国以外。
学习审查、批准和监督
机构被要求提供有关兽医临床研究在其机构开始之前如何审查和批准的信息。50%的人表示仅由机构动物护理和使用委员会(IACUC)审查,4.5%的人表示仅由医院特定兽医审查委员会审查,45.5%的人表示由IACUC和医院特定兽医审查委员会审查。本综述包括95.5%的机构对研究同意书的评估,大多数(90.1%)提供了同意书模板来指导研究者制定同意书。一旦启动,59.1%的应答机构的兽医临床研究接受了某种形式的常规批准后监测。批准后监测发生在每年(69.2%)、每三年(23.1%)或其他(7.7%)未提供其他频率进一步信息的情况下。该过程包括以下内容:要求PI提供迄今为止登记的动物数量(32.4%);要求PI在必要时更新研究方案(27.0%);要求PI在必要时更新研究团队(21.6%);审计同意书(8.1%);研究记录审核(5.4%); and other (5.4 %). Respondents who selected “other” were provided a free-text entry option to allow them to elaborate on what “other” items were monitored or reviewed. No additional information was provided by any of the respondents.
关于不良事件监测和报告,50%的受访者表示,他们的IACUC或医院审查委员会在兽医临床研究中有一个正式的不良事件报告程序。在那些有正式报告机制的机构中,63.6%的机构表示向IACUC报告了不良事件,18.2%的机构表示向其医院的审查委员会报告了不良事件,18.2%的机构表示仅向研究发起人报告了不良事件。
机构受访者被问及一系列关于在研究审查和批准过程中,伦理研究设计的某些元素在多大程度上被考虑。详细答复见表1。所有机构都表示,在审查和批准过程中,调查中提出的大多数要素至少被认为是中等重要的;然而,大多数调查机构认为极其重要的项目包括知情同意和对潜在和已登记受试者的尊重,而社会价值、科学有效性和有利的风险/效益比等项目的权重较低。
研究培训、行为和最佳实践
受访者被问及一系列问题,重点是他们所在机构的研究最佳实践和模式。详细答复见表2。当被要求估计研究者在临床试验开始前进行可行性分析的频率时,最常见的答案是“有时”(45.5%),18.2%和27.3%的机构分别选择了“总是”或“大部分时间”。当被问及使用电子实验室笔记或电子研究记录获取临床研究数据的频率时,最常见的回答是“有时”(54.6%),分别有9.1%和18.2%的受访机构选择“总是”或“大部分时间”。当被问及调查人员完成良好临床实践(GCP)培训的频率时,63.6%的机构选择了“有时”,这是最常见的回答。只有13.6%的机构表示,在开展临床研究之前,他们的研究人员“总是”或“大部分时间”完成了GCP培训。在63.6%的机构中,研究者在开始临床研究之前“总是”或“大部分时间”完成了负责任的研究行为(RCR)的正式培训。在4.6%的机构中,研究人员“总是”或“大部分时间”接受了预算制定方面的正式培训,没有机构表示研究人员在开始临床研究之前“总是”或“大部分时间”完成了拨款管理方面的正式培训。当被问及在研究进行中是否使用数据安全监测委员会或其他实体来监测患者安全和治疗效果时,只有18.2%的机构表示“总是”或“大多数时候”发生这种情况。
几个问题集中在围绕临床研究行为可行性的定量和后勤考虑方面。研究机构指出,68.1%的病例在研究开始前“总是”或“大部分时间”完成了样本大小的确定。当被问及先天的考虑到可能影响研究收益的因素,受访者表示,研究人员考虑了以下标准“总是”或“大部分时间”:一般人群中的疾病频率(91.0%);医院或特定项目的病例量(91.0%);现有的治疗模式或指南(81.8%);可获得替代药物或治疗(72.7%);医院内存在竞争性试验(57.1%);地理区域内存在竞争性试验(22.7%)。
发表研究设计和传播研究结果
该调查询问了几个关于机构对AVMA动物健康研究数据库(AAHSD)的熟悉程度和使用情况的问题,该数据库是新启动和正在进行的兽医临床研究的研究设计出版的集中平台,其目标是协助向北美的兽医和非专业人员传播研究行为和结果。调查对象表示他们“知道”或“不知道”AAHSD作为兽医临床研究营销工具的存在,分别占81.9%和18.2%。在知道该数据库的受访者中,22.7%的人表示他们的机构没有向AAHSD发布任何试验。在那些知道并向AAHSD发布信息的机构中,受访者表示发布了大约42.1%(25.4 - 58.7%)的正在进行的试验。大多数机构(54.5%)表示有指定的机构工作人员负责发布试验。当被问及调查机构多久会跟进公布的研究结果,并在本处提供最终结果或结论时,63.6%最初在本处公布研究结果的机构表示从未公布研究结果。
讨论
本研究的结果构成了对整个北美兽医临床研究实践的广泛调查,并表明即使不是所有的兽医学术机构,也有大多数进行临床研究。此外,存在审查和批准试验的普遍体制基础设施,无论是通过也审查和批准使用目的饲养动物的研究的IACUC,还是通过特定医院的审查委员会,或两者兼而有之。对于95.5%的应答机构,该审查在某种程度上涉及IACUC,对于几乎一半的机构,在开始之前,一个单独的医院审查委员会也审查了研究。兽医临床研究的适当审查可能是复杂的,因为它需要与《动物福利法》中可能与某些基于范围和资金来源的项目相关的部分相关的监管知识,但也包括必要的伦理和研究设计考虑(同意、风险/利益分析、利益冲突、相关结果的选择)的知识,这些知识更类似于irb对人类受试者研究的审查。兽医临床研究的正确审查和批准机构可能取决于当地的专业知识和现有的基础设施。美国兽医协会(AVMA)先前就兽医临床研究的审查机构的适当构成提供了一些指导,各种团体已经权衡了质量保证的方法4,5,6,7。无论哪个机构(或多个机构)审查和批准特定机构的兽医临床研究,我们的调查结果表明,审查标准和特定审查项目的个人重要性权重在不同机构之间存在很大差异。制定更统一的临床研究审查和批准方法,以及为IACUC和兽医医院董事会审查人员制定具体的指导方针和培训材料,有助于协调各机构之间的工作流程,并促进采用更统一的方法来审查多中心兽医临床研究。
这项调查的一个显著结果是,工业赞助的研究频率相对较高,但fda监管的研究频率较低。虽然这项调查并不是为了评估原因而设计的,也没有捕捉到这些研究的具体性质,但作者的经验表明,这些研究中的许多可能是临床前工作,评估研究性新疗法,之后可能打算寻求FDA对人类或兽医方面的批准。如果是这样,在这些研究的早期未能与FDA合作,可能意味着失去了让客户拥有的狗的数据作为未来研究性新药(IND)过程申请的补充材料的机会。兽医临床研究人员与FDA之间有限的互动可能源于研究人员对FDA流程的有限知识,并且可能提供培训机会,可以通过兽医临床试验的方式在转化治疗开发过程中增强兽医疾病模型的使用。
本调查中报告的主要研究是单点兽医临床研究,答复者表示,他们的临床研究组合中只有5%由多点研究组成。虽然这些结果并不令人惊讶,但它们确实强化了这样一个事实,即兽医研究人员在临床研究工作中往往相当“孤立”。受访者表示,他们对在其地理区域内存在竞争性试验的考虑有限,这进一步加强了这一点。多中心试验的重要性在人类临床研究中已经得到了很好的证明,其中包括多个地点可以提高研究结果的普遍性,确保公平的地理代表性,并大大提高试验入组和完成的效率。虽然兽医学最近有一些值得注意的多中心临床研究,如比较肿瘤学试验联盟(COTC)、犬脊髓损伤联盟(CANSORT-SCI)等,但单点研究的优势可能至少部分归因于与多点试验的审查、批准和实施相关的后勤困难8,9,10,11。目前,兽医临床研究的多中心研究的审查和批准是由地方机构委员会逐点管理的。对于多地点研究,目前多个地方评审的现状造成了研究评估方式的不一致,并导致多机构研究在跨地点达到充分功能能力的速度大幅降低6,11。这些障碍反映了在精简、多站点、加速试验资源(SMART) IRB开发之前存在于人类方面的障碍,该平台旨在缓解与启动多站点临床研究相关的常见挑战12,13。为了满足对兽医学中健全、一致和有效的临床研究审查和启动的需求,可能需要新的举措和跨机构流程。
当前调查中的问题集中在研究最佳实践方面,确定了劳动力培训方面的差距,以及开发解决这些差距的资源的机会。具体而言,似乎需要以良好临床实践(GCP)培训、临床研究预算设计、拨款管理、不良事件报告、研究监测和电子数据捕获平台(如研究电子数据捕获(REDCap))的使用为中心的劳动力发展和相关资源。最近,COHA开发并发布了一个针对兽医临床研究的基于网络的GCP培训模块,以及不良事件报告的标准化模板。两者都可以访问https://www.ctsaonehealthalliance.org/。在进行这项调查时,两者都没有公开发布。
结论
该调查显示了加强兽医临床研究基础设施的重要机会,通过有针对性地协调临床研究审查和批准实践,这可能自然地导致多地点研究的扩大。在开展fda资助的研究、GCP、临床研究预算设计、拨款管理、不良事件报告、研究监测和电子数据捕获平台的使用等方面,确定了劳动力发展的额外机会。以提高严谨性和可重复性为目标,旨在加强兽医临床研究前景的研究计划应侧重于这些有记录的需求领域。
数据和材料的可用性
数据共享不适用于本文,因为在本研究中没有生成或分析数据集。
参考文献
Fürdös I, Fazekas J, Singer J, Jensen-Jarolim E.临床试验在动物肿瘤中的应用。J翻译医学。2015; 13:265。2020年8月5日发布。doi:https://doi.org/10.1186/s12967-015-0631-9。
李建军,李建军,李建军,等。伴侣动物:转化科学家最好的新朋友。科学与医学。ps21 2015; 7(308): 308。https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4806851/。2020年4月29日发布。doi:https://doi.org/10.1126/scitranslmed.aaa9116。
李建军,李建军,李建军。基于生物信息学的动物医学、人类医学和“一种健康”研究进展——由美国兽医信息学协会(AVI)和美国兽医信息学会(COHA)联合发表的论文。JAMIA开放。2020; 3(2): 306 - 317。https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7382640/。2020年8月5日发布。doi:https://doi.org/10.1093/jamiaopen/ooaa005。
刘建军,刘建军,张建军,张建军,张建军,张建军。机构动物护理和使用委员会临床研究的审查。美国兽医协会。2018, 253(8): 980 - 984。2020年4月1日发布。doi:https://doi.org/10.2460/javma.253.8.980。
李建军,李建军,李建军,李建军,等。非管制兽医临床研究的质量保证与最佳研究实践。BMC兽医中心。2017; 13。https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5559838/。2020年8月5日发布。doi:https://doi.org/10.1186/s12917-017-1153-x。
Page R, Baneux P, Vail D,等。癌症伴侣动物临床试验的实施、监督和伦理考虑:最佳实践建议研讨会报告。J兽医实习生。2016; 30(2): 527 - 535。2020年8月5日发布。doi:https://doi.org/10.1111/jvim.13916。
建立和使用兽医临床研究委员会。美国兽医协会网站。https://www.avma.org/resources-tools/avma-policies/establishment-and-use-veterinary-clinical-studies-committees。2020年8月5日发布。
Gordon I, Paoloni M, Mazcko C, Khanna C.比较肿瘤试验联盟:利用狗自发发生的癌症为癌症药物开发途径提供信息。科学硕士。2009; 6(10)。https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2753665/。2020年8月5日发布。doi:https://doi.org/10.1371/journal.pmed.1000161。
李建军,李建军,李建军,等。国际犬脊髓损伤(CSCI)观察登记的发展:一个优化SCI转化研究的协作数据共享网络。脊髓。2018; 56(7): 656 - 665。https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6035082/。2020年4月21日发布。doi:https://doi.org/10.1038/s41393-018-0145-4。
兽医创伤登记处。顶级伴侣动物医学。2019; 37:100365。2020年8月5日发布。doi:https://doi.org/10.1016/j.tcam.2019.100365。
张建军,张建军,张建军,等。基于多机构研究网络的翻译数据库研究。顶级伴侣动物医学。2019; 37:100363。2020年8月5日发布。doi:https://doi.org/10.1016/j.tcam.2019.100363。
柯柏N,维特E, cerone M,等。SMART IRB平台:多站点研究的国家IRB审查资源。中华临床医学杂志。2019; 3(4): 129 - 139。2020年8月5日发布。doi:https://doi.org/10.1017/cts.2019.394。
机构审查委员会:目的与挑战。胸部。2015, 148(5): 1148 - 1155。2020年3月12日访问。doi:https://doi.org/10.1378/chest.15-0706。
致谢
不适用。
资金
该项目的部分资金来自CTSA同一健康联盟的试点奖励以及NCATS UL1TR002733和NCATS R21TR003191。资助机构在研究的设计、数据的收集、分析和解释方面没有发挥任何作用。
作者信息
作者及单位
贡献
SAM, AMW, JRC NJO和CL开发了这项调查,并且是撰写手稿的主要贡献者。所有作者都阅读并批准了最终的手稿。
相应的作者
道德声明
伦理批准并同意参与
不适用。
发表同意书
不适用。
相互竞争的利益
作者宣称他们没有竞争利益。
额外的信息
出版商的注意
伟德体育在线施普林格·自然对已出版的地图和机构关系中的管辖权要求保持中立。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,该协议允许以任何媒介或格式使用、共享、改编、分发和复制,只要您适当地注明原作者和来源,提供知识共享许可协议的链接,并注明是否进行了更改。本文中的图像或其他第三方材料包含在文章的知识共享许可协议中,除非在材料的署名中另有说明。如果材料未包含在文章的知识共享许可中,并且您的预期用途不被法律法规允许或超过允许的用途,您将需要直接获得版权所有者的许可。如欲查阅本许可证副本,请浏览http://creativecommons.org/licenses/by/4.0/。创作共用公共领域免责声明(http://creativecommons.org/publicdomain/zero/1.0/)适用于本文中提供的数据,除非在数据的信用额度中另有说明。
关于本文
引用本文
摩尔,s.a.,麦克利利-惠勒,a.a.,科茨,J.R.et al。CTSA同一健康联盟(COHA)对北美兽医机构临床试验基础设施的调查。BMC兽医中心17, 90(2021)。https://doi.org/10.1186/s12917-021-02795-z
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/s12917-021-02795-z