材料与方法
细菌隔离
从玉米中分离到根状细菌(玉米l)越南本特省根际采集。土壤悬浮液是通过在磷酸盐缓冲盐水中以180转/分钟的速度震动根系和粘附的土壤获得的。连续稀释悬浮液,铺于King 'B培养基(KB) [24], 30°C孵育24小时。取单个菌落,在固体KB上重新培养几次,以获得纯培养物。荧光的存在假单胞菌在紫外光下进行检查。用不同浓度的NaCl(0 ~ 10%)培养菌株,评价其耐盐性。
细菌鉴定
表型方面,根据Bergey’s Manual of Determinative Bacteriology的形态学和化学分类学特征对菌株进行鉴定。对于基因分型,使用Wizard基因组DNA纯化试剂盒(Promega, USA)提取和纯化细菌基因组DNA。用通用细菌引物27F和1492R PCR扩增16S rDNA(附加文件)1:表S1) [25].PCR产物测序后用BLASTn进行分析,鉴定菌株属。同时,一个碎片rpoD用引物rpoD 70F和rpoD 70R对基因进行扩增1:表S1) [26,27].亲缘种和属的序列从GenBank中获得。使用ClustalX进行多个序列比对;采用邻居连接法进行系统发育分析。系统发育树用MEGA version 6软件构建[28].
植物生长条件和处理
以确定细菌是否对种子萌发有影响拟南芥在正常和生理盐水条件下,无菌和同步的种子接种细菌悬液(106CFU/ml),或MgCl2作为对照或非促生长菌株的溶液大肠杆菌DH5α作为阴性对照,并在固态、半强度Murashige和Skoog培养基(MS½)上萌发,加或不加150 mM NaCl。将平板放置在22°C的生长室中,光周期为16/8小时(明/暗)。播后4 d (DAS)测定种子发芽率。
研究…的效果假单胞菌PS01上拟南芥在不同NaCl浓度下,4天大的幼苗转移到添加不同浓度盐的固体MS½中。将平板垂直放置在22°C的生长室中,光周期为16/8 h(明/暗)。7 d后测定植株存活率。
RNA提取和实时PCR (RT-PCR)分析
在单独移植到MS½或添加150 mM NaCl 24小时后,对幼苗进行RNA提取。使用Trizol (Invitrogen™,USA)方法获得RNA。RT-PCR使用Luna Universal One-Step RT-PCR试剂盒(New England Biolabs, USA)进行。PCR引物见附加文件2:表S2。相对转录水平(RTL)通过归一化计算ACT2RTL = 2∆∆Ct,其中∆∆Ct =∆Ct(基因)−∆Ct(ACT2).所有试验均进行了3个生物重复和2个技术重复。
统计分析
对于处理间的比较,采用Graphpad Prism 7.0进行方差分析。
结果
细菌鉴定
从玉米根际分离到17株根际细菌。耐盐性能测试结果表明,在17个被测菌株中;只有命名为PS01的分离株在8% NaCl的存在下能够生长3.:图S1)。从其生长曲线来看,PS01菌株的最佳生长温度为30℃。形态学和化学分类学分析显示,PS01为棒状,革兰氏阴性,需氧,不形成孢子,过氧化氢酶阳性和氧化酶阳性,在365 nm紫外光下荧光(附加文件)4:图S2)。对16S rDNA进行BLAST比对GenBank,发现PS01最相似假单胞菌在本属植物中rpoD基因被认为是基因系统发育的最佳生物标志物之一,其与16S rRNA基因具有良好的相关性[26,27,29,30.].因此,rpoD在我们的研究中用来鉴定PS01。的系统发育树rpoD基因提示PS01属于假单胞菌putidasubclade(无花果。1).
假单胞菌PS01在盐胁迫条件下提高种子发芽率
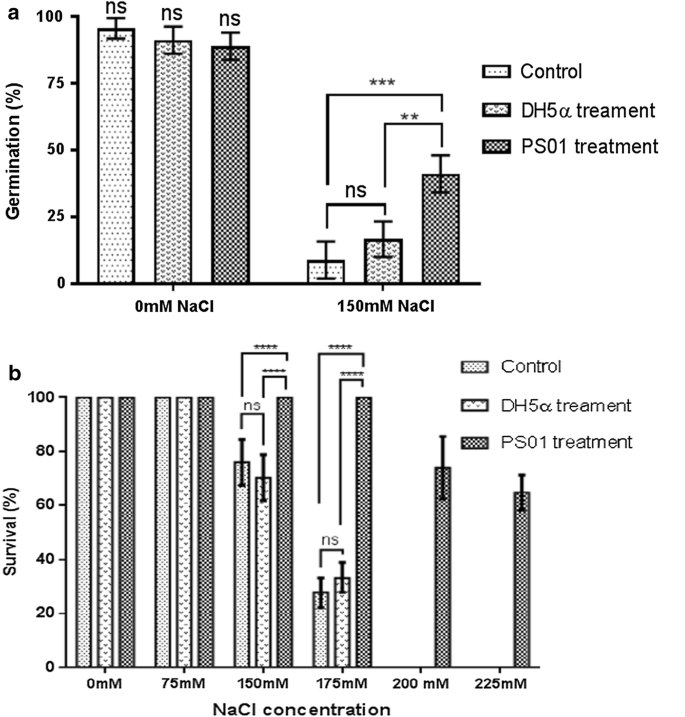
试验PS01是否能提高种子的发芽率答:芥,在MS½介质加150 mM NaCl或不加150 mM NaCl中检测其效果。我们观察到,与对照相比,接种ps01的种子在150 mM NaCl处理下的发芽率显著提高。PS01-treated答:芥种子的发芽率为30.7%,而对照组的发芽率仅为9.5%(图2)。2a).但在MS½中,接种种子与未接种种子的种子发芽率没有显著差异,说明PS01处理对种子发芽率没有影响答:芥在正常条件下萌发。
假单胞菌PS01增强耐盐性
研究了NaCl和PS01对答:芥体外耐盐性,在添加了75 ~ 225 mM NaCl的培养基上,评价了接种和未接种ps01的植株的存活率(%)。在转移到盐胁迫培养基的第7天,拟南芥观察幼苗并拍照以确定存活植株的数量。
PS01根定殖被证明可以增加暴露在75 ~ 225 mM NaCl盐浓度下的植物的存活率(附加文件)5:图S3)。例如,所有接种了PS01的植株都能在175 mM NaCl处理下存活,而对照组只有30-40%(图4)。2b).这些结果表明假单胞菌PS01可能增强答:芥盐胁迫下的生存。
假单胞菌PS01诱导盐胁迫的转录变化答:芥植物
目的:探讨ps01诱导植物耐盐性的分子机制拟南芥,一些与早期盐胁迫反应相关的基因,如ROS清除(APX2)、排毒(GLYI7), ABA信号(RD29A而且RD29B)和JA合成(LOX2)进行RT-PCR定量分析。这些基因的基因表达谱来自4个不同的样品:接种或未接种PS01的幼苗,在MS½中单独生长或转移到添加150 mM NaCl的MS½中生长。
盐胁迫24 h后,所有5个基因的转录表达均显著高于对照(仅在MS½上生长的幼苗)。分析显示没有差异RD29A而且RD29B在NaCl处理下ps01接种苗和未接种苗的表达。相比之下,LOX2在盐胁迫下,接种ps01的植株表达上调APX2而且GLYI7显著下调(图;3.).
讨论
PS01是第一个假单胞菌在越南分离的菌株,减轻了盐度对植物生长的影响。PS01属于假单胞菌putida的子分支rpoD基因树(图1),与…密切相关的p . taiwanensis(GenBank登录号HE577796.1)。有趣的是,p . putida已经知道可以减少盐度对发芽和植物生长的不利影响[7,31].
在这项研究中,假单胞菌PS01提高了种子的发芽率答:芥在盐胁迫介质(MS½加150 mM NaCl)上。与以往重点研究细菌对植物生长的影响相比,其萌发过程加快,萌发周期也延长[32].例如,p . putidaR4和p . chlororaphisR5对NaCl胁迫的响应能力分别提高了64%和73% [7].相比之下,假单胞菌spp. PDMZnCd2003对水稻萌发有负向影响,幼苗茎长和根长减少[33].我们已经证明PS01有助于提高盐胁迫耐受性答:芥幼苗。在盐胁迫条件下,转录水平升高GLYI7而且APX2接种PS01的苗的生长速率低于未接种的苗。在植物的非生物胁迫反应中,乙醛酶可以被认为是一种警报[34].反过来,抗坏血酸过氧化物酶催化H2O2在H2的下调GLYI7而且APX2提示接种PS01可以降低植物的胁迫水平。因此,接种植物在盐胁迫下存活的机制可能与其他分子途径有关。另外,正如最近的报道所示,细菌产生的生物膜可能有利于植物在胁迫条件下的生存,其中细菌胞外多糖(EPS)和生物膜的形成通过减少钠来刺激盐胁迫下植物的生长+被植物吸收[20.,35].然而,EPS的产生或其他可能的机制参与ps01介导的植物耐盐性还需要进一步的验证。
茉莉酸盐(JA)是盐胁迫反应的积极调节因子,在植物受到胁迫时迅速积累[20.,36].LOX2编码脂氧合酶,脂氧合酶是JA合成途径的重要组成部分[37].与未接种苗相比,幼苗对盐胁迫的响应增加LOX2本研究中PS01接种苗的表达与Cho et al.[14]和Poupin et al.[38]一致,他们也报道了PGPR如绿假单胞菌O6而且伯克phytofirmansPsJN通过增加JA途径调控的防御基因的表达来介导对非生物胁迫的系统性抗性[14,38].为了阐明这一途径,我们将分析接种PS01的植物在不同生长阶段的表型变化、转录谱和盐胁迫下的时空响应。
结论
我们的研究表明假单胞菌PS01可以提高拟南芥盐胁迫下种子萌发及成活率。