摘要
背景
了解对SARS-CoV-2病毒的免疫反应对有效监测和控制策略至关重要。先知-19队列对SARS-CoV-2感染后的抗体动力学进行了细致的描述,并在17个月的时间内获得了异常的分辨率。
方法
我们在巴塞罗那北部建立了769名医护人员队列,包括健康的和感染SARS-CoV-2的医护人员,以确定感染医护人员中抗SARS-CoV-2核衣壳(N)的IgM和抗SARS-CoV-2核衣壳(N)的IgG的动力学。研究期间为2020年5月5日至2021年11月11日。我们使用非线性混合模型来研究从诊断之日起17个月的9个时间点测量的IgG和IgM的动力学。该模型包括时间、性别和疾病严重程度(无症状、轻-中度、重-危重)等因素,以评估它们的影响和相互作用。
发现
769名参与者中有474人(61.6%)感染了SARS-CoV-2。所有三种抗体的水平均受性别和疾病严重程度的显著影响。在诊断后270天,无症状和轻中度疾病患者的中位IgM(N)水平已经低于阳性阈值,而IgG(N和S)水平至少分别到450天和270天仍保持阳性。动力学模型显示,直到第30天,IgM(N)和IgG(N)水平普遍上升,随后衰减,衰减速率取决于疾病的严重程度。IgG(S)水平从第15天开始随着时间的推移保持相对稳定。
解释
IgM(N)和IgG(N, S) SARS-CoV-2抗体在17个月的时间内表现出非均质动力学。只有IgG(S)表现出稳定的增加,抗体的水平和动力学随疾病的严重程度而变化。一年多观察到的IgM和IgG的动力学也随临床谱的变化而变化,这对制定成人人群免疫标准的公共卫生政策非常有用。
资金
加泰罗尼亚大区卫生部(呼叫COVID19-PoC SLT16_04;NCT04885478)。
背景
可通过测量病毒特异性抗体水平来检测SARS-CoV-2感染,这反映了对最近或以前感染的免疫反应[1].几项研究描述了SARS-CoV-2感染中针对刺突(S)糖蛋白表位和核衣壳(N)蛋白的各种免疫球蛋白同型(IgA、IgM、IgG)的快速增加[2,3.,4,5].
COVID-19是由SARS-CoV-2引起的疾病,具有广泛的临床谱系,包括从无症状感染到危重疾病的各种临床表现形式。同样,抗体对SARS-CoV-2感染的反应也是异质性的[6].很少有纵向研究在临床范围内进行血清学随访,研究持续时间有限,在80至270天之间[2,3.,4].一项早期研究报告了抗体的快速上升和随后的下降,抗体在后来的时间点稳定下来,表明对SARS-CoV-2的免疫力可能在感染后至少持续120天[7].后来的两项研究表明,这种保护作用至少可持续180天[2,8],而最近的其他报告称,它至少会持续一年[9,10].然而,关于SARS-CoV-2感染的动力学和免疫反应的知识仍然有限,需要更大、更详细的纵向研究来确定抗SARS-CoV-2抗体的半衰期。
在为数不多的研究抗体动力学的研究中,只有一项研究了IgM抗体[10].这些研究都没有超过五项测量值[11].此外,所有的研究都建立了线性或黄土回归模型,这使得无法获得先前动力学研究所表明的代表抗体反应的非线性和异质性的模型。使用非线性模型而不是线性或黄土模型可以获得抗体动力学的更真实的表示,这可以更好地解释抗体的行为。
世卫组织建议,应使用标准化试剂使用酶联免疫吸附测定法(ELISA)或免疫荧光测定法(IFA)进行基于人群的通用血清学检测[12].使用符合世卫组织抗sars - cov -2抗体国际标准的试剂可以评估疫苗的有效性,并联合和比较流行病学和免疫监测研究。在大流行开始时,使用定性测定法确定抗体水平;而使用国际标准化的酶免疫测定法定量检测特异性IgG抗体则是最近的研究[13].拥有更多样本点和更准确统计分析的研究能够更好地评估疾病负担和传播,更好地为应对COVID-19的公共卫生努力提供信息[9,14].
本研究的目的是描述抗SARS-CoV-2抗体IgM (N)和IgG (N, S)的动力学,并评估其与临床谱和其他因素的关系。我们的研究结果详细描述了在抗击大流行方面发挥最关键作用的人群对病毒的免疫反应。我们的研究结果可以指导公共卫生政策制定更有效的COVID-19监测、治疗和预防策略。
方法
研究设计与伦理
ProHEpiC-19是一项前瞻性的纵向研究,涉及巴塞罗那(西班牙)北部大都市区的两组卫生保健工作者(健康和感染)。基金会大学初级卫生保健研究所Jordi Gol i Gurina (IDIAPJGol)(参考文献20/067)和德国Trias i Pujol研究所(IGTP)(参考文献cov20 /00660 (PI-20-205))的伦理委员会批准了该研究方案,该研究方案已在ClinicalTrials.gov上发表(NCT04885478,注册日期为13/5/21)。该研究招募的所有参与者都被充分告知了ProHEpiC-19方案,并签署了参与的知情同意书。他们同意将收集到的数据用于研究,并同意适用的法规、隐私政策和使用条款。根据基于顺序的数字编码系统对参与者数据进行匿名化,并安全地存储在数据库中。该数据库将在研究完成后维持15年。
没有参与者或公众直接参与报告数据的设计或分析。研究的资助方在研究设计、数据收集、数据分析、数据解释或报告撰写中没有任何作用。通讯作者(CV)拥有对所有数据的完全访问权,而LACR、ARLL、DO、JMMD和AP;可以接触到原始数据。
参与者招募,跟进
在2020年3月3日至2021年3月22日期间,招募了在第一、第二或第三波COVID-19期间直接接触患者的卫生保健工作者(医生、护士、护理助理和其他基本工作人员)。纳入标准是同意参加并确认他们在第一次来访后第7、15、30、60、90、180、270、360和450天以及第18、24、30和36个月(基线)的随访时间。第一次随访是在2020年5月5日,最后一次是在2021年11月11日。访问次数少于两次的参与者被认为是辍学生。在基线时,根据RT-PCR以及IgM(N)和IgG(N)抗体测试将参与者分组(感染或未感染):如果两项测试中的任何一项呈阳性,则认为参与者感染了。如果未感染的参与者被感染,他们作为感染的参与者重新开始研究,在上述指定的日期重复血清学测试。本研究报告的分析只包括了SARS-CoV-2抗体阳性的参与者,被认为是感染的参与者。
在基线访问期间,参与者完成了几份临床问卷,并接受了covid -19特异性症状的检测,同时进行了鼻咽拭子RT-PCR检测和抗体测试。在基线随访7天后,第二次随访时重复RT-PCR检测。在基线随访后15、30、60、90、180、270、360和450天重复抗体测试。第0天定义为从诊断之日起的第0天。接种疫苗后,IgG(S)水平的分析停止,IgM(N)和IgG(N)水平的分析继续进行。受感染的参与者根据症状分为三个不同的疾病严重程度亚组:(1)无症状:无症状;(2)轻-中度:有一种或多种具有新冠肺炎特征的临床症状且不需要住院的人;(3)重症:需要住院治疗的患者。包括健康组在内的整个ProHEpiC-19队列在基线时的特征描述在表中1.
SARS-CoV-2的IgM和IgG检测及定量分析
RT-PCR作为主要诊断试验。使用STARMag 2019-nCoV试剂盒,通过液体分配机器人从新鲜样品中提取用于RT-PCR检测的RNA。RNA检测使用Allplex SARS-CoV-2检测方法进行,这是一种多重RT-PCR检测方法,能够在单个试管中检测到4个SARS-CoV-2靶基因。针对抗体测试,我们对6种不同的市售和ivd - ce批准的ELISA测试进行了预验证研究,并根据其性能选择了抗sars - cov -2 IgG(N)和IgM(N)酶免疫测定(ELISA)试剂盒。用DECOV1901 ELISA试剂盒检测和测量感染参与者的抗SARS-CoV-2刺突(S)亚基抗体水平,该试剂盒可定量测量IgG。请参阅研究协议NCT04885478(也作为附加文件附上)1)查阅更多资料。
数据源
我们使用了两个数据源:(1)为ProHEpiC-19队列创建了一个数据库。该数据库在加泰罗尼亚卫生研究所的一个集中数据仓库中存储、管理和验证,适用于管理专业人员的人口统计、社会和临床数据;(2)新型冠状病毒抗体检测结果;(3) RT-PCR检测结果。(4)我们还实现了针对本研究的基于teleform的数据收集,其中包括唯一的数字患者标识符以及血清学和免疫学测试结果。唯一的数字患者标识符允许链接两个数据源。
样本大小
样本量和功率估计可在补充协议中找到。对收集的478个受感染参与者(来自三个亚组的72,367和39)的总样本进行单因素方差分析,估计可以达到100%的检验能力,以0.05显著性水平和η效应量的F检验来检测平均数与相等平均数之间的差异2= 0.06。
统计分析
仅在以下社会人口变量中存在缺失值:教育(3.5%)、婚姻状况(4.6%)和国籍(7.5%)。
抗体检测的演变被认为是一个分类(即阳性/阴性结果)和一个连续的标量变量。采用描述性分析来描述每个时间点的免疫反应,分类变量的出现和频率以及确认非正态分布的数字变量的中位数和四分位间范围。抗体水平根据时间、疾病严重程度和性别进行分析。我们根据确诊后的天数对抗体水平进行分层,用箱线图描述它们,并用Kruskal-Wallis检验比较时间点,然后用Holm-adjusted Dunn 's检验。然后,在每个时间点,根据疾病严重程度(Kruskal-Wallis和Holm-adjusted Dunn测试)和(Mann-Whitney测试)评估差异U测试)。为了更详细地描述抗体动力学,我们还拟合了局部估计的散点图平滑模型(黄土),并计算了其95%置信区间(ci)。黄土是一种探索性的、非参数的技术,灵活、快速、容易地用于确定抗体水平的演变是线性的还是非线性的。黄土对勘探有用,但它不能提供描述演化的回归方程,也不能提供回归系数和p值来进行推断和组间比较。黄土表明抗体的演化是非线性的,并且由于抗体水平是来自不同时间点的重复测量,因此需要使用非线性混合效应模型(NLME)来拟合回归模型。最后,拟合非线性混合效应模型(NLME),得到表征抗体动力学的曲线。在这些模型中,每个参数都假设具有固定和随机效应。黄土和NLME模型首先对所有患者的数据进行拟合,然后根据疾病严重程度和性别对数据进行分层。基于残差分析进行模型诊断,采用赤aike和贝叶斯信息准则(AIC和BIC)检验拟合优度。对于除黄土外的所有分析,从诊断开始的时间被离散到时间箱中,因此在指定时间点之间进行的测试被认为是在较早的时间点进行的。 Therefore, tests performed in the first 14 days since diagnosis are treated as “Day 0” and tests performed between day 450 and 615 (i.e. the last day observed, see Table1)被视为“第450天”。有关时间箱的完整列表和描述,请参见附加文件1:表S1。
所有检验均为双侧检验,统计概率p < 0.05被认为是显著的。所有分析均使用R版本4.0.4进行。参见附加文件1有关统计方法的更多信息。
结果
参与者的特征
共招募了860名参与者,其中769人符合条件;443人(57.6%)在基线时检测呈阳性,31人(4%)在随访期间首次出现SARS-CoV-2抗体检测阳性1:图S1表1).女性通常有无症状或轻微的疾病,而男性往往有更严重的疾病(p值= 0.001)。根据疾病严重程度和性别,具体临床症状流行率的差异见附加文件1:表S2。
Seroprevalence
表格2A表示在每个时间点抗体检测结果的每种可能组合的频率。在基线时,超过三分之一的参与者(38.7%)所有抗体检测均为阴性,但这一比例随着时间的推移而下降。从感染的第15天到第180天,超过45%的参与者的所有抗体检测都呈阳性。然而,从第180天开始,这一比例也下降了,因为IgM(N)值为阳性的参与者数量下降了。到第270天,11.8%的参与者在所有抗体测试中呈阴性,而88.2%的参与者在至少IgG(N)或IgG(S)测试中呈阳性。如表2B显示,68.2%的参与者在第360天仍有高于阳性阈值的IgG(N)值。
按性别和疾病严重程度分层的SARS-CoV-2抗体水平
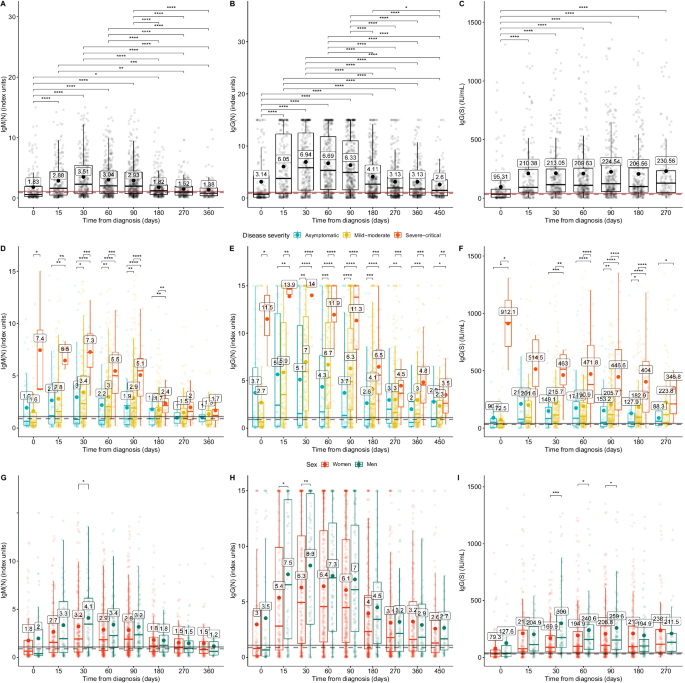
我们发现在不同临床条件下,所有抗体水平在统计学上有显著差异(总体和两两比较p < 0.001)。所有免疫球蛋白的抗体水平在男性和女性之间也有显著差异:IgM(N) (p = 0.01), IgG(N) (p < 0.001), IgG(S) (p = 0.006)。
数字1显示不同时间点抗体水平的差异。两两比较显示,从第270天开始,IgM(N)和IgG(N)水平与第0天不再有显著差异(图2)。1a - b)。IgM(N)和IgG(N)水平从第30天开始呈上升和下降趋势(图)。1A-B),而IgG(S)水平在第15天首次上升后保持相对稳定(图。1C).危重症患者的所有抗体水平在第180天(IgM(N))、第450天(IgG(N)和第270天(IgG(S))时最高(图)。1D-F)。结果的p值如图所示。确诊270天后,无症状和轻度疾病患者的中位IgM(N)水平低于阳性阈值(图。1D)。然而,IgG(N, S)水平在第360天仍然超过了这一阈值(图。1E-F)。在性别方面,男性在第30天所有抗体的水平高于女性(图。1G-I)和IgG(S)的第60天和第90天(图。1我)。
IgM和IgG的动力学
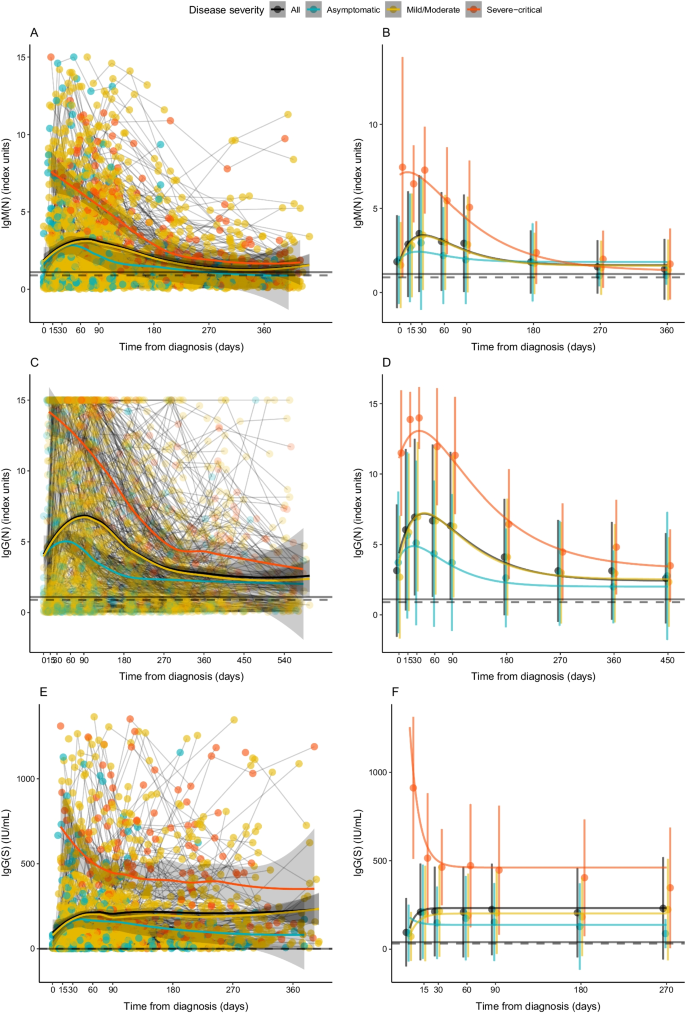
IgG(N)和IgG(S)有不同的动力学过程。与三种抗体按疾病严重程度分层的动力学相关,黄土(Fig。2A, C, E)和NLME(图。2B、D、F)的IgM(N)和IgG(N)水平在第30天普遍升高,随后出现衰减,且峰值的高度和衰减速率均与疾病的严重程度有关。IgG(S)水平在第15天增加,随着时间的推移保持相对稳定。
额外的文件1:表S3显示了对NLME曲线的每个分量估计的参数。每个模型的Q-Q图可在附加文件中找到1:图S2。危重期IgM(N)和IgG(N)初始水平均显著升高。无症状组血清IgM(N)水平下降较快,重症组血清IgM(N)水平下降较轻、中度组慢。这种较慢的下降也发生在IgG(N)中。与之前的分析类似,在所有时间点,IgG(S)水平随着疾病严重程度的增加而增加,在所有组中,从第30天开始,IgG(S)水平几乎保持不变。
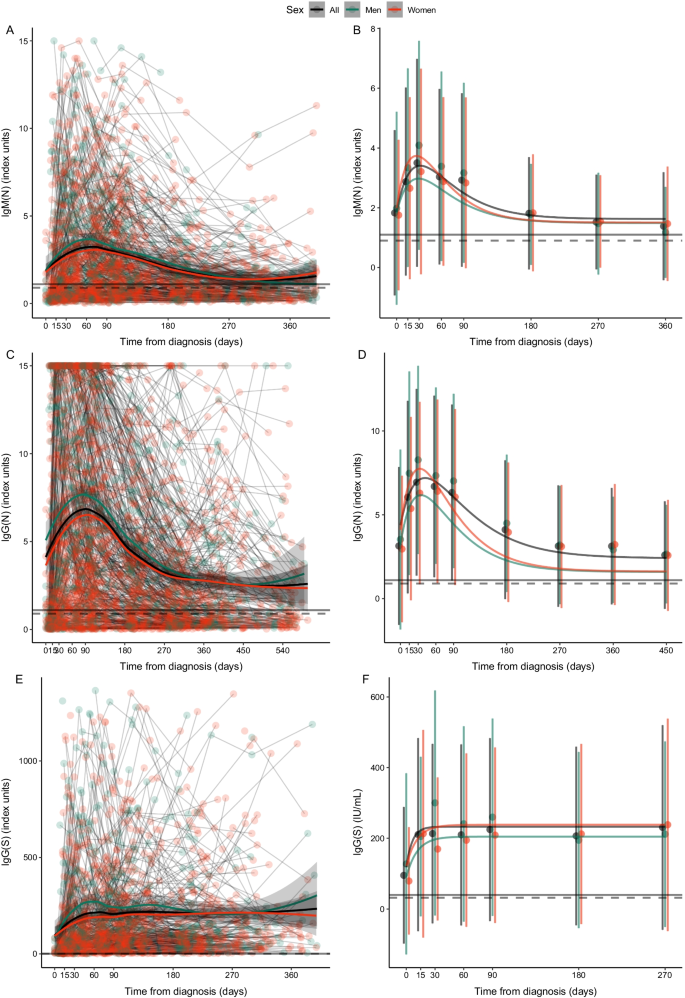
数字3.演示了按性别分层的动力学。除了男性抗体在第30天达到峰值外,这三种抗体的进化模式几乎完全相同。相应地,男性的初始增长率也更高。这些NLME曲线的参数也可以在附加文件中找到1:表S3。
讨论
我们的研究从使用大量的、有代表性的、特征良好的、分层的医疗工作者样本的纵向数据中获得优势。对SARS-CoV-2的免疫反应因疾病严重程度不同而不同。我们的研究结果表明,三种研究的同型抗体反应在感染后15天内开始。此后,它们的行为会根据疾病的严重程度而不同。我们发现,与无症状感染相比,严重感染患者的抗体水平更高[11].我们的结果也证实了IgG(N)和(S)的早期出现[6,14]
无症状患者抗体水平维持在IgM(N)阈值以上长达180天,而IgG(N)和(S)抗体水平维持在阳性阈值以上直到270天。然而,IgG(N)抗体的长期存在及其保护作用需要进一步研究[15,16与无症状患者相比,轻-中度COVID-19患者的IgG抗体水平更高,IgM(N)水平在整个随访过程中也高于阈值。这些发现与IgM(S)纵向研究180天报告的结果相似,可以用B细胞向IgM记忆浆细胞的分化来解释,这些细胞持续产生IgM同型抗体至少一年[17].最近的另一项研究也发现,IgM水平的阳性持续时间长达一年,尽管是IgM(S)而不是IgM(N)的同型。重症患者在随访的前30天抗体水平高于其他组,并在整个随访期间保持所有三种同型抗体的最高水平。这与其他在较短时间内进行的研究结果一致[9,18]
黄土模型描述抗体水平的轨迹,而NLME允许比较分层轨迹,同时考虑抗体水平动力学的非线性。我们的研究进一步阐述了体液免疫反应的动力学,同时适当地解释了其特征和影响因素,并根据模型选择进行了论证。我们的研究结果可以更好地为保持社会距离和(重新)接种疫苗政策提供信息。动态抗体结果对流行病学模型和公共卫生措施的设计和实施至关重要,如社会距离政策和疫苗接种模型。然而,关于抗体动力学的价值以及防止感染或疾病严重程度的额外信息应增加对公共卫生政策决策的影响。此外,通过应用相应的转换因子,我们的分析可以很容易地用于估计在其他单位测量的抗体水平。同样,它们也可用于调查接种疫苗后的动力学,从而将疫苗的有效性与因感染而接种的疫苗进行比较,并告知再接种的标准。
到目前为止,我们的研究对SARS-CoV-2感染后IgG(N)和IgG(S)产生的动力学提供了最详细和比较的描述。IgG(N)水平迅速上升,然后随着疾病的严重程度呈斜率下降,在第270天和360天之间趋于稳定。相反,IgG(S)动力学从感染后第30天开始呈现平台期。另一项研究也报告了这种差异[19],这可能是由于SARS-COV-2的S蛋白和N蛋白在分子结构、病毒颗粒中的丰度以及它们的特定功能方面的差异。前者促进病毒进入宿主细胞,后者则在病毒基因组包装中起作用[20.].监测IgG N和S抗体可以帮助识别由两种不同抗原引发的记忆细胞刺激。特纳等人[17]分析了恢复期患者骨髓中s特异性浆细胞的频率,观察到SARS-CoV-2感染能够诱导静息记忆B细胞和长寿骨髓浆细胞,支持感染者存在强大的体液免疫记忆。Cohen KW等人证实了前一种结果,并分析了SARS COV-2特异性t细胞[21].有趣的是,他们发现CD4 + T细胞的反应同样针对几种SARS-CoV-2蛋白,而CD8 + T细胞则优先针对N蛋白,这凸显了在未来的疫苗中包含这种抗原的潜在重要性[21].此外,IgG(N)反应可以持续一段时间,这一事实支持这种抗原可以与其他参数(特异性T细胞和中和抗体)一起监测,以确定产生有效免疫反应的人群[22,23,24].维持IgG(N)和IgG(S)以及特异性T和B免疫反应可防止可能的再次感染,并使(再次)接种变得多余。需要进一步深入的免疫学研究,以探讨它们在预防严重病例(包括死亡)以及在感染和接种疫苗后再次感染方面的作用[25]
体液免疫反应在男性和女性中似乎有着非常相似的轨迹,尽管我们发现在所有时间点男性的IgG(N)或IgG(S)水平更高。其他随访8个月的研究表明,由于对SARS-CoV-2的免疫记忆差异,性别和疾病严重程度是相关的。然而,对SARS-CoV-2免疫记忆的大部分异质性仍未得到解释,还需要进一步研究细胞免疫的作用,特别是在弱势群体(非血清转化者、免疫缺陷和自身免疫障碍人群)中[2,26]
采用ELISA技术检测抗sars - cov2抗体。检测的IgM(N)和IgG(N)抗体的最高水平甚至可能高于报告的水平,因为在大流行开始时,定量体外诊断技术的可用性有限,所使用的技术是半定量的。虽然世界卫生组织的IgG(S)抗体定量国际标准是在研究开始后建立的,但我们使用定量技术对IgG(S)抗体样本进行回顾性分析。免疫后停止IgG(S)水平的随访,而IgM(N)和IgG(N)水平的随访仍在继续。
对这些结果的解释应考虑到研究的局限性。首先,大多数ProHEpiC-19样本都是欧洲白人,所以研究结果可能无法推广到其他种族。其次,在分析中考虑了性别或疾病严重程度的差异。除了这些,本研究还可以扩展到包括年龄、国籍、社会经济地位或共病等许多其他因素,但样本在这些方面的同质性不允许有足够的统计力量这样做。未来的工作可以扩大样本的招募范围,使这些方面的人更加多样化,以扩大研究结果的普遍性。
随着越来越多的人接种疫苗,了解接种疫苗产生的免疫与感染产生的免疫是否以及如何不同是很重要的。抗体水平的动力学和持续时间相似吗?流行病学建模研究,特别是长期免疫监测,目前主要集中在SARS-CoV-2,但也必须评估SARS-CoV-2与其他冠状病毒之间的相互作用,以便潜在的交叉免疫[25,27].此外,SARS-CoV-2的流行病学建模也可以受益于流感和HIV-1等其他病毒的流行病学建模;反之亦然[28,29].第二,已经有了指定和适合NLME的代码,人们可以根据自己的需要进行开发和扩展,本研究的结果将为评估SARS-COV-2血清流行度的临床实践指南提供参考。
总之,我们对三种抗体进行了17个月的监测,并分析了它们的水平和动力学,同时也考虑了性别和疾病严重程度的影响。NLME模型可以更详细地了解这些轨迹,证实感染者可以由于IgG同型的血清普遍存在时间延长而保持免疫力。由于医护人员在抗击疫情中的重要性,我们的研究聚焦于医护人员,但更大规模、更多样化的样本和更长的随访期可以提供更好的普遍性,并可能详细阐述进一步的影响。尽管在附加文件中提供了每个抗体水平演化的拟合估计方程1, NMLE模型应该被认为是研究时间演化的一种方法,而不是一个准时估计器。由于对IgG(S)进行了标准化定量评估,我们的动力学模型可以为未来的研究提供参考,并为保持社会距离和接种疫苗策略提供信息。
数据和材料的可用性
由于参与者在知情同意书中同意的隐私条件,在当前研究中生成和/或分析的数据集不对外公开,但在合理的要求下,通信作者可以提供。然而,由原始数据生成的合成数据可在以下网站找到:https://github.com/IDIAPJGol/ProHEpic_Antibodies.
参考文献
Galit和逾越节家宴RGA。抗体监测的力量。英国医学杂志2020;383:1782-4。https://doi.org/10.1056/nejme2029532.
Dan JM, Mateus J, Kato Y, hasttie KM, Yu ED, Faliti CE,等。对感染后长达8个月的SARS-CoV-2免疫记忆进行评估。科学(80 -)。2021.https://doi.org/10.1126/science.abf4063.
Trinité B, Tarrés-Freixas F, Rodon J, Pradenas E, Urrea V, Marfil S,等。SARS-CoV-2感染引起与疾病严重程度相关的快速中和性抗体反应。Sci代表2021年。https://doi.org/10.1038/s41598-021-81862-9.
Carrillo J, Izquierdo-Useros N, Ávila-Nieto C, Pradenas E, Clotet B, Blanco J.抗SARS-CoV-2体液免疫应答与中和抗体;发病机制和保护性免疫的意义。生物化学生物物理学报。2021;538:187-91。https://doi.org/10.1016/j.bbrc.2020.10.108.
王鹏,刘琳,奈尔美思,尹明涛,罗燕,王强,等。SARS-CoV-2中和抗体反应在重症患者中更为强烈。《新兴微生物感染》,2020;9:2091-3。https://doi.org/10.1080/22221751.2020.1823890.
龙庆祥,唐新军,史清良,李强,邓海军,袁杰,等。无症状SARS-CoV-2感染的临床和免疫学评估。Nat Med。2020;26:12 - 4。https://doi.org/10.1038/s41591-020-0965-6.
Gudbjartsson DF, Norddahl GL, Melsted P, Gunnarsdottir K, Holm H, Eythorsson E,等。冰岛对SARS-CoV-2的体液免疫反应。中华医学杂志2020;383:1724-34。https://doi.org/10.1056/nejmoa2026116.
Lumley SF, O 'Donnell D, Stoesser NE, Matthews PC, Howarth A, Hatch SB,等。医护人员抗体状况与SARS-CoV-2感染发生率英国医学杂志。2021;384:533-40。https://doi.org/10.1056/nejmoa2034545.
黄at, Garcia-Carreras B, Hitchings MDT, Yang B, Katzelnick LC, Rattigan SM,等。冠状病毒抗体介导免疫的系统综述:动力学、保护的相关因素以及与严重程度的关系。2020年。https://doi.org/10.1038/s41467-020-18450-4.
Dobaño C, Ramírez-Morros A, Alonso S, Vidal- alaball J, Ruiz-Olalla G, Vidal M,等。COVID-19后12.5个月的医护人员血清阳性和再感染率的持久性和基线决定因素BMC医学2021;19:55。https://doi.org/10.1186/s12916-021-02032-2.
Ortega N, Ribes M, Vidal M, Rubio R, Aguilar R, Williams S,等。SARS-CoV-2抗体的七个月动力学和已有的人冠状病毒抗体的作用Nat comm . 2021; 12:1-10。https://doi.org/10.1038/s41467-021-24979-9.
世卫组织2020年2019冠状病毒感染血清流行病学调查方案;https://www.who.int/publications/i/item/WHO-2019-n.
G . Mattiuzzo, Bentley EM, Hassall M, Routley S.建立世界卫生组织抗sars - cov -2抗体国际标准和参考面板。2020.
陈旭,陈铮,Azman AS,邓旭,孙锐,赵铮,等。人感染SARS-CoV-2的血清学证据:系统综述和荟评分析。《柳叶刀全球健康》,2021;9:e598-609。https://doi.org/10.1016/s2214 - 109 x (21) 00026 - 7.
Harrington WE, Trakhimets O, Andrade DV, Dambrauskas N, Raappana A, Jiang Y,等。在轻度COVID-19康复成人中,中和性抗体的快速下降与IgM的衰减相关。Cell Rep Med. 2021。https://doi.org/10.1016/j.xcrm.2021.100253.
赵军,赵胜,欧俊,张军,兰伟,关伟,等。COVID-19:冠状病毒疫苗研发最新进展。Front Immunol. 2020; 11:1-19。https://doi.org/10.3389/fimmu.2020.602256.
Turner JS, Kim W, Kalaidina E, Goss CW, Rauseo AM, Schmitz AJ,等。SARS-CoV-2感染诱导人类骨髓浆细胞长寿。自然》2021。https://doi.org/10.1038/s41586-021-03647-4.
Graham NR, Whitaker AN, Strother CA, Miles AK, Grier D, McElvany BD,等。针对COVID-19患者中严重急性呼吸综合征-冠状病毒-2刺突蛋白受体结合域抗体的动力学和同型评估与年龄、生物学性别和疾病严重程度的关系。临床转化免疫杂志,2020。https://doi.org/10.1002/cti2.1189.
Alfego D, Sullivan A, Poirier B, Williams J, Adcock D, Letovsky S.基于人群的美国SARS-CoV-2抗体血清阳性寿命分析。EClinicalMedicine。2021年,36:100902。https://doi.org/10.1016/j.eclinm.2021.100902.
Mariano G, Farthing RJ, Lale-Farjat SLM, Bergeron JRC。SARS-CoV-2的结构特征:我们在哪里,我们需要在哪里。生物科学前沿,2020。https://doi.org/10.3389/fmolb.2020.605236.
Cohen KW, Linderman SL, Moodie Z, Czartoski J, Lai L, Mantus G,等。纵向分析显示,SARS-CoV-2感染后具有持久和广泛的免疫记忆,具有持续的抗体反应和记忆B和T细胞。Cell Reports Med. 2021;2: 100354。https://doi.org/10.1016/j.xcrm.2021.100354.
Krammer F, Srivastava K, Alshammary H, Amoako AA, Awawda MH, Beach KF,等。单剂SARS-CoV-2 mRNA疫苗后血清阳性人群的抗体应答中华医学杂志2021;384:1372-4。https://doi.org/10.1056/nejmc2101667.
Maria Prendecki CC, Jonathan Brown AC, Sarah Gleeson MG, Paul Randell ADP, Liz Lightstone X-NX, Wendy Barclay SPM,等。既往SARS-CoV-2感染对单剂BNT162b2疫苗的体液和t细胞应答的影响《柳叶刀》2021年;397年。
Manisty C, Otter AD, Treibel TA, McKnight Á, Altmann DM, Brooks T,等。既往sars - cov -2感染者对第一次BNT162b2剂量的抗体反应。《柳叶刀》杂志。2021;397:1057-8。https://doi.org/10.1016/s0140 - 6736 (21) 00501 - 8.
忠臣L, Braun J, Henze L, Kruse B, Dingeldey M, Reimer U,等。交叉反应性CD4+ T细胞增强了SARS-CoV-2感染和接种后的免疫应答。科学(80 -)。2021.https://doi.org/10.1126/science.abh1823.
Kilpeläinen A, Jimenez-Moyano E, Blanch-Lombarte O, Ouchi D, Quirant-Sanchez B, Chamorro A,等。SARS-CoV-2非血清转化器的高功能细胞免疫与免疫保护相关5。BioRxiv 2021:2021.05.04.438781。
阿贝拉·伊娅,帕辛·C, Schwarzmüller M,埃普·S,希克曼·梅,尚兹MM,等。多因子血清分析分析了已有的人类冠状病毒对SARS-CoV-2免疫应答的贡献。Nat comm . 2021。https://doi.org/10.1038/s41467-021-27040-x.
Petersen E, Koopmans M, Go U, Hamer DH, Petrosillo N, Castelli F,等。比较SARS-CoV-2、SARS-CoV和流感大流行。《柳叶刀感染杂志》2020;20:e238-44。
Fischer W, Giorgi EE, Chakraborty S, Nguyen K, Bhattacharya T, Theiler J, Goloboff PA, Yoon H, Abfalterer W, Foley BT,等。HIV-1和SARS-CoV-2:两种大流行病原体的进化模式细胞宿主微生物。2021;29:1093-100。https://doi.org/10.1016/j.chom.2021.05.012.
致谢
作者真诚地感谢参与者在ProHEpiC-19队列研究中的努力和无私的参与。此外,他们还要感谢管理部、初级保健理事会和大都会北部临床实验室理事会为该项目提供的设施。另外,我们也非常感谢IrsiCaixa的技术人员对样品的处理。我们感谢“CERCA方案/加泰罗尼亚总院”的体制支持。
发表前披露结果:这项工作的以前版本已经发表在MedRxiv上https://www.medrxiv.org/content/10.1101/2021.09.10.21262527v1
研究方案:协议和知情同意发布在ClinicalTrials.gov上(NCT04885478,注册日期为13/05/21)
ProHEpiC-19研究者:Marta Soldevilla Garcia1, Ester Moral Roldan1, Magda Alemany Costa1,伊娃·奥利瓦雷斯·奥特加2阿尔巴Pachón卡马乔1、2Marta Bujalance Devesa说1,玛丽拉·索托·埃斯皮诺萨1,安东尼奥·内格雷特·帕尔马1玛丽安娜·马丁内斯·德·桑José1艾斯特·卢卡斯·瓦拉斯3、7艾斯特·巴迪亚·佩里希2Mónica Piña罗德里格斯2埃琳娜·多梅内克·格拉尔斯2爱德华·莫雷诺·加布里尔1、2、6、22, Victòria Sabaté信达斯2阿格里希González2, Asumció巴斯克斯·杜兰2Alex Ortega Roca说2安娜·德维萨·普拉德尔斯2, Athina Kielpilanen13,奥斯卡·布兰奇·隆巴特13,米格尔·安吉尔·马林·洛佩兹13Julieta Carabelli说13露丝Peña Poderós13Esther Jimenez Moyano说13, Eulalia Grau Segura13莱亚·伯纳德·罗莎13,劳尔Pérez卡巴列罗13费利佩·罗德里格斯·洛扎诺13, Gema Fernández Rivas22索尼娅·莫利诺斯·阿博斯22, Jaume Barallat Martinez de Osaba16,洛伦娜·泰罗·特里戈15克里斯蒂娜·佩雷斯·卡诺23Juan Matllo Aguilar说23, Anabel López Martínez23, Inmaculada Agüera伊格莱西亚斯。23
1西班牙北部城市城市支持研究所'Investigació en Atenció Primària Jordi Gol (IDIAP Jordi Gol), Mataró。2Direcció d'Atenció Primària大都会北学院Català de Salut。西班牙巴塞罗那。3.德国Trias i Pujol研究所(IGTP),巴达罗纳,西班牙。4巴塞罗那大学Autònoma,塞丹约拉德尔Vallès,西班牙。5赫罗纳大学医学院,17003西班牙赫罗纳。6卫生与社会多学科研究小组(2017 SGR 917), 08007西班牙巴塞罗那7细胞生物学、生理学、免疫学学系。FOCIS卓越中心-巴塞罗那大学Autònoma,塞丹约拉德尔Vallès,西班牙。8免疫学。北大都会实验室诊所(LCMN)。德国大学医院,巴达洛纳,西班牙。9Fundació Institut Universitari d'Investigació en Atenció Primària Jordi Gol (IDIAP Jordi Gol),西班牙巴塞罗那。10西班牙塞丹约拉市巴塞罗那大学护理系Autònoma。11巴塞罗那大学医学院医学院,Autónoma de Barcelona,西班牙,08193 Bellaterra。12巴塞罗那大学儿科部'Obstetrícia i Ginecologia i de Medicina prevention, Autónoma de Barcelona,西班牙,08193 Bellaterra。13Irsicaixa艾滋病研究所,巴达洛纳,西班牙。14中心'Atenció Primària La Riera (Mataró 1),学院Català de La Salut,西班牙巴塞罗那15西班牙巴达洛纳德斯特里亚斯普约尔大学医院重症监护室。16临床及生化分析科。北大都会实验室诊所(LCMN)。德国大学医院,巴达洛纳,西班牙。17Lluita contra la SIDA基金会,德国大学医院,巴达洛纳,西班牙。18加泰罗尼亚中央大学(UVic-UCC), 08500维克,西班牙;19西班牙巴达洛纳德德大学医院;Gerència Territorial Metropolitana Nord, Institut Català de la Salut,巴塞罗那,西班牙。20.Investigación Biomédica红红火火的传染病研究中心(CIBERINF),卡洛斯第三卫生研究所(ISCIII)。21巴塞罗那大学医学院医学院,Autònoma de Barcelona,西班牙,08193 Bellaterra22巴塞罗那大学社会心理系Autònoma,西班牙贝拉特拉市塞丹约拉市Vallès22德国普约尔大学医院微生物科,巴达洛纳0891623基本预防科,德国大学北部大都会医院,巴达洛纳08916。
资金
该项目由加泰罗尼亚大区卫生部(命名为COVID19-PoC SLT16_04)、卡洛斯三世卫生研究所(西班牙经济和竞争力部)通过RETICS RD16/0007/0001和RETIC RD16/0025/0041)、欧盟欧洲区域发展基金(ERDF)、加泰罗尼亚政府(拨款号AGAUR 2017 SGR 445)和pi19提供资金法国博士学位证书formación en investigación en salud (AES 2019).
作者信息
作者和隶属关系
财团
贡献
CV、PT-M、JG和EM-C制定了研究概念和设计。BQ、NL-V、RD-A、CCh、FR-R、FP-F、MM、PM、RG-S、FA、CP MB-P和ProHEpiC-19研究者对数据采集有贡献。LC-R-B、JM-D、AR-LL、AP NM-M和DO对数据分析均有贡献。CV、PT、JGP、E - M-C编译了初稿。所有作者都对结果的解释和对手稿的批判性修改做出了贡献。MD、NP、JB、BC、IB对研究监督有贡献。所有作者阅读并批准了最终稿件。
相应的作者
道德声明
伦理批准和同意参与
Jordi Gol i Gurina基础大学初级保健研究所伦理委员会(IDIAPJGol)(参考文献20/067)和德国Trias i Pujol研究所(IGTP)(参考文献cov20 /00660 (PI-20-205))批准了研究方案。参与者签署了参与同意书。所有方法都是根据机构准则和条例进行的,并根据《赫尔辛基宣言》的道德标准进行的。该研究招募的所有参与者都被充分告知了ProHEpiC-19方案,并签署了参与的知情同意书。
发表同意书
不适用。
相互竞争的利益
所有作者已完成ICMJE统一披露表格www.icmje.org/coi_disclosure.pdf并声明提交的工作除经费部分详细列出的以外,没有任何组织的支持。所有其他作者声明没有BMC定义的竞争利益,或其他可能被认为影响本文报告的结果和/或讨论的利益。
额外的信息
出版商的注意
伟德体育在线施普林格自然对出版的地图和机构附属的管辖权要求保持中立。
补充信息
附加文件1:表S1。
每个评估时间点每种SARS-CoV-2抗体的可用样本数量。表S2。根据疾病严重程度和出生时指定的性别,描述参与者的主要症状(N, %)。表S3。SARS-CoV-2抗体(IgM(N), IgG(N), IgG(S)) NLME模型的参数估计图S1。先知covid -19研究参与者流程图,包括招募流程和与Sars-CoV-2的关系类型。分析考虑了“基线或随访期间的阳性”参与者。图S2。非线性混合效应模型的Q-Q图。
权利与权限
开放获取本文遵循创作共用署名4.0国际许可协议(Creative Commons Attribution 4.0 International License),该协议允许在任何媒体或格式中使用、分享、改编、分发和复制,只要您给予原作者和来源适当的署名,提供创作共用许可协议的链接,并说明是否有更改。本文中的图片或其他第三方材料包含在文章的创作共用许可中,除非在材料的信用额度中另有说明。如果材料不包含在文章的创作共用许可中,并且您的预期用途不被法律法规允许或超出了允许的用途,您将需要直接从版权所有者那里获得许可。欲查看此许可证的副本,请访问http://creativecommons.org/licenses/by/4.0/.创作共用公共领域奉献放弃书(http://creativecommons.org/publicdomain/zero/1.0/)适用于本文提供的数据,除非在数据的信用额度中另有说明。
关于本文
引用本文
Violán, C, Torán-Monserrat, P, Quirant, B。et al。西班牙一大批医护人员在COVID-19大流行17个月期间的体液免疫反应动力学:ProHEpiC-19研究BMC感染22, 721(2022)。https://doi.org/10.1186/s12879-022-07696-6
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/s12879-022-07696-6
关键字
- SARS-CoV-2
- 新型冠状病毒肺炎
- 抗体
- 免疫球蛋白
- IgM
- Seroprevalence
- 动力学
- 体液免疫
- 临床表现
- 卫生保健工作者
- 队列
- 非线性混合模型