摘要
9 -独联体-环氧类胡萝卜素双加氧酶(NCED)是高等植物中脱落酸(ABA)生物合成的限速酶。在大米、OsNCED3促进ABA的合成,提高非生物胁迫耐受性,但OsNCED3调节水稻对褐飞虱的防御(摘要研究选择性;BPH)一直不清楚。本研究采用平均伤害水平、功能性植株损失指数和电渗透图分析等参数评价水稻对黑穗病的抗性。水稻线过度表达OsNCED3(OE)对BPH的抗性高于野生型。Zhonghua11 (WT)。对WT、OE和沉默的RNAi转基因株系进行转录组分析OsNCED3;这3个品系均有BPH侵染或未侵染。比较了17个RNA文库,大多数差异表达基因(DEGs)上调。BPH侵染RNAi系中deg的数量显著高于OE和WT系,其中许多deg与胁迫反应和茉莉酸的生物合成有关。本研究表明过表达OsNCED3在水稻育种中具有潜在的价值。
简介
由于人口增长和城市化,粮食安全已成为世界范围内的一个关键问题[1].棕色飞虱(BPH)摘要研究选择性Stål,是水稻的有害害虫(栽培稻L.)在亚洲[2],并在中国造成大面积破坏和毁灭性的产量损失[3.].BPH一般由化学杀虫剂控制;然而,农药滥用会导致严重的环境问题,并可能导致杀虫剂抗药性。为了减少农药的使用,需要采用对环境友好的新病虫害管理战略。
植物激素脱落酸(ABA)控制多种生长和发育过程,包括成熟、休眠和萌发。ABA还调节植物对非生物胁迫的反应,包括寒冷、干旱、盐度和过度浇水[4,5].与植物激素茉莉酸(JA)、水杨酸(SA)和乙烯相比,ABA在植物对昆虫的防御反应中所起的作用的研究有限[6,7].据报道,ABA缺乏会增加植物对草食的敏感性[8,9,10].以往研究表明外源ABA通过促进胼胝质的形成来增强水稻对BPH的抗性[11,12];然而,aba介导的水稻防御的分子机制尚不清楚。
9 -独联体-环氧类胡萝卜素双加氧酶(NCED)是ABA生物合成中的限速酶[13].数控首次报道于Zea mays vp14与野生型植物相比,其内源ABA含量较低,蒸腾速率较高,种子发芽率较低[14].数控同源物已从其他植物物种中分离出来,包括茄属植物lycopersicum[15],Persea美国[16],拟南芥[17,18],马吕斯有明显[19),而芸苔属植物显著[20.].之前的研究表明AtNCED3在拟南芥在干旱胁迫下诱导,其过表达提高了耐旱性[21].在木薯,MeNCED3盐胁迫显著诱导表达;这导致ABA含量增加,耐盐性增强[22].大米中有五种同源物数控基因家族[23];在这其中,OsNCED3在经受非生物胁迫的水稻中表达升高[24].盐度、干旱和H2O2诱导OsNCED3表达,从而表明一个关键的作用OsNCED3水稻对非生物胁迫的反应[24].此外,ABA水平增加时OsNCED3在转基因中表达拟南芥[25],以及转基因水稻过表达OsNCED3在干旱胁迫下ABA水平较高[26].虽然ABA提高了植物对干旱胁迫的抗性,但关于ABA在应对昆虫胁迫中的作用的报道相对较少。
在本研究中,进行了多项评估来评估的作用OsNCED3水稻对黑穗病的抗性,包括功能性植株损失指数、平均损伤水平和电渗透图。通过对水稻叶鞘侵染BPH的转录组分析,进一步评价BPH在水稻叶鞘侵染中的作用OsNCED3在水稻抗性方面。我们证明了OsNCED3该基因在水稻防御系统中发挥了重要作用,这表明它有潜力用于培育抗BPH的水稻品种。
材料与方法
稻米及昆虫材料
宽型水稻cv。实验采用中华11号(ZH11)。水稻线过度表达OsNCED3(OE),和或沉默OsNCED3RNA干扰(RNAi)表达,由华南农业大学生命科学学院提供[26].选择种子,在水中浸泡,发芽,然后播种在含有土壤的塑料盒(长38厘米,宽22厘米,高8厘米)中。幼苗被转移到塑料杯(直径5厘米,高12厘米),并提供肥料和水。在水稻植株的详细年龄(四叶期),水稻系被用于实验。BPH采集自中国水稻研究所(杭州,中国),在扬州大学温室饲养。
测量OsNCED3在不同水稻系中的表达
试验采用WT、OE和RNAi稻系。米叶(0.5 g)用锡箔包好,置于液氮中,然后放入-80℃超低温冷冻室保存,直至需用。
白骨病饲喂后水稻损伤水平的测定
WT、OE稻种(n= 15)被选中。一个由聚氯乙烯(PVC)片制成的柔性圆柱体沿着杯子的边缘插入土壤中。三龄BPH若虫(n= 30)饿死1 h,然后转移到PVC筒和,用纱布密封。每只塑料杯中大米的损伤程度在7天进行检测,并建立分级标准[27]用于评估损伤水平(表1).
BPH饲喂后功能性植物损失指数(FPLI)的测定
确定损伤程度后,将水稻切块,洗净,110℃烘干20 min, 60℃烘干至恒重。干重用精密电子天平测量,功能植物损失指数(FPLI)按前文所述计算[28].
电穿透图(epg)确定的BPH摄食行为
EPG波形的表征和量化如前所述[12].简单地说,将单个水稻幼苗(四叶期)移植到塑料杯中。饥饿1小时后,3号个体理查德·道金斯将成年褐飞虱若虫放置在水稻叶鞘上,用一根长3 ~ 5 cm、直径20 μm的金丝从褐飞虱背部连接至EPG仪。EPG仪器被放置在气候控制室(25±2℃),并连接到运行PROBE软件的计算机(EPG- system, Wageningen,荷兰)。用导电银胶将一根金丝连接到背部,然后允许BPH通过伞膜探测稻鞘。每只昆虫身上的金线和浸在食物中的铜线(直径0.1毫米)连接到CR-8型DC-EPG放大器(武汉普赛斯电子科技有限公司)。数据分析采用ANA v. 3.0软件(Wageningen University)。EPG记录每株昆虫6 h,每个处理10个重复。
RNA文库构建和转录组测序
在分蘖期分别为WT、OE和RNAi水稻选育各6株幼苗。用于BPH饲养的植物用手工塑料覆盖物覆盖,在我们之前工作的基础上,在BPH饲养后12 h进行采样[12].以不饲喂BPH的植物为对照。每个处理重复3次。样品(0.2 g)用箔纸包裹,液氮冷冻,-80℃超低温冷冻室保存。
RNA文库构建,质量控制如前所述[29].使用总RNA试剂盒(Tiangen, Beijing, China)从样品中提取总RNA。利用寡聚(dT)磁吸附富集样品,并作为第一链cDNA合成模板;合成第二链cDNA,用AMPure XP珠进行纯化。cDNA文库先用Qubit 2.0和Agilent 2100进行分析,然后用Illumina HiSeq 2500高通量测序系统(位于中国南京Genepioneer生物技术有限公司)进行测序。质量控制后获得的干净数据读数与参考基因组进行比较(ftp://ftp.ensemblgenomes.org/pub/plants/release-44/fasta/Oryza_sativa /dna/)获取映射数据,用于后续转录本组装和表达计算。使用Cufflinks与参考基因组进行多次比较(http://cole-trapnell-lab.github.io/cufflinks/).计算每千碱基外显子每百万片段的片段数(FPKM)进行基因表达分析。deg被定义为满足以下要求:p-adjust≤0.05,默认差倍数= 2。DAVID24用于分析基因类的过度代表性。利用样本组基因表达水平进行差异表达分析,对差异表达基因(DEGs)进行GO功能标注,KEGG通路富集分析。
DEGs的鉴定及qRT-PCR验证
使用DESeq2软件和日志检测deg2以fold change≥1,虚假发现率(FDR) < 0.05为筛选标准。Fold change表示组间表达比例,通过校正显著性得到fdrP值。选择6个deg进行实时定量PCR,验证了转录组测序的准确性。使用HiScript®Q RT SuperMix for qPCR (+ gDNA wiper) (Vazyme)进行反转录,Primer Premier 5.0用于引物设计。使用ChamQTM SYBR®Color qPCR Master Mix Kit (Vazyme)进行定量PCR。将混合溶液加入96孔板中,反应混合物中含有目的基因引物(0.8 μl)、2 × ChamQ SYBR Color qPCR Master Mix (10 μl)和模板(2 μl)。以水稻鞘中的cDNA为模板,ActinI作为内参,每个样品检测三次。计算各基因的相对表达量−ΔΔCt方法(30.].
统计分析
采用方差分析(ANOVA;Systat Inc.),然后是邓肯的多重范围测试进行多重比较。对于方差分析,如果数据正态分布,则直接进行分析;对非正态分布的数据进行转换,以确保不同组间方差的同质性。数据以均数±SE表示,采用SPSS 11.0软件(SPSS)进行分析。
结果
测量OsNCED3不同水稻系的表达水平
的表达式OsNCED3采用RT-qPCR方法对WT、OE和RNAi水稻系进行检测。的表达OsNCED3与野生型相比,OE水稻中表达量增加了106.30%OsNCED3在RNAi水稻中的表达下调了66.60%(图2)。1).这些结果表明,过表达和敲除实验是成功的。
测定损伤程度、FPLI和BPH摄食行为
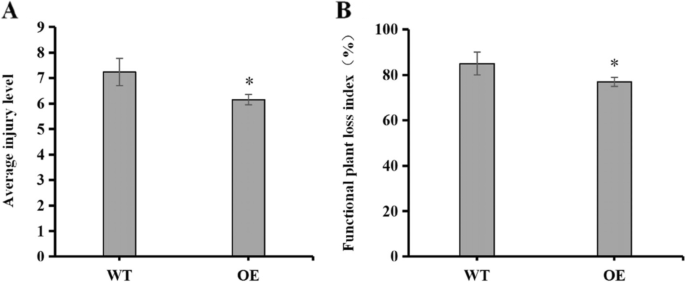
在OE水稻中,平均损伤水平和FPLI值分别比WT低14.64%和9.41%(图2)。2).
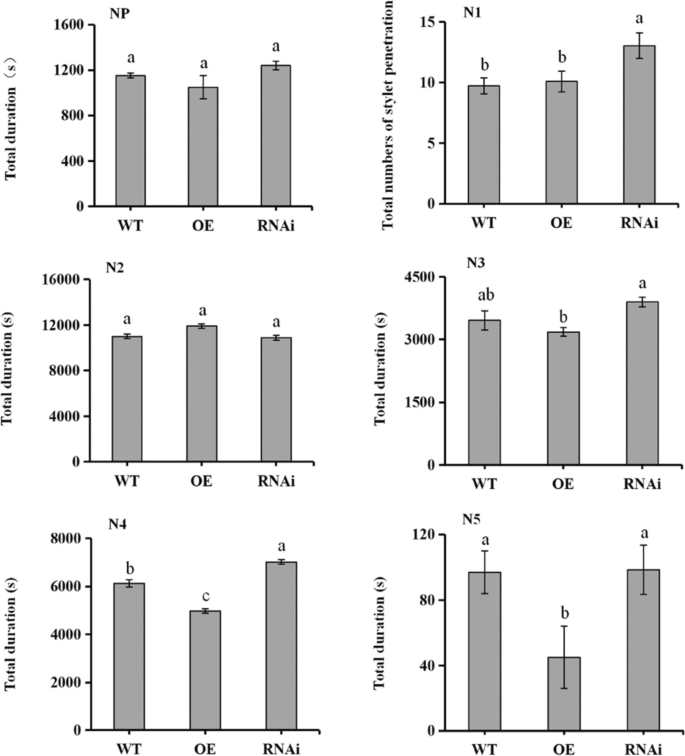
使用EPG的WT、OE和RNAi水稻系的BPH摄食行为如图所示。3..3个水稻系之间的非探测(NP)波形持续时间无显著差异。就探测时间(N1波形)而言,RNAi水稻的波形频率显著高于WT和OE品系。3个水稻株系之间的N2波形持续时间(维管束中穗状体运动的持续时间)没有显著差异。然而,显示韧皮部细胞外微丝移动持续时间的N3波形在OE中明显低于RNAi线。N4波形显示了韧皮部吸收汁液的时间,这在3个水稻品系中存在显著差异。与WT相比,OE水稻的N4波持续时间显著缩短了20.13%,而RNAi系的N4波持续时间增加了16.49%。表明BPH对木质部液体摄取的N5波形在WT和RNAi水稻品系中没有显著差异。与WT相比,OE水稻的N5波形低53.61%,RNAi系的N5波形比OE水稻高118.89%(图2)。3.).这些结果表明过度表达OsNCED3可提高水稻的抗黑穗病能力。
转录组数据
转录组测序数据的质量得到了证明。经质量控制,共获得洁净数据128.00 Gb,每个样品的洁净数据为6.19 Gb及以上。将各样本的Clean reads与参考基因组进行比较,比较效率达91.36%以上。17个水稻样品的Q30百分比超过89.29%,表明数据具有很高的可用性。clean reads中GC含量在48.81% ~ 52.25%之间。总的来说,这些统计数据表明测序结果是合格的,可以用于进一步的分析。
BPH饲喂后OE和RNAi水稻系的DEGs
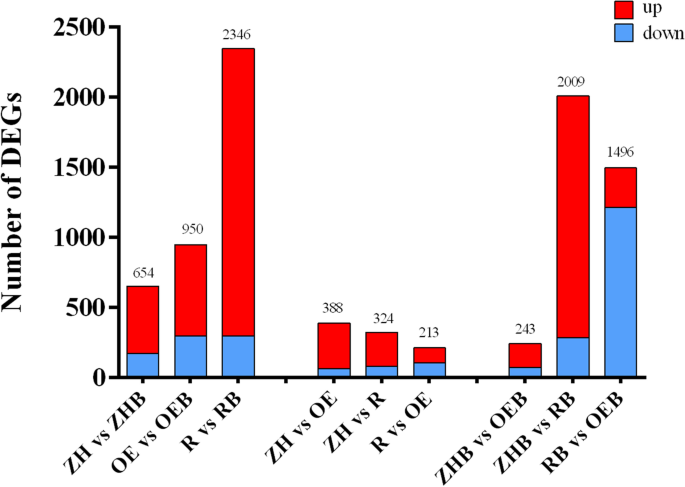
在三个水稻品系中,分别在有BPH和无BPH饲喂时鉴定出了DEGs。4).对3个水稻系的DEGs进行统计分析,得到各组中上调和下调基因的数量(图2)。4).前三列显示了有BPH饲喂的水稻品系(ZHB, OEB, RB)和没有BPH饲喂的水稻品系(ZH, OE, R)的比较。当有BPH饲喂和没有BPH饲喂的水稻品系进行比较时,ZH和ZHB的deg总数为OE和OEB的654,950个,R和RB的2346个。在比较RNAi组和OE组时,没有BPH喂养的deg数量最小,为388个(R vs OE);在有BPH取食和无BPH取食的RNAi系中,deg的数量最高,为2346个(R vs. RB)。数据还显示,RNAi / WT与BPH喂养比较(ZHB vs. RB)中deg的数量远高于没有BPH喂养的比较(ZH vs. R)(图2)。4).
对显示2 - 7倍变化差异的DEGs的分析显示,在四个比较组中有大量的DEGs上调和下调(表2),更多的基因上调或下调。在侵染BPH的RNAi水稻系中,折叠变化差异最大;例如,1724例deg显示折叠变化值≥2,显著多于其他对照组(表22).这些结果表明,在褐飞虱侵染的不同水稻品系中,只有少数几种deg基因普遍表达。
deg的维恩图
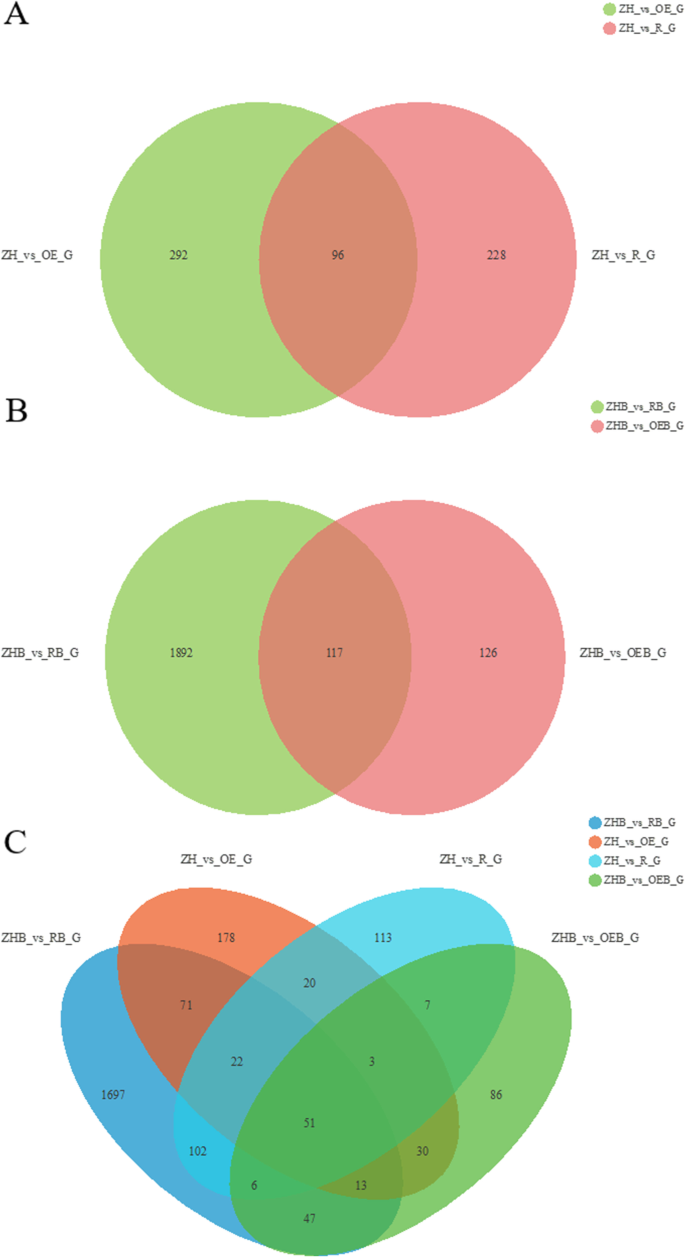
在无BPH摄食的情况下,WT (ZH)组与OE组、WT与RNAi组中重叠的DEGs数量为96个,分别占总数的29.63%和24.74%(图2)。5A). BPH饲喂后,ZHB组与OEB组、ZHB组与RB组有117个重叠的DEGs,分别占WT的48.15%和5.82%(图2)。5B).分析四组比较,共鉴定出51个重叠的DEGs,分别占对照组DEGs总数的2.54%、20.99%、15.75%和13.14%(图。5C).这些结果表明,在不同的褐飞虱侵染水稻品系中,只有少数的deg是共同的。
DEGs的GO功能分析
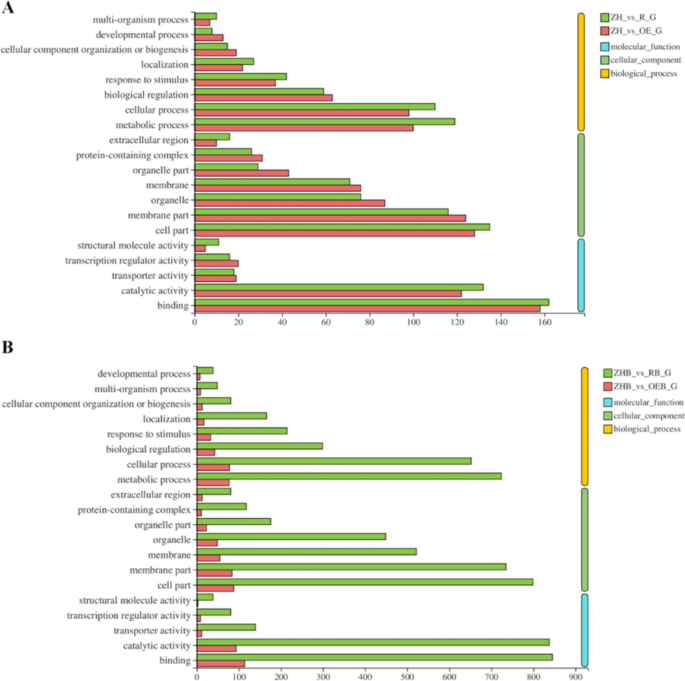
在没有BPH摄食的情况下,ZH (WT)组与OE组以及ZH与R (RNAi)组的DEGs在GO分子功能“结合”(GO:0,005,488)类别中高度代表(图。6A).标注为“催化活性”(GO:0,003,824)、“细胞部分”(GO:0,044,464)、“膜部分”(GO:0,016,020)、“代谢过程”(GO:0,008,152)和“细胞过程”(GO:0,009,987)的deg数量均超过100个(图2)。6一个)。
BPH饲喂后,在RNAi水稻中标记GO功能的deg数量显著增加,其中最高比例(n= 845),其次是“催化活性”、“细胞部分”和“代谢过程”。排在前6位的GO通路中的deg数量分别为“生物调控”、“代谢过程”、“膜部分”、“细胞部分”、“结合”、“催化活性”,超过600个(图2)。6B). BPH饲喂后,OE水稻系标注“结合”的deg数量为114个,其次是“代谢过程”、“细胞过程”和“细胞部分”。然而,在WT和OEB_G中,每个GO途径中的deg数量都小于100个,并且每个GO途径中的deg数量明显少于RNAi水稻系(图2)。6B)。
KEGG功能分析
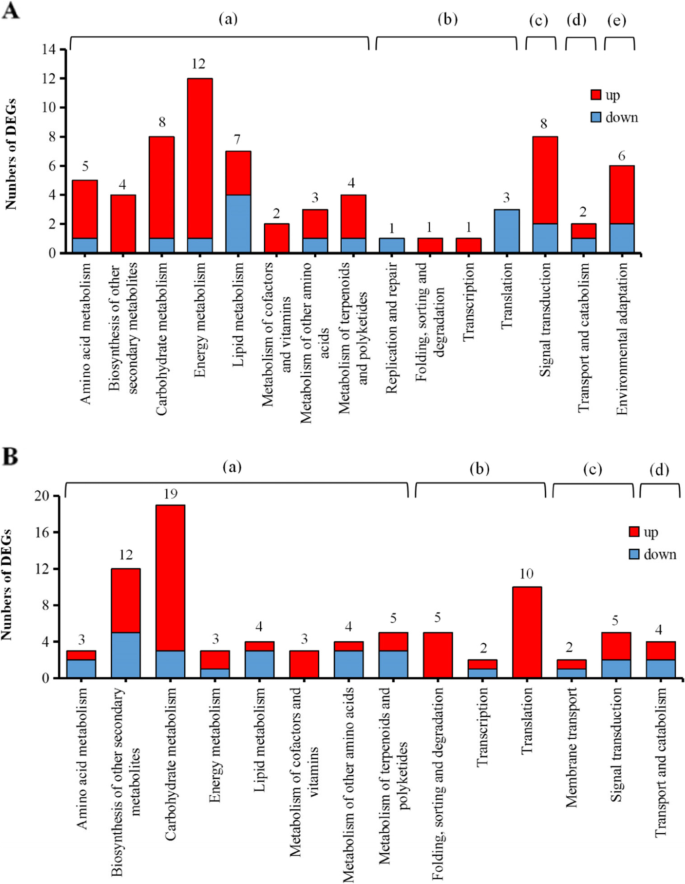
在没有BPH取食的情况下,WT和OE品系的DEGs集中在15条KEGG途径上,包括氨基酸代谢、其他次生代谢产物的生物合成、碳水化合物代谢、能量代谢、脂质代谢、辅因子和维生素代谢、其他氨基酸代谢、萜类和多酮类代谢、信号转导、转运和分解代谢以及环境适应途径(图2)。7A).最大数量的deg (n= 12)参与能量代谢途径,其次是碳水化合物代谢途径(n= 8)、信号转导(n= 8)。
ZH (WT)与RNAi水稻在无BPH投食时,DEGs集中在14条KEGG通路上。包括氨基酸代谢、其他次生代谢产物的生物合成、碳水化合物代谢、能量代谢、脂质代谢、辅助因子和维生素代谢、其他氨基酸代谢、萜类和多酮类代谢、信号转导、转运和分解代谢以及环境适应途径(图2)。7B).最具代表性的途径是碳水化合物代谢(n= 19个DEGs),然后是其他次生代谢产物的生物合成(n= 12)。
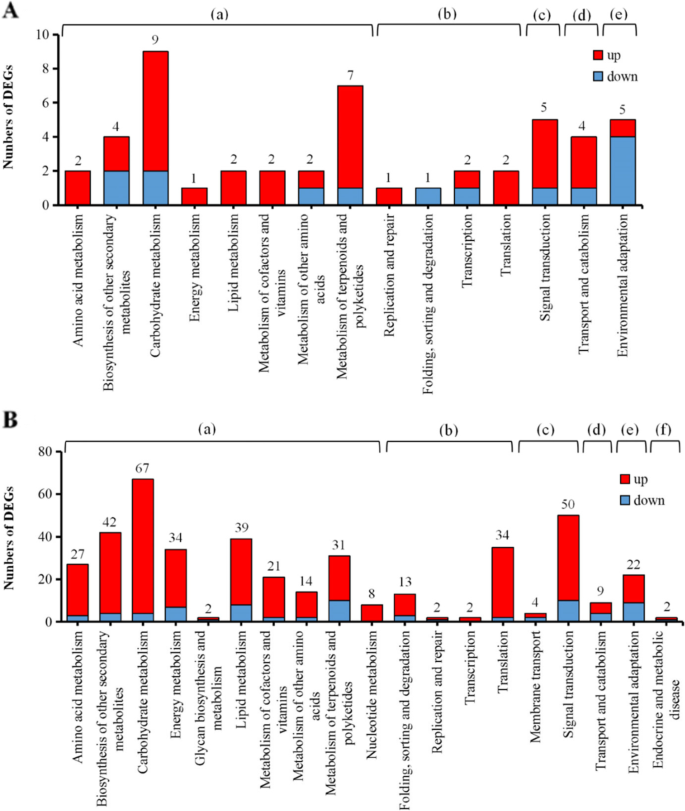
BPH喂养后,OE中KEGG通路和RNAi系的DEGs分配与未BPH喂养的相似。在碳水化合物代谢途径中deg数量最多(n= 9),其次是萜类化合物和多酮类化合物(n= 7)(图8A). BPH以RNAi水稻为食后,DEGs分布在19个KEGG通路中。这包括在没有BPH摄食的情况下未被代表的四种新途径,包括聚糖生物合成和代谢、核苷酸代谢、环境适应、内分泌和代谢性疾病。碳水化合物代谢途径是最具代表性的67个deg,其次是信号转导途径(n= 50)(图8B)。
转录组结果的qRT-PCR验证
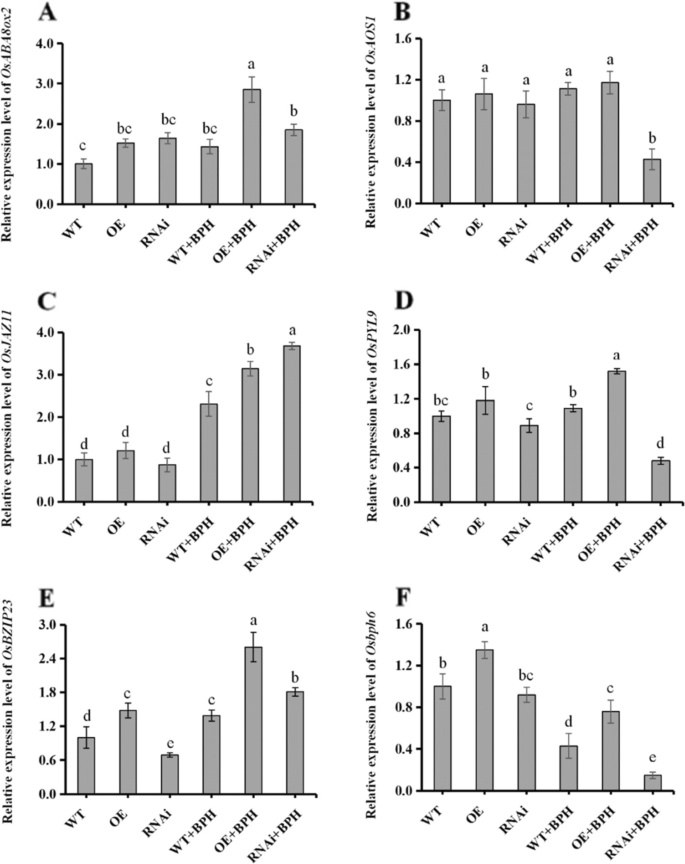
选择6个与激素通路和昆虫防御相关的deg进行qRT-PCR分析。OsABA8ox2(Os08g36860),OsPYL9(Os06g36670)编码ABA降解相关基因和ABA受体。结果表明,BPH饲喂后,这两种基因在OE水稻系中的表达量显著增加(图2)。9a, d)。OsAOS1(Os03g55800)参与JA的生物合成OsJAZ1(Os04g32480)是JA的转录抑制剂。的表达式OsJAZ1增加,而OsAOS1侵染BPH的RNAi水稻株系减少(图;9b, c).水稻抗逆性基因的相对表达OsbZIP23(Os02g52780),以及BPH抗性基因Osbph6(Os04g35210)在OE水稻中持续高于WT(图04g35210)。9e, f). qRT-PCR结果与转录组分析结果一致,RNA-Seq与qPCR结果的相关性支持了我们结果的可靠性。
qRT-PCR验证转录组结果。选择ABA、JA和水稻防御相关的6个基因,通过qRT-PCR检测其相对表达量,并与转录组结果进行比较。基因包括以下内容:(一个)编码ABA8’-羟化酶的OsABA8ox2 (LOC_Os08g36860);(B)编码烯氧化物合酶的OsAOS1 (LOC_Os03g55800);(C)编码茉莉酸ZIM-domain蛋白的OsJAZ11 (LOC_Os04g32480);(D)编码吡rabactin抗性样脱落酸受体(LOC_Os06g36670)的OsPYL9;(E) OsBZIP23编码bZIP转录因子(LOC_Os02g52780) l;和(F) Osbph6编码富亮氨酸重复序列家族蛋白(LOC_Os04g35210)。误差柱表示均值±SE (n= 3);进行了三个或更多的独立实验。不同字母的列表示在P邓肯多极差检验< 0.05
讨论
EPG分析用于探究昆虫的取食行为,可以准确记录针孔在寄主组织中的位置[31];因此,EPG技术可作为评价植物抗虫性的生物测定方法[32,33].在本研究中,EPG分析、平均损伤水平和FPLI值的结果表明OsNCED3过表达增加了水稻对BPH的抗性。N4波形表明韧皮部汁液吸收的持续时间,是衡量植物抗性的重要标志。在本研究中,BPH饲喂后,OE水稻N4波持续时间减少,而RNAi水稻则增加(图2)。3.).这些结果表明OsNCED3结果表明,过表达对BPH在韧皮部的取食无促进作用OsNCED3是水稻抗黑穗病的重要指标。
在初步调查中,我们在BPH取食后检查了几个不同的时间点(例如2、4、8、12、24和48小时)。我们选择12小时的时间点是因为在这个采样时间内,许多参与植物防御的酶和激素发生了变化,包括超氧化物歧化酶、过氧化物酶、过氧化氢酶、多酚氧化酶以及JA、SA和ABA。
野生型、OE型和RNAi型水稻中deg的数量受到BPH饲喂的影响。RNAi水稻中deg的数量显著高于OE水稻,特别是在BPH饲喂后(图2)。4).在这种情况下,我们的发现与之前的一份报告一致,即易感水稻品种在BPH饲喂反应中比抗性水稻品种具有更多的deg [34].我们的结果表明,损失OsNCED3BPH摄食后影响水稻基因调控,导致许多基因上调。
在OE水稻中发现的DEGs与木质素、几丁质和血清素的合成有关。OsCCR17编码肉桂酰辅酶a还原酶17,参与木质素和其他次生代谢产物的生物合成。先前的研究表明,编码肉桂酰辅酶a还原酶的水稻同源物在生物和非生物胁迫下被诱导,包括病原体入侵、紫外线照射和高盐度,因此表明在防御相关过程中发挥作用[35].CmMYB15在菊花中编码一种转录因子,与木质素生物合成基因上游区域结合,增强对蚜虫的抗性[36].
在碳水化合物代谢途径中,我们鉴定出三个几丁质酶编码基因,即Oscht1,Oscht4,而且Oscht5;Oscht1与野生型相比,在有或无BPH饲养的情况下,OE水稻中BPH的表达均有所升高。Oscht4而且Oscht5饲喂BPH后,OE水稻中BPH含量显著增加。几丁质酶在植物防御中起作用,过多表达几丁质酶基因的辣椒等转基因植物增强了抗病性和抗逆性[37,38].Rajendran等人(2011)证明,几丁质酶活性的增加与蚜虫数量的减少有关,这表明几丁质酶在抵御昆虫和病原体方面发挥了作用[39].几丁质酶存在于各种植物组织中,包括叶子、果实、种子和根;它被认为是一种与防御有关的酶,对真菌和害虫有一定的保护作用[40].
OsTDC1编码色氨酸脱羧酶,催化色氨酸转化为色氨酸。色胺经色胺5-羟化酶进一步代谢生成5-羟色胺/血清素[41].在我们的研究中,OsTDC1在BPH饲喂后,在氨基酸和次级代谢产物途径中都存在,这表明BPH在水稻防御反应中起作用。在一项相关研究中,水稻突变系中5-羟色胺水平的增加导致对害虫的抗性下降[42,43]
JA被认为是植物抗虫的关键激素。在我们的研究中,JA合成基因OsHI-LOX(13-lipoxygenase),OsLOX7(脂氧合酶7),和OsOPR10(12-oxo-phytodienoic acid reducase 10)在褐飞虱侵染的OE植物中大量表达。功能丧失的研究OsHI-LOX使水稻更容易受到咀嚼昆虫的攻击,但增强了对韧皮部昆虫的抵抗力[44].OsOPR10在OE水稻中上调,表明其在水稻防御中起作用。OPRs参与JA的生物合成,并响应各种生物和非生物应激源,包括机械损伤、盐度、植物信号分子和病原体感染[45].
RT-qPCR结果显示ABA降解基因的表达OsABA8ox2,在OE水稻中显著增加。的表达式OsPYL9编码ABA受体的基因在OE水稻中显著高于RNAi水稻。OsPYLs在种子萌发过程中正向调节ABA的反应,并过度表达OsPYL9水稻抗旱性和耐寒性显著提高[46].我们推测,BPH饲喂后OE水稻中ABA含量增加,过量的ABA被水解。
JA生物合成基因表达OsAOS1在BPH侵染的RNAi水稻中被抑制,这可能是导致JA合成减少的原因。OsJAZ11在BPH侵染的WT、OE和RNAi系中表达上调,并可能抑制JA通路中的信号转导。JAZ蛋白负向调节植物对生物和非生物胁迫的防御[47,48].我们的qPCR数据表明OsNCED3,而且OsBZIP23对BPH防御起协同作用。OsbBZIP23在水稻的非生物胁迫耐受性中起作用[49].OsBph6是一种广谱抗性基因,通过抗生素作用和protaxis对各种BPH生物型和白背飞虱产生抗性。OsBph6对水稻生长和产量没有负面影响,对籼稻和粳稻都有很高的抗性[50].的表达式Osbph6无论有无BPH,在OE水稻中均显著高于WT。9F),表明OE水稻对BPH抗性较高。
结论
根据我们的研究结果,我们得出结论OsNCED3提高水稻对黑穗病的抗性。OsNCED3-介导的防御可能通过增加木质素、甲壳素和其他防御相关物质的合成而产生,如ABA和JA。的潜在用途OsNCED3在水稻育种计划中有优点,但需要进一步验证。
缩写
- 阿坝:
-
脱落酸
- 是:
-
茉莉酸
- 等:
-
乙烯
- 良性前列腺增生:
-
褐飞虱
- nc:
-
9-Cis-epoxycarotenoid加双氧酶
- OE:
-
超表达
- RNAi:
-
RNA干扰
- WT:
-
野生型
- EPG:
-
电侵图
- FPLI:
-
功能性植物损失指数
- 度:
-
差异表达基因
- ZH11:
-
中华11
- PVC:
-
聚氯乙烯
- FPKM:
-
每千碱基的片段数
- RT-qPCR:
-
实时定量聚合酶链式反应
- 走:
-
基因本体论
- KEGG:
-
京都基因和基因组百科全书
参考文献
王超,张震,费旭。维持中国粮食生产与安全的效率与风险:来自粳稻生产微观面板数据分析的证据。可持续性。2018;10(4):1282。https://doi.org/10.3390/su10041282.
薛娟,包依友,李宝宝,程亚波,彭志智,刘辉,徐海军,朱祖荣,娄毅刚,程佳,张彩霞。褐飞虱的转录组分析摘要研究选择性.PLoS ONE。2010; 5 (12): e14233。
程佳,朱志荣。2005年长江地区褐飞虱暴发关键因素分析植物保护科学,2006;32:1-4。
黄霞,陈明明,杨丽林,李烨,吴建民。外源脱落酸对冷胁迫下甘蔗幼苗叶片细胞膜和内源激素含量的影响糖科技,2015;17:59-64。https://doi.org/10.1007/s12355-014-0343-0.
罗德里格斯,马志刚,李志刚,杨晓明,杨晓明。干旱胁迫对凤梨叶片个体发育的影响Guzmania monostachia.植物理化学报。2016;108:400-11。
周永德,孙丽兰,王松,谢福平,刘建林。一个关键的ABA水解酶基因,OsABA8ox3水稻是否涉及抗性摘要研究选择性通过影响胼胝质的沉积。中国昆虫学报,2019;22:625-31。
李超,罗超,周震,王锐,凌峰,肖林,林勇,陈辉。两种水稻基因型对褐飞虱侵染的基因表达和激素水平。BMC植物学报,2017;17(1):57。
塞勒JS,博斯托克RM。脱落酸介导的反应与植物对病原体和昆虫抗性的相互作用。生态。2004;85:48-58。https://doi.org/10.1890/02-0710.
李志强,李志强,李志强,等。拟南芥对植食性昆虫抗性的信号通路研究。植物微生物相互作用。2007;20(11):1406-20。
丁海涛,李志强,李志强,等。植物诱导调控1基因可提高植物对草食动物的aba水平和防御能力烟草attenuata则植物。中国生物医学工程学报,2013;29(4):366 - 366。https://doi.org/10.1104/pp.113.221150.
刘建林,陈霞,张红梅,杨霞,黄安。外源植物生长调节剂脱落酸诱导水稻抗性对卵黄蛋白mRNA表达的影响摘要研究选择性(半翅目:蝇科)成年雌蝇。中国昆虫学报(自然科学版)2014;https://doi.org/10.1093/jisesa/ieu075.
刘健,杜辉,丁霞,周勇,谢萍,吴娟。外源脱落酸调控水稻胼胝体沉积的机制及其与水稻抗病性的关系摘要研究选择性Stål(半翅目:蝇科)。中国生物医学工程学报,2017;29(6):344 - 344。https://doi.org/10.1002/ps.4655.
侯赛因,戈麦斯MM,矢野K,南巴拉。脱落酸与其他激素之间的相互作用。Adv Bot res 2019; 92:225-80https://doi.org/10.1016/bs.abr.2019.09.001.
谭建平,王志强,王志强,等。玉米脱落酸生物合成的遗传控制。美国国家科学研究院。1997; 94(22): 12235 - 40。https://doi.org/10.1073/pnas.94.22.12235.
Burbidge A, Grieve TM, Jackson A, Thompson A, McCarty DR, Taylor IB. aba缺失番茄突变体的鉴定及其与玉米Vp14的关系。植物学报,1999;17(4):427-31。https://doi.org/10.1046/j.1365-313x.1999.00386.x.
Chernys JT, Zeevaart JA。9-顺式环氧类胡萝卜素双加氧酶基因家族的鉴定及其对鳄梨脱落酸生物合成的调控。植物科学进展。2000;30(1):343-53。https://doi.org/10.1104/pp.124.1.343.
摇滚CD, Zeevaart JA。的阿坝突变体的拟南芥在环氧类胡萝卜素生物合成中受损。中国科学院学报(自然科学版),2001;29(3):344 - 344。https://doi.org/10.1073/pnas.88.17.7496.
谭崇斌,刘林,邓文伟,李秋波,等。拟南芥9-顺式环氧类胡萝卜素双加氧酶基因家族的分子特征。植物学报,2003;35(1):44-56。https://doi.org/10.1046/j.1365-313x.2003.01786.x.
夏红,吴松,马峰。9-顺式环氧类胡萝卜素双加氧酶基因在苹果果实发育和胁迫中的克隆与表达。Mol生物学杂志2014;41(10):6795-802。https://doi.org/10.1007/s11033-014-3565-z.
徐萍,蔡伟。BnNCED3基因在植物中的功能特征芸苔属植物显著.植物科学学报,2017;26(2):344 - 344。https://doi.org/10.1016/j.plantsci.2016.11.012.
贾庆林JJ。孟XP。刘荣,夏明。过度的AtNCED3水稻基因在转基因植株中表现出较强的抗旱性。复旦大学学报(自然科学版)2008;288 - 294。
丁志华,付丽丽,铁文伟,闫艳,胡伟MeNCED3木薯中的基因。生物技术牛。2016;32:148-53。
倪惠鹏,徐庆峰,蓝燕,陈qq,张建峰,周玉军。RBSDV感染对水稻脱落酸代谢相关基因转录表达的影响。中国水稻科学,2015;15:319-26。
黄艳,郭艳,刘艳,张峰,王铮,王辉,王芳,李冬,毛冬,栾松,梁明,陈林。9-顺式环氧类胡萝卜素双加氧酶3调控水稻生长及增强水稻多重非生物胁迫耐受力。前沿植物科学2018;9:162。2018年3月6日发布。https://doi:https://doi.org/10.3389/fpls.2018.00162
黄顺生,陈华昌,黄文文,朱永春,史春涛,程文华。水稻OsNCED3在拟南芥中异位表达可增加ABA水平并改变叶片形态。植物科学2010;178-12-22。https://doi.org/10.1016/j.plantsci.2009.09.014
徐秀珍,王涛,万伟,李硕,朱海华。ABA生物合成基因OsNCED3使水稻具有耐旱性。作物学报。2018;44:24-31。
吴荣荣,陶丽丽,陈飞,胡格薇。水稻抗白背飞虱的筛选方法探讨。刑事司法学报,1986;29:453-5。
陈建民,于XP,程佳。不同水稻品种对褐飞虱(BPH)抗性特性的评价。褐飞虱Stål作物学报2009;35:795-801。
王娟,朱军,张勇,范峰,李伟,王峰,钟伟,王超,杨娟。籼稻耐盐敏感基因型苗期对盐胁迫的分子响应比较转录组分析。科学通报2018;8(1):2085。https://doi.org/10.1038/s41598 - 018 - 19984 - whttps: / / doi: https://doi.org/10.1038/s41598 - 018 - 19984 - w。
Livak KJ, Schmittgen TD。利用实时定量PCR和2(-Delta Delta C(T))方法分析相关基因表达数据。方法。2001;25(4):402 - 8。https://doi.org/10.1006/meth.2001.1262.
苗军,韩碧。水杨酸甲酯诱导茶树对茶绿叶蝉取食影响的DC-EPG分析。中国植物学报。2008;35(5):344 - 344。
雷浩,徐荣荣。温室白蝇取食行为的EPG研究。生物学报。1998;41:113-23。
罗晨,岳明,徐海峰,张志林。EPG技术在昆虫学研究中的应用与进展。中国生物医学工程学报,2005;48:437-43。
赵Lv W, Du B,上官X, Y,潘Y,朱L,他Y, g . BAC和RNA序列揭示了褐飞虱抗性基因的重组冷点BPH15调和一个独特的防御机制。BMC基因组学杂志,2014;15(1):674。https://doi.org/10.1186/1471-2164-15-674.
公园霍奇金淋巴瘤,Bhoo SH, Kwon M,李西南,秋MH。生化和表达分析水稻cinnamoyl-CoA还原酶基因家族。中国植物科学,2017;8:2099。https://doi.org/10.3389/fpls.2017.02099.
安超,盛磊,杜霞,王艳,张艳,宋安,姜杰,管志,方伟,陈峰,陈松CmMYB15通过调节木质素的生物合成,提供菊花对蚜虫的抗性。Hortic Res. 2019;6:84。https://doi.org/10.1038/s41438-019-0166-y.
洪俊杰,黄柏凯。PR-1蛋白、β-1,3-葡聚糖酶和几丁质酶基因在生物和非生物胁迫防御反应中的功能特征甜椒.植物病理学杂志,2005;29(2):389 - 389。
Asrorov AM, Matušíková I, Gálová Z, Gregorová Z, Mészáros P, Dalimova S, Salikhov S.棉花几丁质酶家族。微生物与生物技术食品科学,2017;6:1284 - 1289。
李志刚,李志刚,李志刚。内生植物枯草芽孢杆菌丰富甲壳素可诱导棉花对蚜虫的系统性抗性。中国植物科学,2011;14(3):366 - 366。
Silva NC, Conceição JG, Ventury KE, De Sá LF, Oliveira EA, Santos IS, Gomes VM, Costa MN, Ferreira AT, Perales J, Xavier-Filho J, Fernandes KV, Oliveira AE。大豆种皮几丁质酶对贮藏物害虫黄斑胼胝体的防御蛋白。中国生物防治学报,2018;26(6):344 - 344。
Hayashi K, Fujita Y, Ashizawa T, Suzuki F, Nagamura Y, Hayano-Saito Y. 5 -羟色胺可以减弱生物应激,并导致由过敏反应引起的病变褐变Magnaporthe oryzae在大米中渗透。植物学报,2016;26(1):344 - 344。
姜坤,金玉生,朴秀林,白建平。水稻叶片衰老诱导血清素生物合成及其延缓衰老的作用。植物科学进展。2009;30(3):344 - 344。https://doi.org/10.1104/pp.109.138552.
卢和辉,罗涛,付宏伟,王磊,谭永元,黄建忠,王强,叶光宇,Gatehouse AMR,娄永刚,舒启勇。抑制5 -羟色胺生物合成介导水稻对害虫的抗性。植物学报。2018;4(6):338-44。https://doi.org/10.1038/s41477-018-0152-7.
周刚,齐军,任宁,程军,毛波,娄勇。沉默OsHI-LOX使水稻对咀嚼食草动物更敏感,但增强了对韧皮部喂食器的抗性。植物学报,2009;26(4):344 - 344。https://doi.org/10.1111/j.1365-313X.2009.03988.x.
张s, Cho K,柴藤J, Han O, Iwahashi H, Tamogami S, Zargar SM, Kubo A, Masuo Y, Agrawal GK。水稻ooprs: oopr1对不同环境刺激的转录谱分析和生化分析。植物科学进展。2009;
田霞,王震,李霞,吕涛,刘红,王玲,牛红,卜强。水稻耐吡螨素类脱落酸受体家族的鉴定与功能分析。水稻(N Y). 2015;8(1):28。https://doi.org/10.1186/s12284-015-0061-6.
茉莉花素是一种受体,是防御激素的目标。植物生物学,2009;60:183 - 205。https://doi.org/10.1146/annurev.arplant.043008.092007.PMID: 19025383。
付健,吴华,马松,向东,刘锐,熊磊。OsJAZ1通过调控水稻JA和ABA信号通路降低水稻抗旱性。中国植物科学,2017;8:2108。https://doi.org/10.3389/fpls.2017.02108.
朴硕,郑宗杰,李赫,金玉敏,都崔勇,金志强。OsbZIP23和OsbZIP45是水稻碱性亮氨酸拉链转录因子家族的成员,与耐旱性有关。植物生物技术,2015;9:89-96。
植物学报,2018;50(2):297-306。https://doi.org/10.1038/s41588-018-0039-6.
郭旭,陈峰,高峰,李磊,刘凯,尤林,华超,杨峰,刘伟,彭超,王磊,杨鑫,周峰,童娟,蔡娟,李铮,万斌,张磊,杨涛,张敏,杨凌,杨艳,曾伟,王波,魏旭,徐旭。CNSA:组学数据归档库。数据库(牛津大学)。2020;2020: baaa055。https://doi.org/10.1093/database/baaa055.
冯志才,李建勇,范勇,李宁伟,肖伟伟。CNGBdb:中国基因数据库。Hereditas。2020;42(8):799 - 809。
确认
所有作者在此感谢中国国家自然科学基金对这项工作的支持。
资金
国家自然科学基金资助(31871978,32172426)。
作者信息
作者及隶属关系
贡献
《概念化》刘景兰陈林;实验,孙丽彤,李季彤,刘永燕;分析,孙立同,李季同;原稿准备,孙立桐;李季同,刘景兰;编辑并回复评论者,Jinglan Liu和Ali Noman。所有作者均已阅读并同意该手稿的出版版本。
相应的作者
道德声明
伦理批准和参与同意书
本文中没有涉及人类或动物的研究。这些程序是按照适用的规范和条例进行的。所有实验方案均经扬州大学、扬州大学园艺系、植物保护系授权。
发表同意书
不适用。
相互竞争的利益
作者声明,这项研究是在没有任何可能被解释为潜在利益冲突的商业或财务关系的情况下进行的。
额外的信息
出版商的注意
伟德体育在线施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
补充信息
附加文件1:
表S1。17个样本的RNA-seq质量。表S2。实时定量PCR引物序列。表S3。富集的基因涉及不同途径。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可协议中,除非在材料的信用额度中另有说明。如果材料未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。如欲查看本牌照的副本,请浏览http://creativecommons.org/licenses/by/4.0/.创作共用公共领域奉献弃权书(http://creativecommons.org/publicdomain/zero/1.0/)适用于本条所提供的资料,除非在资料的信用额度中另有说明。
关于本文
引用本文
阳光、L。,J。,刘,Y。et al。在水稻中的转录组分析揭示了一种积极的作用OsNCED3为了抵御棕色飞虱,摘要研究选择性.BMC基因组学23, 634(2022)。https://doi.org/10.1186/s12864-022-08846-5
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/s12864-022-08846-5
关键字
- 脱落酸
- OsNCED3
- 摘要研究选择性
- 抗虫性
- 转录组分析