摘要
背景
年龄和性别特异性参考区间是解释儿童甲状腺激素测量的重要前提。然而,只有少数研究报道了TSH的年龄和性别特异性儿科参考值基底(TSH),游离T3 (fT3),游离T4 (fT4)。已知参考区间依赖于方法和种群。本研究的目的是建立从出生到18岁的血清TSH、fT3和fT4的参考区间,并评估性别差异。
方法
来自医院儿科人群的2194例甲状腺激素检测被纳入我们的回顾性分析。被诊断为可能影响甲状腺功能或药物可能影响甲状腺功能的个体主要被排除在外,如果诊断组与纯健康亚组不同,也被排除在外(n = 414)。年龄分别为1天~ 1个月、1 ~ 12个月、1 ~ 5岁、6 ~ 10岁、11 ~ 14岁和15 ~ 18岁。Advia法测定fT3、fT4、TSH水平®Centaur™自动免疫分析系统。
结果
创建参考数据的最终样本量TSH为1209,fT3为1395,fT4为1229。计算每个年龄组的中位数和2.5/10/25/75/90/97.5百分位。男性平均fT3浓度高于女性(p < 0.001)。TSH和fT4在年龄匹配的血清样本中没有发现性别差异。fT3、fT4和TSH的中位浓度在出生后的第一个月最高,随后随着年龄的增长持续下降。
结论
我们的研究结果证实了先前的研究结果,即甲状腺激素水平在儿童时期发生了显著变化,而成人参考区间并不普遍适用于儿童。此外,与以往研究相比,我们的参考区间存在差异,这可能是由于不同分析方法的抗体特征不同,不同人群或不确定的地理协变量,如碘和硒状态。
背景
儿童甲状腺功能减退与身体和/或认知发育受损有关。因此,大多数发达国家已经建立了新生儿甲状腺素(TSH)筛查,及时诊断和治疗先天性甲状腺功能减退,以预防严重的智力发育迟缓。在儿童和青少年时期,基础TSH水平被认为是诊断甲状腺功能减退和甲状腺功能亢进以及监测甲状腺替代治疗的最有价值的参数。然而,测量游离T4 (fT4)对于确认这些诊断是必不可少的,因为它直接反映了甲状腺的激素分泌[1].游离T3 (fT3)的测量只能间接反映甲状腺激素的产生,但可以提供额外的信息,因为大多数fT3是由脱碘酶在细胞内转化产生的。
尽管甲状腺功能在临床实践中对解释个体结果很重要,但儿科甲状腺功能参考值很少,且已发表的规范数据通常只包括少数患者[2- - - - - -7].此外,参考值差异很大,因为它们是人群和分析特异性的。已经观察到生长过程中甲状腺激素水平的显著变化,但与普遍的误解相反,青春期发育并不影响儿童甲状腺激素的浓度[3.].关于性别差异的数据不一致。营养和生活方式等生物学变量也可能影响甲状腺功能。
我们研究的目的是:1)建立健康儿童血清TSH、fT3和fT4浓度的年龄特异性参考区间;2)评估甲状腺功能的性别差异;3)将我们的结果与以前发表的参考数据进行比较。
方法
主题
2002年7月至2003年10月,从医院1天至18岁儿童人群的现有实验室数据中收集了血清TSH、fT3和fT4的常规结果。进出诊所的病人由于各种原因被送入因斯布鲁克医科大学儿科。受试者按年龄分组,分别为1天至1个月、1 - 12个月、1 - 5岁、6 - 10岁、11 - 14岁和15 - 18岁。年龄组的分类主要基于先前发表的研究,以方便可靠的比较结果,也具体根据所获得值的年龄相关病程。从410名患者中提取了两份或两份以上的血清样本,1085名患者仅提取了一份血清样本。所有程序都是按照《赫尔辛基宣言》办理的。
根据标准程序,在临床实践设置中定期收集数据。孩子们的父母知情同意了。在临床实践之外,没有采取进一步的措施。
使用国际疾病分类(ICD-10)代码对患者进行诊断分类。有可能影响甲状腺功能的疾病或伴随药物的儿童被排除在参照组[8].饮食失调、脑垂体疾病或染色体异常的患者也不包括在分析中。在临床检查中发现出现身高或体重偏差的患者,并将其归类为正常生长变异(ICD E34.3和E34.4),包括家族或体质因素。所有的诊断组都包含在一个单独的Excel文件中(附加材料)。各诊断组比较Z00.0进行统计学评估(n = 414;对无投诉和报告诊断的人进行一般检查和调查),使用单向方差分析事后分析(数据未显示)。具有以下ICD-10诊断代码提示甲状腺功能障碍的患者的血清样本被先验排除(n = 665):先天性甲状腺功能减退伴或不伴弥漫性甲状腺肿(E03.0, E03.1),其他非毒性甲状腺肿(E04.0 - E04.9),激素遗传不良甲状腺肿(E07.1),甲状腺毒症(E05.0 - E05.9),自身免疫性甲状腺炎和未指明的甲状腺炎(E06.3, E06.9),任何甲状腺肿瘤(C73和D44.0),术后甲状腺功能减退(E89.0),以及其他特定或未指明的甲状腺功能减退(E03.8, E03.9)。
方法
儿童和青少年未稀释血清样本的TSH、fT3和fT4在自动免疫分析系统(Advia®Centaur™,拜耳医疗诊断,奥地利维也纳),根据制造商说明使用直接化学发光检测系统[9,10].TSH采用两位点固相法进行分析,而fT3和fT4的分析采用竞争性分析。TSH、fT3和fT4的检测内变异系数分别< 8.7%、< 3.5%和< 8.1%。使用该免疫测定系统的成年患者的参考值最近已发表在BMC内分泌疾病和甲状腺[11,12].
统计分析
除上述总参照组的选择标准外,各诊断组的血清TSH、fT3和fT4值还与基本健康儿童和青少年亚组(n = 414)进行了方差分析和后Tukey's试验比较。统计上没有差异的组与健康参照组合并。检测甲状腺激素的正态分布。由于TSH值的强右尾偏态分布,需要进行自然对数变换[13,14].年龄组间比较采用单因素方差分析检验和事后Tukey检验。使用学生t检验对年龄组和性别之间的平均值进行进一步的事后比较。采用Pearson法进行相关分析。
p < 0.05为双侧差异有统计学意义。中位数和百分位数(2.5th到97.5th),作为参考区间。社会科学统计包(SPSS Inc.,芝加哥,伊利诺伊州,美国,版本12.0)用于统计分析和创建百分位数。
结果
TSH
TSH评估的最终样本量为1209。男性血清TSH浓度无差异(n = 636;52.6%)和女性(n = 573;47.4%)的儿童和青少年(p = 0.689)。因此,将两性结合起来计算百分位数。由于TSH值呈显著的右尾偏态分布,在分析前进行了对数变换。
97.5th0 - 1月龄组的百分位明显高于其他年龄组。TSH值随着年龄的增长而持续下降,特别是在生命的第一年。2.5th与出生后的第一年相比,第一个月的百分位数较低,随后也随着年龄的增长而下降(图2)1和表1)。TSH的方差在出生后第一个月最大,并随着年龄的增加而缩小(0-1个月:var = 15.04;1-12个月:var = 3.55;1-5年:var = 2.96;6-10年:var = 1.46;11-14年:var = 1.08;15-18年:var = 0.98)。反复评估甲状腺功能的32例患者的纵向亚组显示TSH最初升高,但fT3和fT4水平正常,在未治疗的3至6个月内自发下降并恢复正常。这些患者的年龄与整个组的年龄相符(1 - 18岁)。TSH最初升高的原因尚未发现。 The follow-up evaluations discarded the presence of subclinical hypothyroidism so that their TSH values were included. The initially elevated TSH levels were detected as outliers.
发生
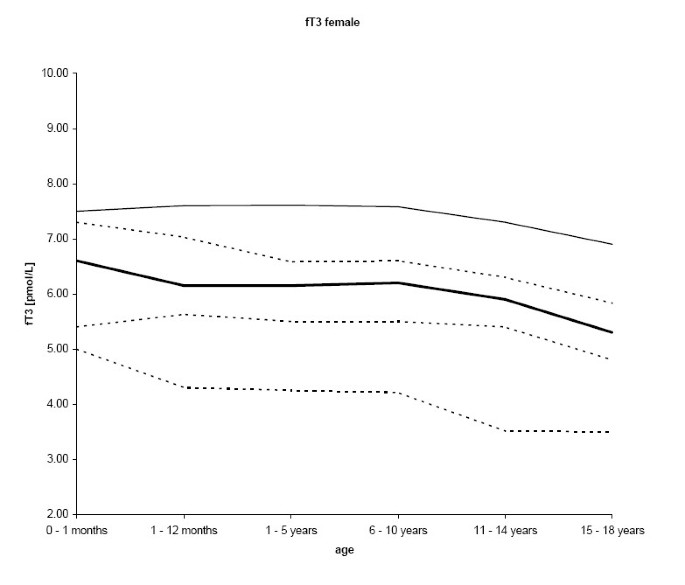
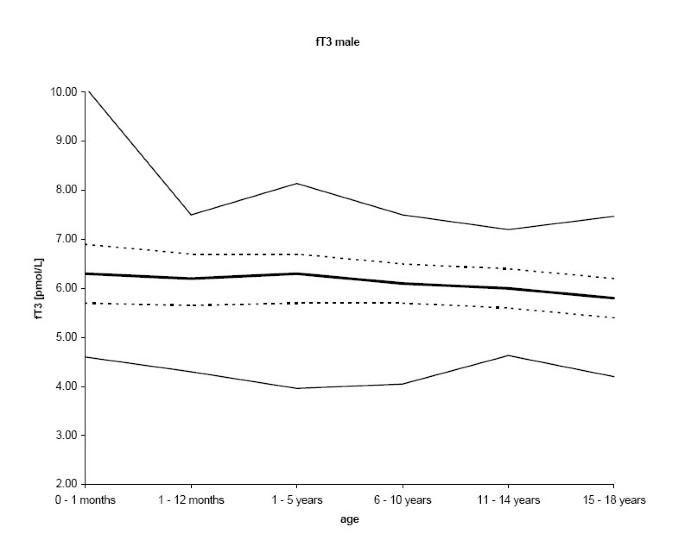
fT3的最终样本数为1395。fT3的结果呈正态分布。正如预期的那样,fT3的中位数浓度在一个月前的年龄组中最高,之后随着年龄的增长呈现持续下降的趋势(p < 0.001;女性R = -0.266,男性R = -0.196), 1 - 5岁男性和6 - 10岁女性除外。男性的平均fT3浓度更高(p < 0.001) (n = 824;59.1%)高于女性(n = 571;40.9%)。2.5的下降th与97.5相比,百分位更明显th百分位(数字2和3.、表2)。
fT4
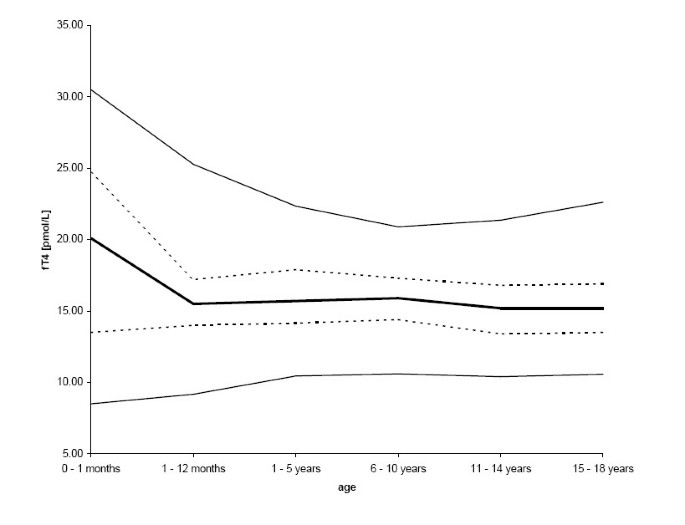
fT4的最终样本量为1229人(638名男性= 51.9%;女性591人(48.1%)。fT4值在各年龄组间无性别差异(p = 0.268),结果呈正态分布。fT4值与年龄呈显著负相关(p < 0.001;R = -0.122)。fT4的方差在出生后第一个月最大,然后随着年龄的增长而变小(0-1个月:var = 45.91;1-12个月:var = 8.60;1-5年:var = 7.68;6-10年:var = 6.13;11-14年:var = 8.20; 15–18 years: var = 8.08) (figure4)。97.5th在出生后的第一个月,每百分位的峰值为30.5 pmol/L,随后浓度稳定在20 - 22.5 pmol/L之间。50thfT4的百分比也在出生后的第一个月最大,在出生后的第一年迅速下降,随后一直保持不变,直到18岁(表4)3.)。
讨论
本研究为使用Advia的健康奥地利儿童和青少年提供了TSH、fT3和fT4的新的儿科参考区间®半人马™试验。成人甲状腺功能的参考值已经确定,尽管正常TSH值的上限目前也在讨论中[13,15- - - - - -19].最近成人甲状腺功能参数的参考值使用Advia®我们的研究组已经定义了Centaur™检测方法[11,12].在儿童和青少年中,可靠的年龄和性别特异性参考区间是正确解释个体甲状腺功能不可或缺的先决条件。然而,甲状腺激素值取决于人群和方法[20.,21].因此,使用不同的分析方法和不同受试者数量的抗体特征,发表了一系列儿童甲状腺参考数据[2- - - - - -7].据我们所知,只有一项针对儿童和青少年的小规模研究使用了Advia®Centaur™检测,广泛应用于临床实验室[4].
我们清楚地知道,同位素稀释串联质谱技术在测定游离甲状腺激素方面取得了方法上的进步[22- - - - - -29]这与平衡透析程序有更好的相关性[30.].尽管有这种优势,我们仍然主张使用免疫分析程序,正如我们在本研究中所做的那样。在以前的出版物中,我们广泛评估了这种系统用于确定成人参考值的临床适用性[11].在实践方面,Advia Centaur的免疫分析程序®[5]将在20分钟内提供符合临床使用要求的fT3、fT4、TSH、甲状腺球蛋白抗体和甲状腺过氧化物酶抗体检测结果[9,31].这些实用的便利超过了高额资本开支的需要[32].
我们的研究的一个局限性是它包括以医院为基础的人群。理想情况下,应使用从大量健康受试者队列中获得的血液样本来确定参考区间。然而,由于儿童的伦理和实际考虑,参考区间的确定往往依赖于大型医院数据库,通过应用适当的选择标准,确保足够数量的样本[33,34].本研究和其他类似研究中的参照组没有显著的人口基础,结果可能略有分歧。为了解决这一问题,我们排除了所有可能影响甲状腺功能的诊断和伴随药物的受试者。由此,受试者达到了ICD10 Z00类所预见的健康人口标准。
除1 - 5岁男性和6 - 10岁女性的fT3值外,所有甲状腺参数的中位数浓度在出生后的第一个月最高,随后随着年龄的增长而下降。总的来说,我们的参考数据与以往使用各种分析方法的儿童队列研究一致。与以前的研究相比,我们的参考区间略有差异(表4,5,6)可以用不同的分析分析、种族、人口或地理衍生的协变量(如生活方式、盐碘化和营养)来解释。我们研究组在2000年对成年患者进行的最后一次碘状态评估显示尿排泄的平均值为120 μg碘/gr肌酐(R. Moncayo, 2002年分析的未发表数据)。
在我们的研究队列中,只有fT3存在显著的性别差异。有趣的是,Hübner等人发现,在使用相同Advia的11 - 14岁年龄组中,对fT3残差也有性别特异性影响®Centaur™分析仪系统[4].索尔丁等[5]报告了性别特异性参考范围,而没有测试统计显著性,Djemli等人。[6]发现只有在15 - 17岁年龄组,女孩和男孩在fT4残差上存在显著差异,而Elmlinger等人[3.]没有发现任何性别差异,这也是通过调整青春期阶段得出的结论。这些不一致的发现的原因尚不清楚。需要在儿童和青少年中进行进一步的研究,以调查性别对甲状腺激素水平是否有显著的影响,以证明有明确的参考区间。
有趣的是,在32名儿童的纵向亚组中,在第一个血清样本中TSH水平最初升高,TSH在3 - 6个月内未经治疗就降至正常。决定不治疗这些儿童是基于临床状态,因为它不对应于亚临床或临床甲状腺功能减退,即使初始TSH值升高。这一现象表明存在影响甲状腺功能的短暂良性疾病。因此,我们建议最初TSH值升高的患者应在考虑替代疗法之前,每隔约3至6个月重新检测一次[35].此外,在将儿童或青少年归类为甲状腺功能减退之前,还应考虑fT3、fT4水平、甲状腺过氧化物酶抗体的存在,以及在特定情况下刺激TSH升高的程度[36,37].进一步的儿童前瞻性研究,类似于Huber等人的研究。[38],需要研究儿童和青少年亚临床甲状腺功能减退的自发过程,并确定显性甲状腺功能减退发展的危险因素。
除了15 - 18岁年龄组外,成人人群,特别是TSH,与公布的参考区间存在差异。最近,一些作者主张将成人TSH的上限范围降低到2.5 mU/L或稍微温和一些的3.0 mU/L [15,16,39,40].将这一上限应用于儿科患者可能会导致相当多的甲状腺功能减退误诊,并导致不必要的终身替代治疗。成人TSH参考值也有类似的情况[41].
总之,本研究为中欧人群提供了从出生到青年时期甲状腺功能检测的儿科参考区间。甲状腺激素水平在儿童时期显著变化,除fT3外,没有明显的性别差异。此外,我们的参考区间与以往研究相比存在差异,这可能是由于不同分析方法的抗体特征不同、人群不同或地理协变量未知所致。我们的研究结果支持成人参考区间并不普遍适用于儿童。这些参考区间可作为正确解释儿童和青少年个体甲状腺激素结果的工具。
结论
我们的研究结果证实了先前的研究结果,即甲状腺激素水平在儿童时期发生了显著变化,而成人参考区间并不普遍适用于儿童。此外,与以往研究相比,我们的参考区间存在差异,这可能是由于不同分析方法的抗体特征不同,不同人群或不确定的地理协变量,如碘和硒状态。
缩写
- TSH:
-
促甲状腺素
- 发生:
-
免费trioiodithyronine
- fT4:
-
免费的甲状腺素。
参考文献
大燕CM:甲状腺功能检查的解释。《柳叶刀》,2001,357:619-624。10.1016 / s0140 - 6736(00) 04060 - 5。
Zurakowski D, Di Canzio J, Majzoub JA:儿童血清甲状腺素、三碘甲状腺原氨酸、促甲状腺素和游离甲状腺素的参考区间。中华临床医学杂志,1999,30(4):344 - 344。
Elmlinger MW, Kuhnel W, Lambrecht HG, Ranke MB:从出生到成年血清甲状腺素(T4),三碘甲状腺原氨酸(T3),游离T3,游离T4,甲状腺素结合球蛋白(TBG)和促甲状腺素(TSH)的参考区间。中华临床医学杂志,2001,39:973-979。10.1515 / CCLM.2001.158。
Hubner U, Englisch C, Werkmann H, Butz H, Georgs T, Zabransky S, Herrmann W:使用ADVIA半人马座分析仪建立新生儿、婴儿、儿童和青少年甲状腺激素的连续年龄依赖参考范围。中华医学杂志,2002,30(4):344 - 344。10.1515 / CCLM.2002.182。
Soldin SJ, Morales A, Albalos F, Lenherr S, Rifai N:雅培IMx的FSH, LH,催乳素,TSH, T4, T3,游离T4,游离T3, t摄取,IgE和铁蛋白的儿科参考范围。中国生物医学工程学报,1998,28(3):344 - 344。10.1016 / 0009 - 9120(95) 00038 - 5。
Djemli A, Van Vliet G, Belgoudi J, Lambert M, Delvin EE:魁北克新生儿、儿童和青少年游离甲状腺素、总三碘甲状腺原氨酸、促甲状腺素和甲状腺球蛋白的参考区间。中华生物医学杂志,2004,37:328-330。10.1016 / j.clinbiochem.2003.12.006。
Wiedemann G, Jonetz-Mentzel L, Panse R:新生儿、婴儿、儿童和青少年中促甲状腺素、三碘甲状腺原氨酸、甲状腺素和游离甲状腺素参考范围的建立。中华临床生化杂志,1993,31:377 - 377。
Surks MI, Sievert R:药物与甲状腺功能。中华实用医学杂志,2003,26(3):344 - 344。10.1056 / NEJM199512213332507。
Vogeser M, Weigand M, Fraunberger P, Fischer H, Cremer P: ADVIA Centaur TSH-3试验的评价。中华临床医学杂志,2000,38:331-334。10.1515 / CCLM.2000.048。
罗林斯ML,罗伯茨WL:六种第三代甲状腺激素测定的性能特征。中国生物医学工程学报,2004,27(3):344 - 344。10.1373 / clinchem.2004.039156。
Moncayo R, Moncayo H, Virgolini I:促甲状腺素参考值。中国生物医学工程学报,2005,30(4):344 - 344。
Moncayo H, Dapunt O, Moncayo R:基于静脉TRH刺激试验的基础TSH测定的诊断准确性:2570次试验的评估和与文献的比较中国生物医学工程学报,2007,27(3):366 - 366。
Surks MI, Goswami G, Daniels GH:促甲状腺素参考范围应保持不变。中华内分泌杂志,2005,30(4):589 - 596。10.1210 / jc.2005 - 0170。
Draper NR:应用回归分析书目更新1994-97。交通统计理论与方法,1998,27:2581-2623。10.1080 / 03610929808832244。
Baskin HJ, Cobin RH, Duick DS, Gharib H, Guttler RB, Kaplan MM, Segal RL:美国临床内分泌学家协会评估甲亢和甲减治疗的临床实践医学指南。中国生物医学工程学报,2002,8:457-467。
国家临床生物化学学会:NACB检验医学实践指南。[http://www.nacb.org/lmpg/main.stm]
Zophel K, Wunderlich G, Gruning T, Koch R, Doge H, Kotzerke J:[亚临床甲状腺功能减退从哪里开始?]对甲状腺刺激激素上参考限值定义的启示]。核医学杂志,2005,44:56-61。
Zophel K, Wunderlich G, Kotzerke J:甲状腺激素参考区间的定义是否需要确定一个参考人群?中国生物医学工程学报,2006,29(3):329- 329。10.1373 / clinchem.2005.060111。
Kratzsch J, Fiedler GM, Leichtle A, Brugel M, Buchbinder S, Otto L, Sabri O, Matthes G, Thiery J:基于国家临床生物化学学会标准和常规甲状腺超声检查的促甲状腺激素和甲状腺激素的新参考区间。中国生物医学工程学报,2005,29(4):344 - 344。10.1373 / clinchem.2004.047399。
d’herbomez M, Forzy G, Gasser F, Massart C, Beaudonnet A, Sapin R: 9种游离甲状腺素检测的临床评价:特定人群的持续性问题。中华临床医学杂志,2003,41:942-947。10.1515 / CCLM.2003.143。
Demers LM, Spencer CA:实验室医学实践指南:甲状腺疾病诊断和监测的实验室支持。临床内分泌(Oxf)。2003, 35(4): 344 - 344。10.1046 / j.1365-2265.2003.01681.x。
Soukhova N, Soldin OP, Soldin SJ: T4/T3同位素稀释串联质谱测定方法。临床化学学报,2004,37(3):344 - 344。10.1016 / j.cccn.2004.01.007。
顾娟,苏廷平,苏廷平,等:同位素稀释串联质谱同时测定游离三碘甲状腺原氨酸和游离甲状腺素。中国生物医学工程学报,2007,30(4):344 - 344。10.1016 / j.clinbiochem.2007.08.007。
苏晓燕,王志强,王志强,等。同位素稀释串联质谱法测定游离甲状腺素的研究。临床化学学报,2005,37(5):531 - 531。10.1016 / j.cccn.2005.02.010。
Despres N, Grant AM:甲状腺检测中的抗体干扰:临床误诊的潜在原因。中华临床医学杂志,1998,44:444 -454。
Landau-Levine M, Way BA, Clutter WE, Scott MG, Gronowski AM:用Abbott AxSym免疫分析法检测促甲状腺激素抗体干扰。临床化学学报,1999,29(1):377 - 382。10.1016 / s0009 - 8981(98) 00213 - 7。
Martel J, Despres N, Ahnadi CE, Lachance JF, Monticello JE, Fink G, Ardemagni A, Banfi G, Tovey J, Dykes P:使用不同自动化免疫分析平台和抗体干扰高风险标本进行甲状腺检测的多中心比较研究。中华临床医学杂志,2000,38:785-793。10.1515 / CCLM.2000.112。
Kricka LJ:免疫检测的干扰仍然是一个威胁。中华临床医学杂志,2000,29(4):344 - 344。
Ekins R:类似物游离甲状腺素免疫测定的有效性。中华临床医学杂志,1997,33(3):337 - 344。
kahricic - janicic N, Soldin SJ, Soldin OP, West T, Gu J, Jonklaas J:串联质谱提高了妊娠期游离甲状腺素测量的准确性。中国生物医学工程学报,2007,27(3):344 - 344。10.1089 / thy.2006.0303。
Waskiewicz D, Burkhardt A, Emancipator K: 6种第三代促甲状腺激素检测方法的性能特征。中华临床医学杂志,2005,29(4):531 - 531。10.1373 / clinchem.2005.055632。
Singh RJ, Eisenhofer G:高通量、自动化和精确的嗜铬细胞瘤生化筛查:我们已经做到了吗?中国生物医学工程学报,2007,29(3):344 - 344。10.1373 / clinchem.2007.089128。
Kouri T, Kairisto V, Virtanen A, Uusipaikka E, Rajamaki A, Finneman H, Juva K, Koivula T, Nanto V:从住院患者的数据中得到参考区间:基于实验室和诊断数据结合的计算机化方法中华临床医学杂志,1994,30(4):529 - 529。
Harwood SJ, Cole GW:基于入院实验室数据的参考值。《美国医学协会杂志》上。1978, 30(4): 344 - 344。10.1001 / jama.240.3.270。
Diez JJ, Iglesias P, Burman KD:亚临床甲状腺功能减退患者促甲状腺素浓度的自发正常化。中华内分泌杂志,2005,30(4):344 - 344。10.1210 / jc.2005 - 0375。
Ladenson PW, Singer PA, Ain KB, Bagchi N, Bigos ST, Levy EG, Smith SA, Daniels GH:美国甲状腺协会甲状腺功能障碍检测指南。中华医学杂志,2000,26(3):357 - 357。10.1001 / archinte.160.11.1573。
Cooper博士:临床实践。亚临床甲状腺功能减退。中华实用医学杂志,2001,34(3):366 - 366。10.1056 / NEJM200107263450406。
Huber G, Staub JJ, Meier C, Mitrache C, Guglielmetti M, Huber P, Braverman LE:亚临床甲状腺功能减退自发性病程的前瞻性研究:促甲状腺素、甲状腺储备和甲状腺抗体的预后价值。中华内分泌杂志,2002,27(3):344 - 344。10.1210 / jc.87.7.3221。
Stephens PA:内分泌学会:甲状腺疾病管理的当前问题。环境科学学报,2004,29:23-26。
Dayan CM, Saravanan P, Bayly G:谁的甲状腺功能正常比较好,你的还是我的?《医学杂志》,2002,36:353-10.1016/S0140-6736(02)09602-2。
Fatourechi V, Klee GG, Grebe SK, Bahn RS, Brennan MD, Hay ID, McIver B, Morris JC:降低正常TSH值上限的影响。《美国医学协会杂志》上。2003, 29(4): 366 - 366。10.1001 / jama.290.24.3195-b。
出版前的历史
本文发表前的历史可以在这里访问://www.mivven.com/1472-6823/8/15/prepub
确认
我们感谢因斯布鲁克医科大学核医学系的技术人员所做的分析工作。
作者信息
作者及隶属关系
相应的作者
额外的信息
相互竞争的利益
作者宣称他们之间没有利益冲突。
作者的贡献
KK与RM共同起草手稿,设计和协调研究。CK收集患者资料,与RM一起进行统计分析。RM和IV负责免疫检测。WH和KS参与了患者数据的收集。所有作者都阅读并批准了最终的手稿。
权利和权限
本文由BioMed Central Ltd授权发布。这是一篇开放获取文章,根据创作共用属性许可协议(http://creativecommons.org/licenses/by/2.0),允许在任何媒介上不受限制地使用、传播和复制,前提是正确地引用原始作品。
关于本文
引用本文
卡佩拉里,K., Kirchlechner, C., Högler, W.;et al。从出生到成年甲状腺激素水平的儿科参考区间:一项回顾性研究。BMC Endocr不一致8, 15(2008)。https://doi.org/10.1186/1472-6823-8-15
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/1472-6823-8-15
关键字
- 甲状腺激素
- 甲状腺肿
- 参考区间
- 亚临床甲状腺功能减退
- 先天性甲状腺功能减退