摘要
颞叶癫痫(TLE)很难治疗,因为它往往难以治疗。除了传统的药物治疗外,手术切除也是一种治疗选择,但手术可能会导致明显的认知障碍。因此,使用有针对性和可调节的刺激故障脑回路的治疗策略已经开发出来。这些使用电和磁神经调节方法的神经调节疗法已经在临床上用于难治性癫痫,而其他如光遗传学、化学遗传学和超声调节等正在临床前TLE动物模型中进行测试。在这篇综述中,我们对临床可用的神经调节方法进行了深入的文献检索,重点研究了可能的作用机制和包括不良反应在内的临床结果。还讨论了目前在临床前动物模型中探索的技术,但在未来可能具有治疗应用。不同神经调节方法的疗效和不良反应各不相同,其中一些在TLE治疗中的作用机制尚不清楚。还需要进一步的研究来评估其益处和潜在的局限性。继续研究癫痫的治疗机制和癫痫脑网络对于改善TLE的治疗至关重要。
背景
全世界约有5,000万人患有癫痫[1].国际抗癫痫联盟将癫痫定义为"一种症状,其特征是在超过24小时的时间内出现两次或两次以上的反复癫痫发作,且无任何立即确定的病因引起" [2].根据发作的来源,癫痫可分为广泛性或局灶性发作[2,3.].在局灶性癫痫发作中,颞叶癫痫(TLE)最为常见,影响40%的青少年和成人癫痫患者[1].TLE可同时影响大脑的两个叶,但常以单侧病灶为主[3.].
TLE也是一种最常见的耐药癫痫[4,5),因此它的管理仍然具有挑战性。TLE常与潜在的组织病理改变有关,主要是海马硬化(HS) [6],这与耐药发生率增加有关[4,6].出现耐药的患者可从手术中获益,手术包括部分或全部切除内侧颞叶结构[4].然而,即使切除,30%-40%的TLE患者仍未表现出临床改善[5,7].此外,当致痫灶位于双侧或高功能皮质区时,切除可能不可行[8].因此,需要新的治疗方式来解决治疗差距。
虽然癫痫发作是癫痫最突出的临床特征,但TLE患者的几种共病风险增加,包括认知功能障碍,如记忆、注意力和行为缺陷。尽管认知障碍主要与癫痫发作有关,但已发现无癫痫发作期间的异常电活动(发作间活动)也在认知共病中发挥作用[9].此外,癫痫发作间期脑电图(EEG)变化在TLE中比在其他癫痫中更常见[10,11],在临床管理中具有重要意义,需要进一步研究。
对癫痫网络的更好理解导致了新疗法的确定,其中包括神经调节。“神经调节”是一种可逆和有效的治疗方案,通过有针对性的外部或内部刺激大脑来改变特定神经群体的行为。不同的神经调节方法已经开发用于癫痫的管理,如脑深部刺激(DBS),经颅直流电刺激(TDCS),迷走神经刺激(VNS)和经颅磁刺激(TMS)。这些方法已在难治性TLE患者的随机对照试验中得到广泛验证[12,13,14,15].
在这篇综述中,我们讨论了这些神经调节方法在难治性TLE临床管理中的疗效。对于每种疗法,我们提供临床试验的主要和次要结果。我们还回顾了神经调节在临床前动物模型中的应用,并讨论了它们在未来转化为人类患者的潜力。
文献检索
在PubMed、MedLine和Clinicaltrials.gov上进行文献检索,检索词为“颞叶癫痫”、“癫痫发作”,干预的MESH特定术语为“脑深部刺激”或“经颅直流电刺激”或“迷走神经刺激”或“经颅磁刺激”。选择了对难治性TLE患者进行干预的随机对照试验、双盲或单盲或非盲或安慰剂对照研究。如果患者在接受至少两种一线抗癫痫药物的充分治疗后出现不受控制的癫痫发作,则被认为是耐药患者[16].搜索仅限于人类研究和用英语发表的论文。在每篇论文的参考文献中,将被评审的论文进一步扩展到相关文章。
星展银行
DBS包括通过由电池供电的脉冲发生器控制的立体战术植入电极对皮层下结构进行直接电刺激,以治疗性地改变神经功能。DBS在改善肌张力障碍、帕金森病和图雷特综合征的运动功能方面显示出巨大的前景[17,18].这一成功已将其应用范围从治疗运动障碍扩展到治疗抑郁症等精神障碍[19]和强迫症[20.].DBS也被应用于治疗各种形式的癫痫发作障碍,从主要的运动性癫痫到无症状癫痫,以及广泛性和局灶性癫痫,如TLE [21].在癫痫治疗中,DBS系统集成了感应电极,可检测癫痫发作并仅在需要时进行电刺激,从而形成“闭环刺激”。
作用机制
神经调节在DBS中的作用机制尚不清楚。然而,早期的研究表明,这种影响本质上是抑制性的。研究表明,刺激丘脑下核可抑制帕金森病患者的神经元活动[17]和动物模型[18].这导致了“抑制假说”的引入[19],这表明癫痫焦点的抑制是由于电压门控离子通道去极化或失活的阻断[20.,21,22].DBS的效果与消融性手术如pallidotomy和thalamotomy相当。一些研究还表明,电极植入和刺激过程中产生的微病变可以解释DBS减少癫痫发作的方式[20.,23,24].DBS对神经抑制的另一种解释是刺激期间和刺激后γ -氨基丁酸(GABA)水平的增加和GABA- b受体表达的上调[20.,25].
DBS的结果和疗效是复杂的,它们取决于内在的神经元特征和刺激参数。这些参数包括植入电极与目标区域的接近程度,以及刺激振幅、频率和脉冲宽度[26].一项模拟研究表明,在刺激频率下,电极周围约2毫米内的大部分细胞将被激发,而那些在阈值以下水平上被激发的细胞将被抑制[27].先前的一项研究表明,神经结构也在决定刺激结果方面发挥着作用。有髓鞘的轴突具有最低的激活阈值,而无髓鞘的轴突、树突和细胞体具有较高的激活阈值[28].此外,神经化学机制、基因和蛋白质表达也会影响DBS的疗效[29].
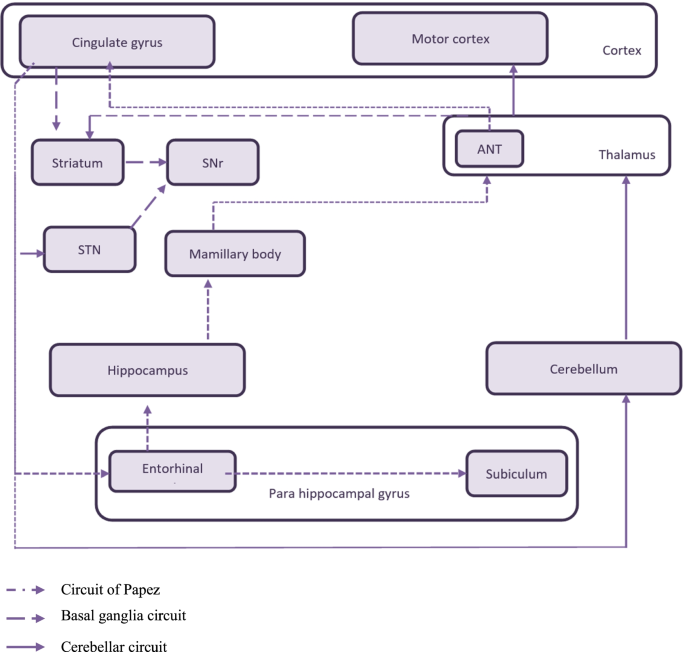
尽管局灶性癫痫发作(如TLE)起源于特定的大脑区域,但它们通常沿不同的神经通路传播(图2)。1) [10,22].关于这些途径的知识,结合动物模型的损伤研究,可以为神经调节的目标提供见解。此外,由于沿着这些回路的皮层和皮层下大脑区域在功能上和解剖学上是相连的,一个区域的活动最终会影响其他区域的活动。例如,丘脑水平的网络中断已被发现会改变额叶和颞叶癫痫的癫痫发作传播[23,24].此外,一项临床试验表明,刺激小脑齿状核可抑制癫痫的泛化。因此,这是对齿状-丘脑-皮质通路的间接抑制[25].通过刺激丘脑下核(STN)对黑质网状部(SNr)的神经调节也被用于癫痫的治疗[5,26].高频刺激STN已被证明可以通过减少STN到SNr的兴奋性输入来抑制SNr [27,28].尽管颞叶和STN之间缺乏直接联系,但有人认为颞叶和STN之间存在间接通路[29].STN也可能是癫痫发作通过运动皮层传播的原因,从而导致普遍化[30.].
丘脑前核
DBS的疗效因癫痫发作病灶的位置而异[31].在一项纵向研究中,对癫痫患者的丘脑前核进行刺激,癫痫发作集中在颞叶的患者癫痫发作的中位下降幅度更大(44.2%),而接受对照治疗的患者癫痫发作的中位下降幅度为21.8%。然而,与对照组相比,癫痫发作集中在额叶、顶叶或枕叶区域的受试者在刺激后癫痫发作减少方面没有表现出显著差异[31].
海马结构
为了本综述的目的,海马的形成是指齿状回,海马体本身(即,角氨),和亚丘皮层。在大多数研究中,海马刺激有令人鼓舞的结果,超过50%的参与者不再癫痫发作[32,33,34].然而,伴有HS的TLE患者的效果不如无HS的TLE患者[35].原因可能是对刺激的反应依赖于完整的局部神经元网络,因此,HS患者的胶质细胞增生阻碍了神经调节[36].矛盾的是,一些研究报告了HS患者的结果比MRI检查正常的患者更好[33,34].此外,关于电极植入引起的微损伤效应的报道也显示出相互矛盾的结果。而一些研究报告无病变或不明显病变[36,37],也有研究将良好的结果归因于电极植入引起的微小病变[34].
小脑
由于样本量小,评估小脑DBS在癫痫治疗中的使用的研究有限,特别是TLE。一项研究表明,刺激小脑齿状核减弱发作和发作间期发作活动[25].
基底神经节
Chkhenkeli等人证明,对尾状头的单侧低频刺激不仅能抑制双侧癫痫放电,还能减少同侧癫痫发作间放电[25].这种刺激也抑制癫痫泛化。同样,一个病例报告显示,STN-DBS可使TLE患者的癫痫发作减少50% [28].
安全性和耐受性
DBS的不良反应通常是手术并发症的结果,其中电极迁移、手术部位感染、电极放置部位皮肤腐蚀、脑出血和脑水肿是最常见的不良反应[31,35,38].除此之外,还发现了刺激区域特异性效应。例如,对边缘结构的刺激已被发现会影响记忆和情绪[33,34,39];STN刺激与运动障碍相关[28];小脑刺激与共济失调和运动障碍有关[25,37].神经心理学测试显示,在认知、情绪或记忆方面没有明显变化。31,38].
TDCS
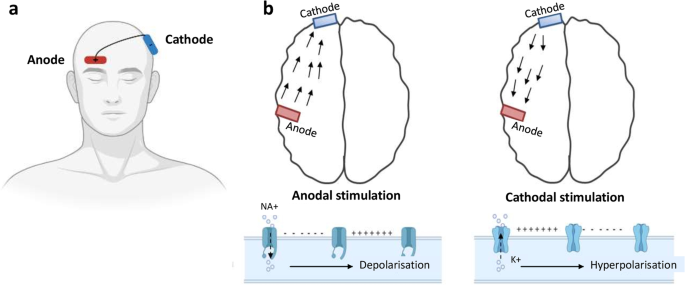
TDCS是一种非侵入性神经电刺激技术,通过头皮上的电极传递低电流以产生负(阴极)或正(阳极)刺激。该装置由一个刺激电极/活性电极和一个附着在头皮上的返回电极组成。电极的准确位置取决于刺激区域。然后将电极连接到外部刺激器[40].TDCS已被用于治疗抑郁症[41]、纤维肌痛[42],以及癫痫[43].
作用机制
TDCS使用低强度电流(1-2 mA),通过阴极或阳极刺激两种方式之一改变皮层兴奋性。阴极刺激引起超极化,从而抑制神经,而阳极刺激通过去极化刺激神经元(图。2) [44].癫痫中的兴奋/抑制不平衡因此可以通过这种应用来减弱。癫痫的治疗侧重于阴极刺激。TDCS在细胞和突触水平起作用[45]即蛋白质合成的变化,细胞内循环amp [46]和钙含量[47]被观察到。研究发现,即使停止刺激,影响仍会持续。48,对确定增产方案具有重要意义。这种刺激的“Hebbian”性质与长期增强和抑郁有关[49].
最近一项关于TDCS在癫痫治疗中的应用的综述报告了有希望的结果,癫痫发作减少67%,发作间癫痫样活动减少83%。该综述包括6项研究中的65名参与者,但没有具体说明那些患有TLE的人,因此很难评估TDCS对TLE的疗效[50].针对TLE中TDCS的研究报告,10例(83.3%)TLE患者无癫痫发作(癫痫发作减少50%),而其他6例患者在刺激后1个月无癫痫发作,2例患者被认为无反应[51].另一项研究报告称,只有42.14%的耐药TLE患者发作频率降低,但刺激具有持续的效果,因为一名患者接受2天的刺激后发作频率降低了4个月[52].在另一项研究中,主动组与假手术组相比,刺激后最初没有明显的癫痫减轻。然而,在两个月的随访后,活跃组的平均癫痫发作频率降低了48%,皮质兴奋性显著降低[53].
不同的结果可能是由于不同的刺激方案和治疗期间持续使用抗癫痫药物所致。研究发现,刺激强度、持续时间和间隔等参数对TDCS的效果有很大影响。例如,长时间的高强度刺激会导致更深的刺激,从而导致脱靶效应[52,54].因此,增产的主要目标是达到最大的疗效和最小的不良副作用。一项研究表明,应用18分钟阴极TDCS,前9分钟后间隔20分钟(9-20-9方案)将增加抑制作用[52,54].此外,重复刺激也已被证明通过影响神经可塑性而具有延长的抑制作用[50,51,54].
安全性和耐受性
TDCS已被发现副作用很小或没有副作用。然而,在某些情况下,高强度刺激与刺激部位的疼痛有关[55].
迷走神经刺激法
迷走神经刺激包括人工或电刺激迷走神经以达到治疗目的。VNS的设置包括位于左锁骨下方的表面脉冲发生器和位于迷走神经颈段的刺激器。VNS用于癫痫发作调节的早期证据首次出现在17世纪,当时发现手动按摩颈动脉可以抑制癫痫发作[56].这为VNS在癫痫中的治疗应用提供了思路,并为后续的研究铺平了道路。电VNS在动物实验中进行,并证明具有抗惊厥作用[57].这项技术随后被批准用于治疗耐药性癫痫[58].
迷走神经麻醉可应用于左侧或右侧迷走神经,但不首选右侧迷走神经,因为右侧常伴有心动过缓和血糖升高[59,60,61].左颈迷走神经系统已获批准用于治疗耐药性癫痫和抑郁症,而右颈迷走神经系统已在临床试验中被研究用于治疗心力衰竭[62].刺激器的输出电流由脉冲发生器根据患者的耐受性调节,还可以向患者提供磁铁,以便在发生不良事件时立即停止刺激。
作用机制
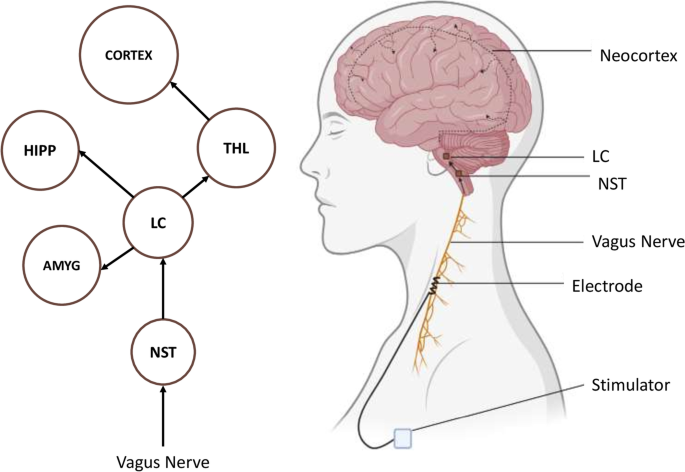
迷走神经是由感觉/传入纤维和运动/传出纤维组成的混合脑神经。感觉纤维起源于心脏、主动脉、肺和胃肠道[63]并构成80%的神经纤维,而传出纤维构成自主神经系统(副交感神经)的一部分。传入纤维投射到孤束核(NST),广泛投射到前脑和脑干的几个区域,是VNS治疗应用的靶点。NST向旁巨细胞核发送兴奋性输出,旁巨细胞核又向蓝斑(LC)发送兴奋性输出。然后LC将肾上腺素能输入到海马体和杏仁核(图。3.) [64,65].vns诱导的癫痫减轻机制包括抑制从NST到LC的边缘投射,因为LC已被确定为癫痫发生和癫痫泛化的区域[65].当损伤大鼠的LC时,VNS的抗惊厥作用被阻断,已经证明了这一点[66].
对VNS的研究已经报道了双侧TLE患者的长期癫痫发作减少[15]及双边[67,68]癫痫灶。即使停止刺激,VNS对癫痫发作减少的影响仍然存在。反复刺激可增加治疗效果[69].García-Navarrete等人报道80%的参与者癫痫发作减少63% [15].这些结果与其他研究相似,其他研究报告了5名双颞叶TLE患者的癫痫发作减少了60%,刺激一年后癫痫发作平均减少了50% [67].另一项研究报告了持续的效果,刺激后18个月癫痫发作减少42% [68].
发作间癫痫样放电的减少已被发现是良好预后结果的主要预测因素。Janszky等人证实了这一点。[70],他发现双侧发作间癫痫样放电的缺失与良好的结果相关。然而,一项研究报道,与双侧发作间期放电的患者相比,唯一一名发作间期无放电的患者在癫痫发作减轻方面没有差异[67].
安全性和耐受性
一项评估VNS并发症和安全性的纵向回顾性研究显示,总体并发症发生率为12.4% [71].这些并发症包括手术并发症,如血肿、手术部位感染、器械移位等,以及迷走神经损伤所带来的并发症,如声带麻痹及随后的声音沙哑[15,67,68,70].由于迷走神经具有自主神经功能,其特性的变化是刺激的结果,具有自主神经影响。这些影响被认为在心脏表现为心动过缓和血流动力学不稳定[59,71].相比之下,最近的研究发现VNS患者的心率变异性和血压没有显著变化[72].在之前的一项研究中,一些TLE患者出现了严重的副作用,最终导致植入物被移除[15].副作用包括两名患者感染,一名患者吞咽疼痛,一名患者先前存在的行为问题恶化,表现出严重的攻击性[15].
经颅磁刺激
经颅磁刺激是一种利用外部磁场调节神经行为的干预手段。将磁化线圈放置在想要的目标上,并产生约2 t的磁场。为了定位致痫病灶,使用脑电图监测和磁共振成像(MRI)来精确放置线圈。经颅磁刺激可用于治疗中风、抑郁症和肌萎缩性侧索硬化症[73,74,75,76].经颅磁刺激具有改变皮层兴奋性的能力,因此也被应用于癫痫的治疗[77].除药物治疗外,经颅磁刺激还可用于神经回路研究,因为它能勾画出特定的目标[78].综上所述,经颅磁刺激是一种无创、相对无痛的治疗方法,在反复刺激后产生持续的疗效[79],使其成为神经调节的首选方法。
作用机制
经颅磁刺激装置由铜线圈组成,产生磁脉冲,进而诱导电流,使附近的轴突去极化。Reithler等人假设低频刺激通过延长突触抑制/长期抑制导致目标神经群体的抑制[80].这已在动物研究中得到证实,TMS引起初始兴奋,随后是延迟抑制[81].TMS作用的确切机制尚不清楚;然而,根据刺激的强度,甚至是受刺激的神经元类型,其效果也有所不同。有证据表明,重复的TMS诱导了主要神经元上特定突触的可塑性,而10hz刺激引起的是树突抑制,而不是躯体抑制[82],虽然靠近锥体神经元体的小树突棘可能不会有相同的反应[82,83].这一特征在TLE中特别有趣,因为皮层的刺激可以促进沿丘脑-皮层投射的可塑性。该装置的作用范围可以根据刺激的频率、强度、持续时间以及所使用线圈的位置和尺寸来改变。虽然局部刺激可达2厘米深,但经颅磁刺激也可影响较远的区域[80].
我们发现很少证据表明经颅磁刺激对TLE有效[84,85,86].虽然经颅磁刺激对实现癫痫发作自由的治疗效果最小,但一项研究进一步比较了不同刺激强度的效果,发现高强度(90%静息运动阈值)刺激比低频(20%静息运动阈值)刺激更能降低癫痫发作频率(降低79.8% vs 2.3%) [84].所使用的频率为0.5 Hz,这与其他观察到皮层抑制的研究一致[14,86,87].在有反应的患者中,观察到新皮质病灶患者的癫痫发作减轻程度大于颞近侧病灶患者[85,88].
TLE对TMS的不良反应可能与TLE近端发作灶的深度有关。经颅磁刺激的效果随距离的平方而变差;因此,对皮层下结构的直接影响很小[89].直接刺激正确的癫痫病灶被发现是改善经颅磁刺激反应的关键[14,43];然而,基于TLE癫痫灶的解剖位置,定位可能很困难。此外,经颅磁刺激已被证明对癫痫灶位于皮质凸起的患者有效[85],尽管也有人注意到经颅磁刺激可以沿着特定的神经网络对远处的目标施加影响[90,91].后者已通过发现初级感觉运动皮层的刺激与深层结构(如壳核和丘脑)的激活相关而得到证明[90].这种效应是有希望的,因为它允许进一步研究TLE的间接神经调节。
安全性和耐受性
讨论
本文就神经调节在TLE治疗中的临床应用作一综述。神经调节在TLE治疗中有广阔的应用前景,但效果不一。除了治疗结果,应用技术的差异(侵入性与非侵入性)也在选择治疗方法时发挥作用。由于这些疗法在应用上差异很大,建议使用其中一种而不是另一种是不可行的。然而,要对神经调节在TLE临床治疗中的应用提出一般性建议,必须接受潜在收益和危害之间的妥协.这些决定应在与患者的主治医生讨论后在个人基础上做出。在本节中,我们将根据所观察到的缺陷,就未来如何改进临床试验提出建议。
神经调节研究的主要局限性之一是研究参与者数量少,特别是TLE患者。在潜在的神经调节技术中,只有少数在随机和双盲试验环境中进行了研究,正在进行的试验中TLE患者的样本量很小。鉴于目前可用的研究有限,需要更多的临床试验来提供神经调节治疗TLE的有效性和安全性的证据。大样本量可能会降低偏倚风险,并为在TLE临床管理中引入神经调节提供证据。然而,由于患者招募困难,在多个中心进行的小型试验将增加可用证据,并允许获得更简明的结果。
另一个限制是缺乏必要的长期随访试验。长期随访可深入了解刺激反应的持续性,包括冲洗期的反应,以及慢性刺激可能产生的副作用。此外,更长时间的跟踪可以清楚地解释增产参数。例如,一项评估海马电刺激对TLE的影响的研究表明,在停止刺激后的三个月内,两名患者的癫痫发作继续减少25% [35].如果DBS植入后在刺激开始前没有相关评估,植入过程中的微小病变可能被遗漏。同样,HS的存在也会影响对治疗的反应。一项使用DBS的研究指出,一个月的随访期不足以让HS患者表现出缓解[39].因此,在方案中引入洗脱期或使用替代研究设计,如平行研究设计,可以评估任何遗留效应。
此外,另一个局限性是报告的结果测量的变化。几乎所有回顾的论文都将癫痫发作频率作为主要结局指标,少数研究报告了发作间期放电,而将神经心理学测试和生活质量作为次要结局的研究就更少了。由于受影响的大脑区域,TLE通常与认知障碍有关;此外,相关的发作间期活动进一步增加认知障碍[9].因此,作为治疗方案的一部分,测量发作间期活动和进行神经心理测试是很重要的。
未来的方向
有一些令人兴奋的工具可以以非凡的特异性调节神经元种群,这可能为改进TLE干预铺平道路。其中包括靶向基因疗法,如光遗传学和化学遗传学。光遗传学利用兴奋性通道或抑制通道中的视蛋白,通过特定波长的光控制视蛋白,来调节神经元的活动[93].另一方面,化学遗传学使用设计受体,这种受体只有被设计药物激活才能用于特殊设计的配体[94].鉴于它们的选择性表达,光遗传学和化学遗传学可以以令人难以置信的特异性和显著的时间精度调节神经元种群。此外,它们允许直接调节癫痫中的兴奋性/抑制性不平衡,因为它们根据实验设计来激发或抑制电路。这种特异性最大限度地减少脱靶效应,从而提供针对性的治疗,副作用更少。
化学遗传学和光遗传学已导致急性和慢性模型(包括TLE的动物模型)的癫痫显著减少[95,96].除此之外,体外抑制癫痫放电也已被证实[97].除了潜在的治疗应用,这些工具还可以促进我们对癫痫神经回路的理解。93],从而为间接神经调节提供了潜在的靶点。已经有几篇论文讨论了化学遗传学和光遗传学在临床前动物模型中的应用;然而,在转化为临床应用之前,仍有一些担忧。
他们翻译的一个主要问题是病人的安全。虽然病毒载体已用于临床试验,没有重大副作用[98,但人们仍然担心这种工具在人类身上的实用性。其中一个关注点是针对视蛋白表达所需的神经群体。此外,人们还担心基因疗法的长期影响。化学遗传学特别关注的是配体氯氮平- n -氧化物(CNO)的药效学/药代动力学效应。CNO很容易代谢成氯氮平[99然后可以连接到其他几个受体上。这种影响可以通过使用奥氮平等替代配体来克服,奥氮平已经被批准用于人体,副作用最小。除此之外,随着化学遗传学的最新发展,药理学选择性致动器和效应器模块(PSAM/PSEM)使用修饰过的内源性受体和专门设计的配体进行神经调节[94].
在光遗传学的情况下,光传递的模式是一个独特的挑战,包括植入的安全性和刺激的充分性。光探针的植入可能与电刺激中的电极类似,前提是探针很坚固。然而,适当的光刺激是一个较具挑战性的问题,因为通常使用的波长很容易被脑组织吸收[One hundred.].为了缓解这个问题,可以使用不同波长的光,因此必须开发对这些波长敏感的视蛋白。红光敏感视蛋白的研究[101,102已经取得了一些成功,因为红光被脑组织吸收的较少,因此能够穿透到皮层下结构。在病毒传递和表达的问题上,腺相关病毒已在若干I期和II期临床试验中安全使用[98].从啮齿动物模型进行临床转化的另一个瓶颈是大脑大小的差异。人类的大脑∼比老鼠大1000倍,因此有必要研究更大的动物。在帕金森猴模型中使用光遗传学的研究已显示出积极的结果,并证明它们可能是从啮齿动物到人类的合适过渡[103].这种大小的差异给病毒体积注射、转导特异性以及光照覆盖带来了挑战。由于探针必须足够薄以避免结构损伤,并且光强必须足够低以避免光毒性,因此可能需要更好的探针设计。为此,Tønnesen和Kokaia设计了一种具有多个纤维束的光极,可以覆盖更大的区域[104].
结论
已经取得的进展是非常令人鼓舞的使用调节疗法,以改善癫痫网络功能障碍。然而,由于样本量小、纳入标准不同(双侧与单侧癫痫灶、硬化症的存在)以及缺乏对参与者的长期随访,无法就最佳实践得出明确的结论。此外,大多数研究没有报告发作间性癫痫样结果。技术改进和患者安全是临床前实验转化的关键。考虑到有希望但不稳定的结果,需要更多精心设计的研究来评估这些治疗的疗效,并将其与其他神经调节方法以及现有的手术和药物治疗进行比较。
数据和材料的可用性
不适用。
缩写
- 星展银行:
-
深部脑刺激
- 脑电图:
-
脑电描记法
- GABA:
-
氨基丁酸
- 海关:
-
海马硬化
- LC:
-
蓝斑
- 核磁共振成像:
-
磁共振成像
- 望远镜:
-
孤束的核
- 信噪比:
-
黑质网状部
- STN:
-
Sub-thalamic核
- 框架:
-
颞叶癫痫
- 经颅磁刺激:
-
经颅磁刺激
- 迷走神经刺激法:
-
迷走神经刺激
- PSAM:
-
药理学选择性执行器模块
- PSEM:
-
药理学选择性效应器模块
参考文献
近颞叶癫痫综合征:最新综述。癫痫临床神经生理学杂志,2005;11(3):141-4。
Scheffer IE, Berkovic S, Capovilla G, Connolly MB, French J, Guilhoto L,等。ILAE癫痫分类:ILAE分类和术语委员会的立场文件。Epilepsia。2017;58(4):512 - 21所示。
Ergene E, Shih JJ, Blum DE, So NK。颞叶癫痫患者双颞独立发作间期癫痫样放电的频率。Epilepsia。2000;41(2):213 - 8。
Engel J, McDermott MP, Wiebe S, Langfitt JT, Stern JM, Dewar S,等。耐药颞叶癫痫的早期手术治疗:一项随机试验。《美国医学协会杂志》上。307(9): 922 - 2012; 30。
Tellez-Zenteno JF, McLachlan RS,家长A, Kubu CS, Wiebe S.海马电刺激治疗近侧颞叶癫痫。神经学。2006;66(10):1490 - 4。
Téllez-Zenteno JF, Hernández-Ronquillo L.颞叶癫痫的流行病学综述。癫痫治疗。2012;2012:630853。
布莱尔读数。颞叶癫痫符号学。癫痫治疗。2012;2012:1 - 10。
Kapur N, Prevett M.意外健忘症:从单侧颞叶手术后的健忘症病例中,我们可以吸取教训吗?《大脑》,2003;26(Pt 12): 2573-85。
张志刚,张志刚,张志刚。慢性癫痫与认知。中华神经医学杂志2004;3(11):663-72。
拉迪诺LD, Moien-Afshari F, Téllez-Zenteno JF。颞叶癫痫的综合综述。神经障碍临床方法。第1版iConcept出版社;2014.1-35页。
张志刚,Rémi J.脑电图在癫痫中的作用:一个重要的回顾。癫痫行为学杂志,2009;15(1):22-33。
韩春林,胡伟,Stead M,张涛,张建国,Worrell GA,等。海马体电刺激治疗难治性颞叶癫痫。Brain Res Bull. 2014; 109:13-21。
Kwon CS, Ripa V, Al-Awar O, Panov F, Ghatan S, Jetté N.癫痫与神经调节的随机对照试验。中国脑科学,2018;8(4):69。
周永勇,韩世杰,郑世伟,赵建伟,徐德伟,洪雪生。低频重复经颅磁刺激对不同刺激时间和部位抗癫痫的影响。临床神经物理。2007;118(3):702-8。
García-Navarrete E, Torres CV, Gallego I, Navas M, Pastor J, Sola RG。长期服用抗癫痫药物的成人难治性癫痫迷走神经刺激的长期结果。扣押。2013;22(1):卖地。
Kwan P, Schachter SC, Brodie MJ。耐药性癫痫。中华实用医学杂志,2011;29(4):344 - 344。
Kim W, Pouratian N.脑深部刺激治疗图雷特综合症。神经外科杂志2014;25(1):117-35。
脑深部刺激的起源和发展。前沿整合神经科学2011;5(8):1-5。
holtzzheimer PE, Kelley ME, Gross RE, Megan M, Garlow SJ, Barrocas A,等。美国卫生与公众访问。2015;69(2):150-8。
布洛斯戴德P, Sjöberg RL,韩松M,博德隆德O,哈里兹MI.深部脑刺激在强迫症治疗中的应用。中华神经外科杂志,2013;30(6):344 - 344。
Salanova V.深部脑刺激治疗癫痫。癫痫行为学杂志,2018;88:21-4。
大川浩,李志刚,李志刚,李志刚。近颞叶硬化症的MRI诊断。神经放射学。2001;43(3):205 - 10。
张志刚,张志刚。癫痫发生机制的研究。治疗癫痫第三版,2009;14(5):67-79。
深部脑刺激治疗难治性癫痫的临床疗效。临床神经外科杂志。2016;140:11-25。
Chkhenkeli SA, Šramka M, Lortkipanidze GS, Rakviashvili TN, Bregvadze ES, Magalashvili GE,等。直接脑刺激治疗顽固性癫痫的电生理效应及临床结果。中华神经外科杂志,2004;16(4):318-29。
宋杰,宋海峰,宋华。成人神经发生对海马神经回路的影响。神经科学进展。2012;32(7):1032-43。
帕金森病和肌张力障碍的后腹侧姑息切开术发生了什么?神经病治疗。2008;5(2):281 - 93。
讲义A, DeSalles AAF, Krahl SE。脑深部丘脑下核刺激作为难治性癫痫的辅助治疗。Epilepsia。2006;47(7):1239 - 41。
Bröer S.不是颞叶的一部分,但仍然重要?癫痫的黑质和丘脑下核。神经科学。2020;14:581826。
Bolam JP, Hanley JJ, Booth PAC, Bevan MD.基底神经节的突触组织。王志强。2000;19(4):527 - 427。
Fisher R, Salanova V, Witt T, Worth R, Henry T, Gross R,等。电刺激丘脑前核治疗难治性癫痫。51 Epilepsia。2010;(5):899 - 908。
Boon P, Vonck K, De Herdt V, Van Dycke A, Goethals M, Goossens L,等。顽固性颞叶癫痫患者的深部脑刺激。Epilepsia。2007年,48(8):1551 - 60。
Cukiert A, Cukiert CM, Burattini JA, Lima AM。顽固性颞叶癫痫患者海马深部脑刺激后的癫痫发作结果。扣押。2014;23(1):6 - 9。
Cukiert A, Cukiert CM, Burattini JA, Mariani PP, Bezerra DF。顽固性颞叶癫痫患者海马深部脑刺激后癫痫发作结局:一项前瞻性、对照、随机、双盲研究Epilepsia。2017;58(10):1728 - 33所示。
McLachlan RS, Pigott S, Tellez-Zenteno JF, Wiebe S,父母A.双侧海马刺激治疗顽治性颞叶癫痫:对癫痫发作和记忆的影响。51 Epilepsia。2010;(2):304 - 7。
Cuéllar-Herrera M, Velasco M, Velasco F, Velasco AL, Jiménez F, Orozco S,等。亚急性电刺激后颞叶癫痫患者海马旁GABA系统及细胞损伤的评价。Epilepsia。2004;45(5):459 - 66。
Velasco F, Carrillo-Ruiz JD, Brito F, Velasco M, Velasco AL, Marquez I,等。双侧小脑刺激治疗顽固性运动性癫痫的双盲、随机对照试点研究。Epilepsia。2005;46(7):1071 - 81。
Osorio I, Overman J, Giftakis J, Wilkinson SB.高频丘脑刺激治疗不能手术的近颞叶癫痫。Epilepsia。2007;48(8):1561 - 71。
Velasco AL, Velasco F, Velasco M, Trejo D, Castro G, Carrillo-Ruiz JD。电刺激海马癫痫病灶以控制癫痫发作:一项双盲长期随访研究。Epilepsia。2007;48(10):1895 - 903。
Thair H, Holloway AL, Newport R, Smith AD。经颅直流电刺激(tDCS):设计和实施的初学者指南。前沿神经科学,2017;11(11月):1-13。
Ferrucci R, Bortolomasi M, Vergari M, Tadini L, Salvoro B, Giacopuzzi M,等。经颅直流电刺激治疗重度耐药抑郁症。情感失调。2009;29(1):1-3。
Mendonca ME, Simis M, Grecco LC, Battistella LR, Baptista AF, Fregni f经颅直流电刺激联合有氧运动优化纤维肌痛的镇痛反应:一项随机安慰剂对照临床试验神经科学。2016;10:68。
弗雷尼F, Otachi PTM, Do Valle A, Boggio PS, Thut G, Rigonatti SP,等。反复经颅磁刺激治疗难治性癫痫的随机临床试验。神经科学进展。2006;60(4):447-55。
Nitsche MA, Cohen LG, Wassermann EM, Priori A, Lang N, Antal A,等。经颅直流电刺激:2008年的最新进展。脑刺激。2008;1(3):206-23。
极化后大鼠大脑皮层神经元放电速率持续增加的机制:蛋白质合成的作用。大自然。1968;220(5165):383 - 4。
李志刚,李志刚,李志刚。极化电流对大鼠大脑皮层腺苷敏感生成的影响。神经科学杂志1990;116(3):320-4。
李志刚,李志刚,李志刚。大鼠脑内钙离子含量的研究。大脑决议1995;684(2):206-8。
极化后大鼠大脑皮层神经元放电速率持续增加的机制:混响回路或突触电导的改变?大自然。1968;220(5165):382 - 3。
Kronberg G, Rahman A, Sharma M, Bikson M, Parra LC。直流电刺激可提高离体hebian的可塑性。脑刺激。2020;13(2):287-301。
San-Juan D, Morales-Quezada L, Orozco Garduño AJ, Alonso-Vanegas M, González-Aragón MF, López DAE,等。经颅直流电刺激治疗癫痫。脑刺激。2015;8(3):455-64。
Tekturk P, Erdogan ET, Kurt A, Vanli-yavuz EN, Ekizoglu E, Kocagoncu E,等。经颅直流电刺激对近颞叶癫痫合并海马硬化患者癫痫发作频率的影响。临床神经外科杂志。2016;149:27-32。
Zoghi M, O 'brien TJ, Kwan P, Cook MJ, Galea M, Jaberzadeh S.阴极经颅直流电刺激治疗耐药颞叶癫痫:一项初步随机对照试验。癫痫病公开赛2016;1(3-4):130-5。
Juan Orta DS, Espinoza López AA, Gregorio RV, Trenado C, Gonzalez-Aragon MF, Morales-Quezada L,等。经颅直流电刺激治疗近颞叶癫痫和海马硬化。临床神经物理。2017;10(1):28-35。
Monte-Silva K, Kuo MF, Liebetanz D, Paulus W, Nitsche MA。阴极经颅直流电刺激(tDCS)的最佳重复间隔。中华神经医学杂志,2010;36(4):339 - 339。
古林聪,Terao Y, Arai N, Okabe S,望月H, Hanajima R,等。短时间和长时间经颅直流电刺激(tDCS)在人的手运动区域。中国脑科学,2008;29(2):369 - 369。
Lanska DJJL。康宁和迷走神经刺激治疗癫痫。神经学。2002;58(3):452 - 9。
重复迷走神经刺激对犬实验性癫痫的抑制作用。Epilepsia。1992;33(6):1005 - 12所示。
Ben-Menachem E, Rydenhag B, Silander H.迷走神经刺激新系统治疗难治性局灶性发作的初步经验。癫痫行为学杂志,2013;29(2):416-9。
Stauss嗯。左右颈迷走神经刺激大鼠血流动力学和呼吸的差异反应。物理学报2017;5(7):e13244。
Stauss HM, Stangl H, Clark KC, Kwitek AE, Lira VA.清醒大鼠颈迷走神经刺激损害葡萄糖耐量和抑制胰岛素释放。物理学报2018;6(24):e13953。
Castellanos-Diaz J, Amole M, Surabhi S, Kadiyala S.高血糖与迷走神经刺激的应用。J Endocr Soc 2021;5(增刊1):A386。
De Ferrari GM, Schwartz PJ。迷走神经刺激:从临床前到临床应用:挑战和未来方向。心脏衰竭,2011;16(2):195-203。
Browning KN, Verheijden S, Boeckxstaens GE。迷走神经在食欲调节、情绪和肠道炎症中的作用。胃肠病学。2017;152(4):730 - 44。
张志刚,张志刚,张志刚。副巨细胞核蓝斑位点的激活:一种新的大脑兴奋性氨基酸通路。神经科学杂志,1988;8(10):3644-57。
傅乃华,李丽娟,李丽娟,等。迷走神经刺激诱导蓝斑位点抗癫痫活性的研究。中华神经科学杂志,2011;33(12):2169-78。
克拉尔SE,克拉克KB,史密斯DC,勃朗宁RA。蓝斑病灶抑制迷走神经刺激的癫痫减弱作用。Epilepsia。1998;39(7):709 - 14所示。
Alsaadi TM, Laxer KD, Barbaro NM, Marks WJ, Garcia PA。迷走神经刺激治疗双侧独立颞叶癫痫。Epilepsia。2001;42(7):954 - 6。
王晓明,张晓明,张晓明,张晓明。迷走神经刺激对双颞叶癫痫患者的影响。中华神经外科杂志2003;10(1):91-4。
高谷M,特里WJ,成德DK。迷走神经刺激可诱导持续的抗惊厥作用。37 Epilepsia。1996;(11):1111 - 6。
Janszky J, Hoppe M, Behne F, Tuxhorn I, Pannek HW, Ebner A.迷走神经刺激:癫痫发作自由的预测因子。中华神经外科杂志。2005;36(3):384-9。
Révész D, Rydenhag B, Ben-Menachem e迷走神经刺激的并发症和安全性:单一中心25年的经验。儿科神经外科杂志,2016;18(1):97-104。
garmendi - ruiz I, Gómez-Esteban JC。迷走神经刺激的心血管自主效应。中国临床医学杂志2019;29(2):183-94。
Weise D, Mann J, Ridding M, Eskandar K, Huss M, Rumpf JJ,等。参与配对联想刺激诱导的皮质脊髓兴奋性降低的微回路机制。中国生物医学工程杂志,2013;29(4):344 - 344。
Sonmez AI, Camsari DD, Nandakumar AL, Voort JLV, Kung S, Lewis CP,等。抑郁症的加速经颅磁刺激:系统回顾和荟萃分析。精神病学决议2019;273:770-81。
Vucic S, Ziemann U, Eisen A, Hallett M, Kiernan MC.经颅磁刺激与肌萎缩性侧索硬化症:病理生理学见解。中华神经外科杂志,2013;29(3):344 - 344。
Bergey GK, Morrell MJ, Mizrahi EM, Goldman A, King-Stephens D, Nair D,等。对成人难治性部分癫痫的长期脑刺激治疗。神经学。2015;84(8):810 - 7。
Kimiskidis VK。经颅磁刺激治疗耐药癫痫:原理和临床经验。神经科学杂志,2010;63(4):205-10。
罗宏宁,王晓峰,王晓峰。导航经颅磁刺激。神经生理学杂志,2010;40(1):7-17。
George MS, Nahas Z, Molloy M, Speer AM, Oliver NC, Li XB,等。每日左前额叶皮层经颅磁刺激治疗抑郁症的对照试验。生物精神病学杂志2000;48(10):962-70。
雷瑟勒J,彼得斯JC,萨克。多模态经颅磁刺激:使用并发神经成像揭示无创脑刺激的神经网络动态。神经生物学进展。2011;94(2):149-65。
赵玉玲,赵玉玲,王晓霞,等。经颅磁刺激对猫初级视觉皮层单单元活动的影响。中国生物医学工程杂志,2003;29(3):344 - 344。
Lenz M, Galanis C, Müller-Dahlhaus F, Opitz A, Wierenga CJ, Szabó G,等。重复磁刺激诱导抑制性突触的可塑性。Nat Commun. 2016;7:10020。
Vlachos A, Funke K, Ziemann U.评估和调节皮质抑制使用经颅磁刺激。e-Neuroforum。2017; 23(1):上行线。
孙伟,毛伟,孟x,王东,乔林,陶伟,等。低频重复经颅磁刺激治疗难治性部分癫痫:一项对照临床研究。Epilepsia。2012;53(10):1782 - 9。
王志强,陈晓明,王志强,等。经颅磁刺激治疗癫痫:一项对照研究神经学。2002;59(4):560 - 2。
孙伟,付伟,毛伟,王东,王艳。低频重复经颅磁刺激治疗难治性部分癫痫。脑电图与神经科学。2011;42(1):40-4。
弗雷尼F, Otachi PTM, Do Valle A, Boggio PS, Thut G, Rigonatti SP,等。反复经颅磁刺激治疗难治性癫痫的随机临床试验。神经科学进展。2006;60(4):447-55。
Daniele O, Brighina F, Piazza A, Giglia G, Scalia S, Fierro B.低频经颅磁刺激对皮质发育不良患者的初步研究。中华神经科学杂志,2003;26(6):761-2。
陈晓峰,陈晓峰,陈晓峰。经颅磁刺激的三维头部模型模拟。生物工程学报,2004;51(9):1586-98。
Bestmann S, Baudewig J, Siebner HR, Rothwell JC, Frahm J.经颅磁刺激对皮层和皮层下运动回路直接影响的功能MRI。中华神经科学杂志2004;19(7):1950-62。
Valero-Cabré A, Payne BR, Rushmore J, Lomber SG, Pascual-Leone A.顶叶皮层重复经颅磁刺激对代谢脑活动的影响:猫的14C-2DG示踪研究。大脑科学,2005;(1):1 - 12。
王旭,杨东,王松,赵旭,张磊,陈忠,等。低频重复经颅磁刺激对偶极子源定位后15例颞叶癫痫患者脑电图和癫痫发作频率的影响神经再生学报,2008;3(11):1257-60。
张晓明,张晓明,张晓明,等。颞叶癫痫自发性发作的光基因控制。Nat Commun. 2013; 4:1-8。
斯特恩森,罗斯。化学发生工具来询问大脑功能。神经科学。2014;37:387-407。
Kätzel D, Nicholson E, Schorge S, Walker MC, Kullmann DM.局灶性新皮层癫痫的化学-遗传衰减。Nat Commun. 2014;5:3847。
王志强,王志强,王志强,等。癫痫:光遗传学和钾通道基因治疗在鼠局灶性新皮质癫痫模型。中国生物医学工程学报,2012;26 (4):426 rs32。
李文杰,李文杰,李文杰,李文杰,等。化学诱导小鼠超同步爆破的光遗传抑制。神经生物学杂志2014;65:133-41。
Simonato M, Bennett J, Boulis NM, Castro MG, Fink DJ, Goins WF,等。神经系统疾病基因治疗研究进展。神经科学进展。2013;9(5):277-91。
张文华,林雪峰,连海飞,魏长峰,胡文华,林永富,等。精神分裂症患者氯氮平和氧化氯氮平的可逆代谢。神经精神药理学进展。1998;22(5):723-39。
王玲,王强,王志强,王志强,等。光遗传刺激下大鼠脑内的光分布和热效应。生物光子学学报,2016;9(6):576-85。
Häusser M.光遗传学:光的时代。Nat Methods. 2014;11(10): 1012-4。
林建勇,桑思生,周凯,Nabavi S, Proulx CD, Malinow R,等。发色团辅助光失活(CALI)对突触释放的光遗传抑制。神经元。2013;79(2):241 - 53年。
史陶佛,李志强,李志强,李志强,等。猕猴多巴胺神经元特异性光遗传刺激。细胞。2016;166(6):1564 - 71。
Tønnesen J, Kokaia M.癫痫与光遗传学:光能控制癫痫发作吗?中国生物医学工程杂志2017;31(14):1605-16。
确认
感谢Alfredo-Gonzalez Sulser博士在本研究期间的持续支持。
资金
不适用。
作者信息
作者及隶属关系
贡献
AAE检索并回顾了现有的研究。AT还审阅了最终稿并提出了宝贵的建议,是稿件写作的主要贡献者。所有作者都阅读并批准了最终的手稿。
相应的作者
道德声明
伦理批准并同意参与
不适用。
发表同意书
不适用。
相互竞争的利益
作者宣称他们之间没有利益冲突。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可协议中,除非在材料的信用额度中另有说明。如果材料未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。如欲查看本牌照的副本,请浏览http://creativecommons.org/licenses/by/4.0/.
关于本文
引用本文
Ebrahim, a.a., Tungu, a .颞叶癫痫的神经调节:范围综述。Acta Epileptologica4, 25(2022)。https://doi.org/10.1186/s42494-022-00086-0
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/s42494-022-00086-0
关键字
- 深部脑刺激
- 耐药性癫痫
- 神经刺激
- 迷走神经刺激
- 经颅直流电刺激
- 经颅磁刺激