摘要
脊椎关节炎是一组以轴性和/或外周关节炎症以及关节外表现为特征的慢性炎性全身性疾病。当脊柱和/或骶髂关节主要受累时,采用轴性颈椎病的分类。此版本的建议取代了2013年5月发布的先前指南。
通过系统的文献综述,选取237项研究,提出29项建议,回答15个临床问题,分为4个部分:诊断、非药物治疗、常规药物治疗和生物治疗。对于每一项建议,都告知了支持的证据级别(可用的最高级别),根据牛津大学的强度等级,以及专家的一致程度(评分者之间的可靠性)。
这些指南提供了关于轴向SpA患者临床管理的循证信息,包括诊断、治疗和预后。
介绍
根据最近的定义,脊椎关节炎(SpA)是一组以脊柱和周围关节炎症以及关节外表现为特征的疾病,包括前葡萄膜炎,牛皮癣和炎症性肠病,具有与人类白细胞抗原B27 (HLA-B27)相关的遗传易感。SpA谱系包括强直性脊柱炎(AS)、银屑病关节炎(PsA)、反应性关节炎(ReA)、肠病性关节炎(EA)和未分化性脊柱炎(uSpA)。根据国际脊椎关节炎协会(ASAS)的分类标准,脊柱和/或骶髂关节受累被命名为轴性脊椎关节炎(axial SpA) [1,2]。仅累及阑尾关节被称为周围型颈椎病(p-SpA)。另一方面,如果患者同时具有两种临床特征,则应根据优势(即主要是轴向受累或主要是外周受累)对其进行分类。
这些指南的目的是为风湿病学家、全科医生、联合专家(皮肤科、眼科和胃肠病学)和其他联合专业人员(如物理治疗师)提供关于轴向SpA患者临床管理的循证信息,包括诊断、治疗和预后。此版本取代2013年5月26日发布的先前指南[3.],并应每四年更新一次。
方法
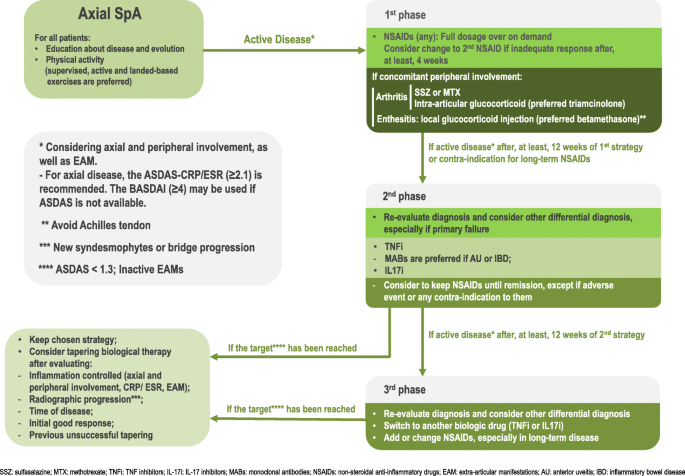
进行了系统的文献综述,并对巴西医学协会的一个专门小组进行了外部审查。使用PICO (Patient | Intervention | Comparison | Outcome)策略定义的关键词,并在以下数据库中搜索自2012年3月1日至2018年12月31日的记录:MEDLINE、EMBASE、SciELO/ LILACS和Cochrane Library。根据2009年的ASAS分类标准,目标人群包括患有3个月或以上背痛且年龄小于45岁的患者[1,2]。选择237项研究,并用于制定29项建议,回答15个临床问题,这些问题分为四个部分:诊断、非药物治疗、常规药物治疗和生物治疗。对于每一项建议,根据牛津循证医学中心2001年的证据水平,提供支持的证据级别(现有的最高)和强度等级[4是知情的。文献研究的方法细节和牛津证据水平的表格可在附加文件中获得1.通过在线匿名调查,采用德尔菲法确定专家认同程度(评分者间信度)。表格1总结了这些建议,图。1给出了一种轴向SpA管理的指导算法。
在可能的情况下,结果以绝对值形式呈现,然后是效应量测量,以突出其临床意义或实际相关性。在治疗和未治疗(安慰剂)比例的比较中,需要治疗的数量(NNT)或需要伤害的数量(NNH),以及各自的置信区间(95% CI)是使用正态近似计算的,这是统计上最稳健的方法。从用于定义这些间隔的每个研究中检索的数据可在附加文件中获得2.在配对均数(治疗前和治疗后)的比较中,使用科恩方法计算效应量(均数之间的差除以组的合并标准差)。效应大小被认为是0.2到0.4之间的小效应,0.4到0.8之间的中效应和大于0.8的大效应。
临床问题
1.诊断患有脊椎关节炎的临床标准是什么?
2009年,ASAS小组在所有成员的参与下,进行了一项基于德尔菲法的研究,并选择了应评估轴向SpA患者的所有可能变量。这些变量在一项前瞻性研究中进行了评估,该研究包括来自16个国家的25所大学中心的647名患者,他们经历了3个月以上的背痛,没有明确的原因或已知的诊断,有或没有外周症状,症状在45岁之前开始。
提出了基于两个主要变量的分类标准(表2).基于这些标准的敏感性为82.9%,特异性为84.4% [1,2) (1 b).虽然轴向性SpA的一些病例可能在45岁后开始,但将这一年龄设置为分界点,以强调在这一年龄后引起背痛的许多其他原因,特别是退行性疾病,可以模拟轴向性SpA的影像学变化特征。尽管对ASAS提出的用于建立SpA分类标准的方法提出了具体的批评,但它们代表了我们对SpA谱的理解取得了相当大的进步,并已被国际社会广泛采用。
一项旨在评估ASAS提出的轴向SpA分类标准在中国患者中表现的研究发现,ASAS标准的诊断一致性优于欧洲脊椎关节病研究小组(ESSG)和Bernard Amor建立的标准。ESSG、Amor和ASAS标准的敏感性值为81.5,特异性值分别为78.6、87.7、89.4%,分别为76.7及86.4% [5) (2 b).
另一项名为propa(轴向SpA患病率)的研究评估了另一人群中ASAS标准的表现:18岁以上的美国人,45岁前出现慢性背痛。在这项研究中,直接应用ASAS组提出的分类标准,可以诊断47%的轴向SpA患者。ASAS标准的特异性和敏感性分别为79和81%,略低于其他“精选”人群中报道的值,可能与hla - b27阳性个体患病率较低有关[6) (2 b).2016年,基于ASAS分类标准,对轴向SpA队列(N = 394例患者)的长期随访(平均4.4年)数据显示,阳性预测值为86 ~ 96% [7) (2 b).
尽管ASAS标准已经有了很好的表现,如上所示,但其在诊断不同人群中的有效性有所不同,特别是在慢性背痛和轴向SpA预测概率较低的个体中。考虑到45岁以后开始出现背痛的患者,在临床实践中,ASAS轴向标准在将其归类为晚发型轴向SpA方面的表现也是最好的[8) (2 b).
建议
| 应采用2009年ASAS标准对轴性脊椎关节炎患者进行分类。诊断应由有经验的医生或风湿病专家进行。证据等级:1B;推荐强度:A(强);一致度:9.2。 |
2.磁共振成像(MRI)对轴向SpA的初步评估有什么作用?
骶髂关节(SIJ)和脊柱成像对轴向SpA患者的诊断、分型、监测和预后起着关键作用。骨结构改变通常是晚发性的,可通过常规x线摄影清楚地发现[9) (2摄氏度),而通常较早出现的炎症改变,使用核磁共振成像更能评估[10,11) (2 b).
诊断
2009年,ASAS/风湿病预后测量(OMERACT) MRI工作组发表了明确的骨髓水肿和骨炎的存在(在一片切片中至少有两个部位或在连续的两片切片中有一个部位)是诊断活动性骶髂炎的必要条件。在静脉(IV)造影剂(钆)注射后,通过短tau反转恢复(STIR)图像和带有脂肪抑制(FS)的T1加权(T1W)序列(T1与gd后FS)均可见活动性炎症病变[12) (5).2012年,一项研究评估了29例早期炎症性背痛(IBP)患者的基线SIJ MRI扫描,这些患者随后根据ASAS标准被诊断为轴性SpA,以验证ASAS对活动性骶髂炎的定义。该研究报告的敏感性为79%,特异性为89%,阳性似然比(LR+)为7.1,阴性似然比(LR-)为0.2 [13) (2 b).在另一项采用回顾性设计的研究中,分析了110例转诊接受SIJ MRI检查的患者(其中28例后来被诊断为轴向SpA),骶骨区以及骶骨和髂区骨髓水肿的存在是诊断的独立预测因子,优势比(or)分别为7.07 (95% CI 1.05-47.6)和36 (95% CI 5.61-23.1) [14) (2 b).
一项多中心研究评估了187人(75例强直性脊柱炎(AS)患者,27例放射前IBP患者,26例非特异性背痛患者和59例健康对照)的SIJ MRI扫描的诊断实用性,结果显示,骨髓水肿、糜蚀、脂肪化生和强直对轴性SpA诊断的敏感性为90%,特异性为97%,LR+ = 30,因此,轴向SpA阳性诊断确定性为97%,轴向SpA阴性诊断确定性为91% [11) (1).根据其他三项研究,在定义骶髂炎(除骨髓水肿外)时,包括糜烂,但不包括脂肪化生,可增加敏感性而不损失特异性[15,16,17) (2 b).在DESIR队列中,包括短期轴向SpA患者(IBP≥3个月,≤3年),SIJ MRI上的结构性病变(≥5个糜烂或脂肪化生)可靠地使用,而不是阳性x线摄影[18) (2 b).相反,在SPACE队列中,5个慢性病变(糜烂或脂肪化生)的任何组合在区分有无轴向SpA患者时确保特异性>95% [19) (2 b).在同一队列(SPACE)的SIJ MRI中,使用静脉MRI造影剂(钆)对检测滑膜炎和/或囊炎至关重要,但与单独使用STIR相比,未能提高检测的敏感性,因为这些急性病变仅在同时出现骨髓水肿的患者中观察到(在STIR上可见)[20.) (2 b).此外,获取扩散加权图像(DWI)是使用造影剂的一种替代方法,降低了肾毒性的风险,尽管没有表现出比STIR成像分析更好的性能[21,22) (2 b).
关于脊柱MRI扫描,轴向SpA相关的MRI阳性值和最佳定义仍存在争议,不同研究的数据存在较大异质性。2012年,ASAS/OMERACT MRI工作组将3个或3个以上部位(角部炎症病变)存在骨髓水肿(BME)定义为脊柱MRI阳性(炎症)[23) (5).一些研究结果证实了其作为诊断工具的使用,提示当骶髂炎不存在时,脊柱MRI具有一定的价值。研究结果包括观察T1W图像中超信号识别的超过5个角脂肪病变(CFL)与背痛患者轴向SpA的诊断相关,诊断确定性为86% (LR为12.6)[24) (2 b);在60例确诊为轴性SpA的患者中,20例无骶髂炎(XR或MRI)患者中有50%的脊柱MRI扫描中发现病变(包括炎性和结构性病变)[25) (2 b);109例(49%)非x线轴向SpA患者中有53例(无骶髂炎)纳入临床试验[26) (2 b).相反,一些证据也质疑脊柱MRI在怀疑有轴性SpA但没有骶髂炎的患者中的价值。在SPACE和DESIR队列中,将脊髓MRI作为成像标准纳入ASAS标准导致非常小比例的患者(1-2%)重新分类[27) (2 b).在另一项对130名年龄小于50岁的慢性背痛患者和20名健康对照组的研究中,脊柱MRI(使用ASAS/OMERACT定义和其他几种替代方法)与SIJ MRI的组合对最终的准确性影响很小,主要是由于大量的假阳性(11-16%的患者被诊断为非特异性背痛,17.5%的健康对照组有脊柱病变)[28) (2 b).在2009年标准得到验证的ASAS队列中,235例SIJ和脊柱MRI患者中只有5.4%有脊髓炎症[2) (2 b).
预后
对于近期发作的IBP(<2年)患者的评估,根据利兹评分系统(任何SIJ象限>75%受骨髓水肿影响),结合mri明显的严重骶髂炎,并添加阳性HLA-B27,预测8年后放射学上明显的AS的未来发展,敏感性为62%,特异性为92%,测试后阳性概率为80%,测试后阴性概率为83%。仅严重的骶髂炎可预测该诊断,测试后阳性概率为50%,测试后阴性概率为84% [10) (2 b).基于对轴向SpA患者2 - 7年的随访,SIJ MRI变化评估(丹麦评分:糜蚀、水肿和脂肪浸润)显示基线时的慢性变化与AS的未来发展有关。基线时,活动评分≥2、总慢性评分≥1、糜烂评分≥1和脂肪化生评分≥4的SIJ MRI扫描对x线骶髂炎的预测能力分别为74、77、79和68%。[29) (1 b).在另一项研究中,脂肪化生和强直性脊柱炎患者在基线SIJ MRI扫描时的影像学进展(使用改良的斯托克强直性脊柱炎脊柱评分[mSASSS]测量)在随访期间明显大于没有这些病变的患者[30.) (2 b).同样关于脊柱MRI,在随访2年后,AS患者中存在角炎性病变(CILs),预测新的联合赘生物的发展增加14.9% (NNH = 7)。在使用TNF抑制剂后,无炎症的椎体角的风险比有炎症的椎体角高11.4% (NNH = 9) [31) (1 b).高洗浴强直性脊柱炎计量指数(BASMI;AS患者功能限制程度的指标)评分已经与强直性脊柱炎脊柱磁共振成像活动(ASspiMRI-a;(MRI上的脊髓炎症活动指数)评分,特别是在患病时间≤3年且mSASSS评分(放射学进展指数)较高的患者中。综上所述,脊柱的活动能力是由可逆的脊髓炎症(MRI上)和不可逆的结构损伤(XR上)独立决定的[32) (2 b).
建议
| 对于临床怀疑轴性SpA,但骶髂x线检查不确定的患者,建议进行骶髂关节(SIJ) MRI检查。证据等级:1A;推荐强度:A(强);一致度:9.0。 SIJ MRI扫描应在T1W和STIR和/或T2脂肪饱和度(FATSAT)序列中进行。常规不建议静脉磁共振造影剂(钆)。证据等级:2B;推荐强度:B(中等);一致度:9.5。 对于怀疑轴向SpA且图像上没有骶髂炎的患者,不建议常规进行脊柱MRI扫描。证据等级:1B;推荐强度:A(强);一致度:8.5。 |
3.HLA-B27在轴性颈椎病中的作用是什么?
诊断
HLA-B27代表了ASAS分类标准的一个重要分支(也称为临床分支)。结合其他变量(如影像学和其他临床标准),HLA-B27可对轴向SpA进行分类[2) (2 b).当HLA-B27与MRI诊断的骶髂炎相关时,与单独MRI相比,后者对AS的诊断特异性从62%提高到77%,而不改变敏感性。单是HLA-B27检测阳性,预测该疾病的概率为48%,阴性的HLA-B27检测排除该疾病的概率为88% [10) (2 b).由于缺乏证据,HLA-B27在巴西人群中作为诊断工具的价值仍然未知。
遗传因素已经与AS易感性相关,正如一项测量AS患者亲属发生AS风险的研究的荟萃分析所显示的那样。在同卵双胞胎中观察到63%的风险,在一级亲属中观察到8.2%的风险,在二级和三级亲属中观察到的风险分别为1.0和0.7% [33) (2).根据一项招募了348名献血者的研究,其中20人被诊断为SpA,在hla - b27阳性个体中发生SpA的相对风险(RR)为20 (95% CI 4.6-94)。在同一研究中,50%的hla - b27阳性IBP患者SIJ MRI显示有骶髂炎[34) (2 b).AS和SpA的总体发病率和患病率强烈依赖于特定人群中HLA-B27的患病率,并与之直接相关。事实上,在不同的国家,它们的患病率差异很大:AS为0.14-1.4%;SpA为0.30-1.73%;HLA-B27为5.4-16% [35,36) (2 b).目前,已经鉴定出超过160种HLA-B27亚型(HLA-B*27:01至HLA-B*27:161),并由213个等位变异编码,这些变异与种族有关[37) (5).
预后
在hla - b27阳性AS患者中,数据显示疾病持续时间较长(症状和诊断较早),非甾体抗炎药摄入量较高,生物制剂治疗频率较高,疾病严重程度较高(包括关节外表现),功能(巴斯强直性脊柱炎功能指数- BASFI)和疾病活动性(BASDAI)评分较高[38,39) (2 b).在另一项研究中,hla - b27阳性的AS患者表现出明显更多的轴向和髋关节受累;阳性家族史发生率较高;hla - b27阳性AS患者的男性比例高于hla - b27阴性AS患者[40) (2 b).在AS患者(预后较差)中HLA-B27与BASMI(计量指标)有显著相关性[41) (2 b).在中国AS患者中,HLA-B27阳性与严重SIJ受累和早发型疾病之间存在显著相关性[42) (2 b).事实上,当AS患者按照起病年龄(<20岁、21-30岁、31-40岁、> - 40岁)进行分类时,HLA-B27的阳性率分别为94.6、90.2、74.1和61.2%。在非x线成像的轴向SpA患者中也观察到相同的模式[43) (2 b).一项系统的文献综述包括近3万例HLA-B27阳性AS患者葡萄膜炎的可能性提高了4倍[44) (2).
建议
| 由于预后原因(轴性受累更严重,前葡萄膜炎风险更高,轴性SpA家族史),建议临床怀疑轴性SpA的患者进行HLA-B27检测。虽然它经常被用作诊断工具,在我们的人口,有非常有限的证据,其价值.证据等级:2A;推荐强度:B(中等);一致度:9.2。 |
4.在轴向SpA患者中使用物理康复的证据是什么?
根据国际协会/欧洲抗风湿病联盟(ASAS/EULAR)小组的脊椎关节炎评估,轴向SpA患者的最佳管理需要结合非药物和药物治疗方式[45) (1).在非药物疗法中,运动被认为是维持或改善活动能力和身体功能以及预防畸形的重要工具[46,47,48) (1).
指导下锻炼
一项随机对照试验(RCT)比较了40名AS患者使用整体体位再教育(GPR)方法或传统运动的治疗;两种运动干预均在6-8例患者组中进行,每周1小时,持续4个月。结果是使用BASMI评估活动能力,使用BASDAI评估活动能力,使用BASFI评分身体功能。4个月(15个疗程)后,GPR组的BASFI(效应量为0.32)和所有BASMI参数(效应量为0.36至1.1)显著改善,但BASDAI没有显著改善。对照组仅耳屏至壁距和腰侧屈曲有明显改善。两种治疗方式的比较表明,在为期一年的随访期间,采用GPR方法进行姿势康复治疗的组比采用常规训练治疗的组效果更好[49,50) (2 b).在另一项研究中,AS患者接受了为期16周的监督GPR计划(n = 22)或无监督训练(n = 16),也得到了类似的结果。评估晨僵、疼痛、脊柱活动、身体功能(健康评估问卷-脊椎关节病- HAQ-S)、生活质量(医疗结果研究36 -项目简式健康调查- SF-36)和疾病活动性(BASDAI),两组治疗前后所有研究参数均有显著改善。GPR组在晨僵、脊柱活动和SF-36的物理成分方面的结果明显优于对照组[51) (2 b).与这些发现一致的是,与接受传统物理治疗(经典运动疗法)的一组(n = 48)患者相比,接受普拉提、McKenzie和Heckscher技术联合训练的一组AS患者(n = 48)的BASDAI、BASMI和BASFI指数均有显著改善[52) (2 b).
住院病人的锻炼
根据强直性脊柱炎工作组的改善标准评估(ASAS-IC;临床试验中最常用的反应标准,包括四个领域:身体功能、脊柱疼痛、患者整体评估和炎症)。这些项目对物理治疗、团体锻炼、被动治疗、放松和患者教育进行了个性化评估,其中有两个部分有所不同——耐力训练(位于挪威的中心)或灵活性训练(位于地中海的中心)。16周后,两种方法均显著改善了所有变量(除了BASDAI(脊柱疼痛)、胸椎可扩张性和红细胞沉降率(ESR)问题2外)。在第16周,以运动为中心的康复组达到ASAS20和ASAS40的患者数量比以耐力训练为中心的康复组分别高出27% (NNT = 4)和19% (NNT = 5)。这种差异虽然不显著,但一直持续到最终评估(第28周)[53) (2 b).另一项随机临床试验也报告了支持3周住院康复计划的证据(n = 46),而不是“常规治疗”,没有系统的康复(n = 49)。结果显示,随访4个月后,SF-36的BASDAI(效应大小= 1.38)和身体、情绪、活力和疼痛成分均有显著改善。然而,12个月后,在任何研究结果中均未观察到显著差异,因此表明康复的短暂效应[54) (2 b).
教育和居家锻炼
一项非随机临床试验(n = 66)比较了每周进行5次家庭运动(由物理治疗师进行理论和实践咨询)(每次至少30分钟)的AS患者与每周运动少于5次的患者(对照组)。随访3个月后,治疗组疼痛、晨僵、脊柱活动能力、BASFI、BASDAI、强直性脊柱炎生活质量问卷(ASQol)及肺功能指标用力肺活量(FVC)、1 s用力呼气量(FEV1)等各项评估参数均较基线值有明显改善,对照组无明显变化,部分参数(刚度、活动能力、ASQol)甚至出现恶化。在组间比较中,只有3个月时的生活质量评分(ASQol)有显著差异,有利于治疗组[55) (2 b).另一项随机对照试验比较了短期(5天)教育和运动计划,随后是无监督的训练,以及常规治疗(无运动)。该试验包括41例AS患者,在3个月的随访后,观察到与基线相比,教育+运动组的BASDAI、BASFI、ASQol和SF-36有显著改善。没有观察到BASMI或炎症标志物的改善[56) (2 b).在另一项RCT (n = 756)中,也调查了教育干预的有效性(2小时的会议,有疾病指导和无监督的体育活动计划),其中381名患者被分配到实验组,375名患者被分配到对照组(没有任何特定的干预)。6个月后,实验组的生活质量(ASQoL)、身体功能(BASFI)、整体疼痛和疾病活动评分(BASDAI)明显优于对照组,即使在调整基线值、性别、年龄和教育程度后也是如此。效应量范围为0.20至0.28 [57) (2 b).2015年的一项荟萃分析包括来自6项研究的数据,包括1098名患者,并得出结论,即使没有监督,运动也能显著改善身体功能(使用BASFI测量)、疾病活动度(使用BASDAI测量)以及抑郁和疼痛评分[58) (2).
有氧运动
一项随机对照试验(RCT)比较了70例AS患者(每组35例)在有氧运动(50分钟步行,每周3次,持续3个月)后进行拉伸运动(干预组)和单独拉伸(对照组)的效果。两组BASMI、BASFI、HAQ-S、BASDAI和ASDAS评分均有改善,组间差异无统计学意义。与对照组相比,干预组的6分钟步行测试和有氧能力(在跑步机上使用麦角肺活量测定法进行评估)显著改善[59) (2 b).另一项临床试验包括106名AS患者,他们被随机分配到有氧运动组(每周3次)或对照组(每周进行一次拉伸运动)。3个月后,有氧运动组的体能(以瓦为单位)和BASDAI外周疼痛成分明显优于对照组[60) (2 b).在另一项非随机试验中,46名轴向SpA患者接受了为期6个月的体育锻炼计划,包括有氧训练(60分钟,每周两次),并与另外29名性别和年龄匹配的轴向SpA患者(对照组,无任何干预)进行了比较。在最终评估中,两组的ASDAS-CRP和BASMI值均有明显改善,且运动组优于对照组[61) (2摄氏度).另一项研究也报道了有氧运动(40-60分钟,每周3次)对28例轴向SpA患者的益处,这些患者被随机分配到运动组或对照组。12周后,运动组在疾病活跃性(BASDAI)、身体功能(BASFI)、心肺健康(峰值氧容量(VO))方面有显著差异2)、体成分(总脂肪百分比和腹部脂肪)和动脉僵硬标记(增强指数和脉搏波速度)。因此,这种干预措施降低了心血管危险因素[62) (2 b).
水上运动
一项临床试验在对69名AS患者进行实际演示后,将水上运动(20次:每周5次,持续4周)与家庭运动进行了比较。两组的所有研究参数(疼痛、BASMI、BASFI、BASDAI和SF-36)在4周和12周后均有显著改善。组间比较显示疼痛和SF-36 8个组成部分中的6个存在显著差异,有利于水上运动[63) (2 b).在另一项随机对照试验中,30例轴向SpA患者被分配到水上运动和拉伸计划(24次:每周3次,共8周)或对照组(无训练)。治疗组在干预前后的生活质量(SF-12)、身体功能(BASFI)和疾病活度(BASDAI)仅存在显著差异(效应值范围为0.44至0.66)[64) (2 b).
然而,重要的是要强调,在推荐AS患者进行一些体育活动之前,无论疾病活动、功能或行动障碍,以及伴随疾病或其他药物,都可以要求进行运动测试[65) (2 b).
建议
| 在疾病的所有阶段,所有被诊断患有轴性脊椎关节炎的患者都应该接受身体康复治疗。证据等级:1A;推荐强度:A(强);一致度:9.8。 虽然专注于提高耐力和心肺健康的项目也是有益的,但主要建议专门专注于提高行动能力的项目。证据等级:2A;推荐强度:B(中等);一致度:9.6。 |
5.轴性SpA患者使用糖皮质激素的证据是什么?
全身糖皮质激素
一项双盲研究比较了单次脉冲治疗和两剂量甲基强的松龙(375mg与静脉注射1000mg,持续3天),对17例非甾体抗炎药无反应的AS患者进行了180天的随访。研究表明,两种剂量给药后,患者的活动能力、疼痛和晨僵都有改善,对疼痛的持续影响(最低剂量下需要重新使用镇痛药和/或非甾体抗炎药的中位时间为8天,最高剂量下为25天)低于晨僵(最低剂量和最高剂量治疗90天和120天后达到预处理水平)。分别)和活动能力(在整个180天的随访期间观察到改善)。剂量之间没有观察到任何结果的显著差异,但样本量非常小,排除了这种比较。在180天的随访期内,未观察到严重不良事件[66) (2 b).另一项采用回顾性设计和小样例量(n = 15)的研究观察到甲基强龙脉冲治疗(250-500 mg / d,持续3-5天)后BASDAI从第一次治疗后评估(治疗后第一天,3.9±2.4,p < 0.001)到3个月(5.3±1.8,p < 0.001)和12个月(5.4,p < 0.001)的改善(基线7.4±1.5)[67) (2摄氏度).相反,低剂量口服糖皮质激素(5.0 mg/天减释强的松)的使用在一项12周无对照研究中进行了评估,该研究包括57名对非甾体抗炎药难治、不耐受或禁忌的轴向SpA患者。在初步评估中,73.7%的患者使用了一种合成的改善疾病的抗风湿药物(DMARD;甲氨蝶呤(MTX)、柳氮柳嗪(SSZ)或来氟米特(LFL)), 7%使用TNFα抑制剂;在整个研究过程中,剂量保持稳定。结果表明,巴斯代的疾病活动性显著降低(从5.5±2.6降至3.0±2.8;p = 0.001),但与活动能力(BASMI)或咽部炎指数(Maastricht强直性脊柱炎咽部炎评分- MASES)无关。12周随访期间未观察到严重不良事件[68) (2摄氏度).另一项包括34名AS患者的短期随机安慰剂对照试验发现,与安慰剂相比,每天口服两剂量强的松龙(20或50 mg)两周可以改善活动指数。虽然治疗组在主要转归(BASDAI50)方面没有明显改善,但50 mg/d剂量组BASDAI (2.39 [1.38-3.40], p = 0.03)和ASDAS-CRP评分(1.56 [0.93-2.20],p = 0.01)显著降低,而20 mg/d剂量组ASDAS-CRP评分仅显著降低(1.16 [0.45-1.88],p = 0.004) [69) (2 b).一项队列研究(n = 830)通过比较AS使用者(n = 555)和非使用者(n = 275)的不良反应发生率,评估了低每日口服剂量(强的松达10mg或等效剂量)的安全性。研究发现,皮肤不良反应的发生率较高,如痤疮、血肿和感染(22.2vs6.6/1000病人-年(PY);P = 0.003)。然而,考虑到平均随访期为1.6年(0.5-15年),糖皮质激素暴露总量为1801 PY,该研究没有发现与低骨量或脂质和葡萄糖血清水平变化相关的差异[70) (2 b).
糖皮质激素浸润
在一项开放标签和非对照研究中,超声引导后跟囊注射20mg甲基强的松龙对18例SpA患者(27例治疗有症状性跟腱炎)改善疼痛(视觉模拟评分(VAS): 7 [4-10]vs3(鹿);p < 0.0001)和超声参数(肌腱厚度和血管密度降低、腱周水肿和滑囊炎以及功率多普勒信号强度),直到研究中每位患者最后一次评估(3至12个月)为止,没有任何并发症记录[71) (2摄氏度).一项系统文献综述(仅包括5项研究,只有一项RCT)对糖皮质激素浸润对跟腱病的长期影响提出了质疑(不仅仅是在SpA患者中),并强调了肌腱损伤和断裂的风险[72) (2).
一项非对照试验包括66例轴向SpA患者,这些患者在使用NSAID 4周后出现至少两个月的炎症性背痛,并在计算机断层扫描(CT)引导下向骶髂关节内注射40mg醋酸曲安奈德。结果显示,从干预后2周(±1)到10个月(±5),疼痛强度显著降低(使用VAS评估)。SIJ MRI还观察到血清炎症标志物(ESR和CRP)和骨髓水肿水平的降低[73) (2摄氏度).
建议
| 不建议长期使用全身性糖皮质激素治疗轴性颈椎病。证据等级:5级;推荐强度:D(很弱);一致度:9.6。 有症状的周围部炎患者可进行腱周糖皮质激素注射。建议谨慎,因为该手术可能会增加断裂的风险,特别是在跟腱。证据等级:2A;推荐强度:B(中等);一致度:9.2。 对非甾体抗炎药(NSAIDs)治疗无反应的孤立性臀部疼痛患者,可在骶髂关节内注射醋酸曲安奈德(triamcinolone acetate)短期获益。证据等级:2C;推荐强度:B(中等);一致度:8.5。 |
6.在哪些情况下,建议对轴向SpA患者持续使用非甾体抗炎药?
基于高至中等质量的证据,2015年发表的一项广泛的系统综述和荟萃分析(Cochrane)(包括2014年6月之前发表的35项研究,包括4356名轴向SpA患者)得出结论,传统的非甾体抗炎药和环氧化酶-2 (COX-2)抑制剂(coxibs)在改善6-12周的疼痛、疾病活动(BASDAI)和身体功能(BASFI)方面比安慰剂更有效。两类非甾体抗炎药的益处或损害没有显著差异[74) (1).另一项系统综述和贝叶斯网络荟萃分析纳入了26项研究,涉及3410名患者(其中约60%与上述Cochrane综述重叠),将诊断局限于AS,并比较了20种不同的非甾体抗炎药。作者还得出结论,证据不足以认为任何非甾体抗炎药在治疗AS方面比其他药物更有效[75) (1).在这些综述之后发表的其他研究证实了coxibs和非选择性非甾体抗炎药之间的相似性。比较两种剂量塞来昔布(每天200毫克和400毫克)和双氯芬酸(每天150毫克)在330名AS患者中没有发现改善疼痛和不良反应的差异[76) (1 b).依妥昔布(每日剂量为60和90 mg)在AS患者中的疗效和耐受性/安全性研究与萘普生(每日剂量为1000 mg/day)的结果相似[77) (1 b).
抑制放射学进展
基于目前的证据,AS患者持续使用非甾体抗炎药可能会减少放射学上脊柱损伤的进展(新骨形成),尽管迄今为止还没有发表将使用非甾体抗炎药与安慰剂进行比较的临床试验。一项随机对照试验比较了非甾体抗炎药(塞来昔布)的持续使用和按需使用。在研究结束时(随访24个月后),虽然两组之间没有观察到活动水平(BASDAI)和身体功能(BASFI)的显著差异,但使用mSASSS评估的放射学进展,按需方案治疗的患者比连续方案治疗的患者高出3倍(0.4±1.7)vs1.5±2.5;p = 0.002)。连续方案组高血压、腹痛、消化不良等不良事件发生频率高于按需方案组,但与按需方案组无显著差异[78]。子群和事后该试验的分析表明,在放射学进展风险较大的患者(炎症试验升高、疾病活动性高和既往存在联合韧带赘生物的患者)中,益处更大,甚至仅对患者有效。[79) (1 b).另一项(回顾性)研究报告了类似的结果。在88例德国脊柱关节炎初始队列(GESPIC)的AS患者中,与低强度使用(NSAID指数<最大推荐剂量的50%)相比,更强烈地使用非甾体抗炎药(每种非甾体抗炎药的摄入量≥推荐最大剂量的50%)与较低的放射学进展可能性相关(定义为在mSASSS上恶化≥2个单位),OR为0.15 (95% CI 0.02-0.96;p = 0.045),即使调整了基线结构损伤、CRP水平和吸烟。相反,在同一队列的76例非x线片轴向SpA患者中,在强或非强NSAID使用者之间没有观察到相同的x线片进展差异,这很可能是由于该亚组中新骨形成的频率普遍较低[80) (2摄氏度).然而,在另一项名为ENRADAS(非甾体抗炎药对强直性脊柱炎放射损伤的影响)的前瞻性研究中得到了相反的结果。在这项随机的多中心试验中,主要结局是使用mSASSS测量脊柱x线进展的差异,AS患者被随机分配到双氯芬酸持续治疗(150mg /天)或按需治疗。在两年随访期结束时,两组患者均表现出明显的影像学进展,连续方案组和按需方案组患者之间无差异(OR = 1.3, 95% CI为0.7-1.9,OR = 0.8, 95% CI为0.2-1.4)。两组在不良事件方面没有观察到差异[81) (1 b).这些结果之间的明显矛盾,包括两个设计非常相似的临床试验,表明非甾体抗炎药对新骨形成的可能有益作用尚未明确确立。
建议
| 非甾体抗炎药应作为主动和症状性轴向SpA的一线治疗。证据等级:1A;推荐强度:A(强);一致度:9.8。 没有证据表明特定的非甾体抗炎药可以被认为优于其他非甾体抗炎药。证据等级:1A;推荐强度:A(强);一致度:9.3。 关于非甾体抗炎药对减少轴向SpA患者影像学进展的影响的证据是相互矛盾的。证据等级:1B;推荐强度:B(中等);一致度:9.3。 |
7.在轴性SpA患者中使用合成的改善疾病的抗风湿药物(甲氨蝶呤、柳氮磺胺和来氟米特)的证据是什么?
甲氨蝶呤
一项系统综述和荟萃分析显示,关于甲氨蝶呤对AS患者影响的证据不足。然而,需要强调的是,仅纳入了5项临床试验(256例患者),结果和治疗存在异质性,阻碍了其有效性[82) (2).在该综述中纳入的研究中,只有一项随机安慰剂对照试验显示35例AS患者以7.5 mg/周剂量甲氨蝶呤治疗24周的阳性结果。在本研究中,以下8项中有5项改善≥20%被认为是一种缓解:a)晨僵强度,b)身体健康,c) BASDAI, d) BASFI, e) HAQ-S, f)医生整体评估(PGA),以及g)患者报告的疾病活动性。结果显示,治疗组有反应的患者比例高于安慰剂组(53%)vs11%)。在意向治疗(ITT)分析中,发现NNT = 3, BASDAI、BASFI和HAQ-S以及其他PROs(患者报告的结果)改善,不良事件报告频率无差异[83) (2 b).在一项涉及51例AS患者的1年随机临床试验(RCT)中,与单独使用萘普生相比,每周7.5 mg剂量的甲氨蝶呤在改善活动、活动能力或身体功能参数方面没有额外的好处,PGA除外[84) (2 b).另一项对30例AS患者进行的24周RCT显示各组间无显著差异[85) (2 b).当对使用英夫利昔单抗的AS患者使用甲氨蝶呤与安慰剂进行比较时,结果也相互矛盾。一项具有高偏倚风险的开放标签、非随机、小规模(n = 19)试验观察到甲氨蝶呤组的BASDAI50和ASAS50反应优于安慰剂组[86) (2摄氏度).在另一项试验中,123名患者在常规输注后按需接受英夫利昔单抗治疗。在这些患者中,62例患者接受甲氨蝶呤治疗(最大剂量为每周12.5 mg), 61例患者单独接受抗tnf α治疗。52周后,根据ASAS对改善结果的定义,没有发现显著差异[87) (2 b).
因此,对于甲氨蝶呤可用于的益处类型或亚人群没有一致意见[88,89,90) (2摄氏度).在一项小型观察性研究中,甲氨蝶呤还降低了前葡萄膜炎的发病率(从2.05/PY降至0.21/PY, p < 0.0001),该研究包括21例复发性急性前葡萄膜炎患者,其中8例(38%)HLA-B27检测阳性[91) (2摄氏度).
柳氮磺胺吡啶
2005年发表的系统文献综述(Cochrane)收录了11项临床试验,并于2014年更新,评估了柳氮柳嗪对AS患者(n = 895)的疗效。作者得出结论,证据不支持该药在减轻疼痛、疾病活动或放射学进展或改善身体功能或活动能力方面的任何有益作用。ESR和脊柱僵硬是唯一显著改善的结果,尽管效果值非常小,且没有临床意义(ESR为−4.8 mm/h [95% CI为−8.8至−0.8];和−13.9 mm (95% CI−22.5至−5.2)(100毫米视觉尺度的刚度)。此外,由于不良反应而中止治疗的风险增加了47%,有严重不良反应(红斑疹、恶心、厌食和失眠)的报告[92,93) (2).
另一项未包括在上述综述中的研究也评估了“非放射科患者”。这项随机对照试验包括230名患者,与安慰剂治疗组相比,他们在每天服用2g柳氮磺胺嘧啶治疗24周后没有表现出改善。令人惊讶的是,在无周围性关节炎的亚组中,BASDAI评分显著改善(由于脊柱疼痛和脊柱僵硬部分的独家改善)[94) (2 b).
两项使用TNFα抑制剂依那西普的研究使用柳氮柳嗪(每天2-3克)作为活性比较物,从中推断出一些疗效的证据。一项试验将187例AS活动性患者分配给柳氮磺胺吡啶治疗。16周后,52.9%的患者达到ASAS20反应,15.5%的患者根据ASAS定义表现出部分缓解[95) (2摄氏度).在另一项试验(ESTHER)中,36例活性、非x线轴向SpA患者接受柳氮磺胺嘧啶治疗48周。研究结束时,42%的治疗患者达到ASAS20缓解,31%达到ASAS40缓解,19%达到ASAS部分缓解,28%达到BASDAI50缓解[96) (2摄氏度).
根据一项观察性研究(NOR-DMARD),关节炎预测了181例接受柳氮磺胺嘧啶作为一线治疗的轴性SpA患者对柳氮磺胺嘧啶的反应(在3个月时)(∆BASDAI -1.4 [1.9]vs−缺席时,0.3 [1.7];p = 0.008)。此外,周围性关节炎患者的3年药物生存率高于无关节炎患者(分别为0.22 vs. 0.10, p = 0.03) [97) (2摄氏度).
一项RCT评估了柳氮柳嗪(2.0 g/天目标剂量)联合90 mg/天依托昔布与单独使用非甾体抗炎药治疗67例轴向SpA患者的疗效。随访6个月后,磺氮磺胺嗪组(67.7%)和安慰剂组(15.1%)应答患者百分比(∆ASDAS>1.1)有显著差异,NNT = 1.90 (95%CI = 1.37-3.12)。柳氮柳嗪组BASDAI评分(3.29±0.97 vs 1.47±0.99)和BASMI评分(3.10±0.87 vs 1.32±0.88)的平均改善也显著高于安慰剂组[98) (2 b).
柳氮磺胺嘧啶的另一个可能作用是降低轴性SpA患者前葡萄膜炎发作的发生率,根据两项研究的数据:一项观察性研究(n = 10),其中年发病率从3.4下降到0.9 (p = 0.007);另一项随机临床试验(n = 22),其中治疗组(0.47/年)和安慰剂组(1.06/年)新发急性葡萄膜炎的相对风险为0.44 (95% CI 0.30-0.64) [99,One hundred.) (2摄氏度).
Leflunomide
只有一项RCT评估了来氟米特对AS患者的影响。24周后,根据ASAS20标准,45名患者对来氟米特有反应的百分比为27%,这一值与安慰剂组(20%)相似。疾病活动性(BASDAI)、功能(BASFI)和活动能力(BASMI)指数、疼痛和关节水肿均未观察到明显差异。然而,胃肠道疾病、呼吸道感染、皮炎、疲劳、静脉血栓形成和肝酶水平升高等不良事件的风险增加了20% (NNH = 5) [101) (2 b).一项仅有20例AS患者的24周开放标签研究是唯一一项仅在外周部分观察到显著改善(p = 0.039)的研究(基线时平均关节计数为1.7,6个月后为0.2),但在BASDAI、BASMI、BASFI和其他PROs方面没有明显改善[102) (2摄氏度).
联合合成DMARDs对生物治疗生存期的影响
两项观察性研究旨在回答合成DMARDs是否影响TNFα抑制剂在轴向SpA患者中的滞留率(药物生存期)这一仍然悬而未决的问题。瑞典生物制剂注册中心ARTIS(瑞典抗风湿病疗法)发现,在使用第一种TNFα抑制剂期间联合用药(n = 2420)产生了有益的效果,使用者的5年停药率低于非使用者(as的风险比(HR) 0.71, 95% CI 0.59-0.85, p < 0.001;未分化SpA的HR 0.82, 95% CI 0.69-0.97, p = 0.020) [103) (2 b).相反,葡萄牙风湿病登记册(n = 954)在13年的随访后未发现对保留率有相同影响的证据(HR 1.07, 95% CI 0.68-1.68) [104) (2 b).
建议
| 当周围性关节炎存在或由于毒性、不耐受或禁忌症而没有其他药物治疗选择时,建议使用甲氨蝶呤和柳氮柳嗪治疗轴性SpA患者。证据等级:2A;推荐强度:B(中等);一致度:8.4。 对于正在使用生物制剂的轴向SpA患者,不建议常规使用甲氨蝶呤或柳氮磺胺作为联合用药。证据等级:2B;推荐强度:B(中等);一致度:9.6。 |
8.有哪些疗效证据支持在轴向SpA患者中使用生物制剂的适应症?
五种TNFα抑制剂(抗TNFα)目前可用于治疗as:抗TNFα单克隆抗体英夫利昔单抗,阿达木单抗和golimumab;certolizumab pegol,它只是抗体的片段抗原结合(Fab)部分;以及TNFα受体类似物依那西普。最后四种化合物也被批准用于治疗非x线轴向SpA。以下白介素-17抑制剂(抗il17a)也可用:secukinumab,已被批准用于AS, ixekizumab(抗il17a /F),尚未被批准用于轴向SpA。
Anti-TNFα
一项包括69例活动性AS患者(BASDAI≥4,背部疼痛≥4mm - VAS)的随机对照试验,在第0、2和6周接受英夫利昔单抗(5.0 mg/kg)或安慰剂的IV治疗,在第12周进行主要预后评估(BASDAI50)。在本试验中,治疗组53%的患者表现出这种反应,而安慰剂组只有9%的患者表现出这种反应(P < 0.0001, NNT = 2.3) [105) (2 b).根据ITT的分析,本研究的开放标签阶段,每6周使用相同的剂量,证实了持续的反应,直到第三年。此外,47%的患者维持初始BASDAI50反应至第54周,41%的患者维持至第102周,47.1%的患者维持至第156周[106,107,108) (2摄氏度).来自同一研究的其他出版物(数据来自5年和8年的随访)证实了长期反应的持久性,尽管没有ITT分析,这往往低估了在如此长随访期间的治疗效果。最初的69例患者中38例(55%)完成了第五年,33例(47%)完成了第八年。在这些患者中,分别有25例(66%)和21例(64%)的BASDAI评分低于初始BASDAI评分的50% [109,110) (2摄氏度).
一项更大的随机对照试验(ASSERT研究)采用相同的疾病活动标准对357例AS患者进行了24周的评估,患者在第0、2、6、12和18周使用英夫利昔单抗(5.0 mg/kg)或安慰剂治疗。该药物有效降低了疾病活动性(ASAS20应答者:61.2% vs.安慰剂组19.2%,NNT = 2.4;ASAS40应答者:47% vs 12%, NNT = 2.8, ASAS部分缓解:22.4% vs 1.3%, NNT = 4.7, BASDAI50: 51% vs 10.7%, NNT = 2.5)。身体功能也得到改善(BASFI评分降低≥2个单位:47.5% vs 13.3%, NNT = 2.9),以及BASMI(−1.0 vs 0.0, p = 0.019)和生活质量(物理成分SF-36:−10.2 vs 0.8, p < 0.001)。Mander enthesitis index (MEI)评分无差异[111) (1 b).
第一个评估依那西普疗效的研究是美国的一项研究,其中40例活跃AS患者(定义为炎性背痛伴晨僵至少45分钟,且有中度疾病活动性的pro)被随机分为每周两次25mg依那西普治疗组或安慰剂组。在4个月的随访结束时,治疗反应增加了50% (NNT = 2),这是由与ASAS20非常相似的综合指数定义的:在疾病活动度的5项测量中,有3项改善≥20%(晨僵持续时间、夜间疼痛强度、BASFI、患者整体评估和关节水肿评分)[112) (2 b).另一项为期24周的跨国随机对照试验包括277名AS活动期患者(VAS评分≥30mm晨僵,且大于三个参数中的两个:患者整体评估、背部疼痛和BASFI),这些患者接受25mg依那西普治疗,每周两次,持续24周或安慰剂。结果显示,12周后ASAS20增加31% (NNT = 3.2), ASAS20增加35% (NNT = 2.9), ASAS部分缓解增加13% (NNT = 7.7), BASDAI, BASFI和BASMI [113) (1 b).该试验的开放标签扩展包括最初纳入的200名患者(72%),随访至96周。所有最初接受安慰剂治疗的患者开始接受依那西普治疗。24周后,70%的患者也达到ASAS20。两年后,接受96周活性药物治疗的患者中有74、61和46%(治疗组),接受72周活性药物治疗的患者中有78、54和38%(安慰剂治疗组)分别达到ASAS20、ASAS50和ASAS70,这表明存在持续缓解[114) (2摄氏度).最后,长达192周的随访包括277例原始试验中的126例(45.5%)。达到ASAS20、ASAS40和ASAS部分缓解反应的患者百分比在治疗组(依那西普从试验开始使用)分别为81、69和44%,在安慰剂治疗组(依那西普在24周后使用)分别为82、68和28% [115) (2摄氏度).
在德国四个中心进行的一项小型试验包括30名患者,其中14名被随机分配到治疗组(每周两次25mg依那西普),16名被分配到安慰剂组,处于双盲期(6周)。在此阶段后,所有患者均接受依那西普治疗12周,然后停用该药,再随访12周。6周治疗后,BASDAI50反应改善51% (NNT = 2.0)。平均时间(标准偏差)到恢复(BASDAI≥4,医生在0- 10分VAS中整体评估≥4)为6(±3)周。30名初始患者中的26名被纳入延长治疗,其中所有患者都恢复了药物治疗。第54周,58%的患者达到了BASDAI50反应,31%的患者达到了ASAS部分缓解。此外,26例患者中有21例(81%)完成了2年的随访治疗,16例(62%)完成了7年的随访治疗。在这16名患者中,31%的患者达到ASAS部分缓解,44%的患者达到ASDAS的非活跃疾病标准[116,117,118) (2 b).另一项RCT在14个欧洲中心进行,包括84例活动性AS患者,他们接受25mg依那西普每周两次(n = 45)或安慰剂(n = 39),持续12周。结果显示,ASAS20反应增加了37% (NNT = 2.7), ASAS50反应增加了50% (NNT = 2.0),但ASAS70反应没有显著差异,尽管数值差异有利于药物组(24.4% vs 10.3%) [119) (1 b).依那西普对晚期和重度AS患者亚群的疗效也进行了评估(即腰椎有2个椎间相邻桥和/或融合,胸椎有3个椎间相邻桥和/或融合,或颈椎有2个椎间相邻桥和/或融合)。患者接受每周50mg依那西普(n = 39)或安慰剂(n = 43)治疗12周。ASAS20提高34% (NNT = 2.9), ASAS40提高21% (NNT = 4.8), BASDAI50提高23% (NNT = 4.4), ASAS部分缓解提高13% (NNT = 7.7)。12周后,结果也显示BASDAI (- 2.6), BASFI (- 2.2), BASMI(- 0.57)显著改善。此外,一些肺功能参数也得到了改善:肺活量(VC)为2.88%(效应值= 0.17),用力VC (FVC)为3.75%(效应值= 0.24)[120) (1 b).ESTHER试验包括轴向SpA (AS和非x线轴向SpA)患者,他们的症状出现时间少于5年,MRI显示轴向骨骼有活动性炎症。患者被随机分配到50mg依那西普/周(n = 40)或柳氮柳嗪(n = 36)治疗12个月。在此期间结束时,未缓解的患者继续进行开放标签的扩展研究,接受依那西普的长期治疗。缓解患者停止用药,病情加重后恢复依那西普。抗tnf α治疗组的炎症评分(SIJ和脊髓MRI)明显优于柳氮磺胺治疗组。BASDAI、BASFI、MASES、EQ-5D和ASQoL也有显著改善。两组的疗效和安全性数据相似。也观察到类似的长期缓解水平(3年随访)[96,121,122) (2摄氏度).另一项随机对照试验(EMBARK)招募了215名患有非x线轴向SpA的患者,他们的症状长达5年。这些个体被随机分配给依那西普(50mg /周)或安慰剂。12周后,治疗组ASAS40反应的改善比安慰剂组好16% (NNT = 6.0)。治疗组SIJ和脊髓MRI的疾病活动性评分也优于安慰剂组。亚组分析观察了CRP水平与MRI(加拿大脊椎关节炎研究协会(SPARCC) MRI评分系统)骶髂炎症之间的相关性,并改善了反应。12周后,所有患者接受依那西普治疗,并在另一项开放标签扩展研究中随访36周。最初在48周分配给依那西普和安慰剂的患者达到ASAS40反应的百分比分别为52%和53% [123,124) (1 b).
一项涉及1570名参与者的系统综述和荟萃分析,通过计算治疗与安慰剂达到ASAS20 (RR = 2.36, 95% CI 2.03-2.74)和ASAS40 (RR = 2.81, 95% CI 2.01-3.92)反应和ASAS部分缓解(RR = 4.31, 95% CI 2.52-7.37)的相对风险(RR),比较了依那西普在白种人与中国人中的疗效[125) (1).
ATLAS研究是一项为期24周的随机对照试验,主要结果在第12周测量,并进行了5年的开放标签扩展,包括315例对非甾体抗炎药无反应的AS患者,他们每隔一周接受40 mg剂量的阿达木单抗(n = 208)或安慰剂(n = 107)治疗。12周后,结果显示ASAS20反应增加37.6% (NNT = 2.7), ASAS40反应增加26.8% (NNT = 3.7), ASAS部分缓解增加17% (NNT = 5.9)。在第12周和第24周,治疗组和对照组在改善方面有显著差异(BASDAI, BASFI, BASMI和MASES)。ASAS20和ASAS40缓解和ASAS部分缓解在治疗后持续2年,分别为64.5%、50.6%和33.5%。这些患者的3年随访显示,使用BASDAI、BASFI、SF-36(物理成分总结)和ASQoL测量持续缓解,最初分配到阿达姆单抗组的125/208(60%)例患者完成了第5年的随访。在这些患者中,70%和77%的患者达到ASDAS40和BASDAI50反应,而51%和56%的患者达到ASAS部分缓解和ASDAS无活性疾病标准[126,127,128,129],分别(1 b).2008年发表的一项RCT,甚至在ASAS标准(2009年)发表之前(该标准定义了非x线轴向SpA的概念),包括炎症性背痛和HLA-B27测试阳性或SIJ或脊柱MRI炎症且没有x线骶髂炎的患者(n = 46)。12周后,使用阿达木单抗(每隔一周40mg)的患者达到ASAS40反应的比例高于安慰剂治疗的患者(54.5%)vs12.5%, nnt = 2.4)。在切换到治疗后,安慰剂组观察到相同水平的反应,并维持到开放标签期的第52周[130) (1 b).另一项已经使用2009年ASAS标准的大型研究(n = 185)也评估了每两周40mg阿达木单抗治疗活动性非x线轴性SpA (BASDAI≥4,轴性疼痛VAS≥4,以及对NSAIDs的不适当反应、不耐受或禁忌症)的疗效。12周后观察到类似的结果。与安慰剂组相比,ASAS40反应显著增加21% (NNT = 4.8), ASAS部分缓解增加11% (NNT = 9), ASDAS非活动性疾病缓解增加20% (NNT = 5)。SIJ和脊柱MRI的BASDAI、ASDAS、HAQ-S、SF-36和SPARCC活性评分的改善也有显著差异。阿达木单抗组和安慰剂组在BASFI、BASMI和MASES方面的改善没有差异。SIJ MRI上基线CRP水平升高和客观炎症强度升高与缓解改善相关[131) (1 b).一项荟萃分析包括8项评估阿达木单抗治疗AS效果的临床试验。第12周,达到ASAS20和BASDAI50的风险比(或RR)分别为RR = 2.26 (95% CI 1.85-2.75)和RR = 2.82 (95% CI 2.14-3.71), [132) (1).
当皮下接受golimumab (50 mg/4周)治疗时,与安慰剂相比,活跃性AS患者(BASDAI≥4,脊柱疼痛VAS≥4,对先前使用非甾体抗炎药或合成DMARDs反应不充分)获得了以下结果:早在第14周,ASAS20反应增加37.6% (NNT = 2.7), BASDAI50反应增加30.5% (NNT = 3.3);第24周ASAS40反应增加28.1% (NNT = 3.6), BASDAI50反应增加36.1% (NNT = 2.8)。接受golimumab治疗的患者也表现出更大的BASDAI、BASFI、SF-36改善,以及睡眠质量(Jenkins睡眠评估问卷(JSEQ))。然而,BASMI [133) (1 b).这些患者的5年随访显示持续缓解[134,135) (2摄氏度).在中国的一项试验(n = 213)中观察到类似的结果,在1年随访中,golimumab治疗使ASAS20反应在14周后提高了24.3% (NNT = 4.1),在24周后提高了27.1% (NNT = 3.7) [136) (2 b).在198名患者(GO-AHEAD研究随机对照试验)中,也评估了golimumab对非x线轴向SpA患者的疗效,这些患者的病程长达5年,随机分配给golimumab (50 mg/4周)或安慰剂治疗。在随访的第16周,接受golimumab治疗的患者比接受安慰剂治疗的患者获得了更多的临床缓解,ASAS20 (NNT = 3.2)和ASAS40 (NNT = 3)的缓解差异显著,分别为31.1%和33.7%。与其他临床试验分析非x线轴向SpA患者人群的结果一致,在没有客观炎症症状的亚组患者(MRI显示CRP水平正常,无骶髂炎)中,格利单抗和安慰剂治疗的ASAS20或ASAS40反应没有显著差异[137) (1 b).在一项28周的随机对照试验(来自8个国家的40个中心)中测试了golimumab的另一种给药途径(静脉注射),其中包括208例活跃AS患者(BASDAI≥4;轴痛VAS≥4;超敏CRP≥0.3 mg/dl)的患者被随机分配到第0、4、12周和此后每8周使用2 mg/kg的golimumab治疗或安慰剂治疗。在本试验中,14.4% [30.]的患者已经使用了另一种抗tnf α抗体而没有主要治疗失败,5.8%(12)的患者在基线时已经表现出完全的脊柱强直。在第16周,golimumab组达到了ASAS20、ASAS40和BASDAI50反应,而安慰剂组没有:73.3%vs26.2% (nnt = 2.1), 47.6%vs8.7% (NNT = 2.6), 41%vs14.6% (NNT = 3.8)。根据ASDAS非活动性疾病标准,17.1%的患者出现缓解(NNT = 5.8), 12.3%的患者出现ASAS部分缓解(NNT = 8.1)。治疗组的BASFI评分也得到了更大程度的改善(−2.4)vs−0.5;p< 0.001) [138) (1 b).
在rapi -axial SpA中评估了certolizumab pegol的疗效,该SpA包括325例活跃轴向SpA患者,其中147例非x线轴向SpA患者,他们被随机分配到两种certolizumab pegol给药方案(剂量为每两周200 mg和每四周400 mg)或安慰剂治疗。基线时,16%的患者已经使用另一种抗tnf α抗体,没有因主要治疗失败而停用。在第12周,57.7%和63.6%的患者分别接受400和200 mg certolizumab pegol治疗,而38.3%的患者接受安慰剂治疗(两种给药方案的NNT分别为5.2和3.95)达到ASAS20反应。接受两种给药方案的患者ASAS40反应显著增加,分别为25.4% (NNT = 3.9)和31% (NNT = 3.2)。与安慰剂组相比,两种certolizumab pegol给药方案的ASAS部分缓解分别增加了19.7% (NNT = 5.1)和20.6% (NNT = 4.8)。此外,接受两种给药方案的25.2%和20.6%的患者达到ASDAS非活性疾病状态,而安慰剂组为0% (NNT = 4和4.8)。总而言之,在第12周和第24周,与安慰剂相比,两个治疗组的BASFI、BASDAI、BASMI和ASDAS均有显著改善[139) (1 b).在第96周和第4年的随访中评估了持续反应,67%(218/325)参与者在研究中继续接受药物治疗,其中31.4%符合ASDAS非活性疾病标准[140,141) (2摄氏度).
Anti-IL17
在MEASURE 1和MEASURE 2 III期试验中,抗il17a单克隆抗体诱导活性AS的体征和症状显著减轻(BASDAI≥4;轴性疼痛VAS≥4),随访第16周。在MEASURE 1试验中(n = 371),治疗组患者在第0周、第2周和第4周接受10mg /kg secukinumab静脉注射,随后每4周接受75或150mg的维持治疗。在MEASURE 2试验(n = 219)中,抗体在第0、1、2和3周皮下注射(75或150 mg secukinumab),随后每4周进行一次SC维持治疗。在MEASURE 1试验中,分别有61、60和29%接受150 mg、75 mg和安慰剂治疗的患者在第16周达到ASAS20反应(与安慰剂比较p < 0.001 [150 mg NNT = 3.1, 75 mg NNT = 3.2])。相反,在MEASURE 2试验中,这些比率分别为61,41和28% (150 mg组p < 0.001)vs安慰剂[NNT = 3], p = 0.10, 75 mgvs安慰剂)。因此,SC注射(强度较小,但同样有效)和150 mg维持剂量,而不是75 mg剂量(无效),被选为最佳治疗。在两项研究中,这些反应水平一直维持到第52周(均为63%)。就最具临床相关性的次要结果而言,仅考虑接受150 mg维持剂量(这是巴西批准的AS剂量)的个体,在MEASURE 1和MEASURE 2试验中,分别有42和36%的患者在第16周和第51周达到ASAS40, 49%的患者在第52周达到ASAS40。就ASAS部分缓解而言,15% (MEASURE 1)和14% (MEASURE 2)的患者在第16周达到这种状态,22%(在两项研究中)在第52周达到这种状态[142) (1 b).比较bio-naïve (n = 134)和抗tnf α失败(n = 85)患者,两种情况下都显示出良好的疗效,尽管效应值较小(第一组ASAS20的NNT = 2.7,第二组NNT = 3.9) [143) (1 b).与安慰剂治疗的患者相比,CRP基线水平升高或未升高的个体以及接受或未接受抗tnf α抗体治疗的患者在第16周时脊柱总疼痛、夜间疼痛和疲劳水平(使用facit疲劳量表测量)显著降低,持续反应持续至第104周[144) (1 b).第24周观察到的临床反应持续到随访第三年[145,146,147) (2摄氏度).
Ixekizumab是另一种抗il17抗体(针对IL17A同型二聚体和IL17A/F异型二聚体),在两项已发表的3期临床试验(COAST-V和COAST-W)中显示出治疗AS的疗效。前者包括341例对非甾体抗炎药反应不充分或不耐受的患者,他们被随机分配(1:1:1:1)接受每2或4周80 mg ixekizumab SC,每2周40 mg adalimumab SC或安慰剂。后一组仅包括先前暴露于一种或两种抗tnf α疗法(反应不充分或不耐受)的患者(n = 316),因此该机制的活性比较器尚未建立。第16周时,bio-naïve亚人群中ASAS40的nnt为3.2 (95% CI 2.3-4.9),阿达木单抗无显著差异,而之前接受抗tnf α治疗的亚人群中nnt为6.5 (95% CI 4.2-15.2) [148,149) (1 b).该药尚未被批准用于轴性SpA的治疗。
建议
| 根据风湿病专家的意见,当初始非甾体抗炎药治疗失败(疾病持续、毒性或禁忌症)时,建议使用生物制剂(TNFα抑制剂或抗il - 17抗体)治疗活性(BASDAI≥4或ASDAS≥2.1)和症状性轴向SpA。证据等级:1A;推荐强度:A(强);一致度:8.9。 当检测到炎症的客观征象,如MRI上CRP水平升高和/或存在骶髂炎时,应使用生物制剂治疗轴向SpA,因为这些参数可以预测反应,特别是在非x线轴向SpA的情况下。证据等级:1B;推荐强度:A(强);一致度:9.6。 抗tnf抑制剂(阿达木单抗、依那西普、格利单抗和certolizumab pegol)被推荐用于非x线轴向SpA的治疗,因为已获得循证批准。证据等级:1B;推荐强度:A(强);一致度:9.7。 |
9.用于治疗轴向SpA患者的生物制剂是否存在疗效差异?
迄今为止,只有三项试验对轴向SpA患者的生物疗法进行了正面比较。
一项开放标签随机对照试验分析了55名AS患者,这些患者被随机分配到英夫利昔单抗或依那西普治疗组。随访12周时,BASDAI (3.5与5.6, p < 0.005)和BASFI (3.5 .与5.0, p < 0.005)有利于英夫利昔单抗。然而,这种差异并没有随着时间的推移而持续(随访104周)。随访第2周、第12周或第104周时,各组间ASAS20或ASAS40反应无差异[150) (2 b).
一项I期随机、双盲、多中心临床试验(PLANETAS研究)比较了英夫利昔单抗与其一种生物类似药(CT-P13)在AS患者(n = 250,每个治疗组125)中的疗效,为期30周。生物仿制药组和原药组在第30周观察到的ASAS20和ASAS40反应为:70.5%vs72.4% (OR = 0.91, 95% CI 0.51 ~ 1.62), 51.8%vs47.4% (OR = 1.19, 95% CI 0.70-2.00),两组间差异无统计学意义[151) (2 b).
另一项开放标签随机对照试验根据ASDAS-CRP比较了在现实生活(常规护理)中接受依那西普(n = 163)或阿达木单抗(n = 82)治疗的AS患者中接受每种药物治疗的患者的生存期和疾病活动性。在两年随访期间,平均ASDAS-CRP无差异(依那西普为2.0±0.9,阿达木单抗为1.9±1.1,p = 0.624)。然而,依那西普治疗患者的生存率明显优于阿达木单抗治疗患者。停用阿达木单抗与停用依那西普的HR为2.5 (95% CI 1.3-4.5, p = 0.006) [152) (2 b).
表3.概述了不同药物治疗期间特定疗效结果的相对频率(相对于安慰剂组)。虽然不同人群的不同研究无法如此简单地进行比较,但有趣的是,对于相同结果的所有可信区间都是重叠的,至少在对照期的短期随访中是如此。
另一种推断不同药物之间疗效差异的方法是间接比较元分析,使用贝叶斯网络或贝叶斯混合治疗比较(MTC)。最近,该方法之一被用于分析16项随机对照试验(rct)中2574名AS患者使用阿达木单抗、依那西普、戈利单抗和英夫利昔单抗的数据,结论是没有证据支持这些药物在以下结果方面的疗效差异:ASAS20、ASAS40和BASDAI50反应[153) (1).另一项系统综述(28项符合条件的rct),包括非x线轴向SpA患者,也没有发现不同TNFα抑制剂之间疗效差异的证据[154) (1).最近,使用secukinumab数据库和ASAS20作为主要结果的18个rct(2971例AS患者)进行了间接比较(Bucher 's法),未发现差异[155) (1).
建议
| TNFα抑制剂和IL17A抑制剂在控制轴性SpA患者的炎症活性方面表现出相似的效果。证据等级:1A;推荐强度:A(强);一致度:8.9。 |
10.轴向SpA患者使用生物制剂的安全性是否不同?
与疗效比较类似,使用间接比较和荟萃分析推断了药物之间的安全性差异。表格4概述了不同药物报告的严重不良事件和治疗中断(均与安慰剂组比较)的rr。有趣的是,短期内rr的置信区间重叠,表明类似的安全状况。
间接比较和不同的元分析(尽管有相当多的数据重叠)得出的结论是,不同生物制剂的数据相似。此外,与对照组相比,严重不良事件(包括与生物治疗相关的严重感染和恶性肿瘤)的发生率没有显著差异[153,156,157) (1).安全分析的主要局限性,如表所示4在引用的荟萃分析中,由于随访时间短(暴露时间短)和根据限制性随机对照试验纳入/排除标准选择暴露人群,事件发生率低。登记研究和队列研究提供了更接近现实场景的长期安全性证据和数据。然而,这些研究中很少有专门针对轴向SpA患者进行的,在下面介绍的一些研究中,其他诊断,如银屑病关节炎(PsA)和类风湿关节炎(RA),被分组进行了风险分析。
加拿大的一项队列研究随访了440例轴向SpA患者,观察时间为1712年。在研究期间,有164例(60%)患者使用TNFα抑制剂,124例(28.2%)患者使用DMARD(甲氨蝶呤-15%,柳氮磺胺-10.9%,来氟米特-1.1%,其他-1.1%),42例(9.5%)患者使用糖皮质激素,平均剂量为14 mg/天。与不使用抗肿瘤坏死因子α抑制剂相比,使用抗肿瘤坏死因子α抑制剂对感染发生率没有显著影响。暴露组和对照组的发病率为19/100 PYvs分别为14/100 PY,几个辅助因素(合并症,糖皮质激素和合成DMARDs的使用)调整后的OR为1.25 (95% CI 0.90-1.73)。在多变量分析中,仅使用dmard可增加感染风险,OR为1.73 (95% CI 1.21-2.48, p = 0.003) [158) (2 b).一项系统综述包括10项随机对照试验和51项观察性研究,以比较13种免疫调节剂(生物制剂和靶向特异性分子)的不良反应风险。将不良反应、因不良反应而停药、严重不良反应、死亡、严重感染、结核病、带状疱疹和恶性肿瘤的发生率作为感兴趣的结局进行分析。然而,70%的研究是在被诊断为RA的患者中进行的,因此限制了对轴向SpA患者的分析能力。然而,在AS、RA和PsA患者中,英夫利昔单抗因不良反应而停药的结局高于阿达木单抗和依那西普[159) (2).
韩国两项关于结核病风险(TB;韩国被认为是结核病负担中等的国家)在抗肿瘤坏死因子α治疗对结核病风险的影响方面显示出相互矛盾的结果。其中一项研究计算了单个中心接受抗tnf α治疗(n = 354)或未接受抗tnf α治疗(n = 919)的AS患者的结核病发病率,未接受抗tnf α治疗的患者为308/10万PY,接受抗tnf α治疗的患者为168/10万PY。未观察到显著差异,RR = 0.53 (95% CI 0.14-1.91),因此表明暴露不会增加风险[160) (2 b).另一项研究还计算了1322名AS患者(336名使用者和986名未暴露对照组)的结核病发病率,发现与非使用者相比,使用者的发病率为600.2/10万PY, RR = 4.87 (95% CI 1.50-15.39) [161) (2 b).另外两项观察性研究均在土耳其(结核病高发国家)进行,旨在确定与抗tnf α药物使用者患结核病风险增加相关的因素(在这两项研究中,仅评估了阿达木单抗、依那西普和英夫利昔单抗)。第一项研究评估了1887例接受抗tnf α治疗的患者的医疗记录,其中705例(37.3%)被诊断为AS。总发病率(所有诊断)为423/100,000 PY。在多因素分析中,使用阿达木单抗(增加9.5倍)、男性(增加15.6倍)和有结核病史(增加11.5倍)被认为是结核病的危险因素[162) (2 b).另一项研究是病例对照研究,将73例(52.1%为AS患者)抗tnf α药物使用者中的结核病例与7695例(50.6%为AS患者)对照组(即无结核的抗tnf α药物使用者)进行比较。在接受抗tnf α治疗的AS患者中,结核病的患病率为0.97%。英夫利昔单抗使用者(考虑所有诊断)中结核病的发生率为1.27%,显著高于阿达木单抗(0.57%)和依那西普(0.3%)[163) (3 b).
尽管数据有限,但暴露于IL-17抑制的患者患结核病的风险似乎很低,因为临床试验中没有病例描述。相反,接受抗- il -17治疗的患者发生念珠菌感染的风险增加[142,147,148,149) (1 b).在轴向SpA患者的治疗中应考虑这些微小的差异。
来自四个注册中心的数据的三篇论文没有发现在SpA患者中使用抗tnf α治疗会增加恶性肿瘤的风险。BIOBADASER注册(761例西班牙AS患者,在其他诊断中,接受抗tnf α治疗并从2001年到2008年随访)计算出标准化发病率为0.92 (95% CI 0.44-1.70)。BIOSPAR登记(2000年至2010年随访的231例接受抗tnf α治疗的比利时SpA患者)发现,与普通人群相比,女性发病率无显著性增加,R = 1.99 (95% CI 0.54-3.82),而男性则无显著性增加,RR = 0.69 (95% CI 0.29-1.66)。DANBIO登记(2001年至2011年随访3255名丹麦SpA患者)和ARTIS登记(2001年至2011年随访5448名瑞典SpA患者)获得抗tnf α治疗患者与未治疗患者之间的相似风险,RR = 0.8 (95% CI 0.7-1.0) [164,165,166) (2 b).
建议
| 生物制剂TNFα抑制剂和抗il17a抑制剂对于严重不良反应和停药的短期风险表现出相似的效应大小。证据等级:1A;推荐强度:A(强);一致度:9.1。 |
11.在轴性SpA患者中,生物治疗是否能够减少结构损伤(影像学进展)?
减少甚至预防轴性SpA患者的结构损伤是治疗这些疾病的一个重要目标,因为除了炎症外,骨新形成引起的损伤也会导致活动能力和功能受损,特别是在早期(症状3年)之后[32) (2 b).观察性研究表明,抗tnf α治疗对影像学进展具有保护作用,特别是如果早期开始或长期延长(≥4年)[167,168,169,170) (2 b).然而,这些药物能够预防或至少减少进展的明确证明仍然是预期的,主要是因为实验研究(概述在表5)尚未提供有关此特性的确切证据。
英夫利昔单抗
在ASSERT研究中,201例AS患者在96周诱导剂量后每6周接受5.0 mg/kg英夫利昔单抗治疗(基线和96周后)的脊柱x线片使用mSASSS进行结构损伤分析。这些患者的放射学进展(第0周和第96周的mSASSS之间的差异)与未接受历史队列(OASIS)生物制剂治疗的AS患者进行了比较,但这种比较存在所有局限性。ASSERT组和OASIS组的平均2年进展值分别为0.9±2.6和1.0±3.2,差异无统计学意义(p = 0.541) [171) (2摄氏度).在另一个队列中,69例AS患者中有33例最初被纳入DIKAS (德国英夫利昔单抗Kohorte für AS)研究,也评估了使用mSASSS的影像学进展,但分为两个时间间隔:基线-2年;2-4年。在该人群中,mSASSS变化为1.6±2.6/4年(低于OASIS队列中的4.4/4年)。然而,这项研究有明显的局限性,包括两组之间的基线疾病活动性和读取x线片的方法的差异。在8年随访结束时,22例患者仍在使用英夫利昔单抗的开放标签扩展期。然后将这些患者的基线进展与另一个历史队列(Herne)中从未接受过抗tnf α治疗的AS患者的34名“对照组”进行比较。有趣的是,虽然前4年两组之间的平均进展率没有差异(p = 0.18),但在后4年的随访中,英夫利昔单抗组有显著差异(p = 0.01) [172,178) (2摄氏度).
道,
同样,依那西普治疗对脊柱结构损伤进展的影响是通过比较257名治疗长达两年的患者(安慰剂治疗组的患者与治疗组的患者分组)与175名OASIS队列的患者进行评估的。同样,依那西普治疗96周后颈椎和腰椎放射学评分(mSASSS)的变化与未接受生物治疗的历史队列患者观察到的变化相似(0.91±2.45)vs0.95±3.18),提示依那西普缺乏“疾病修饰”作用[173) (2摄氏度).
Adalimumab
使用类似的研究设计,ATLAS和M03-606试验比较了307例接受阿达木单抗治疗2年的AS患者的影像学进展与历史OASIS队列中169例接受非生物药物治疗的患者的数据。重要的是,在两项随机对照试验中,最初被分配到安慰剂组并在开放标签阶段开始接受阿达木单抗的患者与在试验开始时被分配到生物制剂的患者一起进行分析。两组间未发现mSASSS变异差异,提示影像学进展相似。历史OASIS队列患者和接受阿达木单抗治疗患者的mSASSS从开始到随访第2年的平均变化分别为0.9±3.3和0.8±2.6 (p = 0.771) [174) (2摄氏度).
Golimumab
GO-RAISE研究还发表了对356名AS患者4年x线进展的分析。138例患者中有111例(80%)最初分配到50 mg golimumab组(巴西批准的唯一皮下剂量)的x线片可用于mSASSS分析。通过计算mSASSS变化,50 mg golimumab组的放射学进展在第一个两年期平均为0.9±2.7,在4年随访期平均为1.3±4.1。2年的分析使用观测数据进行,较长的(4年)分析依赖于通过线性外推完成的9%(26/299)缺失数据。分析上的这种差异大大影响了两个两年期之间的比较。然而,两个间隔(0-2年和0-4年)的平均变化率的稳定性仅仅表明没有发生进展加速[175) (2摄氏度).
Certolizumab pegol
一项关于certolizumab pegol对轴向SpA放射学进展的影响的研究(rapi -轴向SpA试验的一个组)包括174例AS患者和141例非轴向SpA患者,这些患者在基线、第96周和第204周使用mSASSS分析颈椎和腰椎x线片。在4年的研究中,非x线成像轴向SpA患者的损伤进展缓慢(0.06,95% CI−0.17-0.28)。在AS患者中,从0周到204周,mSASSS的平均变化为0.98 (95% CI 0.34-163)。第一个两年期的这一变化(0.67,95% CI 0.21-1.13)大于第二个两年期(0.31,95% CI 0.02-0.60)。这两个时间间隔之间的进展率的降低表明,长期抗tnf α治疗可能抑制结构损伤的进展[176) (2摄氏度).
Secukinumab
MEASURE 1试验还提供了最初在2年内随机分配给secukinumab(75和150 mg)的AS患者的影像学进展数据。150 mg组的97例患者中有86例(88.7%)有可用于mSASSS评估的x线片。从开始到第104周,该分数的平均变化为0.3±2.53个单位。虽然该研究报告了AS患者中使用生物制剂治疗的最低平均放射学进展,并随访了2年,但研究设计和人群的差异排除了这些发现与其他研究结果的比较[145) (2摄氏度).此外,4年的数据已经公布。150mg组的71例患者(73.2%)至少有基线和第208周的x线片。0-2年、2-4年和0-4年的进展率分别为0.5±1.69;0.7±3.32;和1.2±3.91,[177) (2摄氏度).
建议
| 长期使用TNF抑制剂可观察到轴向SpA患者结构损伤进展率的降低(在脊柱x线片上观察到)。证据等级:2B;推荐强度:B(中等);一致度:8.2。 持续使用抗- il - 17 (secukinumab)似乎也观察到对放射学进展的类似影响,但需要在长期研究中证实。证据等级:2C;推荐强度:B(中等);一致度:9.6。 |
12.关于生物制剂治疗轴性SpA患者关节外表现的有效性的证据是什么?
葡萄膜炎
尽管缺乏用于评估生物制剂对轴向SpA相关葡萄膜炎疗效的随机对照试验,但一些观察性、开放标签和非对照研究以及随机对照试验的亚分析合理地弥合了这些治疗疗效的证据差距。
对7项研究的数据进行亚分析,包括397名AS患者,这些患者在安慰剂、英夫利昔单抗和依那西普的累积暴露量分别为70、147和430 PY,计算了三组葡萄膜炎新发作的发生率。抗tnf α药物治疗的患者葡萄膜炎的总发病率为6.8/100 PY,而安慰剂治疗的患者为15.6/100 PY,风险降低了57% (RR = 0.43, 95% CI 0.23-0.81)。英夫利昔单抗治疗患者葡萄膜炎的发生率(3.4/100 PY)与依那西普治疗患者葡萄膜炎的发生率(7.9/100 PY)不同,尽管差异不显著[179) (2).一项开放标签、非随机临床试验包括1250例活动性AS患者,他们接受了20周的阿达木单抗治疗。阿达木单抗治疗前一年的急性前葡萄膜炎发生率为15/100 PY。阿达木单抗治疗将短期发病率(平均暴露时间106天)降低至7.4/100 PY,风险降低50% (RR = 0.50, 95% CI 0.34-0.73) [180) (2摄氏度).在被选为葡萄膜炎频率增加的AS人群中(77例患者在基线前一年发生52次发作),在接受阿达木单抗治疗至少12周后,风险降低幅度甚至更高,从68/100 PY降至14/100 PY (RR = 0.20, 95% CI 0.13-0.32) [181) (2摄氏度).另一个事后对依那西普在AS患者中的8项临床试验的分析发现,依那西普组葡萄膜炎的发生率(8.6/100 PY)比安慰剂组(19.3/100 PY)低55%。从长期来看,考虑到所有在安慰剂对照期和开放标签扩展研究中接受依那西普治疗的患者,发病率为12/100 PY [182) (2摄氏度).较小规模(n≤15)的开放标签和非对照研究也报道了较新的抗tnf α药物golimumab和certolizumab pegol治疗SpA相关前葡萄膜炎的疗效,包括先前接触过另一种抗tnf α药物的患者[183,184,185) (2摄氏度).在speed -轴向SpA试验的双盲期,接受certolizumab pegol治疗的患者葡萄膜炎的发生率低于接受安慰剂治疗的患者(3/100 PY与10.3/100 PY)。在长期随访期间,葡萄膜炎发生率在96周(4.9/100 PY)前保持较低,AS患者和非x线轴向SpA患者之间的发生率相似[186) (2 b).一项开放标签、非随机试验包括93名AS患者,他们接受了12个月的golimumab治疗。比较治疗前12个月和治疗期间前葡萄膜炎的发生率。golimumab治疗可使葡萄膜炎风险从11.1 PY降低80%至2.2/100 PY (RR = 0.20, 95% CI 0.04-0.91) [187) (2摄氏度).最后,2015年发表的一项荟萃分析使用了至少12周的随机对照试验的纳入标准,比较抗tnf α治疗与安慰剂治疗,并描述两组葡萄膜炎的发生率,并得出结论,短期抗tnf α治疗与AS患者葡萄膜炎发作较少相关(OR = 0.35, 95% CI 0.15-0.81)。根据亚组分析的结果,依那西普的治疗效果与安慰剂显著不同,但与单克隆抗体无显著差异。重要的是,计算了该亚分析在比较依那西普与安慰剂时的统计功率(1-β)后验,为99.8%。相反,在单克隆抗体与安慰剂的比较中,较小的样本量仅提供了65.5%的统计效力,因为只有一项certolizumab pegol试验和两项英夫利昔单抗试验符合该研究的纳入标准[188) (2).在分析各种生物制剂的临床试验中报告的葡萄膜炎发病率列于表中6.
一组由抗tnf α治疗引起的悖论性葡萄膜炎病例的发表,强调了融合蛋白(依那西普)和单克隆抗体(包括抗体部分certolizumab pegol)在治疗轴性spa相关葡萄膜炎的疗效(甚至安全性)上的可能差异,提示依那西普治疗后葡萄膜炎新病例的发病率增加[190) (4).随后,几项观察性研究的证据证实了这些发现。一项研究分析了一个大型的美国医疗服务索赔数据库,其中包括大约100个第三方支付者和1.7亿被覆盖的个人。在研究期间被诊断为AS的52,000多名患者中,2115人开始抗tnf α治疗,既往无葡萄膜炎病史。在接受阿达木单抗、英夫利昔单抗和依那西普治疗的患者中,(新)葡萄膜炎病例的发病率分别为2.4、3.2和4.5%,仅阿达木单抗和依那西普之间有显著差异,单克隆抗体更有利[191) (2摄氏度).一项中国回顾性队列研究包括182例有葡萄膜炎病史的AS患者。当时可用的三种抗tnf α药物(阿达木单抗、英夫利昔单抗或依那西普)的治疗同样有效,但可溶性受体的复发率(38%)远高于单克隆抗体(阿达木单抗和英夫利昔单抗分别为6%和11%)。甲氨蝶呤联合抗肿瘤坏死因子α治疗消除了单一治疗之间观察到的疗效差异[192) (2 b).瑞典登记处还分析了1600多名接受阿达木单抗、英夫利昔单抗和依那西普治疗的AS患者前葡萄膜炎的发病率。每种TNFα抑制剂治疗开始前和治疗前两年葡萄膜炎发病率的比较显示,阿达木单抗和英夫利昔单抗治疗的总发病率下降。相反,使用依那西普会增加前葡萄膜炎的发病率。依那西普组葡萄膜炎的调整后HR显著高于阿达木单抗组(HR = 3.86, 95% CI 1.85-8.06),依那西普组显著高于英夫利昔单抗组(HR = 1.99, 95% CI 1.23-3.22),而英夫利昔单抗组与阿达木单抗组之间无差异[193) (2 b).一项涉及1055例AS患者的韩国队列研究分析了抗TNFα抗体(阿达木单抗、英夫利昔单抗或golimumab)、可溶性TNFα受体(依那西普)和非甾体抗炎药(NSAIDs)使用者葡萄膜炎的发生率。与单独使用非甾体抗炎药治疗组相比,抗tnf α单克隆抗体治疗组葡萄膜炎发生率较低(HR = 0.53, 95% CI 0.29-0.96),而依那西普治疗组葡萄膜炎发生率较高(HR = 2.25, 95% CI 1.43-3.53) [194) (2 b).基于这些数据,在抗tnf α抗体中,单克隆抗体比依那西普更有效地预防葡萄膜炎的新发。
关于secukinumab的数据不足以分析其在这一结果方面的疗效。在MEASURE 1和2试验中,观察到治疗组(无论剂量或给药途径)和安慰剂组(RR = 1.20, 95% CI 0.25-5.73)葡萄膜炎发病率无差异[142) (2 b).
牛皮癣和炎性肠病(IBD)
在巴西批准用于治疗轴性SpA的生物制剂中,阿达木单抗和英夫利昔单抗的标签上使用也被批准用于治疗牛皮癣、克罗恩病和溃疡性结肠炎;依那西普和secukinumab治疗斑块性银屑病;certolizumab pegol治疗克罗恩病;还有治疗溃疡性结肠炎的golimumab。在各种生物制剂的临床试验中报告的IBD病例的发病率列于表中6.
目前还没有临床试验专门评估这些药物治疗轴向SpA相关性银屑病的疗效。然而,从银屑病面积和严重程度指数(PASI)的临床反应的疗效分析中,可以合理地推断这些药物的效果,作为替代标记物,在银屑病关节炎的各自研究中,该指数分别为50、75和90。表格7概述了在接受不同药物治疗的患者中这些反应的相对频率(相对于安慰剂组)。此外,尽管人群之间存在差异,甚至在之前接受治疗的情况之间也存在差异,但除了依那西普的结果外,对相同结果可用的各种研究的置信区间重叠,这表明依那西普在控制银屑病方面不如单克隆TNFα抑制剂和secukinumab (2 b).
一项包含9项rct和2项开放标签研究的荟萃分析分析了接受抗tnf α治疗(英夫利昔单抗、阿达木单抗或依那西普,n = 1130)的AS患者中IBD(克罗恩病或溃疡性结肠炎)的发生率,其中6.7% (n = 76)有上述疾病史。在英夫利昔单抗0.2/100 PY、阿达木单抗2.3/100 PY和依那西普2.2/100 PY中,这些患者的治疗与复发和/或新增克罗恩病或溃疡性结肠炎的发生率相关,而安慰剂组的发生率为1.3/100 PY。对于有IBD病史的患者,英夫利昔单抗是本研究中最有效的药物。在新发病例的发病方面,三种药物之间没有观察到差异[189) (2).在MEASURE 1和2试验中,secukinumab治疗患者的克罗恩病单独暴露调整的合并发病率为0.7/100 PY [142) (1 b).在二期临床试验中,依那西普和secukinumab治疗克罗恩病无效[203,204) (2 b).
建议
| 在轴向SpA治疗中复发前葡萄膜炎或活动性炎症性肠病的情况下,抗tnf单克隆抗体(英夫利昔单抗,阿达木单抗,golimumab和certolizumab pegol)在生物制剂中显示出最佳的应答率。因此,建议选择它,最好是别人。证据等级:2A;推荐强度:B(中等);一致度:9.4。 单克隆抗tnf抑制剂(英夫利昔单抗,阿达木单抗,golimumab和certolizumab pegol)和ant-IL17抑制剂已被证明是在轴向SpA中控制活动性银屑病最有效的生物制剂。因此,建议选择它,最好是别人。证据等级:2B;推荐强度:B(中等);一致度:9.4。 |
13.有什么证据支持在轴向SpA患者中切换生物制剂?
轴向SpA患者由于原发性失败(治疗开始后无反应),继发性失败(随着时间的推移对治疗停止反应),甚至毒性,在轴向SpA中长期使用生物药物时,经常需要切换生物药物。关于这个问题,具有高质量设计的研究数量有限,特别是调查最近开发的药物的研究。
一项非对照试验纳入了23例AS患者,他们此前曾接受英夫利昔单抗(最低6次)治疗,未达到ASAS20反应。这些患者转入依那西普50mg /周治疗54周。到第24周,78、52和39%的患者分别达到ASAS20、ASAS50和ASAS70。到第54周,74%的患者至少维持ASAS20反应,61%的患者维持ASAS50反应,39%的患者维持ASAS70反应[205) (2摄氏度).一项对接受抗tnf α药物(英夫利昔单抗、依那西普或阿达木单抗)治疗的AS患者队列的回顾性分析报告,15例患者中93%的患者对第二种抗tnf α药物有临床反应(BASDAI50),其中第一种抗tnf α药物因主要或次要治疗失败、不良反应或患者偏好而切换[206) (2摄氏度).在另一个队列中,16名AS患者(108名抗TNFα药物使用者中的15%)正在接受英夫利昔单抗、依那西普或阿达木单抗治疗,由于无效(67%)或不良事件(28%)而改用不同的TNFα抑制剂。在这些患者中,67%和86%分别在6个月和12个月内达到BASDAI50反应。由于不良反应而切换TNFα抑制剂的患者比由于缺乏疗效而切换的患者更有可能表现出临床反应[207) (2摄氏度).在一项类似的研究中,46例接受抗tnf α治疗的AS患者中有11例(24%)没有临床反应或出现不良反应。接受第二种TNFα抑制剂治疗的患者中有46% (n = 5)有充分的反应,接受第三种抑制剂治疗的患者中有100% (n = 5)有充分的反应[208) (2摄氏度).挪威注册中心(NOR-DMARD)比较了437名使用第一种抗tnf α药物的AS患者和另外77名改用第二种抗tnf α药物的AS患者。3个月后,接受一线治疗的患者中分别有50%和38%达到了BASDAI50和ASAS40应答,而接受二线治疗的患者(转换者)的应答率分别为28%(组间差异p = 0.007)和31% (p = 0.41)。由于无效或不良反应,第二种抗tnf α药物在开关之间的疗效没有显著差异[209) (2 b).丹麦注册中心(DANBIO)还显示,对第二种和第三种抗tnf α药物的反应比第一次使用抗tnf α药物的naïve患者观察到的反应更差,尽管有一半的切换产生了良好的反应。此外,432名转换一次的AS患者和137名转换两次的AS患者与773名未转换的AS患者进行了比较。治疗2年后,79%的一线患者和54%的二线或三线患者维持低疾病活动性,BASDAI<4 (p < 0.0001), 71%和37%的ASDAS<2.1 (p < 0.001) [210) (2 b).回顾性分析了接受抗tnf α药物(阿达木单抗、依那西普、英夫利昔单抗或格利单抗)治疗的AS患者的数据,纳入分析的175例患者中有77例接受了至少两种抗tnf α药物(转换者)。更换第一种药物的主要原因是无效。治疗开始12个月后,切换者的BASDAI50应答率低于非切换者(47%)vs71%),对应OR为0.37 (95% CI 0.26-0.52)。失去反应的其他证据是第一种和第二种抗tnf α疗法的生存时间的差异:分别为63个月(95% CI 57-69)和39个月(95% CI 31-47), p = 0.05 [211) (2 b).
最近,两篇系统文献综述(SLRs)发表的结果支持在治疗失败或发生不良反应时使用第二种抗tnf α药物的策略[212,213) (2).根据一项基于21项研究数据的综述,在接受抗tnf α药物一线治疗的患者中,达到BASDAI50反应的NNT为1.6至2.0。相反,接受二线治疗(使用第二种抗tnf α药物)的患者表现出更高(更糟糕)的nnt,尽管仍然显著,范围为2.5至4.0 [213) (2).
在两种最近推出的抗tnf α药物(golimumab和certolizumab pegol)在轴向SpA患者中的3期试验中,分析了一小部分先前接触过抗tnf α治疗的患者,其中16%在rapi -轴向SpA试验中使用certolizumab pegol, 14.4%在GO-ALIVE试验中使用IV给药golimumab。然而,在这两种情况下都没有报道该亚人群的单独响应数据[138,139) (2摄氏度).
在secukinumab治疗AS的MEASURE 2试验中,38.8%的参与者在开始研究前已经使用了一些抗tnf α药物。随后发表的一篇文章比较了两组的疗效结果(抗tnf α-初发和抗tnf α-反应不足/不耐受),毫不奇怪的是,先前接触组的临床反应也比接受一线生物治疗的组稍差。计算一线和二线治疗的nnt, ASAS20的nnt分别为2.7 (95% CI 1.8-5.6)和3.9 (95% CI 2.0-60);ASAS40为3.9 (95% CI 2.3-14.3)和4.0 (95% CI 2.4-11.2);ASAS部分缓解分别为8.7 (95% CI 4.0-49)和14 (95% CI 6.0-41) [143) (2 b).到目前为止,还没有关于治疗失败或secukinumab毒性反应后二线或三线治疗的疗效的数据。
建议
| 轴向SpA患者如果对生物疗法未表现出初始反应(主要治疗失败)、疗效丧失(次要治疗失败)或不良反应,应切换到另一种已批准的生物制剂,无论其作用机制如何。证据等级:2A;推荐强度:B(中等);一致度:9.4。 第一次生物切换后,反应率略有下降,但仍然显著。关于第二次生物切换的现有证据很少,表明应答率甚至低于二线治疗。证据等级:2A;推荐强度:B(中等);一致度:9.1。 |
14.在轴向SpA患者随访期间,生物制剂应使用多长时间?
考虑到轴向SpA的流行,需要生物制剂的患者比例和所涉及的成本(财务和个人健康相关),必须讨论在被认为患有非活动性疾病的患者中减少和/或停用这些药物的策略。缺乏具有适当方法和足够随访时间的研究进一步复杂化了确定轴向SpA患者缓解的困难任务,以及患者在开始停药前应保持这种假定的非活性状态的最短时间。
停止生物治疗
一项关于轴向SpA患者停止生物治疗的系统综述包括4项RCT扩展和一项非对照试验(n = 220),这些试验在停药前抗tnf α治疗的时间、停药后联合用药的使用以及再激活(突然发作)的定义方面存在高度异质性。1年随访后,76-100%(中位数79%)患者在停药后平均6 - 24周后出现疾病复发。重要的是,在这些研究中,恢复使用这些药物治疗后,获得类似于停药前观察到的良好临床反应的概率很高[214) (2).波兰的一项回顾性研究也得出了类似的结果。在该研究中,74%的轴向SpA患者表现为低疾病活动性(LDA),并完成了抗tnf α治疗的停药,显示疾病复发,在9至48个月的观察期内,平均14周后需要恢复治疗[215) (2摄氏度).相反,在一项随机、双盲对照扩展试验中,capability -3试验纳入了305例专门诊断为非x线轴向SpA的患者,他们正在使用阿达木单抗,并被认为是不活跃的(ASDAS<1.3)至少12周,其中152例患者继续接受阿达木单抗,153例接受安慰剂。经过40周的随访,阿达木单抗组70%的患者和安慰剂组47%的患者没有疾病复发(定义为ASDAS≥2.1)。40周时发作发生率23%的差异对应于4.3戒断后再激活所需的伤害(NNH) (95% CI 2.9-7.9) [216) (1 b).
减少生物治疗剂量
上述系统综述还包括来自八项研究的逐步抗tnf α剂量减少策略的数据,这些研究大多证据级别较低(六项观察性研究,一项对照但非随机试验,只有一项RCT),包括436名AS患者,随访中位时间为12个月。纳入标准在研究中高度异质性,在开始抗tnf α剂量减少前,缓解期或LDA为3 - 6个月。在大多数研究中,缓解被定义为BASDAI<2,正常CRP水平和LDA或BASDAI<4,正常CRP水平。5项研究报告了抗tnf α剂量降低后维持LDA或缓解的患者百分比,范围从53%到100%。其余三项研究报告了抗tnf α剂量减少后BASDAI和CRP水平的平均变化,并没有发现这些参数的相关增加。减量前缓解时间较长的患者以及无外周或关节外表现的患者抗tnf α减量成功率较高[214) (2).荷兰GLAS队列对58例接受LDA抗tnf α治疗的AS患者(BASDAI<4)进行了至少6个月的随访,对这些患者的治疗剂量减少了24个月。依那西普的剂量从50 mg/周减少到25 mg/2周,分4步减少,英夫利昔单抗从5 mg/kg/8周减少到3 mg/kg/10周,阿达木单抗从40 mg/2周减少到40 mg/4周,分2步减少。只有当BASDAI保持<4且主治医生和患者同意随后减少剂量时,剂量才会继续减少。2年后,53%的患者仍采用减剂量方案(平均:标准剂量的62±11%)[217) (2 b).与这些发现一致,其他研究报告了缓解或LDA的轴向SpA患者抗tnf α剂量降低的成功率(范围从标准剂量的50 - 75%不等),随访一年后,成功率从55% - 96%不等[218,219,220,221] 3年后从56%上升到84% [220,222,223]。
在接受相同治疗的患者和缓解期较长的患者中观察到更好的结果[219,221) (2摄氏度).依那西普剂量从50 mg/周降至25 mg/周(或50 mg/2周)的100例AS患者和34例保持标准剂量的对照组患者的药物生存期在4年内保持不变(HR = 0.472, 95% CI 0.155-1.435),从而支持在最长的随访期内减少剂量对缓解/LDA患者的疗效[224) (2 b).韩国的一项研究比较了116例使用减少抗tnf α(依那西普或阿达木单抗)剂量的AS患者和49例使用标准剂量治疗的AS患者在基线后2年和4年的放射学进展。减少组的平均剂量为标准剂量的68%,组间无差异。在进展风险较高的患者(自基线以来伴有联合赘生物的患者)中,仅观察到与标准剂量组(1.23vs1.72户/年;P = 0.023) [225) (2 b).没有研究对轴向SpA患者的secukinumab剂量减少或停药进行研究。
建议
| 对于已达到拟议治疗目标至少6个月的患者,可尝试减少抗tnf α剂量或增加剂量之间的间隔。关于其他行动机制的数据仍然不足。然而,应考虑长期影像学进展的风险。证据等级:1B;推荐强度:B(中等);一致度:8.9。 |
15.是否有证据表明在轴向SpA患者中使用生物制剂和/或靶向特异性小分子与其他作用机制(非tnf αi和非il17i) ?
不可忽视的一部分轴性SpA患者将无法达到预期的活动控制目标、缓解或至少LDA,尽管使用了用于该适应症的常规药物和生物制剂。在这里,我们汇编了目前可用的证据,证明药物与其他作用机制的有效性,包括靶向小分子。
抗cd20,抗il6r和CTLA4-Ig
一项小型(n = 20)、开放标签和非对照试验报告了在有抗tnf α治疗失败史(ASAS20、ASAS40、BASDAI50和ASAS部分缓解的患者分别只有30%、10%、0%和0%)的AS患者对利妥昔单抗(1000mg IV联合100mg甲基强的松龙IV在第0周和第2周)的良好反应。仅在bio-naïve个体中观察到中度缓解(分别有50、40、50和30%的患者获得ASAS20、ASAS40、BASDAI50和ASAS部分缓解)[226) (2摄氏度).有反应的患者(n = 9)随访至48周。4例患者的反应一直维持到研究结束,5例患者出现疾病再激活(定义为BASDAI恶化,对应于达到的最低值的1.5倍,直到第24周),并使用相同剂量治疗,在再治疗后48周内恢复反应[227) (2摄氏度).在两项关于阿巴西普的开放标签和非对照研究中也观察到阴性结果,其中从基线到第24周评估的任何活动参数均未观察到差异[228,229) (2摄氏度).在BUILDER-1研究中分析了IL6受体(IL6R)的治疗性阻断,这是一项II-III期安慰剂对照随机试验,该研究比较了tocilizumab IV (n = 48)与安慰剂(n = 51)在24周随访中治疗AS患者的疗效。12周后,治疗组和对照组中分别有37.3%和27.5%的患者达到ASAS20 (p = 0.28),研究终止[230) (2 b).另一种IL6R抑制剂sarilumab在ALIGN研究中也未能在AS患者中产生临床反应,ALIGN研究是一项涉及301名患者的随机临床试验。在第12周,安慰剂组和试验中任何剂量的sarilumab治疗组之间没有观察到ASAS20反应的差异[231) (2 b).
IL23/IL17轴抑制剂
尽管二期试验的结果很有希望[232], ustekinumab是一种特异性结合IL12和IL23的p40亚单位的抗体,当结果显示安慰剂组和治疗组之间ASAS20、ASAS40和BASDAI50反应的患者比例无差异或ASDAS-CRP或BASFI评分无变化时,三个III期研究(n = 1017)在24周后早期中断[233) (1 b).
靶向小分子
在II期研究中,特异性磷酸二酯酶-4 (PDE-4)抑制剂阿普美司特与安慰剂相比,从基线到第12周,BASDAI、BASFI和BASMI评分没有明显变化。此外,在治疗组和安慰剂组之间没有观察到ASAS20反应频率的差异[234) (2 b).反过来,治疗性阻断Janus激酶(JAK),一个非受体酪氨酸激酶家族,转导各种细胞因子的细胞内信号,在AS患者中产生了有希望的结果。Tofacitinib是JAK-1和JAK-3的选择性抑制剂,在II期试验中对207名患者进行了测试,随机分配到三种治疗剂量(2,5和10mg,每天2次)和安慰剂,其主要结果是第12周的ASAS20反应。5 mg和10 mg托法替尼治疗组与安慰剂组在ASAS20、ASAS40和BASDAI50反应上有显著差异,而在ASAS部分缓解和ASDAS无活性疾病反应上无显著差异。此外,约三分之一接受托法替尼治疗的患者在骶髂关节和脊柱MRI上显示炎症减轻,这是这些患者中最常见的临床反应[235,236) (2 b).另一种JAK抑制剂filgotinib对JAK-1具有选择性,也在TORTUGA试验中进行了测试,这是一项II期临床试验,包括116名AS患者。第12周时,治疗组的ASDAS较基线的变化大于安慰剂组:分别为−1.47(±1.04)和−0.57(0.82),平均差值为−0.85 (95% CI为−1.17至−0.53,p < 0.0001)。第12周时,治疗组患者达到ASAS20和ASAS40反应的比例显著增加,BASDAI、BASMI和BASFI评分下降,超敏CRP水平下降。与安慰剂组相比,治疗组ASDAS无活动性疾病和ASAS部分缓解的患者比例更高,但差异不显著[237) (2 b).
建议
| 不建议使用其他生物制剂和/或靶向小分子(阿巴西普、托西单抗、利妥昔单抗、sarilumab、ustekinumab和apremasast)治疗轴向SpA患者。证据等级:1B;推荐强度:A(强);一致度:9.5。 Janus激酶(JAK)抑制剂tofacitinib和filgotinib在治疗强直性脊椎炎方面显示出良好的临床结果,但在推荐它们之前仍需要更明确的证据(III期随机临床试验)。证据等级:2B;推荐强度:B(中等);一致度:9.1。 |
结论
本文提出的建议旨在为风湿病学家和其他参与治疗轴性脊椎关节炎患者的代理人提供科学证据。在选择应对的每种情况中,考虑的方面包括治疗效果、安全性和成本,以及专家小组的关键评估和经验,以便在国家社会经济背景下对这些情况进行标准化管理,但在选择不同治疗方案时保持医生的自主权。这些建议应该定期更新,因为这一领域的知识发展迅速。
数据和材料的可用性
在线补充1和2。
参考文献
鲁德华列特M, Landewe R, van der Heijde D, Listing J, Brandt J, Braun J,等。脊椎关节炎评估国际学会轴性脊椎关节炎分类标准的制定(第一部分):通过专家意见包括不确定性评估对论文患者进行分类。中国生物医学工程学报,2009;29(6):379 - 379。
李志强,李志强,李志强,等。脊椎关节炎评估的发展国际社会轴性脊椎关节炎分类标准(第二部分):验证和最终选择。中国生物医学工程学报,2009;29(6):379 - 379。
Sampaio-Barros PD, Keiserman M, Meirelles Ede S, Pinheiro Mde M, Ximenes AC, Azevedo VF,等。强直性脊柱炎的管理和治疗建议。《中国日报》,2013;53(3):242-57。
Phillips B, Ball C, Sackett D, Badenoch D, Straus S, Haynes B,等。证据水平。BJU Int. 2010;106: 1424。
林志,廖志,黄娟,金欧,李强,李涛,等。中国慢性背痛患者轴性颈椎病国际学会分类标准的评估:2年随访研究结果中华风湿病杂志;2014;17(7):782-9。
Deodhar A, Mease PJ, Reveille JD, Curtis JR, Chen S, Malhotra K,等。美国风湿病学家为评估慢性背痛所见的患者中轴性脊椎关节炎诊断的频率。风湿性关节炎。2016;68(7):1669-76。
李文杰,李志强,李志强,等。在ASAS队列随访后,ASAS分类标准对轴性和周围型颈椎病的预测有效性:最终分析。中国生物医学工程学报。2016;35(6):1034-42。
Bendahan LT, Machado NP, Mendes JG, Oliveira TL, Pinheiro MM.迟发型轴性颈椎病患者分类标准的表现。Mod Rheumatol. 2018;28(1): 174-81。
茂W, Zeidler H, Mau R, Majewski A, Freyschmidt J, Stangel W,等。强直性脊柱炎患者的临床特点及预后分析。10年随访结果。中华风湿病杂志,1988;15(7):1109-14。
Bennett AN, McGonagle D, O'Connor P, Hensor EM, Sivera F, Coates LC,等。基线磁共振成像明显的骶髂炎的严重程度和早期炎症性背痛的HLA-B27状态可预测8年后放射学上明显的强直性脊柱炎。风湿性关节炎。2008;58(11):3413-8。
Weber U, Lambert RG, Ostergaard M, Hodler J, Pedersen SJ, Maksymowych WP。磁共振成像在脊椎炎中的诊断效用:187个受试者的国际多中心评估。风湿性关节炎。2010;62(10):3048-58。
Rudwaleit M, Jurik AG, Hermann KG, Landewe R, van der Heijde D, Baraliakos X,等。在磁共振成像(MRI)上定义活动性骶髂炎用于轴性脊椎关节炎的分类:ASAS/OMERACT MRI组一致同意的方法。中国生物医学工程学报,2009;29(3):344 - 344。
Aydin SZ, Maksymowych WP, Bennett AN, McGonagle D, Emery P, Marzo-Ortega H.在一项随访8年的轴性脊柱关节炎初始队列中,ASAS标准的验证和骶髂关节MRI阳性的定义。中华神经外科杂志,2012;71(1):56-60。
拉比A, Viala P, Molinari N, Lukas C, Baron MP, Taourel P,等。评估骶髂关节MRI异常及其预测轴性颈椎病的能力:110例患者的回顾性初步研究骨放射。2014;43(3):351-8。
Weber U, Zubler V, Pedersen SJ, Rufibach K, Lambert RG, Chan SM,等。开发和验证磁共振成像参考标准,以确定脊椎关节炎患者的骶髂关节磁共振成像阳性。关节炎护理,2013;65(6):977-85。
Weber U, Pedersen SJ, Zubler V, Rufibach K, Chan SM, Lambert RG,等。骶髂关节磁共振成像上的脂肪浸润对非x线轴性颈椎病的诊断价值有限。风湿病杂志。2014;41(1):75-83。
Weber U, Ostergaard M, Lambert RG, Pedersen SJ, Chan SM, Zubler V,等。两组轴性颈椎病患者中定义骶髂关节MRI阳性的候选病变标准。中国生物医学工程学报(英文版);2015;
巴克尔PA, van den Berg R, Lenczner G, Thevenin F, Reijnierse M, Claudepierre P,等。我们能否根据ASAS的轴性颈椎病标准,可靠地使用骶髂关节MRI上的结构性病变来对患者进行分类?数据来自DESIR队列。中华神经外科杂志,2017;36(2):392-8。
de Hooge M, van den Berg R, Navarro-Compan V, Reijnierse M, van Gaalen F, Fagerli K,等。SPACE队列中患有短时间慢性背痛的患者:哪些骶髂关节的MRI结构性病变和脊柱的炎症性和结构性病变对轴性颈椎病最为特异性?安风湿病。2016;75:1308-1314。
de Hooge M, van den Berg R, Navarro-Compan V, van Gaalen F, van der Heijde D, Huizinga T,等。骶髂关节磁共振成像在颈椎病早期诊断中的应用:与短tau反转恢复序列相比,钆无附加价值。风湿病学。2013;52(7):1220 - 4。
赵玉华,曹云云,张强,梅玉军,肖俊杰,胡淑云,等。弥散加权和增强磁共振成像在鉴别强直性脊柱炎活动性中的作用。中华医学杂志,2017;30(11):1303-8。
Bradbury LA, Hollis KA, Gautier B, Shankaranarayana S, Robinson PC, Saad N,等。弥散加权成像是诊断强直性脊柱炎的一种敏感而特异的磁共振序列。风湿病杂志,2018;45(6):771-8。
Hermann KG, Baraliakos X, van der Heijde DM, Jurik AG, Landewe R, Marzo-Ortega H,等。轴性颈椎病患者脊柱MRI病变的描述和脊柱MRI阳性的定义:ASAS/OMERACT MRI研究组一致同意的方法。中国生物医学工程学报。2012;21(8):1278-88。
Bennett AN, Rehman A, Hensor EM, Marzo-Ortega H, Emery P, McGonagle D.脂肪性Romanus病变:轴性脊柱关节病特有的非炎症性MRI病变。中国生物医学工程学报,2010;69(5):814 - 4。
Lorenzin M, Ortolan A, Frallonardo P, Vio S, Lacognata C, Oliviero F,等。早期轴性颈椎病患者的脊柱和骶髂关节磁共振成像:来自意大利SPACE研究小组的病变患病率和临床和疾病活动指数的相关性Reumatismo。2016;68(2):72 - 82。
van der Heijde D, Sieper J, Maksymowych WP, Brown MA, Lambert RG, Rathmann SS,等。活动性非x线轴型颈椎病患者在磁共振成像上无骶髂关节炎症时的脊柱炎症。风湿性关节炎。2014;66(3):667-73。
Ez-Zaitouni Z, Bakker PA, van Lunteren M, de Hooge M, van den Berg R, Reijnierse M,等。在ASAS分类标准中轴性颈椎病的成像标准:来自SPACE和DESIR队列的结果中国生物医学工程学报。2017;36(10):1731-6。
张文杰,张文杰,张文杰,等。在非x线轴性颈椎病患者中,脊柱MRI是否增加了单纯骶髂关节MRI的诊断价值?中华神经外科杂志,2015;74(6):985-92。
马德森KB, Schiottz-Christensen B, Jurik AG。椎病患者骶髂关节磁共振成像改变的预后意义——一项随访研究。风湿病杂志,2010;37(8):1718-27。
Maksymowych WP, Wichuk S, Chiowchanwisawakit P, Lambert RG, Pedersen SJ。骶髂关节MRI上的脂肪化生增加了脊椎关节病患者脊柱疾病进展的倾向。限制型心肌病开放。3 (1): e000399。2017;
Maksymowych WP, Chiowchanwisawakit P, Clare T, Pedersen SJ, Ostergaard M, Lambert RG。磁共振成像上脊柱的炎症病变预示着强直性脊柱炎中新联合菌的发展:炎症与新骨形成之间关系的证据。风湿性关节炎。2009;60(1):93-102。
Machado P, Landewe R, Braun J, Hermann KG, Baker D, van der Heijde D.脊柱结构损伤和炎症都有助于强直性脊柱炎患者脊柱活动障碍。中国生物医学工程学报,2010;29(3):344 - 344。
李志强,李志强,李志强。强直性脊柱炎复发风险的遗传易感性模型研究。中国生物医学工程学报,2000;39(11):883-6。
张志刚,张志刚,张志刚,张志刚,等。HLA-B27阳性和阴性献血者脊椎病的患病率。风湿性关节炎。1998;41(1):58-67。
Schlosstein L, Terasaki PI, Bluestone R, Pearson CM。HL-A抗原W27与强直性脊柱炎高度相关。中华实用医学杂志,2003,26(4):344 - 344。
李志强,李志强,李志强。脊柱关节炎的流行病学研究进展。临床风湿醇最佳实践研究。2006;20(3):401-17。
汗马。HLA-B*27遗传多态性的研究进展(含213个等位基因,160个亚型(仍在增加))Curr Rheumatol rep 2017;19(2):9。
Freeston J, Barkham N, Hensor E, Emery P, Fraser A.强直性脊柱炎,HLA-B27阳性和生物治疗的必要性。关节与脊柱。2007;74(2):140-3。
强直性脊柱炎功能和活动指标的临床应用中华医学杂志。2014;7(1):78-83。
杨敏,徐敏,潘旭,胡忠,李强,魏勇,等。中国强直性脊柱炎患者HLA-B*27携带者临床表现的流行病学比较中国生物医学工程学报,2013;29(5):344 - 344。
Fallahi S, Mahmoudi M, Nicknam MH, Gharibdoost F, Farhadi E, Saei A,等。HLA-B*27及其亚型对伊朗强直性脊柱炎临床表现及严重程度的影响中国过敏哮喘杂志。2013;12(4):321-30。
熊娟,陈娟,涂军,叶伟,张震,刘强,等。强直性脊柱炎患者HLA-B27状态和性别与骶髂炎的关系巴基斯坦医学杂志,2014;30(1):22-7。
李志强,李志强,李志强,等。轴性脊椎炎的早期疾病阶段:来自德国脊椎炎初始队列的结果。风湿性关节炎。2009;60(3):717-27。
Zeboulon N, Dougados M, Gossec L.葡萄膜炎在脊柱关节病中的患病率和特征:一项系统的文献综述。中华医学杂志,2008;29(7):955-9。
van der Heijde D, Ramiro S, Landewé R, Baraliakos X, van den Bosch F, Sepriano A,等。2016年更新的ASAS-EULAR治疗轴性颈椎病的建议。中华神经外科杂志,2017;76(6):978-91。
van den Berg R, Baraliakos X, Braun J, van der Heijde D.使用非药物和非生物药物治疗强直性脊柱炎的最新证据:关于强直性脊柱炎ASAS/EULAR治疗建议的系统文献综述。51风湿病。2012;(8):1388 - 96。
Dagfinrud H, Kvien TK, Hagen KB。强直性脊柱炎的物理治疗干预。Cochrane Database Syst Rev. 2008;1:CD002822。
雷格尔A, Sepriano A, Baraliakos X, van der Heijde D, Braun J, Landewe R,等。非药物和非生物药物治疗的有效性和安全性:一项系统的文献综述,为2016年更新的ASAS/ euular推荐治疗轴性颈椎病提供信息。限制型心肌病开放。3 (1): e000397。2017;
Fernandez-de-Las-Penas C, Alonso-Blanco C, Morales-Cabezas M, Miangolarra-Page JC。强直性脊柱炎患者的两种运动干预:一项随机对照试验。中华康复医学杂志。2005;34(6):457 - 457。
Fernandez-de-Las-Penas C, Alonso-Blanco C, Alguacil-Diego IM, Miangolarra-Page JC。强直性脊柱炎患者的两种运动干预的一年随访:一项随机对照试验。中华康复医学杂志。2006;85(7):559-67。
Silva EM, Andrade SC, Vilar MJ。全身性体位再教育对强直性脊柱炎患者疗效的评价。风湿病杂志,2012;32(7):2155-63。
Rosu MO, Topa I, Chirieac R, Ancuta C.普拉提、McKenzie和Heckscher训练对强直性脊柱炎患者疾病活动、脊髓运动和肺功能的影响:一项随机对照试验风湿病杂志2014;34(3):367-72。
Staalesen Strumse YA, Nordvag BY, Stanghelle JK, Roisland M, Winther A, Pajunen PA,等。强直性脊柱炎患者的康复疗效:地中海和挪威环境下为期四周的康复计划的比较中华康复医学杂志,2011;43(6):534-42。
Kjeken I, Bo I, Ronningen A, Spada C, Mowinckel P, Hagen KB,等。一项为期三周的多学科住院康复计划对强直性脊柱炎患者具有积极的长期影响:随机对照试验。中华康复医学杂志,2013;45(3):260-7。
Aytekin E, cagar NS, Ozgonenel L, Tutun S, Demiryontar DY, Demir SE。强直性脊柱炎患者的家庭运动疗法:对疼痛、活动能力、疾病活动、生活质量和呼吸功能的影响临床风湿病杂志,2012;31(1):91-7。
刘志刚,张志刚,张志刚。结构化小组教育对强直性脊柱炎患者的治疗效果。临床风湿病杂志,2017;23(3):138-43。
Rodriguez-Lozano C, Juanola X, Cruz-Martinez J, Pena-Arrebola A, Mulero J, Gratacos J,等。强直性脊柱炎患者教育和家庭锻炼项目的结果:一项全国性随机研究。中华风湿病杂志。2013;31(5):739-48。
梁红,张红,季红,王超。家庭运动干预对强直性脊柱炎患者健康相关生活质量的影响:一项meta分析。临床风湿病杂志。2015;34(10):1737-44。
詹宁斯F, Oliveira HA, de Souza MC, Cruz Vda G, Natour J.有氧训练对强直性脊柱炎患者的影响。风湿病杂志,2015;42(12):2347-53。
聂德曼K, Sidelnikov E, Muggli C, Dagfinrud H, Hermann M, Tamborrini G,等。心血管训练对强直性脊柱炎患者体能和感知疾病活动的影响关节炎护理研究。2013;65(11):1844-52。
Levitova A, Hulejova H, Spiritovic M, Pavelka K, Senolt L, Husakova M.强直性脊柱炎和非x线轴性脊柱炎患者强化运动后血清钙保护蛋白水平的临床改善和降低。关节炎治疗。2016;18(1):275。
王志强,王志强,王志强,等。高强度运动对活动性轴性脊髓型关节炎患者疾病活动度和心血管风险的疗效:一项随机对照试点研究PLoS One. 2014;9(9):e108688。
丁达尔,索拉克,托克塔斯,德米尔达尔,苏巴斯,卡武库,等。水上运动对强直性脊柱炎的影响:一项随机对照试验。风湿病杂志2014;34(11):1505-11。
费尔南德斯·加西亚R,桑切斯·桑切斯Lde C,洛佩兹·罗德里格斯Mdel M,桑切斯·格拉纳多斯g[脊椎关节炎患者的运动和放松水上项目的影响:一项随机试验]。中华医学杂志2015;145(9):380-384。
Klemz BN, Reis-Neto ET, Jennings F, Siqueira US, Klemz FK, Pinheiro HH,等。无症状心血管病伴风湿性疾病患者在开始有监督的体育锻炼前进行运动测试的相关性风湿病学(牛津大学)。55 2016;(11): 1978 - 86。
静脉注射甲基强的松龙脉冲治疗强直性脊柱炎。中华风湿病杂志。1992;21(3):134-8。
Rihl MBN, Wiese B, Schmidt RE, Zeidler H.静脉糖皮质激素脉冲治疗活动性,非甾体抗炎药顽固性轴性强直性脊柱炎:12个月的回顾性分析。中华风湿病杂志,2018;7(1):266-9。
Bandinelli F, Scazzariello F, Pimenta da Fonseca E, Barreto Santiago M, Marcassa C, Nacci F,等。小剂量减释强的松治疗轴性颈椎病:3个月疗效及耐受性。药物设计开发治疗。2016;10:3717-24。
Haibel H, Fendler C, Listing J, Callhoff J, Braun J, Sieper J.口服强的松龙治疗活动性强直性脊柱炎的疗效:一项双盲、随机、安慰剂对照的短期试验结果。中华神经外科杂志,2014;29(1):344 - 344。
张亚平,龚颖,曾启勇,侯志东,肖志智。一项关于低剂量糖皮质激素治疗强直性脊柱炎安全性的长期观察性队列研究:不良事件和对骨密度、血脂、血糖水平和体重指数的影响英国医学杂志,2015;5(6):e006957。
超声引导后跟囊皮质类固醇注射治疗血清阴性脊椎病患者难治性跟腱炎:疗效和随访研究。风湿病杂志,2016;36(6):875-80。
张志刚,张志刚,张志刚。糖皮质激素治疗跟腱损伤的临床意义。国际足踝杂志。2009;30(7):665 - 5。
鲍洛,J . Braun, Taupitz M, Haberle J, Reibhauer BH, Paris S,等。ct引导下骶髂关节内皮质类固醇注射在脊柱关节病患者:适应证和MRI增强随访。中国计算机工程学报。1996;20(4):512-21。
Kroon FPB, van der Burg LRA, Ramiro S, Landewé RBM, Buchbinder R, Falzon L,等。非甾体抗炎药(NSAIDs)治疗轴性脊柱炎(强直性脊柱炎和非x线轴性脊柱炎)(综述)。7. Cochrane图书馆2015;
王锐,Dasgupta A, Ward MM.非甾体类抗炎药物治疗强直性脊柱炎的疗效比较:临床试验的贝叶斯网络荟萃分析。安·莱厄姆,2015。
Walker C, Essex MN, Li C, Park PW。塞来昔布与双氯芬酸治疗强直性脊柱炎:挪威患者12周随机研究中华实用医学杂志,2016;44(3):483-95。
李志强,李志强,李志强,等。一项随机临床试验,评估两剂量依托昔布与萘普生在强直性脊柱炎患者中的相对疗效和耐受性。BMC肌肉骨骼失调。2016;17(1):426。
Wanders A, hejde D, Landewe R, Behier JM, Calin A, Olivieri I,等。非甾体类抗炎药物可减少强直性脊柱炎患者的影像学进展:一项随机临床试验风湿性关节炎。2005;52(6):1756-65。
Kroon F, Landewe R, Dougados M, van der Heijde D.在强直性脊柱炎患者中,持续使用非甾体抗炎药逆转炎症对放射学进展的影响。中国生物医学工程学报,2012;29(3):344 - 344。
李志强,李志强,李志强,等。非甾体类抗炎药对轴向型颈椎病患者放射学脊柱进展的影响:来自德国颈椎病初始队列的结果。中国生物医学工程学报,2012;21(10):1616-22。
李志刚,李志刚,李志刚,李志刚,等。双氯芬酸连续与按需治疗强直性脊椎炎2年以上对脊柱放射学进展的影响:来自随机多中心试验(ENRADAS)的结果。安·莱厄姆,2015。
杨震,赵伟,刘伟,吕强,董霞。应用meta分析评价甲氨蝶呤治疗强直性脊柱炎疗效。中华临床药物杂志,2014;52(5):346-51。
Gonzalez-Lopez L, Garcia-Gonzalez A, Vazquez-Del-Mercado M, Munoz-Valle JF, Gamez-Nava JI。甲氨蝶呤治疗强直性脊柱炎的疗效:随机、双盲、安慰剂对照试验。风湿病杂志,2004;31(8):1568-74。
Altan L, Bingol U, Karakoc Y, Aydiner S, Yurtkuran M, Yurtkuran M.甲氨蝶呤治疗强直性脊柱炎的临床研究。中华风湿病杂志,2001;30(5):255-9。
Roychowdhury B, binley - bagot S, Bulgen DY, Thompson RN, Tunn EJ, Moots RJ。甲氨蝶呤对强直性脊柱炎有效吗?41风湿病。2002;(11):1330 - 2。
Perez-Guijo VC, Cravo AR, Castro Mdel C, Font P, Munoz-Gomariz E, Collantes-Estevez E.英夫利昔单抗联合甲氨蝶呤治疗强直性脊柱炎疗效增加。关节与脊柱。2007;74(3):254-8。
Breban M, Ravaud P, Claudepierre P, Baron G, Henry YD, Hudry C,等。强直性脊柱炎英夫利昔单抗治疗的维持:一项比较系统治疗与按需治疗的一年随机对照试验的结果。风湿性关节炎。2008;58(1):88-97。
Creemers MC, Franssen MJ, van de Putte LB, Gribnau FW, van Riel PL.甲氨蝶呤治疗重度强直性脊柱炎:一项开放研究。风湿病杂志,1995;22(6):1104-7。
Biasi D, Carletto A, Caramaschi P, Pacor ML, Maleknia T, Bambara LM。甲氨蝶呤治疗强直性脊柱炎的疗效:一项为期三年的开放研究。临床风湿病杂志2000;19(2):114-7。
桑帕约-巴罗斯PD, Costallat LT, Bertolo MB, Neto JF,萨马拉AM。甲氨蝶呤治疗强直性脊柱炎。中华风湿病杂志,2000;29(3):160-2。
Bachta A, Kisiel B, tuustochowicz M, Raczkiewicz A, rzhakas M, tuustochowicz W.甲氨蝶呤治疗复发性特发性急性前葡萄膜炎的疗效:一项前瞻性研究。中国免疫免疫学杂志,2017;29(1):344 - 344。
陈娟,刘晨。柳氮磺胺吡啶治疗强直性脊柱炎。Cochrane Database Syst Rev. 2005;2:CD004800。
陈娟,林珊珊,刘晨。柳氮磺胺吡啶治疗强直性脊柱炎。Cochrane Database Syst Rev. 2014;11:CD004800。
Braun J, Zochling J, Baraliakos X, Alten R, Burmester G, Grasedyck K,等。柳氮柳嗪治疗未分化性脊柱炎和早期强直性脊柱炎引起的炎症性背痛的疗效:一项多中心随机对照试验中华医学杂志。2006;65(9):1147-53。
黄芳,王志强,王志强,等。依那西普与柳氮柳嗪在强直性脊柱炎患者中的临床疗效和安全性:一项随机、双盲试验。风湿性关节炎。2011;63(6):1543-51。
宋海燕,李志强,李志强,等。依那西普与柳氮柳嗪治疗早期轴性颈椎病对全身MRI (ESTHER)检测的活动性炎症病变的影响:一项48周随机对照试验。中国生物医学工程学报,2011;29(4):489 - 497。
费格里,范·德·海杰德·D,海伯格·MS, Wierod·A, Kalstad S, Rodevand E,等。在TNF抑制时期,磺胺柳嗪在轴型颈椎病中是否有作用?数据来自NOR-DMARD纵向观察研究。风湿病学。2014;53(6):1087 - 94。
kanna Sharma S, Kadiyala V, Naidu G, Dhir V.研究柳氮柳嗪治疗强直性脊柱炎轴性疾病疗效的随机对照试验。中华大黄杂志,2018;21(1):308-14。
Muñoz-Fernández S, Hidalgo V, Fernández-Melón J, schlinker A, Bonilla G, Ruiz-Sancho D,等。柳氮磺胺可在一年内减少急性前葡萄膜炎的发作次数。风湿病杂志,2003;30(6):1277-9。
Benitez-Del-Castillo JM, Garcia-Sanchez J, Iradier T, Bañares A.柳氮磺胺柳氮预防强直性脊柱炎伴前葡萄膜炎。眼睛(Lond)。3 2000; 14 (Pt): 340 - 3。
van Denderen JC, van der Paardt M, Nurmohamed MT, de Ryck YM, Dijkmans BA, van der Horst-Bruinsma IE。来氟米特治疗活动性强直性脊柱炎的双盲、随机、安慰剂对照研究清华大学学报(自然科学版),2005;
来氟米特治疗活动性强直性脊柱炎的6个月开放标签试验。中国科学(d辑),2005;26(1):1 - 6。
李E, Kristensen LE, forsbladd 'Elia H, Zverkova-Sandstrom T, Askling J, Jacobsson LT,等。联合常规合成疾病修饰抗风湿药物对强直性脊柱炎和未分化性脊柱炎患者TNF抑制剂药物生存的影响:来自全国前瞻性研究的结果中国生物医学工程学报,2015;26(6):970-8。
Sepriano A, Ramiro S, van der Heijde D, Avila-Ribeiro P, Fonseca R, Borges J,等。联合常规合成疾病修饰抗风湿药物对颈椎病患者肿瘤坏死因子抑制剂滞留的影响:一项前瞻性队列研究风湿性关节炎。2016;68(11):2671-9。
Braun J, Brandt J, Listing J, Zink A, Alten R, gold W,等。英夫利昔单抗治疗活动性强直性脊柱炎:一项随机对照多中心试验。柳叶刀》。2002;359(9313):1187 - 93。
Braun J, Brandt J, Listing J, Zink A, Alten R, Burmester G,等。英夫利昔单抗治疗强直性脊柱炎的长期疗效和安全性:一项为期三个月、随机、安慰剂对照试验的开放、观察性扩展研究风湿性关节炎。2003;48(8):2224-33。
Braun J, Brandt J, Listing J, Zink A, Alten R, Burmester G,等。英夫利昔单抗治疗强直性脊柱炎的疗效和安全性维持2年。清华大学学报(自然科学版),2005;
张志刚,张志刚,张志刚,等。强直性脊柱炎患者抗tnf - α抗体英夫利昔单抗持续临床反应超过3年。风湿病学。2005;44(5):670 - 6。
张志刚,张志刚,张志刚,等。抗肿瘤坏死因子α联合英夫利昔单抗治疗强直性脊脊炎患者5年以上的持续临床疗效和安全性:不同类型反应的证据。中华医学杂志,2008;37(3):344 - 344。
李志强,李志强,李志强,李志强,等。英夫利昔单抗治疗强直性脊柱炎8年后持续的临床疗效和安全性——早期临床反应预测长期结果。风湿病学。2011;50(9):1690 - 9。
van der Heijde D, Dijkmans B, Geusens P, Sieper J, DeWoody K, Williamson P,等。英夫利昔单抗治疗强直性脊柱炎患者的疗效和安全性:一项随机、安慰剂对照试验(ASSERT)的结果。风湿性关节炎。2005;52(2):582-91。
葛文杰,张志刚,张志刚。肿瘤坏死因子α抑制治疗强直性脊柱炎的临床研究。中华实用医学杂志,2002;29(6):529 - 529。
Davis JC Jr, Van Der Heijde D, Braun J, Dougados M, Cush J, Clegg DO,等。重组人肿瘤坏死因子受体(依那西普)治疗强直性脊柱炎:一项随机对照试验。风湿性关节炎。2003;48(11):3230-6。
Davis JC, van der Heijde DM, Braun J, Dougados M, Cush J, Clegg D,等。依那西普治疗强直性脊柱炎96周的持续耐受性和耐受性。中国科学(d辑),2005;
Davis JC Jr, van der Heijde DM, Braun J, Dougados M, Clegg DO, Kivitz AJ,等。依那西普治疗强直性脊柱炎患者长达192周的疗效和安全性。中华医学杂志。2008;67(3):346-52。
刘志刚,刘志刚,刘志刚,等。依那西普治疗活动性强直性脊柱炎患者的6个月双盲安慰剂对照试验结果。风湿性关节炎。2003;48(6):1667-75。
Brandt J, Listing J, Haibel H, Sorensen H, Schwebig A, Rudwaleit M,等。依那西普治疗活动性强直性脊柱炎后的长期疗效和安全性。风湿病学。2005;44(3):342 - 8。
李志强,李志强,李志强,等。活动性强直性脊柱炎患者服用依那西普的长期结果——7年后持续疗效和安全性。关节炎研究。2013;15(3):R67。
张志强,张志强,张志强,等。依那西普治疗强直性脊柱炎的多中心随机临床试验结果。清华大学学报(自然科学版),2004;
杜格多斯M, Braun J, Szanto S, Combe B, Elbaz M, Geher P,等。依那西普对晚期强直性脊柱炎患者风湿症状和肺功能测试的疗效:一项随机双盲安慰剂对照研究(SPINE)的结果中国生物医学工程学报,2011;29(5):369 - 369。
宋国华,王志强,王志强,等。依那西普治疗1年后,强直性脊柱炎和非x线轴型颈椎病患者的反应率相似:来自ESTHER试验的结果中华神经外科杂志,2013;32(6):823-5。
宋海燕,李志刚,李志刚,等。依那西普连续治疗3年后早期轴性颈椎病患者持续良好的临床反应:ESTHER试验的长期数据。风湿病杂志,2014;41(10):2034-40。
杜格多斯M, van der Heijde D, Sieper J, Braun J, Maksymowych WP, Citera G,等。依那西普的症状疗效及其对早期非x线轴性颈椎病客观炎症征象的影响:一项多中心、随机、双盲、安慰剂对照试验风湿性关节炎。2014;66(8):2091-102。
马西莫威,杨晓娟,陈晓娟,等。依那西普治疗早期非x线轴型颈椎病的临床和MRI反应:来自EMBARK研究的48周结果。神经外科杂志,2016;75(7):1328-35。
李志华,张勇,王杰,史志军。依那西普治疗强直性脊柱炎:一项随机、双盲、安慰剂对照临床试验的荟萃分析,以及高加索和中国人群的比较。中华骨科杂志。2013;23(5):497-506。
van der Heijde D, Kivitz A, Schiff MH, Sieper J, Dijkmans BA, Braun J,等。阿达木单抗在强直性脊柱炎患者中的疗效和安全性:一项多中心、随机、双盲、安慰剂对照试验的结果风湿性关节炎。2006;54(7):2136-46。
van der Heijde D, Schiff MH, Sieper J, Kivitz AJ, Wong RL, Kupper H,等。阿达木单抗治疗强直性脊柱炎的有效性可维持长达2年:ATLAS试验的长期结果。中国生物医学工程学报,2009;26(6):922-9。
van der Heijde DM, Revicki DA, Gooch KL, Wong RL, Kupper H, Harnam N,等。强直性脊柱炎患者接受3年阿达木单抗治疗后的身体功能、疾病活动和与健康相关的生活质量结果关节炎治疗。2009;11(4):R124。
Sieper J, van der Heijde D, Dougados M, Brown LS, Lavie F, Pangan AL.强直性脊柱炎患者对阿达姆单抗的早期反应可预测5年治疗后的长期缓解。中国生物医学工程学报,2012;29(5):344 - 344。
王丽玲,王晓明,王晓明,等。阿达木单抗治疗没有放射学定义的骶髂炎的轴性脊椎炎的疗效:一项12周随机、双盲、安慰剂对照试验的结果,随后开放标签扩展至52周。风湿性关节炎。2008;58(7):1981-91。
Sieper J, van der Heijde D, Dougados M, Mease PJ, Maksymowych WP, Brown MA,等。阿达木单抗对非x线轴性颈椎病患者的疗效和安全性:一项随机安慰剂对照试验的结果(ABILITY-1)。中华神经外科杂志,2013;32(6):815-22。
王华,左东,孙敏,华勇,蔡哲。阿达木单抗治疗强直性脊柱炎疗效和安全性的随机、安慰剂对照和双盲试验:一项meta分析。中华风湿病杂志,2014;17(2):142-8。
尹曼RD, Davis JC Jr, hejde D, Diekman L, Sieper J, Kim SI,等。golimumab治疗强直性脊柱炎患者的有效性和安全性:一项随机、双盲、安慰剂对照、III期试验的结果风湿性关节炎。2008;58(11):3402-12。
张志强,张志强,张志强,等。goimumab在强直性脊柱炎中每4周皮下注射一次:GO-RAISE研究104周结果。中国生物医学工程学报,2012;29(5):661-7。
周勇,徐松,周勇,李志强,等。goimumab在强直性脊柱炎中每4周皮下注射一次:GO-RAISE研究的5年结果。中国生物医学工程学报,2015;34(4):757-61。
鲍晨,黄峰,马可汗,费科,吴震,韩晨,等。golimumab在中国活动性强直性脊柱炎患者中的安全性和有效性:一项多中心、随机、双盲、安慰剂对照III期试验的1年结果风湿病学。2014;53(9):1654 - 63。
Sieper J, van der Heijde D, Dougados M, Maksymowych WP, Scott BB, Boice JA,等。一项随机、双盲、安慰剂对照、16周的皮下golimumab治疗活动性非x线轴性颈椎病患者的研究。中国风湿病杂志。2015;37(10):379 - 379。
Deodhar A, Reveille JD, Harrison DD, Kim L, Lo KH, Leu JH,等。Golimumab静脉注射治疗成人强直性脊柱炎的安全性和有效性:GO-ALIVE研究第28周的结果中国风湿病杂志。2018;45(3):341-8。
Landewé R, Braun J, Deodhar A, Dougados M, Maksymowych WP, Mease PJ,等。certolizumab pegol对包括强直性脊柱炎在内的轴型颈椎病体征和症状的疗效:一项24周的双盲随机安慰剂对照3期研究结果Ann Rheum, 2013; 73:39-47。
李文杰,李文杰,李文杰,等。certolizumab pegol对轴性颈椎病患者96周以上的疗效:来自III期随机试验的结果。风湿性关节炎。2015;67(3):668-77。
van der Heijde D, Dougados M, Landewe R, Sieper J, Maksymowych WP, Rudwaleit M,等。certolizumab pegol治疗轴性颈椎病的持续疗效、安全性和患者报告的结果:quick - axspa的4年结果。风湿病学(牛津大学)。2017; 56(9): 1498 - 509。
王志强,王志强,王志强,等。白介素- 17a抑制剂Secukinumab治疗强直性脊柱炎。中华实用医学杂志,2015;29(4):344 - 344。
李志强,李志强,李志强,等。Secukinumab在抗tnf -naive和抗tnf -经历的活动性强直性脊柱炎患者中的疗效:来自MEASURE 2研究的结果中华神经外科杂志,2017;76(3):571-92。
Deodhar A, Conaghan PG, Kvien TK, Strand V, Sherif B, Porter B,等。Secukinumab可快速持续缓解强直性脊柱炎患者的疼痛和疲劳症状,与基线c反应蛋白水平或既往肿瘤坏死因子抑制剂治疗无关:来自MEASURE 2研究的2年数据。风湿性风湿病。2018。
张志刚,张志刚,张志刚,等。secukinumab对强直性脊柱炎临床和影像学结果的影响:来自随机III期MEASURE 1研究的2年结果中华神经外科杂志,2017;76(6):1070-7。
马佐-奥尔特加,西珀J, Kivitz A, Blanco R, Cohen M, Martin R,等。Secukinumab对活动性强直性脊柱炎患者体征和症状的持续改善长达两年:来自III期研究的结果关节炎护理res 2017;69(7): 1020-9。
Baraliakos X, Kivitz AJ, Deodhar AA, Braun J, Wei JC, Delicha EM,等。白介素- 17a抑制与secukinumab治疗活动性强直性脊柱炎的长期影响:3年疗效和安全性来自3期MEASURE 1试验的延长结果。临床经验风湿病杂志,2018;36(1):50-5。
范德海德D,魏成忠J, Dougados M, Mease P, Deodhar A, Maksymowych WP,等。Ixekizumab是一种白介素- 17a拮抗剂,用于治疗先前未接受生物疾病修饰抗风湿药物(COAST-V)治疗的强直性脊柱炎或x线轴性脊柱炎患者:一项为期16周的随机、双盲、主动对照和安慰剂对照3期试验结果。柳叶刀》。2018;392(10163):2441 - 51。
Deodhar A, Poddubnyy D, Pacheco-Tena C, Salvarani C, lesessailles E, Rahman P,等。Ixekizumab治疗x线轴型颈椎病的疗效和安全性:一项针对既往对肿瘤坏死因子抑制剂反应不充分或不耐受患者的随机、双盲、安慰剂对照3期试验16周结果风湿性关节炎。2019;71(4):599-611。
Giardina AR, Ferrante A, Ciccia F, Impastato R, Miceli MC, Principato A,等。依那西普和英夫利昔单抗治疗强直性脊柱炎患者的疗效和安全性的2年比较开放标签随机研究。风湿病杂志,2010;30(11):1437-40。
朴W, Hrycaj P, Jeka S, Kovalenko V, Lysenko G, Miranda P,等。一项随机、双盲、多中心、平行组、前瞻性研究,比较了CT-P13和innovator英夫利昔单抗治疗强直性脊柱炎患者的药代动力学、安全性和有效性:PLANETAS研究。中国生物医学工程学报,2013;32(10):1605-12。
Ruwaard J, l'Ami MJ, Marsman AF, Kneepkens EL, van Denderen JC, van der Horst-Bruinsma IE,等。依那西普和阿达木单抗治疗强直性脊柱炎患者的药物生存期和临床结果比较。中华风湿病杂志。2018;47(2):122-6。
刘伟,吴永华,张林,刘晓霞,宾旭,宾林,等。tnf - α抑制剂治疗活动性强直性脊柱炎患者的有效性和安全性:网络荟萃分析中的多种治疗比较科学代表2016;6:32768。
Corbett M, Soares M, Jhuti G, Rice S, Spackman E, Sideris E,等。肿瘤坏死因子- α抑制剂治疗强直性脊柱炎和非x线轴性脊柱炎:系统回顾和经济评价。卫生技术评价,2016;20(9):1-334 v-vi。
李国强,李志强,李志强。生物制剂对活动性强直性脊柱炎患者疗效的间接比较:一项系统综述和荟萃分析临床风湿病杂志,2017;36(7):1569-77。
王松,何强,帅哲。强直性脊柱炎和非x线轴性脊柱炎患者生物治疗中严重感染的风险:一项meta分析。临床风湿病杂志。2018;37(2):439-50。
侯立强,蒋广旭,陈玉峰,杨晓明,孟l,薛敏,等。TNF抑制剂在强直性脊柱炎中的相对安全性——14项随机对照试验的meta分析更新中国过敏免疫杂志,2018;54(2):234-43。
Wallis D, Thavaneswaran A, Haroon N, Ayearst R, Inman RD.轴性颈椎病的肿瘤坏死因子抑制剂治疗与感染风险:来自纵向观察队列的结果。风湿病学。2015;54(1):152 - 6。
杜德杰,李志强,李志强,等。与使用靶向免疫调节剂相关的危害比较风险:一项系统综述。关节炎护理研究。2016;68(8):1078-88。
金茵,严伟,裴sc,刘德华,金泰。韩国强直性脊柱炎患者服用肿瘤坏死因子阻滞剂时结核病的发病率。风湿病杂志,2011;38(10):2218-23。
金华伟,朴志强,杨子,尹毅,李永毅,宋耀文,等。中等负担地区肿瘤坏死因子抑制剂治疗中强直性脊柱炎和类风湿关节炎肺结核发病率的比较。临床风湿病杂志。2014;33(9):1307-12。
贾嘉泰,张志刚,张志刚,张志刚,等。1887例接受肿瘤坏死α拮抗剂患者的随访:结核菌素皮试转化与结核病风险中国临床呼吸杂志,2018;12(4):1668-75。
张志刚,张志刚,张志刚,张志刚,等。肿瘤坏死因子- α抑制剂下预测结核病风险的特征:来自高背景患病率的大型多中心队列的报告。风湿病杂志,2016;43(3):524-9。
Carmona L, Abasolo L, Descalzo MA, Perez-Zafrilla B, Sellas A, de Abajo F,等。暴露于TNF拮抗剂的风湿性疾病患者的癌症。中华风湿病杂志。2011;41(1):71-80。
在鲁汶脊椎关节炎生物制剂队列(BIOSPAR)中,Westhovens I, Lories RJ, Westhovens R, Verschueren P, de Vlam K.抗tnf治疗和脊椎关节炎恶性肿瘤。临床经验风湿病杂志,2014;32(1):71-6。
Hellgren K, Dreyer L, Arkema EV, Glintborg B, jacobson LT, Kristensen LE,等。使用TNF抑制剂治疗的颈椎病患者的癌症风险:来自ARTIS和DANBIO登记册的合作研究中华神经外科杂志,2017;76(1):105-11。
李志强,李志强,李志强,等。肿瘤坏死因子α抑制剂对强直性脊柱炎影像学进展的影响。中华风湿病杂志。2013;29(10):344 - 344。
Molnar C, Scherer A, Baraliakos X, de Hooge M, Micheroli R, Exer P,等。TNF阻滞剂通过降低疾病活动性抑制强直性脊柱炎的脊柱放射学进展:来自瑞士临床质量管理队列的结果中华神经外科杂志,2018;77(1):63-9。
Maas F, Spoorenberg A, Brouwer E, Bos R, Efde M, Chaudhry RN,等。接受tnf - α阻断治疗的强直性脊柱炎患者的脊柱放射学进展:一项前瞻性纵向观察队列研究公共科学学报。2015;10(4):e0122693。
金志杰,申志华,金松,成怡华,李松,宋勇,等。根据肿瘤坏死因子阻滞剂暴露的强直性脊柱炎患者的放射学进展:韩国脊椎关节病登记(OSKAR)数据的观察研究关节骨与脊柱。2016;83(5):569-72。
van der Heijde D, Landewe R, Baraliakos X, Houben H, van Tubergen A, Williamson P,等。强直性脊柱炎患者接受英夫利昔单抗治疗两年后的x线检查结果。风湿性关节炎。2008;58(10):3063-70。
李志强,李志强,李志强,李志强,等。强直性脊柱炎患者在抗tnf - α抗体英夫利昔单抗治疗4年后的影像学进展风湿病学(牛津大学)。2007; 46(9): 1450 - 3。
van der Heijde D, Landewe R, Einstein S, Ory P, Vosse D, Ni L,等。依那西普治疗两年后强直性脊柱炎的影像学进展。风湿性关节炎。2008;58(5):1324-31。
van der Heijde D, Salonen D, Weissman BN, Landewe R, Maksymowych WP, Kupper H,等。评估使用阿达木单抗治疗长达2年的强直性脊柱炎患者脊柱的影像学进展。关节炎治疗。2009;11(4):R127。
Braun J, Baraliakos X, Hermann KG, Deodhar A, van der Heijde D, Inman R,等。两种戈利单抗剂量对强直性脊柱炎放射学进展的影响:GO-RAISE试验4年的结果中国生物医学工程学报,2014;29(6):344 - 344。
van der Heijde D, Baraliakos X, Hermann KA, Landewe RBM, Machado PM, Maksymowych WP,等。轴性颈椎病患者放射学进展有限,MRI炎症持续减轻:来自quick - axspa III期随机试验的4年影像学结果中国生物医学工程学报,2018;27(5):699-705。
Braun J, Baraliakos X, Deodhar A, Poddubnyy D, Emery P, deliha EM,等。Secukinumab在强直性脊柱炎中显示持续疗效和低结构进展:来自MEASURE 1研究的4年结果。风湿病学(牛津大学)。58 2019;(5): 859 - 868。
Baraliakos X, Haibel H, Listing J, Sieper J, Braun J.强直性脊柱炎患者连续长期抗tnf治疗不会导致8年以上新骨形成率的增加。中国生物医学工程学报,2014;29(4):344 - 344。
Braun J, Baraliakos X, Listing J, Sieper J.抗肿瘤坏死因子英夫利昔单抗和依那西普治疗强直性脊柱炎患者前葡萄膜炎的发病率降低。风湿性关节炎。2005;52(8):2447-51。
李志强,李志强,李志强,等。阿达木单抗有效降低活动性强直性脊柱炎患者前葡萄膜炎发作率:一项前瞻性开放标签研究的结果中国生物医学工程学报,2009;29(5):696-701。
van Denderen JC, Visman IM, Nurmohamed MT, Suttorp-Schulten MS, van der Horst-Bruinsma IE。阿达木单抗显著降低强直性脊柱炎患者前葡萄膜炎的复发率。风湿病杂志,2014;41(9):1843-8。
谢晓华,李志强,李志强,等。依那西普强直性脊柱炎临床试验葡萄膜炎发生率分析。中国生物医学工程学报,2010;29(1):366 - 366。
张志刚,张志刚,张志刚,张志刚,张志刚,等。golimumab治疗hla - b27阳性强直性脊柱炎复发性葡萄膜炎的疗效中华眼科杂志,2017;37(1):139-45。
Calvo-Rio V, Blanco R, Santos-Gomez M, Rubio-Romero E, Cordero-Coma M, Gallego-Flores A,等。Golimumab治疗与脊椎关节炎相关的难治性葡萄膜炎。15例患者的多中心研究。中华风湿病杂志。2016;46(1):95-101。
Hernández M, Mesquida M, Llorens V, Maza MSdl, Blanco R, Calvo V,等。Certolizumab pegol对其他肿瘤坏死因子抑制剂难治的脊椎关节炎相关葡萄膜炎有效。《中华风湿病杂志》2017;36(增刊2):357 -。
鲁德华列特M, Rosenbaum JT, Landewe R, Marzo-Ortega H, Sieper J, van der Heijde D,等。观察轴性脊椎关节炎患者接受Certolizumab Pegol治疗后葡萄膜炎的发生率。关节炎护理研究。2016;68(6):838-44。
van Bentum RE, Heslinga SC, Nurmohamed MT, Gerards AH, Griep EN, Koehorst C,等。用Golimumab治疗强直性脊柱炎急性前葡萄膜炎的发生率降低- GO-EASY研究。风湿病杂志,2019;46(2):153-159。
吴东,郭云云,徐南宁,赵松,侯丽霞,焦涛,等。抗肿瘤坏死因子治疗强直性脊柱炎患者关节外表现的疗效:一项meta分析。BMC肌肉骨骼紊乱。2015;16:19。
Braun J, Baraliakos X, Listing J, Davis J, van der Heijde D, Haibel H,等。暴露于抗肿瘤坏死因子α药物治疗的强直性脊柱炎患者炎症性肠病发作或新发发生率的差异风湿性关节炎。2007;57(4):639-47。
温德林,J帕库,JM Berthelot, Flipo RM, Guillaume-Czitrom S, Prati C,等。抗肿瘤坏死因子治疗风湿病期间葡萄膜炎的新发。中华风湿病杂志。2011;41(3):503-10。
Wendling D, Joshi A, Reilly P, Jalundhwala YJ, Mittal M, Bao Y.比较开始抗肿瘤坏死因子治疗强直性脊柱炎患者发生葡萄膜炎的风险:一项大型美国索赔数据库的分析。中国医学杂志。2014;30(12):2515-21。
连峰,周娟,魏超,王勇,徐辉,梁林,等。抗tnfalpha药物和甲氨蝶呤在中国人群中与颈椎病相关的葡萄膜炎。临床风湿病杂志。2015;34(11):1913-20。
李E,林德斯特伦U, Zverkova-Sandstrom T, Olsen IC, forsbladd 'Elia H, Askling J,等。肿瘤坏死因子抑制剂治疗和强直性脊柱炎前葡萄膜炎的发生:来自瑞典生物制剂注册的结果。中国生物医学工程学报。2017;76(9):1515-21。
金敏梅,李毅,李毅,宋玉伟,余鸿辉,崔勇,等。肿瘤坏死因子抑制剂与非甾体抗炎药对强直性脊柱炎患者葡萄膜炎的预防作用。临床风湿病杂志。2018;37(10):2763-70。
Kavanaugh A, Krueger GG, Beutler A, Guzzo C, Zhou B, Dooley LT,等。英夫利昔单抗在活动性银屑病关节炎患者中通过1年的治疗保持高度的临床反应:来自IMPACT 2试验的结果中国生物医学工程学报,2007;26(4):498-505。
Mease PJ, Kivitz AJ, Burch FX, Siegel EL, Cohen SB, Ory P,等。依那西普治疗银屑病关节炎:安全性、有效性和对疾病进展的影响风湿性关节炎。2004;50(7):2264-72。
Mease PJ, Goffe BS, Metz J, VanderStoep A, Finck B, Burge DJ。依那西普治疗银屑病关节炎和银屑病:一项随机试验。柳叶刀》。2000;356(9227):385 - 90。
Mease PJ, Gladman DD, Ritchlin CT, Ruderman EM, Steinfeld SD, Choy EH,等。阿达木单抗治疗中重度活动性银屑病关节炎:一项双盲、随机、安慰剂对照试验的结果风湿性关节炎。2005;52(10):3279-89。
Kavanaugh A, McInnes I, Mease P, Krueger GG, Gladman D, Gomez-Reino J,等。Golimumab是一种新的人肿瘤坏死因子α抗体,每四周皮下注射一次用于银屑病关节炎:一项随机、安慰剂对照研究的24周疗效和安全性结果。风湿性关节炎。2009;60(4):976-86。
Mease PJ, Fleischmann R, Deodhar AA, Wollenhaupt J, Khraishi M, Kielar D,等。certolizumab pegol对银屑病关节炎患者体征和症状的影响:一项为期24周的3期双盲随机安慰剂对照研究(RAPID-PsA)结果中国生物医学工程学报,2014;29(1):344 - 344。
Mease PJ, McInnes IB, Kirkham B, Kavanaugh A, Rahman P, van der Heijde D,等。Secukinumab对银屑病关节炎患者白细胞介素- 17a的抑制作用中华实用医学杂志,2015;29(4):529 - 529。
McInnes IB, Mease PJ, Kirkham B, Kavanaugh A, Ritchlin CT, Rahman P,等。Secukinumab是一种人抗白介素- 17a单克隆抗体,用于银屑病关节炎患者(FUTURE 2):一项随机、双盲、安慰剂对照的3期试验。柳叶刀》。2015;386(9999):1137 - 46所示。
王志强,王志强,王志强,等。依那西普治疗活动性克罗恩病:一项随机、双盲、安慰剂对照试验胃肠病学。2001;121(5):1088 - 94。
胡贝尔W, Sands BE, Lewitzky S, Vandemeulebroecke M, Reinisch W, Higgins PD,等。Secukinumab,一种人抗il - 17a单克隆抗体,用于中重度克罗恩病:一项随机、双盲安慰剂对照试验的意外结果。肠道。2012;61(12):1693 - 700。
陈志伟,陈志伟,陈志伟,等。耐药或不耐受强直性脊柱炎患者从英夫利昔单抗转换为每周一次50 mg依那西普:一项54周研究的结果风湿性关节炎。2006;55(5):812-6。
Coates LC, Cawkwell LS, Ng NW, Bennett AN, Bryer DJ, Fraser AD等。真实的生活经验证实了对强直性脊柱炎的长期生物制剂和转换的持续反应。风湿病学。2008;(6):897 - 900。
prdeepdj, Keat AC, Gaffney K, Brooksby A, Leeder J, Harris C.强直性脊柱炎的抗tnf转换治疗。风湿病学。2008;(11):1726 - 7。
Haberhauer G, Strehblow C, Fasching P.在强直性脊柱炎和银屑病关节炎与类风湿关节炎中切换抗tnf药物的观察性研究。中华医学杂志,2010;29(4):344 - 344。
Lie E, van der Heijde D, Uhlig T, Mikkelsen K, Rodevand E, Koldingsnes W,等。强直性脊柱炎中TNF抑制剂切换的有效性:来自NOR-DMARD登记册的数据中国生物医学工程学报,2011;29(1):457 - 457。
李志强,李志强,李志强,等。432名强直性脊柱炎患者转换肿瘤坏死因子α抑制剂治疗后的临床反应、药物生存期及其预测因素:来自丹麦全国DANBIO注册中心的结果中国生物医学工程学报,2013;32(7):1149-55。
李志强,李志强,李志强,等。强直性脊柱炎患者切换tnf - α抑制剂的现实经验。欧洲卫生经济,2014;15(增刊1):S93-100。
Cantini F, Niccoli L, Nannini C, Cassara E, Kaloudi O, Giulio Favalli E,等。类风湿关节炎、银屑病关节炎和强直性脊柱炎的二线生物治疗优化。中华风湿病杂志,2017;47(2):183-92。
杜德华,于东。切换肿瘤坏死因子抑制剂治疗轴性颈椎病的研究。中华风湿病杂志。2017;47(3):343-50。
Navarro-Compan V, Plasencia-Rodriguez C, de Miguel E, Balsa A, Martin-Mola E, Seoane-Mato D,等。轴性颈椎病患者抗tnf停用和逐渐减少策略:系统文献回顾。风湿病学。2016;55(7):1188 - 94。
Sebastian A, Wojtala P, Lubinski L, Mimier M, Chlebicki A, Wiland P.停止TNF抑制剂治疗后轴性颈椎病的疾病活性。55 Reumatologia。2017;(4):157 - 62。
李志强,李志强,李志强,等。继续阿达木单抗治疗与停止阿达木单抗治疗在维持非x线轴性颈椎病患者缓解中的疗效和安全性(ABILITY-3):一项多中心、随机、双盲研究柳叶刀》。2018;392(10142):134 - 44。
Arends S, van der Veer E, Kamps FB, Houtman PM, Bos R, Bootsma H,等。在日常临床实践中,在疾病活动稳定低的强直性脊柱炎患者中,患者定制剂量减少tnf - α阻断剂临床经验风湿病杂志,2015;33(2):174-80。
方伟,霍罗伊德C,戴维森B,阿姆斯特朗R,哈维N,丹尼森E,等。肿瘤坏死因子抑制剂在强直性脊柱炎和银屑病性关节炎中的实际剂量减少策略的有效性。风湿病学。2016;55(10):1837 - 42。
Almirall M, Salman-Monte TC, Lisbona MP, Maymo J.临床缓解期轴性颈椎病患者生物治疗剂量减少:复发患者与疾病活动度仍较低的患者之间是否存在差异?风湿病杂志,2015;35(9):1565-8。
连峰,周娟,王勇,陈冬,徐华,梁磊。依那西普减剂量治疗轴性颈椎病的疗效观察。临床经验风湿病杂志,2018;36(5):884-90。
陈敏敏,李敏敏,廖海涛,陈文生,赖昌昌,蔡春春。类风湿关节炎和强直性脊柱炎患者减量生物治疗后的健康相关生活质量结局。临床风湿病杂志。2018;37(2):429-38。
Redondo C, Martinez-Feito A, plasenicia - rodriguez C, Navarro-Compan V, nno - nuno L, Peiteado D,等。基于脊柱关节炎患者血清药物水平的Golimumab减量策略。风湿性关节炎。2018;70(8):1356-8。
Plasencia C, Kneepkens EL, Wolbink G, Krieckaert CL, Turk S, Navarro-Compan V,等。在低疾病活动度的颈椎病患者中,肿瘤坏死因子抑制剂的减量策略与标准给药方案的比较风湿病杂志,2015;42(9):1638-46。
朴继伟,尹毅,李俊华,朴志杰,李eb,宋耀文,等。强直性脊柱炎维持临床缓解的小剂量依那西普治疗。临床经验风湿病杂志,2016;34(4):592-9。
朴继伟,权敏,朴志强,崔志勇,李eb,宋耀文,等。肿瘤坏死因子抑制剂剂量减少对强直性脊柱炎放射学进展的影响。公共科学学报,2016;11(12):e0168958。
宋海燕,李志强,李志强,等。未使用肿瘤坏死因子阻滞剂的活动性强直性脊柱炎患者和肿瘤坏死因子阻滞剂无效患者对利妥昔单抗的不同反应:一项为期24周的临床试验风湿性关节炎。2010;62(5):1290-7。
宋海燕,李志强,李志强,等。强直性脊柱炎患者对利妥昔单抗治疗的反应和复发时的再治疗的一年随访。中华神经外科杂志,2013;32(2):306 - 6。
宋海燕,王志强,王志强,等。阿巴西普治疗活动性强直性脊柱炎:一项开放标签,24周的初步研究。中国生物医学工程学报,2011;30(6):366 - 366。
Lekpa FK, Farrenq V, Canoui-Poitrine F, Paul M, Chevalier X, Bruckert R,等。阿巴西普对难以抑制肿瘤坏死因子的轴性脊柱关节病缺乏疗效。《关节骨与脊柱》杂志2012;79(1):47-50。
Sieper J, Porter-Brown B, Thompson L, Harari O, Dougados M. tocilizumab治疗强直性脊柱炎的短期症状疗效评估:随机、安慰剂对照试验结果。中国生物医学工程学报,2014;29(1):344 - 344。
王晓燕,王晓燕,王晓燕,等。Sarilumab治疗强直性脊柱炎:II期随机、双盲、安慰剂对照研究(ALIGN)结果中国生物医学工程学报,2015;29(6):1051-7。
Poddubnyy D, Hermann KG, Callhoff J, Listing J, Sieper J. Ustekinumab治疗活动性强直性脊柱炎:一项28周、前瞻性、开放标签、概念验证研究(TOPAS)的结果中国生物医学工程学报,2014;29(5):817-23。
杜德华,王勇,王志强,等。三项多中心、随机、双盲、安慰剂对照研究评估Ustekinumab治疗轴性颈椎病的疗效和安全性风湿性关节炎。2018;71:258-270。
潘森,范罗森,魏斯林顿,杰特,查尔斯,等。口服磷酸二酯酶4抑制剂阿普美司特治疗强直性脊柱炎的疗效和安全性。中国生物医学工程学报,2013;32(9):1475-80。
van der Heijde D, Deodhar A, Wei JC, Drescher E, Fleishaker D, Hendrikx T,等。托法替尼在强直性脊柱炎患者中的应用:一项为期16周、随机、安慰剂对照、剂量范围的II期研究中国生物医学工程学报。2017;36(8):1340-7。
Maksymowych WP, Heijde DV, Baraliakos X, Deodhar A, Sherlock SP, Li D,等。托法替尼与强直性脊柱炎患者轴向磁共振成像炎症的最低重要降低相关。风湿病学。2018;57(8):1390 - 9。
van der Heijde D, Baraliakos X, Gensler LS, Maksymowych WP, Tseluyko V, Nadashkevich O,等。选择性Janus激酶1抑制剂filgotinib在活动性强直性脊柱炎(TORTUGA)患者中的有效性和安全性:来自一项随机、安慰剂对照、2期试验的结果柳叶刀》。2018;392(10162):2378 - 87。
确认
不适用。
资金
巴西风湿病学会。资助机构在研究设计、数据收集、分析和解释以及撰写手稿方面没有任何作用。
作者信息
作者及隶属关系
贡献
所有作者都对数据的获取做出了贡献,参与了手稿的起草或对重要的智力内容进行了批判性的修改,参与了投票,最终批准了即将出版的版本,并充分参与了工作,对内容的适当部分承担了公共责任。
作者的信息
不适用。
相应的作者
道德声明
伦理批准并同意参与
不适用。
发表同意书
不适用。
相互竞争的利益
Gustavo Gomes Resende获得了艾伯维、杨森、诺华、辉瑞和UCB的讲座费;艾伯维、杨森和诺华的顾问委员会;巴西风湿病学会、FAPEMIG和UCB的研究支持;艾伯维(Abbvie)和辉瑞(Pfizer)的临床研究费用;赞助来自艾伯维、杨森、礼来、诺华、辉瑞和UCB的科学活动。
Eduardo de Souza Meirelles作为演讲者从诺华(Novartis)、艾伯维(Abbvie)、雅培(Abbott)和Marjan收取报酬;诺华(Novartis)和辉瑞(Pfizer)的研究资助;支持Aché、辉瑞、诺华、杨森、艾伯维、罗氏和礼来的会议和课程;诺华和玛扬的顾问费。
Cláudia Diniz Lopes Marques接受了艾伯维、杨森、辉瑞和诺华的讲座费;诺华和艾伯维的顾问委员会;艾伯维、杨森、辉瑞、诺华和礼来赞助活动。
Adriano Chiereghin获得杨森、诺华、UCB和辉瑞的荣誉演讲;支持艾伯维、杨森、诺华、UCB和辉瑞的课程和会议;诺华和杨森的顾问委员会
Andre Marun Lyrio收到了杨森Speaker和UCB的付款;支持杨森,艾伯维,辉瑞,UBC,诺华和百合的课程/会议。
Antônio Carlos Ximenes因参与艾伯维、辉瑞、罗氏、BMS和安进的临床研究而获得报酬;辉瑞和Abbivie的科学董事会成员;作为艾伯维、辉瑞和雅培的讲师。
卡拉Gonçalves萨阿德没有利益冲突。
Célio Roberto Gonçalves没有利益冲突。
Charles Lubianca Kohen获得了诺华(Novartis)参与顾问委员会的资金支持;演讲费来自杨森、艾伯维、诺华、辉瑞、UCB;杨森、艾伯维、罗氏、阿斯利康、诺华等公司的活动支持。
Cláudia Goldenstein Schainberg曾参与AbbVie、Janssen、Lilly、Novartis和Pfizer的制药顾问委员会;是艾伯维、杨森、礼来、诺华、辉瑞邀请的演讲嘉宾;没有这些医药行业的库存。
Cristiano Barbosa Campanholo获得了杨森、艾伯维、布里斯托尔、礼来、诺华、辉瑞、UCB等公司的财务支持,以参与咨询委员会;杨森、艾伯维、礼来、诺华、辉瑞、UCB的演讲费;支持杨森,艾伯维,布里斯托尔,诺华和辉瑞的活动。
Júlio西尔维奥·德·索萨·布埃诺·菲尔霍没有利益冲突。
Lenise Brandao Pieruccetti没有利益冲突。
Mauro Waldemar Keiserman接受了艾伯维、Actelion、Biogen、Bristol、Celltrion、礼来、人类基因组科学、杨森、辉瑞、诺华、罗氏、赛诺菲和UCB的讲座、咨询委员会和临床研究的资金支持。
Michel Alexandre Yazbek获得了艾伯维、UCB、诺华和礼来的资金支持。
佩内洛普·埃斯特·帕洛米诺斯没有利益冲突。
Rafaela Silva Guimarães Goncalves接受了杨森、诺华、艾伯维、阿普森、布里斯托尔和辉瑞的讲座费用;詹森的顾问委员会。
Ricardo da Cruz Lage从艾伯维和诺华获得演讲费;杨森、诺华、辉瑞和艾伯维为科学活动提供支持;艾伯维的临床研究费用
罗德里戈·卢皮诺·阿萨德接受了艾伯维、诺华、杨森、UCB、礼来和布里斯托尔的讲座和顾问费;艾伯维和UCB的研究支持。
Rubens Bonfiglioli获得了罗氏、辉瑞、安进和诺华的临床研究资金支持;来自礼来、艾伯维、罗氏和UCB的科学咨询;为罗氏(Roche)、辉瑞(Pfizer)、艾伯维(Abbvie)和诺华(Novartis)的活动提供支持;用于罗氏、辉瑞和杨森的专题讨论会和赞助会议。
Sônia Maria Alvarenga Anti获得了艾伯维、詹森、诺华、礼来和UCB的财政支持。
Sueli Coelho da Silva Carneiro接受了来自艾伯维、杨森、礼来、诺华和辉瑞的荣誉演讲;CNPq和FAPERJ对研究的支持;艾伯维、杨森、诺华、辉瑞、CNPq和FAPERJ的大会支持;杨森、礼来和诺华的顾问委员会。
Thauana Luíza Oliveira收到艾伯维、诺华和杨森的讲师费;艾伯维和杨森对大会的支持。
Valderílio Feijó Azevedo是GRAPPA成员;Edumed Biotech的医疗主任;接受了辉瑞、罗氏、杨森、布里斯托尔、艾伯维、Medimmune、勃林格、GSK、USB、赛诺菲、武田、鸟岩生物和NovoNordisk的临床研究;为辉瑞、Hospira、Roche、MSD、BMS、Merck Senoro、Janssen、Novertis、Celltrion、UCB和AztraZeneca的活动和讲座提供财政支持。
华盛顿·阿尔维斯·比安奇没有利益冲突。
Wanderley Marques Bernardo没有利益冲突。
马塞洛·德·梅代罗斯·皮涅罗(Marcelo de Medeiros Pinheiro)获得了诺华和杨森的顾问委员会资金支持;诺华、杨森、艾伯维的讲座
Percival Degrava Sampaio-Barros曾参加艾伯维、杨森、诺华、辉瑞和UCB实验室的讲座、董事会或科学活动。
额外的信息
出版商的注意
伟德体育在线施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
权利和权限
开放获取本文根据创作共用属性4.0国际许可协议(http://creativecommons.org/licenses/by/4.0/),允许在任何媒介上不受限制地使用、分发和复制,前提是您对原作者和来源给予适当的赞扬,提供到创作共用许可证的链接,并注明是否进行了更改。创作共用公共领域奉献弃权书(http://creativecommons.org/publicdomain/zero/1.0/)除另有说明外,适用于本条所提供的资料。
关于本文
引用本文
雷森德,g.g.,梅雷莱斯,e.d.s.,马奎斯,C.D.L.et al。2019年巴西风湿病学会轴性脊椎关节炎指南。阿德Rheumatol60, 19(2020)。https://doi.org/10.1186/s42358-020-0116-2
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/s42358-020-0116-2